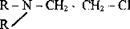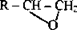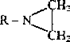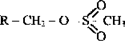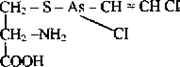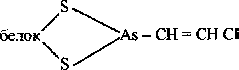|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Механизм действия алнилирующцх ядовВ патохимической классификации химические вещества данной группы именуются алкилирующими ядами. Под алкилированием понимается процесс вытеснения молекулой яда функциональных групп белка вообще и нуклеопротеидов в особенности.
Различают алкилирующее действие общее и избирательное. К общим алкилирующим агентам относятся вещества, имеющие один или несколько активных радикалов следующего строения:
1) производные сернистого иприта: R _ S _ CH2 _ CH2 _ Cl
2) производные азотистого иприта:
3) эпоксиды:
4) этиленимины:
5) эфиры метансульфокислоты:
Ко второй группе кожно-резорбтивных ядов относятся так называемые тиоловые яды. Это такие вещества, которые избирательно алкилируют только тиоловые группы метаболитов тканей. Подобные свойства проявляют соединения трехвалентного мышьяка, и ряд металлоорганических соединений.
Существует три теории механизма действия, которые необходимо рассматривать в совокупности.
1. Механизм действия ипритов основан на вытеснении молекулой яда водородных групп у атома азота азотистых оснований нуклеопротеидов (нуклеотическое действие).
Как известно, дезоксирибонуклеиновая кислота (ДНК) представляет собой цепь дезоксирибонуклеотидов, которые в свою очередь, состоят из пентозного сахара, остатка фосфорной кислоты и азотистого основания. Согласно многочисленным исследованиям, наибольший интерес представляет реакция ипритов с азотистыми основаниями ДНК (аденин-тимин, гуанин-цитозин). Алкилирующие вещества охотнее всего вступают в реакцию с гуанином. Алкилирование гуанина приводит к появлению неустойчивого четвертичного азота. В результате сахарно-фосфорно-азотистый каркас ДНК распадается, что приводит к деполимеризации нуклеопротеидов.
2. Механизм действия основан на внутриклеточной активизации молекулы иприта с образованием в клетке ониевых соединений и в последующем активных радикалов (лучеподобное действие) [Родневич].
При исследовании гидролиза иприта было показано, что в начале гид ролиза образуются так называемые ониевые соединения (ониевые ионы). Сернистый иприт при гидролизе образует сульфониевые ионы, а азотистый иприт этиленимониевые ионы. Эти ионы обладают большой реакционной способностью, благодаря чему их сравнивают с продуктами радиолиза воды. Ониевые ионы могут вступать во взаимодействие с азотом пуринового ядра аденина и гуанина, входящих в структуру нуклеиновых кислот, и алкилировать их и даже «сшивать» цепи нуклеиновых кислот. В результате этого взаимодействия весьма существенно расстраивается функционирование нуклеиновых кислот, что приводит к нарушению синтеза белка, и к подавлению регенерации тканей. Следствием повреждения ДНК является нарушение хромосомного аппарата, и изменение наследственных признаков.
Кроме того, ониевые кислоты могут вызывать появление ионов Н, ОН, НО2, которые также весьма реакционноспособны и оказывают действие на клетки тканей, которое напоминает повреждающее действие ионизирующих излучений.
Однако, между действием ипритов и проникающей радиацией имеются существенные отличия. Р.К. Лякявичус (1967) приводит данные, показывающие, что ядра клеток более чувствительны к иприту, чем к проникающей радиации.
При воздействии проникающей радиации на ядра клеток наблюдаются и хромосомные, и хроматидные аберрации. При действии ипритов наблюдаются только хроматидные аберрации. Цитогенетические эффекты ипритов наблюдаются не ранее, чем через 8 часов, а при облучении они обнаруживаются почти сразу. Кислород не отягощает интоксикации алкилирующими соединениями, а при воздействии ионизирующего излучения количество аберраций в присутствии кислорода возрастает.
3. Теория мостиковых связей (аллергогенное действие). Механизм действия основан на блокировании полипептидной цепи ипритным «замком».
Иприты с двумя или тремя хлорэтильными радикалами более активны. чем с одним хлорэтильным радикалом. Следовательно, бифункциональные иприты взаимодействуют с метаболитом двумя концами своей молекулы, как бы сшивая метаболит, как бы запирая на «замок», образуя мостиковую связь в полипептидном стержне или в нуклеотиде. Имеет место полимеризация ипритных молекул после соединения их с белками. Понятно, что такие белки будут лишены своих реакционных способностей и, по-видимому, они-то и становятся аутоантигенами, определяя некоторые аллергические эффекты ипритов.
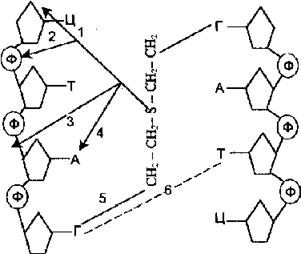
Варианты повреждения ДНК ипритом:
1. Отщепление азотистых оснований.
2. Взаимодействие с остатком фосфорной кислоты.
3. Разрыв цепи ДНК.
4. Взаимодействие с азотистыми основаниями.
5. Сшивание 2-х спиральной цепи ДНК.
6. Ошибка спаривания азотистых оснований.
Действие ипритов на ДНК ведет к токсигенетическим нарушениям, что проявляется:
1) нарушение митозов (цитостатическое действие);
2) нарушение синтеза белков и ферментов;
3) злокачественным повреждением клеток (бластомогенное действие);
4) нарушение развития эмбрионов и плода (тератогенное действие);
5) нарушением иммунитета;
6) нарушением генетических признаков клеток (мутагенное действие).
Особенности механизма действия алкилирующих ядов
с избирательным действием (люизит)
В лабораториях Питерса (Англия) и А.И. Черкеса (Киев) было показано. что соединения с трехвалентным мышьяком охотно вступают в реакцию со свободными аминокислотами, имеющими сульфгидрильные группы (цистеин):
Однако более устойчивую связь трехвалентный мышьяк образует с полипептидами:
Проникая в ткани, люизит повреждает те ферментные системы, которые богаты тиоловыми группами. Наиболее ранимой оказалась пируватокси дазная система, в которую входит липоевая кислота, имеющая две тиоловые группы.
По мнению Питерса (1963). А. И. Черкеса (1964), дигидролипоевая кислота, является первичным объектом воздействия группы тиоловых ядов. Гидролазы (в том числе и холинэстеразы), оксидазы (пируватоксидазная система) и дегидрогеназы, ряд ферментов АТФ, наконец, холинорецепторы содержат тиоловые группы и могут повреждаться при проникновении в ткани люизита.
Кроме того при действии тиоловых ядов отмечается отсутствие лучеподобного действия.
Дата добавления: 2015-02-05 | Просмотры: 574 | Нарушение авторских прав |