|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Г. Владикавказ, 2012 г
А. Ионизация и возбуждение атомов. Б. Увеличение количества электронных слоев. В. Превращение протона ядра в нейтрон.
10. К ионизирующим излучениям относятся: А. квантовое (фотонное) и корпускулярное Б. световое (видимая часть спектра). В. ультрафиолетовое. Г. лазерное Д. инфракрасное.
Ответы:
Государственное бюджетное образовательное учреждение высшего Профессионального образования Минздравсоцразвития России «СЕВЕРО-ОСЕТИНСКАЯ ГОСУДАРТВЕННАЯ МЕДИЦИНСКАЯ АКАДЕМИЯ» Кафедра общей хирургии с курсом лучевой диагностики с лучевой терапией
Тема: «Биологические основы лучевой терапии. Классификация и планирование лучевой терапии. г. Владикавказ, 2012 г. зав.курсом лучевой диагностики и лучевой терапии, зав.кафедрой общей хирургии с курсом лучевой диагностики и лучевой терапии доцент Беслекоев У.С. ассистент курса лучевой диагностики и лучевой терапии доцент Кораева И.Х к.м.н. Ганношенко Е.М. Алиева Е.А. Кубанцева И.Э. Созаонти З.Р.
Тема: «Биологические основы лучевой терапии. Классификация и планирование лучевой терапии.
Цель занятия: Иметь представление о радиоактивности и радиоактивных излучениях, их свойствах. Строение атома. Биологическое действие ионизирующих излучений и основы лучевой терапии.
Конкретные цели занятия: Знать:
Уметь: 1. Определить: активность радиоактивного вещества, выбор режима облучения. 2. Определить показания и противопоказания к лучевой терапии. 3. Определить метод лучевой терапии
База проведения и материальное обеспечение занятия:
5.Видеофильмы, мультимедийные презентации. 6.Истории болезней, рентгенограммы больных, обслуживаемых гамма-кабинетом.
Литература. 1. Кишковский А.Н,Дударев А.Л.»Лучевая терапия неопухолевых заболеваний».М,1977г. 2. Зетгенидзе Г.А. «Клиническая рентгенорадиология». М.1985г. 3. Линденбратен Л.Д., Королюк И.П., «Медицинская радиология и рентгенология», М. «Медицина», 2000г. 4.Г.Е.Труфанов «Лучевая диагностика и лучевая терапия», СПб, 2005. 5. «Лучевая диагностика».Учебник для вузов.Под ред.проф.Труфанова Г.Е. М,2007г.
Блок информации:
ФОТОННОЕ И КОРПУСКУЛЯРНОЕ ИЗЛУЧЕНИЕ
Электромагнитные излучения. В лучевой терапии используют рентгеновское излучение рентгенотерапевтических аппаратов, гамма -излучение радионуклидов и тормозное (рентгеновское) излучение высоких энергий. Рентгеновское излучение — фотонное излучение, состоящее из тормозного и (или) характеристического излучения. Тормозное излучение — коротковолновое электромагнитное излучение, возникающее при изменении скорости (торможении) заряженных частиц при взаимодействии с атомами тормозящего вещества (анода). Длины волн тормозного рентгеновского излучения не зависят от атомного номера тормозящего вещества, а определяются только энергией ускоренных электронов. Спектр тормозного излучения непрерывный, с максимальной энергией фотонов, равной кинетической энергии тормозящихся частиц. Характеристическое излучение возникает при изменении энергетического состояния атомов. При выбивании электрона из внутренней оболочки атома электроном или фотоном атом переходит в возбужденное состояние, а освободившееся место занимает электрон из внешней оболочки. При этом атом возвращается в нормальное состояние и испускает квант характеристического рентгеновского излучения с энергией, равной разности энергий на соответствующих уровнях. Характеристическое излучение имеет линейный спектр с определенными для данного вещества длинами волн, которые, как и интенсивность линий характеристического спектра рентгеновского излучения, определяются атомным номером элемента Z и электронной структурой атома. Интенсивность тормозного излучения обратно пропорциональна квадрату массы заряженной частицы и прямо пропорциональна квадрату атомного номера вещества, в поле которого происходит торможение заряженных частиц. Поэтому для увеличения выхода фотонов используют относительно легкие заряженные частицы — электроны и вещества с большим атомным номером (молибден, вольфрам, платину).
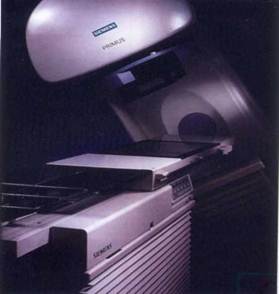
Тормозное излучение высокой энергии, как и тормозное рентгеновское излучение, — это коротковолновое электромагнитное излучение, возникающее при изменении скорости (торможении) заряженных частиц при взаимодействии с атомами мишени. Этот вид излучения отличается от рентгеновского высокой энергией. Источниками тормозного излучения высокой энергии являются линейные ускорители электронов — ЛУЭ с энергией тормозного излучения от 6 до 20 МэВ, а также циклические ускорители — бетатроны. Для получения высокоэнергетического тормозного излучения используют торможение резко ускоренных электронов в вакуумных системах ускорителей
Линейный ускоритель электронов
Гамма-излучение — коротковолновое электромагнитное излучение, испускаемое возбужденными атомными ядрами при радиоактивных превращениях или ядерных реакциях, а также при аннигиляции частицы и античастицы (например, электрона и позитрона). Источниками гамма-излучения являются радионуклиды. Каждый радионуклид испускает у-кванты своей определенной энергии. Радионуклиды производят на ускорителях и в ядерных реакторах. Под активностью радионуклидного источника понимают количество распадов атомов в единицу времени. Измерения производят в Беккерелях (Бк). 1 Бк — активность источника, в котором происходит 1 распад в секунду. Несистемная единица активности — Кюри (Ки). 1 Ки = 3,7 х 10юБк. Источниками у-излучения для дистанционной и внутриполостной лучевой терапии являются б0Со и 137Cs. Наибольшее распространение получили препараты 60Со с энергией фотонов в среднем 1,25 МэВ (1,17 и 1,33 МэВ). Для проведения внутриполостной лучевой терапии применяют 60Со, 137Cs, 192Ir.
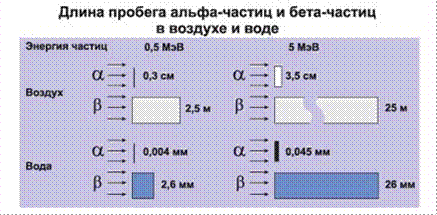
Корпускулярное излучение — потоки заряженных частиц: электронов, протонов, тяжелых ионов (например, ядер углерода) с энергиями в несколько сот МэВ, а также нейтральных частиц — нейтронов. Облучение с помощью потока частиц в настоящее время начали называть адронной терапией. К адронам (от греческого слова hadros — «тяжелый») относятся нуклоны, входящие в них протоны и нейтроны, а также л-мезоны и др. Источниками частиц являются ускорители и ядерные реакторы. Электронный пучок высокой энергии генерируется такими же ускорителями электронов, как и при получении тормозного излучения. Используют пучки электронов с энергией от 6 до 20 МэВ. Электроны высокой энергии обладают большой проникающей способностью. Средняя длина свободного пробега таких электронов может достигать в тканях человеческого организма 10—20 см. Электронный пучок, поглощаясь в тканях, создает дозное поле, при котором максимум ионизации образуется вблизи поверхности тела. За пределами максимума ионизации происходит довольно быстрый спад дозы. На современных линейных ускорителях имеется возможность регулировать энергию пучка электронов, а соответственно, создавать требуемую дозу на необходимой глубине. Нейтрон — частица, не имеющая заряда. Процессы взаимодействия нейтронов (нейтральных частиц) с веществом зависят от энергии нейтронов и атомного состава вещества. Основной эффект действия тепловых (медленных) нейтронов с энергией 0,025 эВ на биологическую ткань происходит под действием протонов, образующихся в реакции (п, р) и теряющих всю свою энергию в месте рождения. Большая часть энергии медленных нейтронов расходуется на возбуждение и расщепление молекул тканей. Почти вся энергия быстрых нейтронов с энергией от 200 кэВ до 20 МэВ теряется в ткани при упругом взаимодействии. Дальнейшее выделение энергии происходит в результате ионизации среды протонами отдачи. Высокая линейная плотность энергии нейтронов препятствует репарации облученных опухолевых клеток. Протон — положительно заряженная частица. Используется метод облучения на «пике Брэгга», когда максимальная энергия заряженных частиц выделяется в конце пробега и локализуется в ограниченном объеме облучаемой опухоли. В результате образуется большой градиент доз на поверхности тела и в глубине облучаемого объекта, после чего происходит резкое затухание энергии. Меняя энергию пучка, можно изменять место его полной остановки в опухоли с большой точностью. Применяются пучки протонов с энергией 70—200 МэВ и техника многопольного облучения с разных направлений, при которой интегральная доза распределяется на большой площади поверхностных тканей. При облучении на синхроциклотроне в ПИЯФ (Петербургский институт ядерной физики) используют фиксированную энергию выведенного протонного пучка — 1000 МэВ и применяют методику облучения напролет. Протоны такой высокой энергии легко проходят сквозь облучаемый объект, производя равномерную ионизацию вдоль своего пути. При этом происходит малое рассеяние протонов в веществе, поэтому сформированный на входе узкий с резкими границами пучок протонов остается практически таким же узким и в зоне облучения внутри объекта. В результате применения облучения напролет в сочетании с ротационной техникой облучения обеспечивается очень высокое отношение дозы в зоне облучения к дозе на поверхности объекта — порядка 200:1 л-мезоны — бесспиновые элементарные частицы с массой, величина которой занимает промежуточное место между массами электрона и протона. л-Мезоны с энергиями 25—100 МэВ проходят весь путь в ткани практически без ядерных взаимодействий, а в конце пробега захватываются ядрами атомов ткани. Акт поглощения л-мезона сопровождается вылетом из разрушенного ядра нейтронов, протонов, ос-частиц, ионов Li, Be и др. Активному внедрению в клиническую практику адронной терапии пока препятствует высокая стоимость технологического обеспечения процесса. альфа-излучение — корпускулярное излучение, состоящее из ядер 4Не (два протона и два нейтрона), испускаемых при радиоактивном распаде ядер или при ядерных реакциях, превращениях. альфа-частицы испускаются при радиоактивном распаде элементов тяжелее свинца или образуются в ядерных реакциях. Альфа-частицы обладают высокой ионизирующей способностью и малой проникающей способностью, несут два положительных заряда.
Радионуклид 225Ас с периодом полураспада 10,0 сут в соединении с моно-клональными антителами применяют для радиоиммунотерапии опухолей. В перспективе — использование для этих целей радионуклида |49ТЬ с периодом полураспада 4,1 ч. ос-Излучатели начали использовать для облучения эндотелиальных клеток в коронарных артериях после проведения операций — аортокоронарного шунтирования.
B-излучение — корпускулярное излучение с непрерывным энергетическим спектром, состоящее из отрицательно или положительно заряженных электронов или позитронов (B~ или B+ частиц) и возникающее при радиоактивном B-распаде ядер или нестабильных частиц. B-Излучатели используются при лечении злокачественных опухолей, локализация которых позволяет обеспечить непосредственный контакт с этими препаратами. Источниками B-излучения являются l06Ru, B~-излучатель с энергией 39,4 кэВ и периодом полураспада 375, 59 дня, l06Rh, B -излучатель с энергией 3540,0 кэВ и периодом полураспада 29,8 с. Оба B-излучателя l06Ru + 106Rh входят в комплекты офтальмологических аппликаторов. B~-излучатель 32Р с энергией 1,71 МэВ и периодом полураспада 14,2 дня используется в кожных аппликаторах для лечения поверхностных заболеваний. Радионуклид 89Sr является практически чистым B-излучателем с периодом полураспада 50,6 дня и средней энергией B-частиц 1,46 МэВ. Раствор 89Sr — хлорида используется для паллиативного лечения костных метастазов. 153Sm с энергиями р-излучения 203,229 и 268 кэВ и с энергиями у-излучения 69,7 и 103 кэВ, периодом полураспада 46,2 ч входит в состав отечественного препарата самария-оксабифора, предназначенного для воздействия на метастазы в костях, а также применяемого у больных с выраженным болевым синдромом в суставах при ревматизме. 90Y с периодом полураспада 64,2 ч и максимальной энергией 2,27 МэВ используется для различных терапевтических целей, включая радиоиммунотерапию с мечеными антителами, лечение опухолей печени и ревматоидного артрита. Радионуклид 59Fe в составе таблетированного радиофармацевтического препарата применяют в Российском научном центре рентгенорадиологии (Москва) для лечения больных раком молочной железы. Принцип действия препарата, по мнению авторов, заключается в распространении железа током крови, избирательном накоплении в клетках опухолевой ткани и воздействии на них р-излучением. 67Си с периодом полураспада 2,6 сут соединяют с моноклональными антителами для радиоиммунной терапии опухолей. l86Re в составе препарата (рения сульфид) с периодом полураспада 3,8 сут используют для лечения болезней суставов, а баллонные катетеры с раствором перрената натрия применяют для проведения эндоваскулярной брахи-терапии. Считается, что есть перспектива для применения Р+-излучателя 48V с периодом полураспада 16,9 сут для проведения внутрикоронарной брахи-терапии с использованием артериального стента из сплава титана и никеля. 13|1 применяют в виде растворов для лечения заболеваний щитовидный железы. 1311 распадается с испусканием сложного спектра Р- и у-излучения. Имеет период полураспада 8,06 дня.
КЛИНИЧЕСКАЯ ДОЗИМЕТРИЯ
Клиническая дозиметрия — раздел дозиметрии ионизирущего излучения, являющийся неотъемлемой частью лучевой терапии. Основная задача клинической дозиметрии состоит в выборе и обосновании средств облучения, обеспечивающих оптимальное пространственно-временное распределение поглощенной энергии излучения в теле облучаемого больного и количественное описание этого распределения. Клиническая дозиметрия использует расчетные и экспериментальные методики. Расчетные методы основаны на уже известных физических законах взаимодействия различных видов излучения с веществом. С помощью экспериментальных методов моделируют лечебные ситуации с измерениями в тканеэквивалентных фантомах. Задачами клинической дозиметрии являются: — измерение радиационных характеристик терапевтических пучков излучения; измерение радиационных полей и поглощенных доз в фантомах; прямые измерения радиационных полей и поглощенных доз на больных;
измерение радиационных полей рассеянного излучения в каньонах с терапевтическими установками (в целях радиационной безопасности пациентов и персонала); проведение абсолютной калибровки детекторов для клинической дозиметрии; проведение экспериментальных исследований новых терапевтических методик облучения. Основными понятиями и величинами клинической дозиметрии являются поглощенная доза, дозное поле, дозиметрический фантом, мишень.
Доза ионизирующего излучения: 1) мера излучения, получаемого облучаемым объектом, поглощенная доза ионизирующего излучения; 2) количественная характеристика поля излучения — экспозиционная доза и керма. Поглощенная доза — это основная дозиметрическая величина, которая равна отношению средней энергии, переданной ионизирующим излучением веществу в элементарном объеме, к массе вещества в этом объеме: D = Е/m, где D — поглощенная доза, Е — средняя энергия излучения, m — масса вещества в единице объема.
В качестве единицы поглощенной дозы излучения в СИ принят Грей (Гр) в честь английского ученого Грея (L. Н. Gray), известного своими трудами в области радиационной дозиметрии. 1 Гр равен поглощенной дозе ионизирующего излучения, при которой веществу массой в 1 кг передается энергия ионизирующего излучения, равная 1 Дж. В практике распространена также внесистемная единица поглощенной дозы — рад (radiation absorbed dose). 1 рад = 10~2Дж/кг = 100 эрг/г = 10~2Гр или 1 Гр = 100 рад. Поглощенная доза зависит от вида, интенсивности излучения, энергетического и качественного его состава, времени облучения, а также от состава вещества. Доза ионизирующего излучения тем больше, чем длительнее время излучения. Приращение дозы в единицу времени называется мощностью дозы, которая характеризует скорость накопления дозы ионизирующего излучения. Допускается использование различных специальных единиц (например, Гр/ч, Гр/мин, Гр/с и др.). Доза фотонного излучения (рентгеновского и гамма-излучения) зависит от атомного номера элементов, входящих в состав вещества. При одинаковых условиях облучения в тяжелых веществах она, как правило, выше, чем в легких. Например, в одном и том же поле рентгеновского излучения поглощенная доза в костях больше, чем в мягких тканях. В поле нейтронного излучения главным фактором, определяющим формирование поглощенной дозы, является ядерный состав вещества, а не атомный номер элементов, входящих в состав биологической ткани. Для мягких тканей поглощенная доза нейтронного излучения во многом определяется взаимодействием нейтронов с ядрами углерода, водорода, кислорода и азота. Поглощенная доза в биологическом веществе зависит от энергии нейтронов, так как нейтроны различной энергии избирательно взаимодействуют с ядрами вещества. При этом могут возникать заряженные частицы, у-излуче-ние, а также образовываться радиоактивные ядра, которые сами становятся источниками ионизирующего излучения.
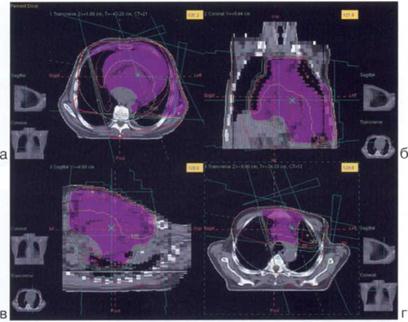
Разные виды ионизирующего излучения при одной и той же поглощенной дозе оказывают на ткани живого организма различный биологический эффект, что определяется их относительной биологической эффективностью – ОБЭ Дозное поле — это пространственное распределение поглощенной дозы (или ее мощности) в облучаемой части тела больного, тканеэквивалентной среде или дозиметрическом фантоме, моделирующем тело больного по физическим эффектам взаимодействия излучения с веществом, форме и размерам органов и тканей и их анатомическим взаимоотношениям. Информацию о дозном поле представляют в виде кривых, соединяющих точки одинаковых значений (абсолютных или относительных) поглощенной дозы. Такие кривые называют изодозами, а их семейства — картами изодоз. За условную единицу (или 100%) можно принять поглощенную дозу в любой точке дозного поля, в частности максимальную поглощенную дозу, которая должна соответствовать подлежащей облучению мишени (то есть области, охватывающей клинически выявленную опухоль и предполагаемую зону ее распространения) Центральный рак легкого. Конформное облучение с двух параллельных полей клиновидными фильтрами. Распределение доз: схемы поперечного сечения разного уровня. а) схема фронтального сечения; б) схема саггитального сечения
Физическая характеристика поля облучения характеризуется различными параметрами. Число частиц, проникших вереду, называют флюенсом. Сумма всех проникших частиц и рассеянных в данной среде частиц составляет поток ионизирующих частиц, а отношение потока к площади составляет плотность потока. Под интенсивностью излучения, или плотностью потока энергии, понимают отношение потока энергии к площади объекта. Интенсивность излучения зависит от плотности потока частиц. Кроме линейной передачи энергии (ЛПЭ), характеризующей средние энергетические потери частиц (фотонов), определяют линейную плотность ионизации (ЛПИ), количество пар ионов на единицу длины пробега (трека) частицы или фотона.
Формирование дозного поля зависит от вида и источника излучения. При формировании дозного поля при фотонном излучении учитывают, что интенсивность фотонного излучения точечного источника падает в среде обратно пропорционально квадрату расстояния до источника. При дозиметрическом планировании используют понятие средней энергии ионизации, которая включает в себя энергию непосредственной ионизации и энергию возбуждения атомов, приводящую ко вторичному излучению, также вызывающему ионизацию. Для фотонного излучения средняя энергия ионизации равна средней энергии ионообразования электронов, освобожденных фотонами.
Дозное распределение пучка у-излучения неравномерно. Участок 100% изодозы имеет сравнительно небольшую ширину, и далее относительная величина дозы падает по кривой достаточно круто. Размер поля облучения определяется по ширине 50 % дозы. При формировании дозного поля тормозного излучения имеется крутой спад дозы на границе поля, определяемый малым размером фокусного пятна. Это приводит к тому, что ширина 100% изодозы близка к ширине 50 % изодозы, которая определяет дозиметрическую величину размера поля облучения. Таким образом, в формировании дозного распределения при облучении пучком тормозного излучения имеются преимущества перед пучком у-излучения, так как уменьшаются дозы облучения здоровых органов и тканей вблизи патологического очага
Глубина расположения 100 %, 80 % и 50 % изодоз при наиболее Дата добавления: 2014-12-12 | Просмотры: 695 | Нарушение авторских прав |
 Источником рентгеновского излучения для целей лучевой терапии является рентгеновская трубка рентгенотерапевтических аппаратов, которые в зависимости от уровня генерируемой энергии делятся на близкофокусные и дистанционные. Рентгеновское излучение близкофокусных рентгенотерапевтических аппаратов генерируется при анодном напряжении менее 100 кВ, дистанционных — до 250 кВ.
Источником рентгеновского излучения для целей лучевой терапии является рентгеновская трубка рентгенотерапевтических аппаратов, которые в зависимости от уровня генерируемой энергии делятся на близкофокусные и дистанционные. Рентгеновское излучение близкофокусных рентгенотерапевтических аппаратов генерируется при анодном напряжении менее 100 кВ, дистанционных — до 250 кВ.