|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Нарушение автоматизмаАвтоматизм — способность ткани сердца спонтанно генерировать потенциал действия (ПД). Нарушение автоматизма: 1. Нарушения нормального автоматизма – нарушение автоматизма СА-узла. 2. Появление аномального автоматизма – автоматизма, который обусловлен активацией пейсмекерной функции в клетках проводящей системы, не являющихся в норме водителями ритма (АВ-узел, ножки пучка Гиса, волокна Пуркинье). Клетки сердца по своим электрофизиологическим свойствам подразделяются на: клетки рабочего миокарда и клетки пейсмекера. Пейсмекер (от англ. pacemaker – водитель ритма) — клетки сердца, способные к спонтанной генерации импульса возбуждения. Наибольшей способностью к автоматии обладает синоатриальный узел (СА-узел). В условиях физиологической нормы в нем возникает возбуждение, которое благодаря проводящей системе сердца, последовательно охватывает предсердия и желудочки. Поэтому СА-узел называют водителем ритма сердца (I порядка), или пейсмекером. Пейсмекер может генерировать большую частоту возбуждений, чем другие участки проводящей системы. Он подавляет автоматию остальных волокон этой системы. Если СА-узел блокирован по каким-то причинам, то водителем ритма становится атриовентрикулярный узел (АВ-узел), который генерирует частоту возбуждений 40-50 в мин. Если водителем ритма станет пучок Гиса, то максимум частоты его возбуждений составляет 30-40 в мин. При такой частоте сокращений сердца даже в состоянии покоя у человека будут проявляться симптомы недостаточности кровообращения. Волокна Пуркинье могут генерировать до 20 импульсов в мин. Клетки пейсмекера обладают автоматизмом, то есть способностью к спонтанной деполяризации (рис. 1). Автоматизм клеток пейсмекера обусловлен особенностями проницаемости мембраны этих клеток и поляризации: 1. низким уровнем трансмембранного потенциала (МП= -60 мВ), 2. наличием спонтанной деполяризации.
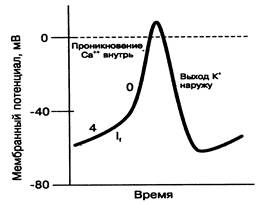
Рис. 1. Потенциал действия пейсмекерной клетки.
Эти свойства во многом определяются особенностями ионных каналов в мембранах клеток пейсмекера. Фаза 4 потенциала действия пейсмекерной клетки характеризуется постепенной, спонтанной деполяризацией (медленная спонтанная диастолическая деполяризация), вызванной пейсмекерным током (If). Пейсмекерный ток переносится преимущественно ионами Na+. Ионные каналы, через которые проходит пейсмекерный ток, отличаются от быстрых Na+ каналов, ответственных за фазу 0 деполяризации клеток рабочего миокарда. Пейсмекерные каналы открываются в период реполяризации клетки, когда МП достигает своего максимального отрицательного значения. Ток ионов Na+ через пейсмекерные каналы способствует тому, что мембранный потенциал (МП) во время фазы 4 становится все менее отрицательным и, при достижении порогового потенциала (~ -40 мВ), происходит возбуждение ПД (фаза 0). Фаза 0 пейсмекерной клетки наступает менее быстро, чем в кардиомиоцитах, так как она обусловлена током ионов Са2+ внутрь клетки через относительно медленные кальциевые каналы. Реполяризация пейсмекерных клеток развивается так же, как и клеток рабочего миокарда – происходит инактивация Са2+-каналов, активация К+-каналов, усиленный выход ионов К+ из клетки. Скорость медленной спонтанной диастолической деполяризации во многом определяет частоту генерации импульсов клетками-пейсмекерами: чем больше скорость спонтанной диастолической деполяризации, тем выше скорость генерации импульсов. Симпатические волокна выделяют норадреналин, который через β-адренорецепторы и систему посредников увеличивает содержания в клетке цАМФ, что приводит к возрастанию скорости диастолической деполяризации и тахикардии. Это влияние опосредуется через увеличение проницаемости мембран кардиомиоцитов для ионов Na+ и Са2+. Парасимпатические волокна посредством медиатора ацетилхолина и М2-рецепторы сердца оказывают обратный эффект – приводят к уменьшению скорости диастолической деполяризации, вызывают брадикардию. Под влиянием ацетилхолина увеличивается проницаемость мембран кардиомиоцитов для ионов К+ и снижается проницаемость их для Са2+. Происходит усиление выхода К+ из клеток и снижение входа Са2+. Это ведет к гиперполяризации мембран и снижению их возбудимости.
Нарушения нормального автоматизма. Известно, что в основе автоматизма лежит медленная спонтанная диастолическая деполяризация, постепенно понижающая МП до порогового уровня, с которого начинается быстрая деполяризация мембраны (фаза 0 ПД). На продолжительность спонтанной деполяризации и, следовательно, на частоту сердечной деятельности оказывают влияние следующие механизмы. 1. Скорость спонтанной диастолической деполяризации. При ее возрастании пороговый потенциал возбуждения достигается быстрее и происходит учащение синусового ритма. Замедление спонтанной диастолической деполяризации, ведет к замедлению синусового ритма. 2. Изменение величины мембранного потенциала покоя СА-узла. Когда мембранный потенциал становится более отрицательным (при гиперполяризации клеточной мембраны, например при действии ацетилхолина), требуется больше времени для достижения порогового потенциала возбуждения, если, разумеется, скорость спонтанной диастолической деполяризации остается неизменной. Следствием такого сдвига будет уменьшение частоты сердечных сокращений (ЧСС). При увеличении мембранного потенциала покоя, когда он становится менее отрицательным, частота сердечных сокращений, напротив, возрастает. 3. Изменение порогового потенциала возбуждения. Его уменьшение (более отрицательный) способствует учащению синусового ритма, а увеличение (менее отрицательный) - брадикардии. Величина порогового потенциала возбуждения кардиомиоцитов определяется свойствами Na+- каналов, а клеток проводящей системы – Ca2+- каналов. В связи с этим следует напомнить, что в основе фазы быстрой деполяризации в клетках рабочего миокарда лежит активация быстрых Na+- каналов, а в клетках специализированной ткани сердца - Ca2+- каналов. 4. Различные комбинации 3-х основных электрофизиологических механизмов, регулирующих автоматизм СА-узла. Аномальный автоматизм (эктопический автоматизм)– это появление пейсмекерной активности в клетках сердца, не являющихся водителями сердечного ритма. В норме эктопическая активность подавляется импульсами, поступающими из СА-узла, но при блокаде проведения импульса по предсердиям главным водителем ритма сердца может стать АВ-узел. Способность к спонтанной деполяризации клеток АВ-узла менее выражена, чем в клетках СА-узла, поэтому в условиях поперечной блокады обычно развивается брадикардия. Еще менее выражена способность к автоматизму у волокон Пуркинье. Однако эти волокна, как и другие клетки проводящей системы, более устойчивы к гипоксии, чем сократительные кардиомиоциты, в связи с чем, не всегда погибают в зоне ишемии. Электрофизиологические свойства ишемизированных волокон Пуркинье существенно отличаются от параметров интактных волокон тем, что у них появляется пейсмекерная активность, а способность к проведению импульса существенно снижается. Кроме того, пейсмекерная активность, возникающая в волокнах Пуркинье, в условиях патологии (например, при ишемии) перестает подавляться импульсами, поступающими из СА-узла, и может быть причиной возникновения желудочковых экстрасистол. Дата добавления: 2016-03-26 | Просмотры: 721 | Нарушение авторских прав |