|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Железодефицитная анемия. Практически до 90% анемий у детей и женщин относятся к дефицитным, причём значительную часть из них составляют железодефицитныеДЕФИЦИТНЫЕ АНЕМИИ Практически до 90% анемий у детей и женщин относятся к дефицитным, причём значительную часть из них составляют железодефицитные. Дефицит железа в той или иной степени присутствует у 30-40% жителей планеты, причём сидеропения развивается в 2 раза чаще, чем анемия, и её выявляют у всех беременных в последнем триместре. В России железодефицитной анемией страдают до 40% детей первых 3 лет жизни, до 1/3 подростков и 44% женщин фертильного возраста. В группу высокого риска входят дети от матерей с неблагополучно протекавшей и/или многоплодной беременностью, недоношенные, дети в возрасте 6-12 мес, крупные и интенсивно растущие дети в любом возрасте, дети, получающие нерациональное и несбалансированное питание, страдающие дис- бактериозом, мальабсорбцией и хроническими воспалительными заболеваниями кишечника, а также девочки-подростки с гиперполименореей. Значение имеют не только возраст и пол, но и уровень жизни в стране. Этиология и патогенез Этиология дефицитных анемий отражена в их названии. Они обычно возникают в периоды бурного роста организма (первые годы жизни, пубертатный период), когда высокие потребности организма в веществах, необходимых для кроветворения (полноценный белок, витамины, микроэлементы, железо) не покрываются пищей. Кроме того, усвоение этих веществ может быть нарушено в силу незрелости ферментных и транспортных систем организма ребёнка. Патогенез зависит от преобладания недостаточности того или иного фактора, необходимого для нормального кроветворения. При преимущественном дефиците белка снижаются продукция эритропоэтина почками, активность ферментов кишечника, всасывание железа и ви- таминов. Вследствие этого нарушается гемопоэз. При недостаточном поступлении витаминов в организм (в первую очередь витаминов В6 и В12) замедляется как включение железа в гем (витамин В6), так и нормальный процесс созревания клеток эритроидного ряда из-за дефекта синтеза ДНК (витамин В12). Однако белково- и витаминодефицитные анемии возникают довольно редко, обычно при грубом нарушении вскармливания. Гораздо чаще развивается дефицит железа, тяжело отражающийся на процессе кроветворения и состоянии всего организма. Это связано с особенностями метаболизма, распределения и усвоения железа, высокими потребностями растущего организма в этом элементе и низким его содержанием в пище. Железодефицитная анемия ОБМЕН ЖЕЛЕЗА В ОРГАНИЗМЕ РЕБЁНКА Плод получает железо от матери через плаценту в течение всей беременности, наиболее интенсивно с 28-32-й недели. В организме доношенного ребёнка содержится около 300-400 мг железа, недоношен- ного - всего 100-200 мг. После рождения запасы железа, полученные от матери, пополняются за счёт утилизации Hb при распаде «лишних» эритроцитов, содержащих HbF. Неонатальное (материнское и эритроцитарное) железо расходуется на синтез Hb, миоглобина, железосодержащих ферментов, необходимых для поддержания нормального обмена веществ и гомеостаза, а также на компенсацию естественных потерь (с калом, мочой, потом), на регенерацию клеток кожи, слизистых оболочек и т.д. Кроме того, ребёнку необходимо создавать резервы железа, т.е. баланс железа должен быть положительным. Потребности доношенного ребёнка до 3-4 мес удовлетворяются за счёт эндогенного железа и молока матери, содержащего железо в среднем в количестве 0,5 мг/л, причём до 50% его (0,25 мг) всасывается в кишечнике с помощью специального белка лактоферрина. Однако уже к 5-6 мес у доношенного и к 3-4 мес у недоношенного ребёнка потребность в железе, составляющая 1 мг/сут, удовлетворяется за счёт указанных источников только на 1/4. Искусственное вскармливание коровьим молоком, употребление сыра, яиц, чая, оксалатов, фосфатов замедляет всасывание железа. Способствуют всасыванию железа аскорбиновая, янтарная и другие органические кислоты, фруктоза, сорбит, животный белок. Всосавшееся в тонкой кишке железо с помощью транспортного белка трансферрина переносится в красный костный мозг и тканевые депо. Различают гемовое (80% железа в организме) и негемовое железо (табл. 8-1). К негемовому железу, кроме указанного в таблице, относят также трансферрин (основной транспортный белок), ферритин и гемосидерин (белки, служащие резервным источником железа в организме). Железо участвует во многих обменных процессах. Без него невозможны нормальные рост и развитие ребёнка. Дефицит железа в организме (сидеропения) проходит три стадии. 1. Прелатентная - недостаточное содержание железа в тканях, концентрация Hb и сывороточного железа не изменены. 2. Латентная - концентрация Hb нормальная, но сывороточного железа снижена. 3. Железодефицитная анемия - изменены все показатели красной крови. Таблица 8-1. Распределение и функции железа в организме
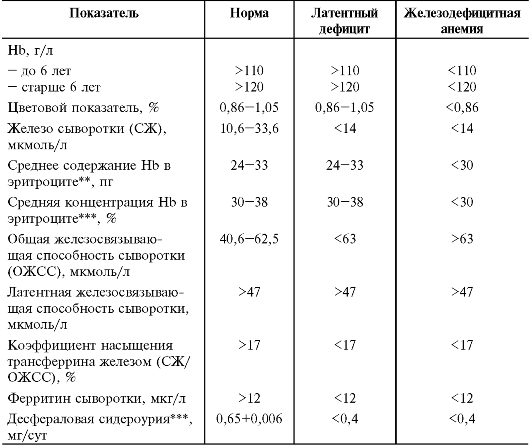
КЛИНИЧЕСКАЯ КАРТИНА ЖЕЛЕЗОДЕФИЦИТНЫХ СОСТОЯНИЙ Клиническая картина железодефицитных состояний (сидеропений) неспецифична и включает несколько синдромов. • Астено-вегетативный синдром - следствие нарушения функций головного мозга. Маленькие дети с железодефицитной анемией отстают в психомоторном развитии. Они плаксивы, раздражительны, капризны, плохо контактируют со сверстниками. У детей старшего возраста страдает интеллектуальное развитие: снижены память, внимание, интерес к учёбе. Появляются признаки СВД. Возможны мышечные боли и гипотония (в частности - мочевого пузыря), энурез. • Эпителиальный синдром включает дистрофию и атрофию барьерных тканей (слизистых оболочек, кожи и её производных - ногтей, волос). К трофическим нарушениям легко присоединяются воспалительные изменения. В результате снижается аппетит, возникают извращение вкуса и обоняния (pica chlorotica), дисфагия, диспептические расстройства, нарушения процессов всасывания в кишечнике, скрытые кишечные кровотечения. Бледность кожи и конъюнктивы выявляют только при значительном снижении концентрации Hb. • Иммунодефицитный синдром проявляется частыми ОРВИ и ОКИ. Около 70% часто болеющих детей страдают сидеропенией. У них снижен как неспецифический (лизоцим, пропердин и т.д.), так и специфический иммунитет. Показано, что в отсутствие железа IgA теряет свою бактерицидную активность. • Сердечно-сосудистый синдром наблюдают при тяжёлой железодефицитной анемии. У детей развиваются повышенная утомляемость, низкое АД, тахикардия, снижение тонуса сердечной мышцы, приглушение тонов, функциональный, довольно грубый систолический шум, хорошо выслушиваемый на сосудах («шум волчка») и связанный с гидремией. Возможны головокружения. • Гепатолиенальный синдром возникает редко, обычно при тяжёлой анемии и сочетании рахита и анемии. Лабораторные критерии сидеропений представлены в табл. 8-2. В последнее время стали обращать внимание на то, что дефицит железа увеличивает абсорбцию свинца в ЖКТ. Это особенно важно для детей, живущих в больших городах, вблизи магистральных дорог. К проявлениям сидеропении в таком случае может присоединиться (особенно у маленьких детей) свинцовая интоксикация, приводящая к тяжёлым психическим и неврологическим расстройствам, нарушениям функций почек и кроветворения. Анемия при этом становится рефрактерной к лечению препаратами железа. Таблица 8-2. Лабораторные критерии железодефицитньгх состояний у детей*
* По Коровиной Н.А. и соавт., 1999. ** Показатели, определяемые автоматически на современных анализаторах красной крови. *** Определяют содержание в суточной моче железа после введения дефероксамина («Десферала») внутримышечно из расчёта 10 мг/кг. ДИАГНОСТИКА ЖЕЛЕЗОДЕФИЦИТНЫХ СОСТОЯНИЙДиагноз железодефицитной анемии и латентного дефицита железа основывают на изложенных выше лабораторных критериях. Основной показатель - содержание ферритина в сыворотке крови. При невозможности получить все указанные данные можно ориентироваться на следующие показатели, доступные в любом медицинском учрежде- нии. • Концентрация Hb. • Цветовой показатель рассчитывают следующим образом: цветовой показатель = [(концентрация Hb, г/л)х3]+(три первые цифры количества эритроцитов без запятой). В норме составляет 0,85-1,05. • Морфология эритроцитов в мазке периферической крови. • Результат от лечения препаратами железа при приёме внутрь: через 10-14 дней концентрация Hb повышается ежедневно на 1-4 г/л, содержание ретикулоцитов увеличивается до 3-4% (ретикулоцитарный криз). КЛИНИЧЕСКИЕ ФОРМЫ ПРЕИМУЩЕСТВЕННО ЖЕЛЕЗОДЕФИЦИТНЫХ АНЕМИЙ Ранняя анемия недоношенных Ранняя анемия недоношенных имеет сложный патогенез и развивается на 1-2-м месяце жизни более чем у половины недоношенных и изредка у доношенных детей («физиологическая» доброкачественная анемия), особенно при неблагоприятном преморбидном фоне. При объективном обследовании отмечают только бледность (при снижении концентрации Hb до 80 г/л). При исследовании периферической крови обнаруживают нормоили гиперхромную норморегенераторную анемию, часто достигающую тяжёлой степени. Основными причинами развития ранней анемии считают усиленный «физиологический» гемолиз эритроцитов, содержащих HbF, недостаточную функциональную и морфологическую зрелость красного костного мозга, снижение продукции тканевых эритропоэтинов вследствие гипероксии, имевшей место при рождении ребёнка. Большое значение имеет также дефицит многих необходимых для кроветворения веществ, откладывающихся в депо только в последние 2 мес беременности (белок, витамины C, E, группы B, медь, кобальт) и обеспечивающих всасывание, транспорт, обмен и фиксацию железа в молекуле гема, а также стабильность оболочек и мембран эритроцитов. Присутствует и дефицит железа в депо, временно компенсированный текущим гемолизом, но чётко выявляемый путём обнаружения микроцитоза и гипохромии части эритроцитов, снижения концентрации сывороточного железа и количества сидероцитов в пунктате красного костного мозга. Как только неонатальные запасы железа истощаются, ранняя анемия переходит в позднюю анемию недоношенных. Лечение ранней анемии вызывает затруднения. Ранее по жизненным показаниям переливали эритроцитарную массу, сейчас с успе- хом применяют эпоэтин бета (эритропоэтин человека рекомбинантный). Назначают 10 инъекций в дозе 200 ЕД/кг п/к 3 раза в неделю. Одновременно назначают препараты железа (2 мг элементарного железа в сутки), фолиевую кислоту (0,001 г/сут) и витамин E (25 мг/сут в течение 2-3 мес). Поздняя анемия недоношенных Поздняя анемия недоношенных (конституциональная) развивается на 3-4-м месяце жизни в результате истощения неонатальных запасов железа в депо. Клинические проявления обычно незначительны, лабораторные данные свидетельствуют о преимущественном дефиците железа. Алиментарная и инфекционная анемии Алиментарная и инфекционная анемии развиваются во втором полугодии жизни у доношенных детей. В происхождении алиментарной анемии играют роль нарушения вскармливания, одновременно вызы- вающие и дистрофию. Инфекционные заболевания, чаще всего ОРВИ и отиты, обычно способствуют более тяжёлому течению алиментарной анемии. Клинические и лабораторные проявления характерны для преобладания дефицита железа. Хлороз Хлороз - редкое заболевание девочек в период полового созревания. Развивается на фоне нарушения режима и эндокринной дисфункции. Проявляется слабостью, повышенной утомляемостью, анорексией, извращением вкуса, головокружениями, иногда обмороками, сердцебиением, болями в эпигастральной области, тошнотой, рвотой, запорами. Характерны «алебастровая», в некоторых случаях с зеленоватым оттенком, бледность кожи, нарушения менструального цикла (олигоили аменорея). Выздоровление обычно самопроизвольное, возможны рецидивы. Лабораторные исследования указывают на преимущественный дефицит железа. ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ДЕФИЦИТНЫХ АНЕМИЙ Дифференциальную диагностику железодефицитной анемии проводят с другими дефицитными анемиями, талассемией и сидеробластными анемиями - свинцовой и пиридоксинзависимой, при которых эритропоэз нарушен в результате нарушения включения железа в гем. Гипохромия эритроцитов в последнем случае сочетается с повышением концентрации сывороточного железа. • Клинические проявления приобретённой сидеробластной анемии, вызванной свинцовой интоксикацией, более манифестны, чем при железодефицитной анемии: схваткообразные боли в животе, выраженные диспептические проявления, бледность с землистым оттенком, психические и неврологические расстройства. В анализах крови - базофильная зернистость, гипохромия эритроцитов, повышение концентрации сывороточного железа. В анализах мочи определяют аминолевулиновую кислоту. • При наследственной пиридоксинзависимой сидеробластной анемии синтез гема нарушается на последнем этапе. В гипохромных эритроцитах накапливается свободный протопорфирин, концентрация сывороточного железа повышена, в красном костном мозге много сидеробластов. • Белководефицитная анемия сопровождается более выраженной бледностью и дисхромией кожи и волос, блефаритами, пастозностью тканей или отёками, анорексией, рвотой, диареей. Концентрация Hb снижена до 40-90 г/л, цветовой показатель в пределах нормальных значений, выражены анизо- и пойкилоцитоз. • Витаминодефицитная анемия (дефицит витаминов В12, С) проявляется астенизацией, парестезиями, бледностью с лимонно-жёлтым оттенком, субиктеричностью склер, глосситом, афтозным стоматитом, умеренной гепатомегалией. Концентрация Hb снижена, как и содержание эритроцитов, нормо- и гиперхромных, цветовой показатель повышен (более 1,0). Появляются макро-, пойкило- и анизоцитоз, тельца Жолли, кольца Кэбота, мегалобласты, гигантские метамиелоциты. В пунктате красного костного мозга выявляют мегалобластный тип кроветворения. ЛЕЧЕНИЕ Лечение железодефицитной анемии проводят в три этапа (табл. 8-3). Обязательная и наиболее важная составная часть каждого из этапов - приём препаратов железа. Препараты железа в подавляющем большинстве случаев принимают перорально. При лечении железоде- фицитной анемии и латентного дефицита железа, помимо препаратов железа, необходимо соблюдение режима и диеты, сбалансированной по основным ингредиентам; нормализация всасывания железа при его нарушении (например, сочетанное лечение ферментными препаратами при синдроме мальабсорбции), дозированная физическая активность. Таблица 8-3. Этапы лечения железодефицитной анемии*
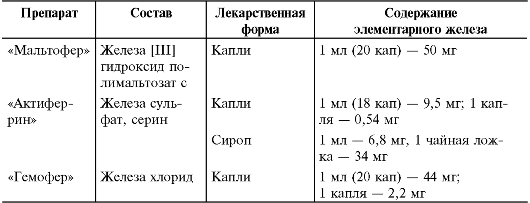
* По Аркадьевой Г.В., 1999. Лечение пероральными препаратами железа К наиболее часто применяемым соединениям железа относят железа [III] гидроксид полимальтозат и соли двухвалентного железа - сульфат, фумарат, хлорид и глюконат. Для улучшения всасывания соли двухвалентного железа комбинируют с органическими кислотами, аминокислотами и другими соединениями. • Детям раннего возраста показаны жидкие лекарственные формы, позволяющие более точно дозировать железо (табл. 8-4). Таблица 8-4. Препараты железа, применяемые у детей раннего возраста
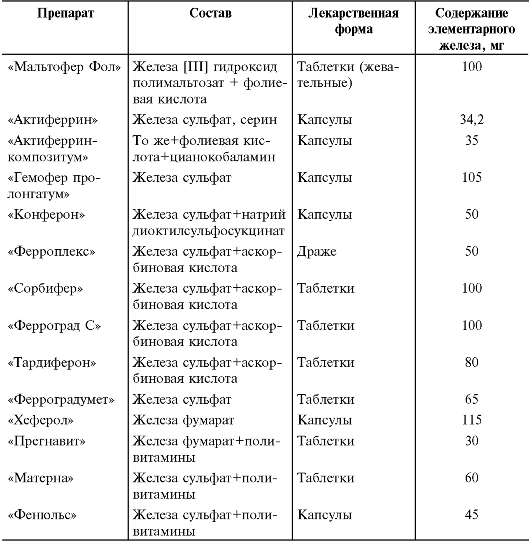
• Детям старшего возраста и подросткам назначают таблетки и капсулы, содержащие железо. В последнее время в основном с профилактической целью применяют комбинированные препараты, содержащие кроме железа витамины и другие микроэлементы (табл. 8-5). Препаратом выбора служит мальтофер, содержащий железо в неионной форме, не вызывающий побочных действий, обладающий приятным вкусом, принимаемый сразу после или во время еды. Его можно добавлять в любые соки и блюда. Остальные препараты принимают между при- ёмами пищи, запивают фруктовыми соками (лучше цитрусовыми). Одновременно принимают возрастную дозу аскорбиновой кислоты. Таблица 8-5. Наиболее часто применяемые препараты железа*
* По Аркадьевой Г.В., 1999. Суточную дозу всех препаратов распределяют на три приёма. В начале лечения в течение нескольких дней препараты назначают в половинной дозе для уточнения их индивидуальной переносимости. При отсутствии диспептических явлений и других побочных эффектов переходят к возрастной дозе. Комбинированные препараты, назначаемые с профилактической целью, принимают 1 раз в сутки. Препараты железа для парентерального введения Парентерально препараты железа вводят только при наличии соответствующих показаний. • Состояния после операций на ЖКТ. • Синдром нарушенного всасывания в тонкой кишке. • Хронический энтероколит и неспецифический язвенный колит. • Непереносимость железа при приёме внутрь. Основной препарат для парентерального введения - железа (III) гидроксид полиизомальтозат («Феррум лек»). Средние суточные дозы представлены в табл. 8-6. Таблица 8-6. Средние суточные дозы препаратов железа для парентерального введения (расчёт по элементарному железу)*
* По Коровиной Н.А. и соавт., 1999. Расчёт курсовой дозы элементарного железа для парентерального введения проводят по формуле: Количество элементарного железа = М х (78 - 0,35 х Hb), где М - масса тела пациента, кг; Hb - концентрация Hb, г/л. Курсовую дозу препарата для парентерального введения вычисляют по формуле: Количество препарата на курс = КДЖ/СЖП, где КДЖ - курсовая доза железа, мг; СЖП - содержание железа в мг в 1 мл препарата. При парентеральном введении препаратов железа нередко возникают побочные эффекты: диспептические расстройства, аллергические реакции (вплоть до развития анафилактического шока), гемосидероз. Переливание эритроцитарной массы проводят только при снижении концентрации Hb менее 60 г/л. ПРОФИЛАКТИКА Антенатальная профилактика. В течение всей беременности женщине следует принимать пролонгированные или комплексные препараты железа с поливитаминами («Тардиферон», «Ферроградумет», «Матерна» и др.). Приём этих препаратов необходимо продолжать и во время кормления ребёнка грудью. Кроме того, имеют значение предупреждение и лечение невынашивания и гестозов, полноценное питание, дозированная физическая нагрузка. Дата добавления: 2016-03-26 | Просмотры: 624 | Нарушение авторских прав |