 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Механизмы, пути и факторы передачи инфекции.
Персистенция – длительное проживание микроба в МакроО, т.е. формирование хронического инфицирования микробом и из хозяина не выделяется. Суперинфекции. От смешанных инфекций следует отличать вторичные инфекции (суперинфекции), возникающие на фоне уже имеющегося заболевания. Реинфекция — случай повторного заражения одним и тем же возбудителем. Реинфекции не следует рассматривать как рецидивы. Рецидивы инфекции формируются под действием популяции инфекционного агента, уже циркулирующего в организме, а не в результате нового заражения.
1. Патогенность – видовой признак, определяющий способность конкретного возбудителя вызывать определенное заболевание со специфичностью патологического процесса. Патогенность обеспечивает: · Проникновение возбудителя в макроорганизм (инфективность); · Способность вызывать определенное заболевание с конкретным механизмом развития (патогенез).
2. Вирулентность – фенотипический признак, мера или степень патогенности. Особенности вирулентности: · Специфичность; · Органотропность – способность повреждать определенные органы; · Входные ворота – определяют локализацию возбудителя и механизм течения заболевания. Количественная характеристика вирулентности: · Инфицирующая доза – это минимальное количество возбудителя, способное вызвать данное заболевание. Чем выше инфицирующая доза, тем выше вирулентность. · Летальная доза (DL – dosis letalis) – это минимальное количество возбудителец, вызывающих гибель конкретного количества животных, взятых в эксперимент. · Смертельная доза - DCL (dosis certe letslis) - это количество микробово или токсина, вызывающих гибель 100% лабораторных животных. DCL 50 – количество патогенных микроорганизмов, способные гибель 50% экспериментально зараженных лабораторных животных.
Качественные критерии вирулентности: 1) Инфиктивность – способность бактерии вызывать инфекцию в организме в естественных условиях 2) Инвазивность – способность проникать в ткани и распространяться по организму при помощи ферментов, повышающих проницаемость ткани хозяина 3) Токсичность – способность бактерий выделять токсины. Факторы патогенности: 1. Адгезия и колонизация – это заселение зоны первичного инфицирования, т.е. входных ворот; 2. Инвазия и агрессия – это выход за пределы зоны первичного инфицирования, противостояние защитным силам макроорганизма и размножение в нем; 3. Токсигенность (экзотоксины) и токсичность (эндотоксины); 4. Персистенция – длительное проживание микроба в макроорганизме;
I. Факторы патогенности (классификация по О.В. Бухарину) I. Факторы адгезии и колонизации Механизмы адгезии
Неспецифический Специфическая Неспецифическая адгезия: 1. Электростатические взаимодействия; 2. Ван-дер-Ваальсовы вз-я 3. Броуновское движение 4. Гидрофобные вз-я Специфическая адгезия – происходит в результате молекулярных взаимодействий между адгезином микробной клетки и рецептором клетки хозяина. Адгезины – это поверхностные структуры микробных клеток. Гр+, их адгезины: белки и тейхоевые кислоты клеточной стенки; Гр-, их адгезины: белки наружной мембраны, липополисахарид (ЛПС) и пили. Капсульные: капсула. Микоплазмы: макромолекулы, входящие в состав выростов цитоплазматической мембраны (ЦПМ). Вирусы: специфические структуры белковой и полисахаридной природы. Колонизация зависит от: ü Дозы микробов; ü Наличия рецепторов на клетках макроорганизма; ü Тропности к тканям. ü II. Факторы агрессии и инвазии (факторы вирулентности): 1. Ферменты способствующие разрушение тканей:
2. Токсины:
III. Факторы персистенции: Ã Капсула – «экранирует» (защищает) клеточную стенку; Ã L-формы – микробы без клеточной стенки; Ã Антигенная мимикрия – сходство с АГ макроорганизма (антигены миокарда, почек и др.); Ã Секреторные факторы – факторы неспецифической защиты: · АЛА – антилизоцимная активность; · АКА – антикомплементарная активность; · АИА – антиинтерфероновая активность; Ã Внутриклеточный паразитизм. Ã Образование сообществ МО (Биопленки – сообщества, прикрепляемые к субстрату и ограничивающиеся микробным матриксом).
Иммунитет – это способ защиты организма от генетически чужеродных веществ – антигенов экзогенного и эндогенного происхождения, направленный на поддержание и сохранение гомеостаза, структурной и функциональной целостности организма, биологической (антигенной)индивидуальности каждого организма и вида в целом. Различают несколько основных видов иммунитета. Врожденный, иди видовой, иммунитет, он же наследственный, генетический, конституциональный — это выработанная в процессе филогенеза генетически закрепленная, передающаяся по наследству невосприимчивость данного вида и его индивидов к какому-либо антигену (или микроорганизму), обусловленная биологическими особенностями самого организма, свойствами данного антигена, а также особенностями их взаимодействия. Примером может служить невосприимчивость человека к некоторым возбудителям, в том числе к особо опасным для сельскохозяйственных животных (чума крупного рогатого скота, болезнь Ньюкасла, поражающая птиц, оспа лошадей и др.), нечувствительность человека к бактериофагам, поражающим клетки бактерий. К генетическому иммунитету можно также отнести отсутствие взаимных иммунных реакций на тканевые антигены у однояйцовых близнецов; различают чувствительность к одним и тем же антигенам у различных линий животных, т. е. животных с различным генотипом. Видовой иммунитет может быть абсолютным и относительным. Например, нечувствительные к столбнячному токсину лягушки могут реагировать на его введение, если повысить температуру их тела. Белые мыши, не чувствительные к какому-либо антигену, приобретают способность реагировать на него, если воздействовать на них иммунодепрессантами или удалить у них центральный орган иммунитета — тимус. Приобретенный иммунитет — это невосприимчивость к антигену чувствительного к нему организма человека, животных и пр., приобретаемая в процессе онтогенеза в результате естественной встречи с этим антигеном организма, например, при вакцинации. Примером естественного приобретенного иммунитета у человека может служить невосприимчивость к инфекции, возникающая после перенесенного заболевания, так называемый постинфекционный иммунитет (например, после брюшного тифа, дифтерии и других инфекций), а также «проиммуниция», т. е. приобретение невосприимчивости к ряду микроорганизмов, обитающих в окружающей среде и в организме человека и постепенно воздействующих на иммунную систему своими антигенами. В отличие от приобретенного иммунитета в результате перенесенного инфекционного заболевания или «скрытной» иммунизации, на практике широко используют преднамеренную иммунизацию антигенами для создания к ним невосприимчивости организма. С этой целью применяют вакцинацию, а также введение специфических иммуноглобулинов, сывороточных препаратов или иммунокомпетентных клеток. Приобретаемый при этом иммунитет называют поствакцинальным, и служит он для защиты от возбудителей инфекционных болезней, а также других чужеродных антигенов. Приобретенный иммунитет может быть активным и пассивным. Активный иммунитет обусловлен активной реакцией, активным вовлечением в процесс иммунной системы при встрече с данным антигеном (например, поствакцинальный, постинфекционный иммунитет), а пассивный иммунитет формируется за счет введения в организм уже готовых иммунореагентов, способных обеспечить защиту от антигена. К таким иммунореагентам относятся антитела, т. е. специфические иммуноглобулины и иммунные сыворотки, а также иммунные лимфоциты. Иммуноглобулины широко используют для пассивной иммунизации, а также для специфического лечения при многих инфекциях (дифтерия, ботулизм, бешенство, корь и др.). Пассивный иммунитет у новорожденных детей создается иммуноглобулинами при плацентарной внутриутробной передаче антител от матери ребенку ииграет существенную роль в защите от многих детских инфекций в первые месяцы жизни ребенка. Поскольку в формировании иммунитета принимают участие клетки иммунной системы и гуморальные факторы, принято активный иммунитет дифференцировать в зависимости от того, какой из компонентов иммунных реакций играет ведущую роль в формировании защиты от антигена. В связи с этим различают клеточный, гуморальный, клеточно-гуморальный и гуморально-клеточ-ный иммунитет. Примером клеточного иммунитета может служить противоопухолевый, а также трансплантационный иммунитет, когда ведущую роль в иммунитете играют цитотоксические Т-лимфоциты-киллеры; иммунитет при ток-синемических инфекциях (столбняк, ботулизм, дифтерия) обусловлен в основном антителами (антитоксинами); при туберкулезе ведущую роль играют иммунокомпетентные клетки (лимфоциты, фагоциты) с участием специфических антител; при некоторых вирусных инфекциях (натуральная оспа, корь и др.) роль в защите играют специфические антитела, а также клетки иммунной системы. В инфекционной и неинфекционной патологии и иммунологии для уточнения характера иммунитета в зависимости от природы и свойств антигена пользуются также такой терминологией: антитоксический, противовирусный, противогрибковый, противобактериальный, противопротозойный, трансплантационный, противоопухолевый и другие виды иммунитета. Наконец, иммунное состояние, т. е. активный иммунитет, может поддерживаться, сохраняться либо в отсутствие, либо только в присутствии антигена в организме. В первом случае антиген играет роль пускового фактора, а иммунитет называют стерильным. Во втором случае иммунитет трактуют как нестерильный. Примером стерильного иммунитета является поствакцинальный иммунитет при введении убитых вакцин, а нестерильного— иммунитет при туберкулезе, который сохраняется только в присутствии в организме микобактерий туберкулеза. Иммунитет (резистентность к антигену) может быть системным, т. е. генерализованным, и местным, при котором наблюдается более выраженная резистентность отдельных органов и тканей, например слизистых верхних дыхательных путей (поэтому иногда его называют мукозальным).
Факторы неспецифической защиты 1. Функциональная защита: ü Естественные барьеры (кожа, слизистые, сальные и потовые железы, пищеварительные ферменты); ü Нормальная микрофлора; ü Температурный гомеостаз; ü Лихорадка; ü Сосудистые реакции; ü Дезинтоксикационная функция печени; ü Выделительная функция почек и ЖКТ. 2. Гуморальная защита: · Ферменты: ü Лизоцим; ü Лактоферрин; ü Трансферрин. · Антимикробное действие: ü Система комплемента; ü Белки острой фазы; ü Лизины; ü Пропердин; ü Лейкин. · Ингибиторы: ü Интерфероны; ü Цитокины. 3. Клеточная защита (за счёт клеток): · Ареактивность клеток (отсутствие рецепторов для адгезии); · Система естественной цитотоксичности (NK-клетки); · Неспецифический фагоцитоз; · Доиммунное воспаление. Характеристика функциональной защиты · Большинство возбудителей не проникают во внутреннюю среду организма, благодаря физическим и биохимическим барьерам; · Неповрежденная кожа и слизистые – мощный внешний барьер. Характеристика клеточных механизмов 1883 г. – И.И. Мечников создал фагоцитарную теорию иммунитета. Все фагоцитарные клетки делятся: ü Микрофаги: · Базофилы; · Эозинофилы; · Нейтрофилы; ü Макрофаги: · Моноциты; · Мононуклеарные макрофаги. Основные функции макрофагов: ü Фагоцитоз; ü Презентация антигена Т-лимфоцитам; ü Секреция цитокинов. Фагоцитоз – поглощение фагоцитом корпускул, микробов или макромолекулярных комплексов. 4 стадии фагоцитоза: 1. Стадия хемотаксиса (приближения); · Силы физико-химических взаимодействий; · Передвижения фагоцита по градиенту концентрации; 2. Стадия адгезии (прилипания); · Опсонины (АТ, С3b, фибронектин, сурфактан) белки, обволакивающие микробы. Опсонины – обволакивающие белки делают поглощение более эффективным. · Силы физико-химических взаимодействий; 3. Стадия эндоцитоза (поглощения); · Образование фагосомы; · Слияние фагосомы с лизосомой; 4. Стадия внутриклеточного переваривания; Механизмы микробоцитности: · Кислороднезависимые (ферменты); · Кислородзависимые (радикалы). Механизмы незавершенного фагоцитоза: 1. Нарушение слияния фагосомы с лизосомой (микобактерии туберкулеза, простейшие, токсоплазмы). 2. Нарушение активности лизосомальных ферментов (гонококки, стрептококки гр.А, микобактерии, возбудители чумы). 3. Длительное персистирование возбудителя в цитоплазме фагоцита (риккетсии, хламидии). Характеристика гуморальной защиты Одним из важнейших гуморальных факторов является система комплемента. Комплемент – это сложный комплекс белков сыворотки крови, который находится в неактивном состоянии и, при наличии в организме чужеродного антигена, могут каскадно последовательно активироваться. Компоненты комплемента обозначают буквой «С» и цифрой (С1-С9). Комплемент образуется клетками печени и мононуклеарными фагоцитами. Функции комплемента: ü Лизис чужеродных клеток; ü Стимуляция фагоцитоза; ü Опсонизация чужеродных клеток, которые становятся более доступными для макрофагов, благодаря феномену иммунноприлипания; ü Стимуляция синтеза БАВ.
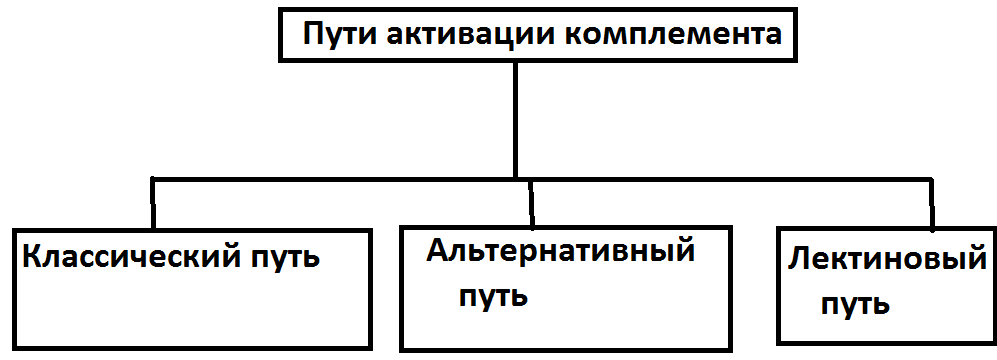
Классический путь: Активация комплемента начинается с присоединения фракции С1 к комплексу антиген-антитело. Комплементсвязывающей активностью обладают антитела классов G (IgG1, IgG3) и М (IgM). Дальнейшая активация комплемента приводит к образованию мембраноатакующего комплекса, который приводит к гибели клетки-мишени. Альтернативный путь: Происходит без участия антител и задолго до их появления. Этот путь характерен для защиты от Гр «-» микробов, иммунных комплексов, вирусов и др. Активация комплемента развивается в результате активации системы комплемента компонентами микробов или агрегатами белков (Аг). Кальций зависимый процесс. В начале активируется С3 и факторы В,D,P,H с образованием С3/С5-конвертаз (протеаз) альтернативного пути. В дальнейшем также образуется мембраноатакующий комплекс, который лизирует клетку-мишень.
Антигены обладают рядом характерных свойств: антигенностью, специфичностью и иммуногенностью. Антигенность. Под антигенностью понимают потенциальную способность молекулы антигена активировать компоненты иммунной системы и специфически взаимодействовать с факторами иммунитета (антитела, клон эффекторных лимфоцитов). Иными словами, антиген должен выступать специфическим раздражителем по отношению к иммунокомпетентным клеткам. При этом взаимодействие компоненты иммунной системы происходит не со всей молекулой одновременно, а только с ее небольшим участком, который получил название «антигенная детерминанта», или «эпитоп». Чужеродность является обязательным условием для реализации антигенности. По этому критерию система приобретенного иммунитета дифференцирует потенциально опасные объекты биологического мира, синтезированные с чужеродной генетической матрицы. Понятие «чужеродность» относительное, так как имму-нокомпетентные клетки не способны напрямую анализировать чужеродный генетический код. Они воспринимают лишь опосредованную информацию, которая, как в зеркале, отражена в молекулярной структуре вещества. Иммуногенность — потенциальная способность антигена вызывать по отношению к себе в макроорганизме специфическую защитную реакцию. Степень иммуногенности зависит от ряда факторов, которые можно объединить в три группы: 1. Молекулярные особенности антигена; 2. Клиренс антигена в организме; 3. Реактивность макроорганизма. К первой группе факторов отнесены природа, химический состав, молекулярный вес, структура и некоторые другие характеристики. Иммуногенность в значительной степени зависит от природы антигена. Важна также оптическая изомерия аминокислот, составляющих молекулу белка. Большое значение имеет размер и молекулярная масса антигена. На степень иммуногенности также оказывает влияние пространственная структура антигена. Оказалась также существенной стерическая стабильность молекулы антигена. Еще одним важным условием иммуногенности является растворимость антигена. Вторая группа факторов связана с динамикой поступления антигена в организм и его выведения. Так, хорошо известна зависимость иммуногенности антигена от способа его введения. На иммунный ответ влияет количество поступающего антигена: чем его больше, тем более выражен иммунный ответ. Третья группа объединяет факторы, определяющие зависимость иммуногенности от состояния макроорганизма. В этой связи на первый план выступают наследственные факторы. Специфичностью называют способность антигена индуцировать иммунный ответ к строго определенному эпитопу. Это свойство обусловлено особенностями формирования иммунного ответа — необходима комплементарность рецепторного аппарата иммунокомпетентных клеток к конкретной антигенной детерминанте. Поэтому специфичность антигена во многом определяется свойствами составляющих его эпитопов. Однако при этом следует учитывать условность границ эпитопов, их структурное разнообразие и гетерогенность клонов антигенреактивных лимфоцитовой специфичности. В результате этого организм на антигенное раздражение всегда отвечает поликлональными иммунным ответом. Антигены бактериальной клетки. В структуре бактериальной клетки различают жгутиковые, соматические, капсульные и некоторые другие антигены. Жгутиковые, или Н-антигены, локализуются в локомоторном аппарате бактерий — их жгутиках. Они представляют собой эпитопы сократительного белка флагеллина. При нагревании флагеллин денатурирует, и Н-антиген теряет свою специфичность. Фенол не действует на этот антиген. Соматический, или О-антиген, связан с клеточной стенкой бактерий. Его основу составляют ЛПС. О-антиген проявляет термостабильные свойства — он не разрушается при длительном кипячении. Однако соматический антиген подвержен действию альдегидов (например, формалина) и спиртов, которые нарушают его структуру. Капсулъные, или К-антигены, располагаются на поверхности клеточной стенки. Встречаются у бактерий, образующих капсулу. Как правило, К-антигены состоят из кислых полисахаридов (уроновые кислоты). В то же время у бациллы сибирской язвы этот антиген построен из полипептидных цепей. По чувствительности к нагреванию различают три типа К-антигена: А, В, и L. Наибольшая термостабильность характерна для типа А, он не денатурирует даже при длительном кипячении. Тип В выдерживает непродолжительное нагревание (около 1 часа) до 60 "С. Тип L быстро разрушается при этой температуре. Поэтому частичное удаление К-антигена возможно путем длительного кипячения бактериальной культуры. На поверхности возбудителя брюшного тифа и других энтеробактерий, которые обладают высокой вирулентностью, можно обнаружить особый вариант капсульного антигена. Он получил название антигена вирулентности, или Vi-антигена. Обнаружение этого антигена или специфичных к нему антител имеет большое диагностическое значение. Антигенными свойствами обладают также бактериальные белковые токсины, ферменты и некоторые другие белки, которые секретируются бактериями в окружающую среду (например, туберкулин). При взаимодействии со специфическими антителами токсины, ферменты и другие биологически активные молекулы бактериального происхождения теряют свою активность. Столбнячный, дифтерийный и ботулинический токсины относятся к числу сильных полноценных антигенов, поэтому их используют для получения анатоксинов для вакцинации людей. В антигенном составе некоторых бактерий выделяется группа антигенов с сильно выраженной иммуногенностью, чья биологическая активность играет ключевую роль в формировании патогенности возбудителя. Связывание таких антигенов специфическими антителами практически полностью инактивирует вирулентные свойства микроорганизма и обеспечивает иммунитет к нему. Описываемые антигены получили название протективных. Впервые протективный антиген был обнаружен в гнойном отделяемом карбункула, вызванного бациллой сибирской язвы. Это вещество является субъединицей белкового токсина, которая ответственна за активацию других, собственно вирулентных субъединиц — так называемого отечного и летального факторов. 38. Структура и функции иммунной системы. Кооперация иммунокомпетентных клеток. Формы иммунного ответа. Структура иммунной системы. Иммунная система представлена лимфоидной тканью. Это специализированная, анатомически обособленная ткань, разбросанная по всему организму в виде различных лимфоидных образований. К лимфоидной ткани относятся вилочковая, или зобная, железа, костный мозг, селезенка, лимфатические узлы (групповые лимфатические фолликулы, или пейеровы бляшки, миндалины, подмышечные, паховые и другие лимфатические образования, разбросанные по всему организму), а также циркулирующие в крови лимфоциты. Лимфоидная ткань состоит из ретикулярных клеток, составляющих остов ткани, и лимфоцитов, находящихся между этими клетками. Основными функциональными клетками иммунной системы являются лимфоциты, подразделяющиеся на Т- и В-лимфоциты и их субпопуляции. Общее число лимфоцитов в человеческом организме достигает 1012, а общая масса лимфоидной ткани составляет примерно 1—2 % от массы тела. Лимфоидные органы делят на центральные (первичные) и периферические (вторичные). Функции иммунной системы. Иммунная система выполняет функцию специфической зашиты от антигенов, представляющую собой лимфоидную ткань, способную комплексом клеточных и гуморальных реакций, осуществляемых с помощью набора иммунореагентов, нейтрализовать, обезвредить, удалить, разрушить генетически чужеродный антиген, попавший в организм извне или образовавшийся в самом организме. Специфическая функция иммунной системы в обезвреживании антигенов дополняется комплексом механизмов и реакций неспецифического характера, направленных на обеспечение резистентности организма к воздействию любых чужеродных веществ, в том числе и антигенов. Кооперация иммунокомпетентных клеток. Иммунная реакция организма может иметь различный характер, но всегда начинается с захвата антигена макрофагами крови и тканей или же со связывания со стромой лимфоидных органов. Нередко антиген адсорбируется также на клетках паренхиматозных органов. В макрофагах он может полностью разрушаться, но чаше подвергается лишь частичной деградации. В частности, большинство антигенов в лизосомах фагоцитов в печение часа подвергается ограниченной денатурации и протеолизу. Оставшиеся от них пептиды (как правило, два-три остатка аминокислот) комплексируются с экспрессированными на внешней мембране макрофагов молекулами МНС. Макрофаги и все другие вспомогательные клетки, несущие на внешней мембране антигены, называются антигенпрезентирующими, именно благодаря им Т- и В-лимфоциты, выполняя функцию презентации, позволяют быстро распознавать антиген. Иммунный ответ в виде антителообразования происходит при распознавании В-клетками антигена, который индуцирует их пролиферацию и дифференциацию в плазмоцит. Прямое воздействие на В-клетку без участия Т-клеток могут оказать только тимуснезависимые антигены. В этом случае В-клетки кооперируются с Т-хелперами и макрофагами. Кооперация на тимусза-висимый антиген начинается с его презентации на макрофаге Т-хелперу. В механизме этого распознавания ключевую роль имеют молекулы МНС, так как рецепторы Т-хелперов распознают номинальный антиген как комплекс в целом или же как модифицированные номинальным антигеном молекулы МНС, приобретшие чужеродность. Распознав антиген, Т-хелперы секретируют γ-интерферон, который активирует макрофаги и способствует уничтожению захваченных ими микроорганизмов. Хелперный эффект на В-клетки проявляется пролиферацией и дифференциацией их в плазмоциты. В распознавании антигена при клеточном характере иммунного ответа, кроме Т-хелперов, участвуют также Т-киллеры, которые обнаруживают антиген на тех антигенпрезентирующих клетках, где он комплексируется с молекулами МНС. Более того, Т-киллеры, обусловливающие цитолиз, способны распознавать не только трансформированный, но и нативный антиген. Приобретая способность вызывать цитолиз, Т-киллеры связываются с комплексом антиген + молекулы МНС класса 1 на клетках-мишенях; привлекают к месту соприкосновения с ними цитоплазма-тические гранулы; повреждают мембраны мишеней после экзоцитоза их содержимого. В результате продуцируемые Т-киллерами лимфотоксины вызывают гибель всех трансформированных клеток организма, причем особенно чувствительны к нему клетки, зараженные вирусом. При этом наряду с лимфотоксином активированные Т-киллеры синтезируют интерферон, который препятствует проникновению вирусов в окружающие клетки и индуцирует в клетках образование рецепторов лимфотоксина, тем самым повышая их чувствительность к литическому действию Т-киллеров. Кооперируясь в распознавании и элиминации антигенов, Т-хелперы и Т-киллеры не только активируют друг друга и своих предшественников, но и макрофагов. Те же, в свою очередь, стимулируют активность различных субпопуляций лимфоцитов. Регуляция клеточного иммунного ответа, как и гуморального, осуществляется Т-супрессорами, которые воздействуют на пролиферацию цитотоксических и антигенпрезентирующих клеток. Цитокины. Все процессы кооперативных взаимодействий им-мунокомпетентных клеток, независимо от характера иммунного ответа, обусловливаются особыми веществами с медиаторными свойствами, которые секретируются Т-хелперами, Т-киллерами, мононуклеарными фагоцитами и некоторыми другими клетками, участвующими в реализации клеточного иммунитета. Все их многообразие принято называть цитокинами. По структуре цитокины являются протеинами, а по эффекту действия — медиаторами. Вырабатываются они при иммунных реакциях и обладают потенциирующим и аддитивным действием; быстро синтезируясь, цитокины расходуются в короткие сроки. При угасании иммунной реакции синтез цитокинов прекращается.
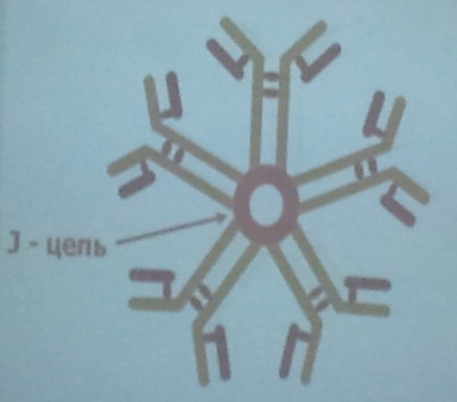
Иммуноглобулины по структуре, антигенным и иммунобиологическим свойствам разделяются на пять классов: IgM, IgG, IgA, IgE, IgD. Свойства IgM: · 6% от всех иммуноглобулинов Ig=1,0+/- 0,3 г/л; · Обнаруживается внутри сосудистого русла; · Является главным иммуноглобулином первичного иммунного ответа; · К этому классу относятся Ат к групповым Аг системы АВ0 крови; · Наличие IgM к Аг конкретного возбудителя указывает на острый инфекционный процесс; · Это основной класс, синтезируемый у новорожденных и младенцев. Свойства IgG: · 80% от всех иммуноглобулинов Ig=10+/-0,3 г/л; · Обнаруживается в крови, лимфе, внесосудистых жидкостях организма; · Единственный класс, который проникает через плаценту и обеспечивает пассивный иммунитет плода; · Участвует в связывании и активации комплемента по классическому пути; · Вырабатывается на поздних этапах иммунного ответа и является основным при вторичном иммунном ответе; · Высокие титры IgG указывают на то, что организм находится на стадии выздоровления или конкретное заболевание перенесено недавно. Свойства IgA:
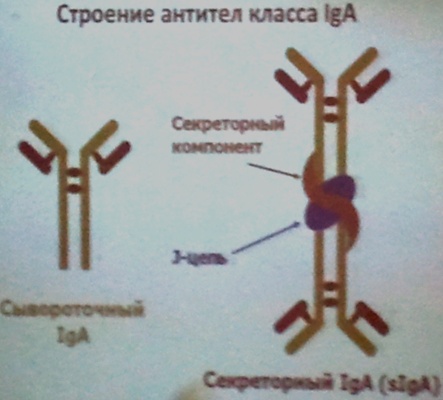
a) Сывороточный: · 13% от всех Ig = 1,9+/-0,1 г/л; · Защищает слизистые оболочки ЖКТ и респираторного тракта от проникновения микроорганизмов; · Нейтрализует энетеротоксин; · Активирует комплемент и фагоцитоз; · Участвует в местном иммунитете; · Играет основную роль в иммунной защите вскармливаемых грудью детей от кишечных инфекций. b) Секреторный находятся в секретах биологических жидкостей (слезы, молоко, секрет клеток кишечника).
· 1% от всех Ig менее 1 г/л; · Имеется на поверхности В-лимфоцитов; · Участвует в развитии местного иммунитета; · Участвует в дифференцировке В-клеток; · Обладает антивирусной активностью; · Участвует в аутоиммунных процессах. Строение IgE:
· IgE имеет существенное значение в развитии антигельминтозного иммунитета; · IgE защищает участки тела, подверженные травматическим повреждениям и микробной атаке. Инициирует острое воспаление; · Присутствует в малых количествах в сыворотке, связывается с тучными клетками; · При контакте с аллергеном образуется комплекс: Аг+IgE+тучная клетка; · Дегрануляция тучной клетки при образовании комплекса способствует появлению в крови БАВ (гистамин), которые и вызывают аллергические реакции. Иммунный ответ – это совокупность процессов в иммунной системе на введение антигена. Клетки, участвующие в формировании иммунного ответа (Т- и В-лимфоциты и макрофаги), называются ИММУНОКОМПЕТЕНТНЫМИ. Классификация иммунокомпетентных клеток: ü Антиген – презентирующие клетки – макрофаги, дендритные клетки1 и 2, В-лимфоциты; ü Регуляторные клетки – Т-индукторы, Т-хелперы, Т-регуляторы. ü Эффекторные клетки: - Плазматические клетки (образуются из В-лимфоцитов); - Цитотоксические Т-клетки с фенотипом СD8+ (Т-киллеры); - Эффекторные Т-клетки воспаления с фенотипом CD4+ (Т-ГЗТ (гиперчувствительность замедленного типа)); - Нейтрофилы, эозинофилы, базофилы, макрофаги, тучные клетки, NK-клетки. ü Клетки памяти – Т-клетки памяти с фенотипом CD8+ и CD4+. У всех иммунокомпетентных клеток есть антигены-маркеры – они обозначаются CD иди гликопротеиды. Иммунный ответ проходит в две фазы: - Непродуктивная – распознавание антигенов и взаимодействие иммунокомпетентных клеток; - Продуктивная - пролиферация клеток-эффекторов или продукция антител. Иммунный ответе может быть: - Первичным – при первой встрече с антигеном; - Вторичный – при повторной встрече с этим же антигеном. - Формы иммунного ответа: ü Гуморальный иммунный ответ; ü Клеточный иммунный ответ; ü Иммунологическая память; ü Иммунологическая толерантность; ü Аллергия. Основа гуморального иммунного ответа – активация В-лимфоцитов и их дифференцировка в антителообразующие плазматические клетки (Р). Основные этапы при гуморальном иммунном ответе: ü Распознавание антигена; ü Презентация антигена антиген-презентирующими клетками и представление его в комплексе с антигенами ГКГ 2; ü Активация Т-хелперов при участии интерлейкина-1; ü Образование клеток памяти; ü Созревание В-лимфоцитов в плазматические клетки, синтезирующие IgМ; ü Переключение плазматических клеток на синтез IgG и А с помощью Т-хелперов при участии интерлейкинов 4 и 5. Клеточный иммунный ответ Этапы: ü Распознавание антигена АПК; ü Презентация антигена антиген-презентирующими клетками и представление его Т-хелперам вместе с антигенами ГКГ 2 класса (помогает отличить своего от чужого); ü Активация Т-киллеров при участии интерлейкина 2; ü Образование клеток памяти; ü Разрушение инфицированной клетки активированными Т-киллерами при участии перфоринов, гранзимов.
Изучение молекулярных механизмов аллергии привело к созданию Джеллом и Кумбсом в 1968 г. новой классификации. В соответствии с ней различают четыре основных типа аллергии: анафилактический (I тип), цитотоксический (II тип), иммунокомплексный (III тип) и опосредованный клетками (IV тип). Первые три типа относятся к ГНТ, четвертый — к ГЗТ. Ведущая роль в запуске ГНТ играют антитела (IgE, G и М), а ГЗТ — лимфоидно-макрофагальная реакция. Аллергическая реакция I типа связана с биологическими эффектами IgE и G4, названных реагинами, которые обладают цитофильностью — сродством к тучным клеткам и базофилам. Эти клетки несут на поверхности высокоаффинный FcR, связывающий IgE и G4 и использующий их как ко-рецепторный фактор специфического взаимодействия с эпитопом аллергена. Связывание аллергена с рецепторным комплексом вызывает дегрануляцию базофила и тучной клетки — залповый выброс биологически активных соединений (гистамин, гепарин и др.), содержащихся в гранулах, в межклеточное пространство. В результате развиваются бронхоспазм, вазодилатация, отек и прочие симптомы, характерные для анафилаксии. Вырабатываемые цитокины стимулируют клеточное звено иммунитета: образование Т2-хелпера и эозинофилогенез. Цитотоксические антитела (IgG, IgM), направленные против поверхностных структур (антигенов) соматических клеток макроорганизма, связываются с клеточными мембранами клеток-мишеней и запускают различные механизмы антителозависимой цитотоксичности (аллергическая реакция II типа). Массивный цитолиз сопровождается соответствующими клиническими проявлениями. Классическим примером является гемолитическая болезнь в результате резус-конфликта или переливания иногруппной крови. Цитотоксическим действием обладают также комплексы атиген—антитело, образующиеся в организме пациента в большом количестве после введения массивной дозы антигена (аллергическая реакция III типа). В связи с кумулятивным эффектом клиническая симптоматика аллергической реакции III типа имеет отсроченную манифестацию, иногда на срок более 7 суток. Тем не менее этот тип реакции относят к ГНТ. Реакция может проявляться как одно из осложнений от применения иммунных гетерологичных сывороток с лечебно-профилактической целью («сывороточная болезнь»), а также при вдыхании белковой пыли («легкое фермера»). НЕТ 4 ТИПА!!! Лабораторная диагностика аллергии при аллергических реакциях I типа основана на выявлении суммарных и специфических реагинов (IgE, IgG4) в сыворотке крови пациента. При аллергических реакциях II типа в сыворотке крови определяют цитотоксические антитела (антиэритроцитарные, антилейкоцитарные, антитромбоцитарные и др.). При аллергических реакциях III типа в сыворотке крови выявляют иммунные комплексы. Для обнаружения аллергических реакций IV типа применяют кожно-аллергические пробы, которые широко используют в диагностике некоторых инфекционных и паразитарных заболеваний и микозов (туберкулез, лепра, бруцеллез, туляремия и др.).
Гиперчувствительность немедленного типа (ГНТ) — гиперчувствительность, обусловленная антителами (IgE, IgG, IgM) против аллергенов. Развивается через несколько минут или часов после воздействия аллергена: расширяются сосуды, повышается их проницаемость, развиваются зуд, бронхоспазм, сыпь, отеки. Поздняя фаза ГНТ дополняется действием продуктов эозинофилов и нейтрофилов. К ГНТ относятся I, II и III типы аллергических реакций (по Джеллу и Кумбсу): I тип — анафилактический, обусловленный главным образом действием IgE; IIтип — цитотоксический, обусловленный действием IgG, IgM; III тип — иммунокомплексный, развивающийся при образовании иммунного комплекса IgG,IgM с антигенами. В отдельный тип выделяют антирецепторные реакции. Дата добавления: 2016-06-05 | Просмотры: 788 | Нарушение авторских прав |
 Свойства IgD:
Свойства IgD: 0,002% от всех Ig=3,9 на 10 в -9 г/л
0,002% от всех Ig=3,9 на 10 в -9 г/л