|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Неглерии и акантамебыТип Простейшие. Класс Саркодовые. Неглерии и акантамебы относятся к почвенным свободноживущим аэробным амебам. Однако, иногда они могут инвазировать человека и вызывать тяжелые заболевания. У этих амеб в отличие от дизентерийной и кишечной имеется комплекс Гольджи и множество митохондрий. У них хорошо развита эндоплазматическая сеть и имеются сократительные вакуоли. Способность повреждать ткани млекопитающих впервые была обнаружена в 1958 году на примере мышей при интраназальном (через нос) заражении. Амебы из рода Naegleria могут вызывать острый менингоэнцефалит, который почти всегда заканчивается летальным исходом. Морфология. В жизненном цикле неглерии выделяют 3 стадии: амебоидный трофозоит (15 – 40 мкм), двужгутиковая вегетативная форма (17 – 20 мкм) и округлая циста (10 – 20 мкм) с гладкой двойной стенкой.
Цитоплазма трофозоитов отчетливо подразделяется на экто- и эндоплазму. На окрашенных препаратах видны ядра диаметром около 5 мкм с кариосомой внутри. В отличие от дизентерийной амебы, неглерия имеет пластинчатый комплекс Гольджи, выраженную ЭПС и сократительную вакуоль. Амебоидный трофозоит передвигается, выбрасывая короткие, широкие и прозрачные псевдоподии. Жизненный цикл. Неглерия обитает в пресных водоемах (сточные воды, бассейны, термальные источники и др.). Обычно в воде встречается в небольших количествах, однако при повышении температуры воды до 35˚C неглерии начинают активно размножаться, и численность их значительно возрастает. Часть амеб при резких колебаниях температуры и изменении pH-среды формируют два жгутика и активно плавают в толще воды в течение суток, затем вновь переходят в амебоидную форму. При наступлении неблагоприятных условий неглерии легко инцистируются, но в пораженных тканях – цист не образуют Инвазионная стадия и пути инвазии. Заражение человека амебами происходит при попадании их в носовую полость во время ныряния в загрязненной воде. Амебоидные трофозоиты по ходу обонятельного нерва проникают в богато васкулизированное субарахноидальное пространство, откуда распространяются во все отделы мозга. В тканях мозга они локализуются вокруг кровеносных сосудов и бурно размножаются. В результате в сером и белом веществе мозга возникают кровоизлияния и некроз. Развивается первичный амебный менингоэнцефалит. Эпидемиология. Заражаются неглериями чаще всего дети и молодые люди. Вспышки заболевания обычно приходятся на жаркие периоды года (сезонный характер) при купании в открытых богатых илом водоемах с теплой водой. Кроме того, отмечаются случаи заражения в бассейнах, термальных источниках. Географическое распространение. Неглерии распространены повсеместно, но чаще встречаются в районах с тропическим и субтропическим климатом. Несколько видов амеб из рода Acanthamoeba будучи свободноживущими организмами, они, тем не менее, часто обнаруживаются в мазках из носоглотки и в фекалиях здоровых людей, проходят желудочно-кишечный тракт, не повреждая его. Однако, они могут оказывать патогенное действие на ослабленных больных, страдающих другими заболеваниями, или же проникать через поврежденную кожу или роговицу глаз. В связи с этим акантамебы относятся к условно патогенным (факультативным) паразитам. Клинически поражение организма акантамебами выражается в образовании гранулем в коже, легких, мозге, среднем ухе и в слизистой оболочке желудка. Описаны острый менингоэнцефалит и очаговые изъязвления роговицы. Лабораторная диагностика основана на микроскопировании биоптатов поврежденных тканей. Трофозоиты неглерии можно обнаружить в свежеприготовленных препаратах спинномозговой жидкости. ТОКСОПЛАЗМА
Этот паразит вызывает повсеместно встречающееся заболевание токсоплазмоз. Кроме человека, токсоплазмы могут болеть и различные теплокровные животные. Окончательным хозяином для токсоплазмоза являются животные из семейства кошачьих, а промежуточным - человек, многие виды млекопитающих и птиц. При этом возбудитель токсоплазмоза может циркулировать в природе независимо от человека между дикими и домашними животными.
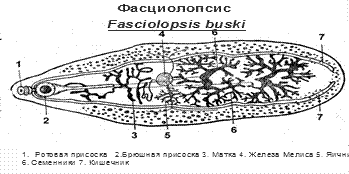
Для эндозоитов характерно бесполое размножение в форме продольного деления или эндогонии (внутреннее почкование). В результате таких делений в цитоплазме пораженных клеток накапливается большое количество эндозоитов и образуются псевдоцисты (ложные цисты). При хроническом течении токсоплазмоза появляются покрытые толстой защитной оболочкой истинные цисты, содержащие сотни токсоплазм (цистозоитов). Цисты локализуются преимущественно в головном мозге, в мышцах, в миокарде, нередко в глазах. В других органах и тканях они образуются реже. В цистозоитах заметны только ядра, поскольку их цитоплазма плохо окрашивается обычными цитоплазматическими красителями. Сами цистозоиты погружены в бесструктурную желатинообразную субстанцию. Инцистирование обеспечивает многолетнее, а часто и пожизненное существование токсоплазм в организме инвазированного человека. В старых крупных цистах можно обнаружить мертвых паразитов, однако, большая часть токсоплазм сохраняет не только жизнеспособность, но и продолжает медленно размножаться. Во внешней среде эндозоиты быстро погибают. В слюне, молоке, моче они могут сохраняться только несколько часов и погибают при нагревании, высушивании, под действием ультрафиолетовых лучей. Цистозоиты значительно устойчивее к факторам внешней среды, в том числе к действию пищеварительных ферментов и химиотерапевтических препаратов, применяемых для лечения токсоплазмоза. Окончательные хозяева (кошачьи) заражаются при поедании мяса, зараженного эндозоитами и цистозоитами, или же при поедании загрязненной спороцистами пищи. При этом, проникнув в эпителий кишечника, токсоплазмы размножаются путем шизогонии и образуются мерозоиты. Часть мерозоитов трансформируется в микро- и макрогаметы, которые, сливаясь, образуют зиготу (половой цикл развития). Зигота одевается защитной оболочкой и образуется ооциста. Ооцисты попадают в просвет кишечника и вместе с калом выделяются во внешнюю среду, где через несколько дней в них образуется по две спороцисты, в каждой из которых содержится по 4 спорозиота. Инвазирование промежуточных хозяев, в том числе и человека, происходит либо спороцистами при несоблюдении правил личной гигиены, либо эндозоитами и цистозоитами при употреблении недостаточно термически обработанного мяса и яиц от инвазированных токсоплазмами животных или же при разделывании зараженных туш при наличии ссадин и царапин на коже человека. Патогенное действие токсоплазмы и клинические симптомы токсоплазмоза Существуют две основные формы токсоплазмоза: приобретенный и врожденный (при внутриутробном заражении). Заболевание возникает далеко не во всех случаях попадания паразитов в организм человека. Многое зависит от количества возбудителей, их биологических свойств (например, вирулентности), путей передачи и реактивности макроорганизма. Приобретенный токсоплазмоз поражает человека в любом возрасте, но чаще всего - в детском. Он может протекать остро или латентно (скрытое течение). Иногда встречаются тяжелые и даже смертельные формы. Заражение человека осуществляется пероральным путем при употреблении инфицированных продуктов (мясо, яйца) или спороцистами. Воротами инвазии при приобретенном токсоплазмозе является кишечник, но в ряде случаев и кожа при разделывании туш животных, пораженных токсоплазмозом. Попадая в организм человека, токсоплазмы по лимфатическим сосудам проникают в лимфоузлы, которые играют важную роль в задержании и разрушении токсоплазмы. При достаточно выраженных барьерных механизмах заболевание может и не возникнуть. Недостаточность же их способствует размножению и накоплению паразитов, которые с током крови заносятся в органы и ткани. На 7-12 сутки после заражения в организме появляются антитела, что сопровождается гибелью эндозоитов, находящихся в клетках (псевдоцистах) и циркулирующих в крови. Устойчивыми оказываются лишь цистозоиты. Клинические симптомы приобретенного токсоплазмоза зависят от стадии заболевания (острая или хроническая) и реактивности макроорганизма. В начальных стадиях, как правило, имеет место мезаденит (воспаление брыжеечных лимфатических узлов) Затем явления мезаденита стихают, паразиты гематогенно с током крови заносятся в клетки органов и тканей, где размножаются и разрушают их. Это соответствует острому периоду токсоплазмоза и характеризуется разнообразием клинических симптомов, зависящих от того, какие органы оказываются наиболее пораженными. По частоте поражения на первом месте находятся лимфатическая, нервная, сердечно-сосудистая системы и печень. Отсюда и многообразная клиническая симптоматика: кроме увеличения лимфатических узлов наблюдаются боли в области сердца, одышка, сердцебиение, субфебрильная температура, явления пневмонии, бронхита, гепатита, неврологические симптомы и др. Нередко токсоплазмоз с самого начала приобретает хроническое течение без выраженных клинических симптомов. Врожденный токсоплазмоз развивается при трансплацентарном заражении плода, если беременность протекает на фоне острого токсоплазмоза или обострения хронического. При попадании токсоплазм в плод на ранних сроках развития, когда еще не сформировалась иммунная система, может развиться тяжелый токсоплазмоз, приводящий к гибели плода или же врожденным порокам развития: олигофрения, гидроцефалия, эпилептические припадки и другие симптомы. При инвазии на более поздних сроках беременности, когда иммунная система плода становится более функционально развитой, заражение происходит не всегда, но если это все же наблюдается, оно не всегда приводит к патологии плода. Со временем, в результате иммунной реакции пораженного организма, размножение токсоплазм замедляется, пролиферативные формы (эндозоиты) исчезают и формируются истинные цисты с цистозоитами. Болезнь переходит в хроническую стадию, когда клинические симптомы токсоплазмоза практически исчезают. Лабораторная диагностика токсоплазмоза. Распознание токсоплазмоза вызывает большие трудности, что обусловлено рядом причин: широким распространением инвазии среди практически здоровых лиц (латентные формы), полиморфизмом клинических проявлений манифестных форм заболевания и особенностями лабораторной диагностики. Применяются серологические и аллергологические реакции, но они не могут надежно подтвердить диагноз, так как могут быть положительными и при других заболеваниях, не связанных с токсоплазмозом. Эти методы применимы в основном для острых форм токсоплазмоза и для обследования беременных женщин в динамике. Бесспорным подтверждением токсоплазмоза является обнаружение возбудителей в крови, в тканях плода или в спинномозговой жидкости. Но такие находки редки и поэтому не могут быть основным методом подтверждения диагноза. Профилактика токсоплазмоза. Хотя профилактика токсоплазмоза из-за его широкого распространения носит актуальный характер, многое в этом вопросе не имеет окончательного решения. Трудности профилактики обусловлены наличием большого числа промежуточных хозяев, особенностями развития паразита, возможностью внутриутробного заражения и другими причинами. Для профилактики врожденного токсоплазмоза важное значение имеет выявление и лечение беременных женщин с острым токсоплазмозом или обострением хронического. Предупреждение приобретенного токсоплазмоза направлено на соблюдение правил личной гигиены, мытье овощей и фруктов перед едой, а также соблюдение правил приготовления мясных и яичных блюд с достаточной их термической обработкой. Специфических методов профилактики, таких как вакцинация, пока нет. Фасциолопсис (Fasciolopsis) Тип Плоские черви. Класс Сосальщики. Фасциолопсис – наиболее крупная трематода, размерами от 2 см до 7,5 см. Возбудитель фасциолопсидоза.
Имеет овальное или листовидное тело. Тело покрыто красновато-оранжевой кутикулой с рядами чешуек. Присоски сближены, брюшная присоска в 4–5 раз крупнее ротовой. Кишечные каналы без боковых ответвлений, доходят почти до заднего конца тела. Семенники ветвистые, находятся в задней половине тела. В средней части тела располагается небольшой ветвистый яичник и тельце Мелиса. Матка лежит перед яичником. Яйца крупные (до 130–140 мкм), слегка ассиметричные, желто-коричневые, с небольшой крышечкой, на заднем конце имеется линейное утолщение оболочки. В сутки фасциолопсис откладывает около 25 тыс. яиц с личинкой внутри. Цикл развития. Марита фасциолопсиса паразитирует в тонком кишечнике и желудке у свиней, собак, редко – у человека. Яйца для дальнейшего развития должны попасть в воду. Там из них выходит мирацидий, проникающий в тело моллюска из рода Планорбис или Сегментина, в которых проходят следующие стадии развития паразита: спороцисты → редии → церкарии. Последние, покидая тело моллюска, инцистируются на водных растениях (на плодах и листьях водяного ореха, на водяном луке, лотосе и др.). Попав вместе с пищей в тонкий кишечник окончательного хозяина, личинки выходят из оболочек и развиваются до половозрелой формы. Патогенноедействие и клиника. Данный сосальщик вызывает механическое повреждение слизистого и подслизистого слоев кишечника мощными присосками и чешуйками кутикулы. В местах прикрепления фасциолопсиса развивается воспаление, изъязвления и кровотечения. Может возникнуть обструкция кишечника вследствие его спазма или закупорки трематидами. число которых может доходить до 35 тыс. экземпляров. Продукты жизнедеятельности фасциолопсиса могут вызывать аллергические реакции, геморрагии в легких, почках, печени, селезенке и жировую дистрофию печени. В зависимости от интенсивности инвазии и состояния организма хозяина фасциолопсидоз может протекать бессимптомно, в легкой, среднетяжелой и тяжелой формах. Лабораторная диагностика: нахождение в фекалиях или в рвотных массах яиц факциолопсиса. Прогноз при своевременно начатом лечении – благоприятный, при хроническом течении и отсутствии лечения – серьезный. Фасциолопсидоз распространен в южных районах Китая, о.Тайвань, во Вьетнаме, Индии, Таиланде. В России регистрируются завозные случаи фасциолопсидоза.
Крысиный цепень (Hymenolepis diminuta) Тип Плоские черви. Класс Ленточные черви (Цестоды) Крысиный цепень - это цестода длиной от 20 до 60 см. Яйца желтого цвета, крупные, круглые. Онкосфера покрыта оболочкой, при этом сама Онкосфера значительно мельче, чем яйцо. Цепень является обычным паразитом кишечника мышей, и крыс. Человек может заразиться, случайно заглатывая вместе с непропеченным хлебом и другими мучными изделиями такого вредителя зерновых культур, как хрущак. Последний может оказаться зараженным личинками цепня. У человека крысиный цепень паразитирует в кишечнике, вызывая заболевание крысиный гименолепидоз. Лабораторный диагноз ставится на основании нахождения в испражнениях яиц крысиного цепня. Тыквовидный цепень (Dipylidium caninum) Дата добавления: 2015-02-06 | Просмотры: 1336 | Нарушение авторских прав |





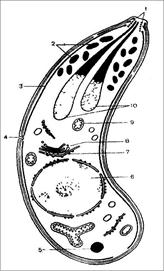 Токсоплазма является внутриклеточным паразитом. Она относится к типу Protozoa, к классу Sporozoa, отряду Coccidia. Впервые была обнаружена в 1908 году у грызунов гонди.
Токсоплазма является внутриклеточным паразитом. Она относится к типу Protozoa, к классу Sporozoa, отряду Coccidia. Впервые была обнаружена в 1908 году у грызунов гонди. В тело промежуточных хозяев паразиты в основном проникают через тонкий кишечник. Оттуда они попадают в лимфу и с током лимфы - в лимфатические узлы, где размножаются, а затем с током крови заносятся в органы окончательной локализации. Проникшие в клетки пораженных органов токсоплазмы называются эндозоитами. Последние имеют форму полумесяца или дольки апельсина (греч. toxon - арка, дуга). Их длина равна 4-7 мкм. Задний конец закруглен, а передний заострен. Имеется одно ядро. Пелликула, покрывающая тело токсоплазмы, состоит из трех мембран и имеет микропоры, служащие для поглощения питательных веществ из клеток хозяина. Под пелликулой располагаются микротрубочки, образующие вместе с ней наружный скелет, а на переднем конце тела токсоплазмы находится коноид. Он имеет форму усеченного конуса и содержит спирально закрученные микрофибриллы. Полагают, что коноид способствует фиксации токсоплазм при проникновении их в клетки хозяев. От коноида в цитоплазме идут мешковидно расширяющиеся на концах трубки - роптрии и тонкие волокна - токсонемы. Роптрии выделяют вещества, необходимые для проникновения паразитов в клетки. Предполагают, что токсонемы тоже участвуют в обеспечении проникновения токсоплазмы в клетки хозяев.
В тело промежуточных хозяев паразиты в основном проникают через тонкий кишечник. Оттуда они попадают в лимфу и с током лимфы - в лимфатические узлы, где размножаются, а затем с током крови заносятся в органы окончательной локализации. Проникшие в клетки пораженных органов токсоплазмы называются эндозоитами. Последние имеют форму полумесяца или дольки апельсина (греч. toxon - арка, дуга). Их длина равна 4-7 мкм. Задний конец закруглен, а передний заострен. Имеется одно ядро. Пелликула, покрывающая тело токсоплазмы, состоит из трех мембран и имеет микропоры, служащие для поглощения питательных веществ из клеток хозяина. Под пелликулой располагаются микротрубочки, образующие вместе с ней наружный скелет, а на переднем конце тела токсоплазмы находится коноид. Он имеет форму усеченного конуса и содержит спирально закрученные микрофибриллы. Полагают, что коноид способствует фиксации токсоплазм при проникновении их в клетки хозяев. От коноида в цитоплазме идут мешковидно расширяющиеся на концах трубки - роптрии и тонкие волокна - токсонемы. Роптрии выделяют вещества, необходимые для проникновения паразитов в клетки. Предполагают, что токсонемы тоже участвуют в обеспечении проникновения токсоплазмы в клетки хозяев.