|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
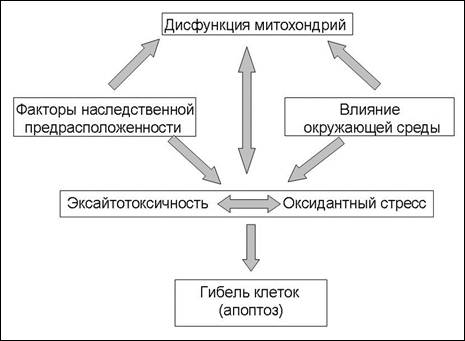
ПАТОГЕНЕЗ. Патогенез заболевания связан с недостаточностью дофаминергической системы мозга, его нигро-стриарного пучкаПатогенез заболевания связан с недостаточностью дофаминергической системы мозга, его нигро-стриарного пучка, основным медиатором которого является дофамин. Происходит повреждение нигральных дофаминергических нейронов, приводящее к резкому снижению концентрации дофамина в полосатом теле и значимым изменениям его функционального состояния. При этом относительно или абсолютно повышается активность холинергической системы. Показано, что в субталамическом ядре (nSTh) нарушаются процессы торможения, что приводит к патологической возбудимости внутреннего сегмента globus pallidus (Gpi) и pars reticulata черной субстанции (SNpr). Нарушение нормальных взаимодействий в системе Gpi- nSTh-SNpr приводят к развитию основных симптомов болезни. В базальных ганглиях больных паркинсонизмом (в хвостатом ядре, скорлупе, бледном шаре) снижено содержание не только дофамина, но и других биогенных аминов: норадреналина и серотонина, снижена активность тирозингидроксилазы. Наблюдаются значительные изменения норадренергической, холинергической, серотонинергической нейротрансмиссии. Происходит гибель дофаминовых рецепторов неостриатума (преимущественно рецепторы Д-2 типа). В патологический процесс вовлекаются и другие нейропептиды (ацетилхолин, ГАМК, энкефалины). Таким образом, при паркинсонизме дисбаланс одного медиатора (дофамина) приводит к патологическому нарушению многих медиаторов и дезорганизации деятельности всего головного мозга и экстрапирамидной системы прежде всего. Дисфункция дофаминергической системы обуславливает развитие двигательных, эмоциональных и психических расстройств, норадренергической системы – вегетативных, когнитивных и постуральных, холинергической – когнетивных и психических, глутаматэргической – дискинезий, когнитивных и психических, серотонинэргической - эмоциональных и психических. Важное значение имеют факторы аутоиммунноагрессии, и, как следствие, появление антител к собственным катехоламинам и особенно к дофамину. Ключевыми патогенетическими процессами, приводящими к гибели меланинсодержащих нигральных нейронов, являются оксидантный стресс, эксайтотоксичность и митохондриальные нарушения. В процессе катаболизма дофамина черной субстанции при участии МАО-В в тканях мозга формируется избыток перекиси водорода и свободных радикалов, которые в свою очередь вызывают перекисное окисление липидов, повреждение мембран и гибель клетки. Гиперактивность глутаматергической иннервации стриатума сопровождается активацией NMDA- рецепторов, избыточным выделением нейротрансмиттера глутамата и повышением внутриклеточной концентрации Са2+, что инициирует генерацию свободных радикалов посредством активации нейронной синтазы NO, которая участвует в образовании оксида азота. Выделяемый в результате этого NO выполняет роль посредника нейротоксического действия глутамата на клетку. Свободные радикалы вызывают перекисное окисление липидов клеточной мембраны и обуславливают развитие митохондриальной дисфункции. Однако, оксид азота оказывает на клетку и прямое цитотоксическое действие, обусловленное образованием пероксинитрита ONOO-, как продукта взаимодействия NO и супероксида аниона – О2--. Многочисленные исследования последнего десятилетия показали, что одним из механизмов гибели нервной клетки при дегенеративных заболеваниях нервной системы, и в частности при болезни Паркинсона, является апоптоз. Программированная гибель клеток, наблюдаемая при физиологическом процессе старения, может усиливаться под влиянием различных экзогенных и эндогенных факторов.
Рис. 3 Факторы и процессы, приводящие к гибели клетки.
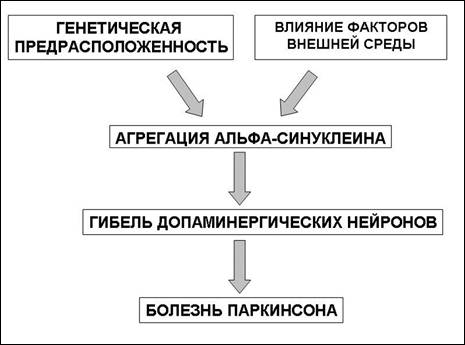
Уменьшение числа меланин-содержащих дофаминергических нейронов компактной части черной субстанции, наличие внутриклеточных эозинофильных, включений (телец Леви) в сохранившихся нейронах является важнейшим признаком болезни Паркинсона. Паталогоанатомические исследования выявляют значительное уменьшение числа пигментированных нейронов черной субстанции среднего мозга по сравнению с нормой (400 000). Тяжесть клинической картины, как правило, прямо пропорционально зависит от количества дофаминергических нейронов черной субстанции. Чем меньше количество нейронов, тем тяжелее клинические проявления заболевания и в первую очередь выраженность брадикинезии. У умерших снижено количество допаминергических нейронов более 90%, первые симптомы болезни появляются при гибели примерно 70%-80% и асимптомное течение наблюдается при гибели 50% нейронов. Тельца Леви могут быть обнаружены в черной субстанции, голубом пятне, дорзальном двигательном ядре блуждающего нерва, таламусе, гипоталамусе, а также в коре головного мозга преимущественно пожилых пациентов с длительной историей течения болезни Паркинсона, у которых развились симптомы деменции. Тельца Леви содержат протеин под названием альфа- синуклеин, основной функцией которого является модуляция синаптической пластичности. Появление и роль альфа- синуклеина в гибели нейронов объясняют с позиций оксидантного стресса, а также наличием генетических мутаций, ведущих к повреждению и интранейрональному его накоплению.
Рис. 4. Факторы, влияющие на агрегацию альфа-синуклеина
Дата добавления: 2015-01-18 | Просмотры: 662 | Нарушение авторских прав |