и третьего уровней мониторинга
У пациентов, которым проводят
второй и третий уровень монито-
ринга, оценивают регистрируемые
параметры при поступлении в отде-
ление интенсивной терапии. Даль-
нейшая периодичность их регистра-
ции зависит от особенностей вы-
полненного оперативного вмеша-
тельства. Оценку кровопотери, не-
врологического статуса и лабора-
торных показателей осуществляют
по принципам, изложенным в пре-
дыдущем разделе. У больных, опе-
рированных на органах грудной
клетки, выполняют контрольную
рентгенографию (в первые сутки —
однократно, затем — после удале-
ния дренажей или при возникнове-
нии специальных показаний). Ге-
матологический профиль и биохи-
мический анализ крови оценивают
в первые сутки после операции, за-
тем в зависимости от индивидуаль-
ных показаний. У больных, полу-
чающих антикоагулянтную и анти-
агрегантную терапию, контроли-
руют состояние свертывающей сис-
темы крови, количество и функ-
циональное состояние тромбоци-
тов.
3.10.2.3. Контроль за состоянием
свертывающей системы крови
и профилактика тромботических
осложнений
У пациентов, оперированных на со-
судах, одна из наиболее важных за-
дач заключается в соблюдении ба-
ланса между риском тромбообразо-
вания и кровотечения, что предпо-
лагает обязательные контроль за
состоянием системы свертывания
крови и проведение антитромботи-
ческой профилактики.
Исследование активности раз-
личных компонентов системы ге-
мостаза выполняют в момент по-
ступления больного в ОРИТ и в
первые сутки после операции у па-
циентов без осложнений, а у боль-
ных с осложнениями — в зависимо-
сти от клинической ситуации.
Полноценное обследование пред-
полагает выполнение коагулограм-
мы и анализ реологических свойств
крови методами вискозиметрии, аг-
регометрии и ригидометрии [Ройт-
ман Е.В. и др., 2000].
Коагулограмма. Минимально не-
обходимый для диагностики тром-
боопасных состояний набор тестов
включает в себя следующие измере-
ния:
• определение активированного
частичного тромбопластинового
времени (АЧТВ), что позволяет вы-
явить суммарную активность внут-
ренних факторов системы сверты-
вания крови. В раннем послеопера-
ционном периоде допустимый диа-
пазон АЧТВ составляет 25—40 с.
Для тромбогенной ситуации харак-
терно снижение величины этого
показателя < 25 с;
• определение протромбинового
времени используют для общей ха-
рактеристики активности внешнего
пути системы гемостаза. Результаты
этого исследования должны быть
представлены величиной междуна-
родного нормализованного соотно-
шения (MHO). В раннем послеопе-
рационном периоде допустимый
диапазон MHO составляет 1,1 — 1,8.
Значения MHO менее 1,1 указыва-
ют на склонность к тромбообразо-
ванию;
• определение концентрации
фибриногена дает информацию об
основном коагулирующем субстра-
те (в норме 1,80—3,60 г/л). При
этом риск тромбообразования при
гиперфибриногенемии повышается
и не зависит от ее причины;
• определение тромбинового вре-
мени (в норме 12—17 с). Укороче-
ние этого теста свидетельствует о
недостаточности антикоагулянтных
и фибринолитических механизмов
и указывает на повышенный риск
тромбообразования;
• определение количества тром-
боцитов: допустимый интервал зна-
чений — от 85 до 220 тыс. в 1 мкл;
• определение степени агрегации
тромбоцитов: допустимые в раннем
послеоперационном периоде вели-
чины — 45—60 %. Более высокие
значения увеличивают риск тром-
бообразования;
• определение содержания рас-
творимых фибринмономерных ком-
плексов (РФМК), являющихся мар-
керами активности диссеминиро-
ванного свертывания крови (ДВС).
Допустимые величины этого пока-
зателя — до 7—8 мг%, повышение
указывает на наличие тромбоген-
ной ситуации и активацию ДВС
крови;
• определение времени свертыва-
ния цельной крови по Ли—Уайту
позволяет оценить общий результат
взаимодействия про- и антикоагу-
лянтных систем и фибринолиза.
Для оперированных больных допус-
тимы значения 6—12 мин; укороче-
ние свидетельствует о тенденции к
гиперкоагуляции;
• определение гематокрита в ка-
честве характеристики гемоконцен-
трации.
На основании перечисленных те-
стов возможно получить достаточно
полное представление о свертываю-
щем и противосвертывающем по-
тенциале крови пациента. Следует
понимать, что совершенно не обя-
зательно, чтобы все тесты сразу
указывали на гиперкоагуляцию.
Вполне достаточно сочетания ги-
перкоагуляционных изменений в
2—3 показателях.
Выбор методов профилактики
тромботических осложнений зави-
сит от категории больных, но в
основном определяется их клини-
ческим состоянием.
Необходимым условием для про-
филактики тромботических ослож-
нений является создание изоволе-
мической гемодилюции до уровня
гематокрита 30—36 % [Дементье-
ва И.И. и др., 1996].
Перспективным средством для ее
наведения представляются инфузи-
онные препараты модифицирован-
ного жидкого желатина (гелофу-
зин), не оказывающие непосредст-
венного влияния на систему гемо-
стаза, или растворы гидроксиэтил-
крахмала, введение которых допол-
няют инфузией растворов кристал-
лоидов.
Наличие повышенной агрегации
тромбоцитов даже при их невысо-
ком общем содержании в крови
предполагает назначение антиагре-
гантов.
В последнее время изменилось
отношение к нефракционирован-
ному гепарину. Прежде всего пре-
парат при дробном введении не
обеспечивает устойчивый анти-
тромботический эффект. При дли-
тельном его применении существу-
ет опасность развития тромбоцито-
пении и тромбоцитопении с тром-
бозами.
Предпочтение отдают низкомо-
лекулярным гепаринам (НМГ).
В отличие от нефракционированно-
го гепарина НМГ обладают силь-
ным антитромботическим эффек-
том при слабом антикоагулянтном
действии. Разовая лечебная доза
для НМГ (фраксипарин, фрагмин,
клексан) составляет 150—250 ME
анти-ф. Ха-активности на 1 кг мас-
сы тела, кратность введения — 1 —
2 раза в сутки в зависимости от
темпа послеоперационной кровопо-
тери и динамики показателей коа-
гулограммы. Первая инъекция дол-
жна быть выполнена внутривенно,
последующие — подкожно. Для па-
циентов с осложнениями продол-
жительность терапии НМГ может
составлять более 20 сут. Действие
препарата наступает через 2—4 ч,
продолжительность эффекта со-
ставляет 12—28 ч. Эффект препара-
та оценивают по динамике актив-
ности фактора Ха, которая в ответ
на разовое введение должна снизи-
ться в 1,5—2 раза по сравнению с
исходной (в среднем до 40—60 %).
Для профилактических целей до-
статочно 1—2-кратного введения
25 тыс. ЕД фрагмина.
Применение обычного нефрак-
ционированного гепарина (НФГ) в
виде ингаляций показано при на-
личии у пациента явлений дыхате-
льной недостаточности. От 15 000
до 30 000 ЕД ингалируют 1 раз в
сутки либо через интубационную
трубку или вентиляционную маску
с применением небулайзера, уста-
новленного в контуре аппарата
ИВЛ, либо с использованием ульт-
развукового ингалятора. Действие
препарата наступает через 2—4 ч,
продолжительность эффекта —
12—24 ч. Антитромботический эф-
фект данного метода достигается
при стойком удлинении АЧТВ до
64-80 с.
Хорошим антитромботическим
эффектом обладает сочетание трен-
тала (400—800 мг/сут) и реополи-
глюкина (400—800 мл/сут) в виде
постоянной внутривенной инфу-
зии. Обычно у больных после AKHI
данную терапию начинают через
3—4 ч после операции; предварите-
льно необходимо убедиться в отсут-
ствии кровотечения. У больных с
артериальными анастомозами по-
вышен риск образования тромбо-
цитарных тромбов, поэтому ранняя
антиагрегантная терапия у них
чрезвычайно важна. Согласно реко-
мендациям Американской ассоциа-
ции сердца и Американского кол-
леджа, пациентам данной катего-
рии необходимо назначать аспирин
не позднее 48 ч после операции,
поскольку более позднее назначе-
ние препарата уже не влияет на ча-
стоту тромбоза шунтов. По нашему
опыту, ранняя антиагрегантная те-
рапия тренталом и реополиглюки-
ном оправдана, поскольку перора-
льную форму аспирина у данной
категории пациентов можно назна-
чить только после экстубации тра-
хеи.
В осложненных случаях, при
длительной ИВЛ внутривенная ан-
тиагрегантная терапия является ра-
зумной альтернативой аспирину.
Даже при ее назначении в первые
часы после операции мы не наблю-
дали увеличения кровопотери. Ас-
пирин необходимо назначать под
контролем анализа агрегации тром-
боцитов, поскольку встречаются
больные, резистентные к этому
препарату. Таким пациентам назна-
чают клопидогрель (плавикс), при-
чем обычно бывает достаточно не-
больших доз (1/2—1/4 таблетки 75 мг
1 раз в сутки).
Для профилактики спазма арте-
риальных шунтов, например при
маммарокоронарном шунтирова-
нии, сразу после операции назнача-
ют постоянную инфузию дилтиазе-
ма в дозе 3—5 нг/(кг • мин).
Пациентам, которым, помимо
операции на сосудах, выполняют
протезирование клапанов сердца
или пластику межжелудочковой пе-
регородки из ксеноматериалов, в
течение первой недели назначают
НМГ, затем переходят на непрямые
антикоагулянты.
3.10.2.4. Профилактическое
применение антибиотиков
Выбор схемы профилактической
антибактериальной терапии зави-
сит от особенностей выполняемого
оперативного вмешательства и со-
путствующих заболеваний пациен-
та. При больших оперативных вме-
шательствах важное значение име-
ют предоперационная деконтами-
нация и подготовка кишечника.
В целях проведения деконтамина-
ции за 2 сут до операции назна-
чают 80 мг гентамицина в вод-
ном растворе, 500 мг трихопола и
500 000 ЕД нистатина 2 раза в сут-
ки внутрь.
При операциях, выполняемых в
условиях ИК (протезирование кла-
панов, АКШ, операции на грудном
отделе аорты), назначают цефало-
спорины второго-третьего поколе-
ний — цефуроксим, цефаклор, це-
фоперазон, цефотаксим, цефтази-
дим, цефтизоксим, цефтриаксон.
При операциях на брюшном от-
деле аорты, почечных артериях,
при аортобедренном шунтировании
также используют цефалоспорины
второго-третьего поколений во вре-
мя оперативного вмешательства.
Затем, проводят сочетанную анти-
бактериальную терапию с добавле-
нием к цефалоспоринам метрони-
дазола и одного из аминогликози-
дов второго поколения (амикацин,
нетромицин).
При сопутствующих заболевани-
ях печени и почек в послеопераци-
онном периоде назначают препара-
ты с двойным путем выведения —
цефалоспорины (цефоперазон,
цефтазидим, цефтриаксон) в соче-
тании с метронидазолом или пре-
параты группы фторхинолонов
(офлоксацин, ципрофлоксацин и
т.д.) в сочетании с амоксицилли-
ном.
При реваскуляризации нижних
конечностей используют сочетан-
ную терапию линкомицином с од-
ним из аминогликозидов и метро-
нидазолом или клиндамицином в
сочетании с аминогликозидом. Мо-
жет быть также использован докси-
циклин в сочетании с метронидазо-
лом или препараты фторхинолоно-
вого ряда.
Послеоперационную профилак-
тику антибиотиками назначают на
48 ч. При появлении специальных
показаний антибактериальную те-
рапию проводят в соответствии с
результатами бактериологического
исследования и чувствительности
микрофлоры к препаратам.
3.10.3. Осложнения раннего
послеоперационного периода
3.10.3.1. Острая недостаточность
кровообращения
Синдрому острой недостаточности
кровообращения принадлежит ве-
дущее место в структуре осложне-
ний и летальности у больных, опе-
рированных на сердце и сосудах
[Константинов Б.А., 1981; Бураков-
ский В.И. и др., 1982; Лебеде-
ва Р.Н. и др., 1983; Покров-
ский А.В. и др., 2000; Белов Ю.В. и
др., 2000; Tarhan J. et al., 1982].
Крайней степенью ОНК является
циркуляторный шок, который пред-
ставляет собой клинический синд-
ром, характеризующийся неадек-
ватной тканевой оксигенацией
(ТО2), приводящей к снижению по-
требления кислорода (ТО2), ана-
эробному метаболизму и лактат-
ацидозу.
В зависимости от этиологическо-
го фактора у оперированных боль-
ных выделяют следующие виды
шока.
Кардиогенный шок (острая сер-
дечная недостаточность):
• исходно низкие функциональ-
ные резервы миокарда;
• периоперационный инфаркт
миокарда;
• операционная травма миокарда;
• дефекты операционной техники
и кардиоплегии;
• недостаточность сократитель-
ной функции миокарда;
• синдром малой полости левого
желудочка (при операциях, связан-
ных с его ремоделированием);
• нарушения ритма и проводимо-
сти сердца;
• тампонада перикарда;
• повышение сопротивления из-
гнанию крови из левого желудочка
(постнагрузки).
Гиповолемический шок (снижение
ОЦК):
• кровотечение;
• дегидратация.
Дистрибутивный шок (увеличе-
ние емкости сосудистой системы):
• анафилактический шок;
• септический шок;
• неврогенный шок.
Обструктивный шок (обструкция
магистральных сосудов):
• тромбоэмболия легочной арте-
рии;
• синдром верхней полой вены.
Классическими клиническими
признаками шока считаются нару-
шения сознания, снижение темпе-
ратуры конечностей, бледность и
мраморная окраска кожных покро-
вов, частый пульс слабого наполне-
ния, падение АД и снижение темпа
мочеотделения (олиго- или ан-
урия). Поскольку в раннем после-
операционном периоде на клиниче-
ские показатели больных влияет
комплексная терапия, которую
проводят с момента возникновения
кардиореспираторных нарушений,
общепринятые критерии и класси-
фикации шока к ним трудно при-
менимы. Синонимами данного тер-
мина являются синдром низкого
сердечного выброса и острая недо-
статочность кровообращения, одна-
ко все эти термины объединяет об-
щий результат, заключающийся в
несоответствии перфузии тканей их
метаболическому запросу.
Интегральным показателем, от-
ражающим доставку кислорода ор-
ганам и тканям, является артериа-
льный транспорт кислорода, основ-
ные детерминанты которого — сер-
дечный выброс, содержание гемо-
глобина в крови и насыщение кис-
лородом гемоглобина артериальной
крови [Баркрофт Дж., 1937; Shoe-
maker C.W. et al., 1977].
Следует обратить внимание на
некоторые методические особенно-
сти, способные повлиять на вели-
чину ТО2. Прежде всего точность
определения СВ зависит от методи-
ки его измерения. Поскольку в ряде
клинических ситуаций может воз-
растать содержание в крови патоло-
гических форм гемоглобина (кар-
боксигемоглобина, метгемоглоби-
на, сульфгемоглобина, а в педиат-
рической практике — фетального
гемоглобина), целесообразно поль-
зоваться приборами, позволяющи-
ми определять содержание в крови
эффективного (кислородперенося-
щего) гемоглобина, а также изме-
рять Cta02.
Константа Хюффнера, характе-
ризующая способность гемоглобина
крови связывать кислород, может
варьировать в пределах от 1,32 до
1,39, однако в связи с тем что аппа-
ратура, с помощью которой ее из-
меряют, имеется в очень ограни-
ченном числе отделений, а отличие
в несколько сотых единиц вряд ли
окажет большое влияние на общий
результат вычисления, рекоменду-
ется наиболее часто встречаемая ве-
личина, составляющая 1,36.
Важное значение имеет прямое
определение величины артериаль-
ного Нb02, поскольку в ряде случа-
ев, когда в газоанализаторе отсутст-
вует гемоксиметрический блок,
данный параметр рассчитывают,
исходя из значений РаО2. При от-
клонениях положения кривой дис-
социации оксигемоглобина разли-
чия между измеренными и расчет-
ными значениями НbО2 могут быть
очень значительными.
Падение производительности сер-
дца (сердечного выброса) является
основной причиной острой недо-
статочности кровообращения и раз-
вивающейся в результате нее цир-
куляторной гипоксии у опериро-
ванных больных.
Снижение тканевой перфузии
ниже критического уровня, необхо-
димого для нормального протека-
ния обязательных метаболических
процессов, приводит к анаэробно-
му метаболизму и тяжелым по-
вреждениям клеточных структур
[Вейль М.Г., Шубин Г., Shumer W.,
1982]. В связи с этим при диагнос-
тике синдрома циркуляторного
шока и оценке его тяжести на пер-
вый план выступает глубина нару-
шений транспорта кислорода, мик-
роциркуляции и клеточного мета-
болизма [Лабори А., 1970; Раби К.,
1974; Дементьева И.И., 1982].
Помимо тяжести гемодинамиче-
ских нарушений, выраженность
острой недостаточности кровообра-
щения зависит от ряда факторов,
которые в ряде случаев могут при-
водить к неадекватному снабжению
органов и тканей кислородом на
фоне относительно нормального
состояния центральной гемодина-
мики:
• низкая кислородная емкость
крови (анемия и/или артериальная
гипоксемия);
• гуморальный дисбаланс;
• нарушения КЩР и водно-элек-
тролитного баланса;
• периферическое артериовеноз-
ное шунтирование крови;
• увеличение скорости кровотока
на фоне снижения уровня метабо-
лических процессов;
• капиллярный стаз вследствие
недостаточной перфузии и
ДВС-синдрома;
• повышение уровня метаболиче-
ских процессов при отсутствии ре-
зервов производительности сердца;
• нарушение диффузии кислоро-
да через стенку капилляра в резуль-
тате нарастания тканевого отека.
Поскольку транспорт кислорода
определяется не только величиной
сердечного выброса, но и содержа-
нием О2 в крови, адекватность тка-
невой оксигенации зависит от со-
стоятельности дыхательной функ-
ции легких, а также содержания ге-
моглобина в крови и его сродства к
кислороду [Nunn J.F., 1977]. В ран-
нем послеоперационном периоде
возникает повышение уровня мета-
болических процессов, обусловлен-
ное влиянием хирургической агрес-
сии, активацией симпатико-адрена-
ловой системы, повышением тем-
пературы тела, метаболизацией
кислородной задолженности орга-
низма, затратами энергии на согре-
вание вводимых парентерально хо-
лодных растворов, послеопераци-
онную дрожь и др. [Рябов Г.А.,
1979; Дементьева И.И., 1982].
В связи с этим прирост сердечного
выброса по окончании операции
рассматривается как адекватная ре-
акция системы кровообращения на
операционную травму. Однако ги-
пердинамическое состояние крово-
обращения может наблюдаться так-
же на фоне артериальной гипертен-
зии и периферической вазоконст-
рикции [Лебедева Р.Н. и др., 1979;
Walinsky P., 1977]. В клинической
практике в качестве критериев
адекватности кровообращения ис-
пользуется целый ряд параметров:
напряжение и насыщение Нb в ар-
териальной крови, в смешанной,
венозной крови, потребление O2,
артериовенозная разница по кисло-
роду. О степени нарушений окис-
лительных процессов судят по ве-
личине лактата артериальной кро-
ви. Согласно нашему опыту, диа-
гностическая ценность всех пере-
численных параметров, если их
рассматривать по отдельности, не-
велика.
В частности, на фоне интенсив-
ной терапии дефицит кислородного
снабжения тканей может наблюда-
ться на фоне нормальных или по-
вышенных значений ПО2, а также
АВРО2, PvO2 и НbО2 смешанной,
венозной крови могут быть повы-
шенными или нормальными на
фоне вазоконстрикции или пе-
риферического артериовенозного
шунтирования. Низкие значения
PvO2 менее 30 мм рт.ст. и НbО2 <
< 60 % достоверно указывают на
дефицит доставки кислорода. Абсо-
лютное значение лактата артериа-
льной крови также не имеет боль-
шого диагностического значения.
Этот показатель необходимо оцени-
вать в динамике.
Мы наблюдали больных с высо-
кими значениями лактата — более
12 ммоль/л, у которых на фоне те-
рапии этот показатель снижался до
нормальных величин. В то же вре-
мя его нарастание является небла-
гоприятным прогностическим при-
знаком.
При острой сердечной недоста-
точности компенсация, направлен-
ная на поддержание СВ, происхо-
дит за счет увеличения конечно-
диастолического объема левого же-
лудочка, а также повышения актив-
ности симпатико-адреналовой сис-
темы, приводящего к возрастанию
частоты сердечных сокращений, ве-
нозного возврата и перераспределе-
нию регионарного кровотока и
жидкостных пространств организма
[Константинов Б.А., 1981; Браун-
вальд Е. и др., 1974].
Острое падение производитель-
ности сердца может компенсирова-
ться в основном за счет сдвига кри-
вой диссоциации НbО2 и увеличе-
ния тканевой экстракции кислоро-
да [Aberrnan A., 1982].
Компенсация низкой доставки
О2 на тканевом уровне осуществля-
ется за счет микроциркуляторно-
го резерва и тканевого резерва [Wo-
ods R.D., 1979].
Действие перечисленных ком-
пенсаторных механизмов наиболее
эффективно при хронических нару-
шениях основных детерминант
транспорта кислорода. В случаях
острых расстройств их роль значи-
тельно сужается.
3.10.3.2. Регуляция
производительности сердца
Принципы коррекции низкой про-
изводительности сердца у кардио-
хирургических больных были сфор-
мулированы J.Kirklin и N.Kouchou-
kos в 1974 г. Предложенный подход
основан на оценке основных детер-
минант сердечного выброса: конт-
рактильности, преднагрузки, пост-
нагрузки и частоты сердечных со-
кращений. Алгоритм содержит ряд
допущений. Во-первых, адекват-
ность преднагрузки желудочков
сердца оценивается по величине
давлений наполнения желудочков
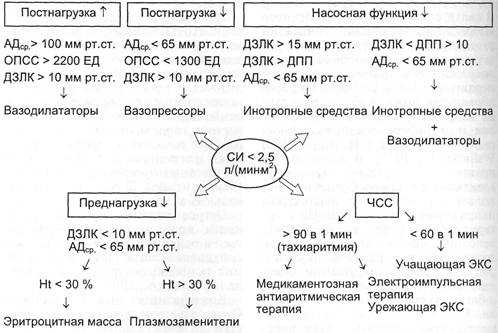
Схема 3.2. МОДИФИЦИРОВАННЫЙ АЛГОРИТМ КОРРЕКЦИИ НИЗКОГО СЕРДЕЧ-
НОГО ВЫБРОСА
сердца, в то время как состояние
притока крови к сердцу более точно
отражает конечно-диастолический
объем желудочков сердца. У ряда
больных между этими параметрами
нет прямой корреляционной зави-
симости. Кроме того, ДЗЛК соот-
ветствует КДД левого желудочка
при отсутствии легочной гипертен-
зии, а среднее давление в правом
предсердии соответствует КДД пра-
вого желудочка при интактном три-
куспидальном клапане. Во-вторых,
описывая состояния, характеризую-
щиеся высоким давлением напол-
нения желудочков сердца и низким
СВ, авторы пользуются термином
«контрактильность», т.е. сократите-
льная функция миокарда, в то
время как в физиологии для этих
целей пользуются параметрами, ха-
рактеризующими силу и скорость
сокращения мышечных волокон
сердца. С нашей точки зрения, бо-
лее корректно пользоваться терми-
ном «насосная функция сердца»,
хотя для лечения подобных состоя-
ний используют препараты, улуч-
шающие контрактильность. В-тре-
тьих, при оценке сопротивления
изгнанию крови, т.е. постнагрузки,
по величине среднего АД можно
судить при отсутствии патологии
аортального клапана. И наконец,
алгоритмом можно пользоваться,
исключив такие осложнения, как
тампонада миокарда, падение про-
изводительности сердца при сдав-
лении полых вен или смещении
средостения в результате пневмото-
ракса и массивного гемо- или гид-
роторакса, а также нарушений рит-
ма сердца.
Модифицированный алгоритм
коррекции низкого сердечного вы-
броса представлен на схеме 3.2.
Падение СВ на фоне высоких
значений давления наполнения же-
лудочков сердца является показа-
нием к назначению препаратов с
положительным инотропным эф-
фектом. Подбор препарата и его
дозы осуществляют индивидуально
под контролем показателей гемоди-
намики и кислородтранспортной
функции. Более подробно совре-
менные подходы к назначению
препаратов этой группы изложены
в разделе «Симпатомиметики».
В комплексной терапии сердеч-
ной недостаточности также исполь-
зуют диуретики и препараты, улуч-
шающие метаболизм и энергетиче-
ский потенциал миокарда (40 %
раствор глюкозы с инсулином, фос-
фокреатин, цитомак, альфа-токо-
ферол). Низкая производительность
сердца может наблюдаться в случа-
ях изолированной или превалирую-
щей правожелудочковой недоста-
точности. При этом давление на-
полнения правого желудочка серд-
ца выше ДЗЛК. Лечение заключает-
ся в назначении инотропных пре-
паратов в сочетании с вазодилата-
торами.
При снижении преднагрузки, ха-
рактеризующемся падением СВ на
фоне низких давлений наполнения
желудочков сердца, показана инфу-
зия плазмозаменителей, а если на-
блюдаются низкие значения гема-
токрита, — эритроцитной массы
(см. раздел «Послеоперационные
кровотечения»).
Для определения оптимального
давления наполнения желудочков
сердца целесообразно пользоваться
пробой с нагрузкой объемом жидко-
сти. Для этого в центральную вену в
быстром темпе вводят раствор плаз-
мозаменителя, регистрируя измене-
ние СВ при увеличении ДЗЛК и
ДПП на 1—2 мм рт.ст. Если во
время проведения пробы СВ снижа-
ется, инфузию жидкости прекраща-
ют. На рис. 3.30 представлены вари-
анты кривых функции левого желу-
дочка сердца. При нормальном от-
вете на пробу значения СИ достига-
ют 2,5— 3,5 л/(мин • м2) после воз-
растания ДЗЛК до 10—12 мм рт.ст.
(кривая 1). У некоторых больных
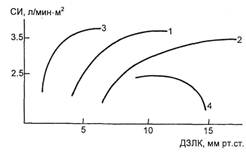
Рис. 3.30. Алгоритм регуляции сердеч-
ного выброса. Объяснение в тексте.
нормальная производительность
сердца наблюдается при высоких
давлениях наполнения, достигаю-
щих 18—20 мм рт.ст. (кривая 2).
Встречаются случаи, когда нормаль-
ная производительность сердца на-
блюдается при относительно невы-
соких значениях показателей пред-
нагрузки (кривая 3). У ряда пациен-
тов при низких давлениях наполне-
ния желудочков сердца инфузия не-
больших объемов приводит к резко-
му падению СИ, что свидетельству-
ет о низких функциональных резер-
вах миокарда и необходимости ино-
тропной поддержки (кривая 4). В
этих случаях возможно введение
жидкости в медленном темпе под
прикрытием симпатомиметиков.
Высокое сопротивление изгна-
нию крови (постнагрузка) характе-
ризуется повышением среднего АД
и ОПСС. В этих случаях необходи-
мо прежде всего исключить цент-
рализацию кровообращения в резу-
льтате гиповолемии, поэтому пер-
воначально производят восполне-
ние ОЦК до нормальных значений
давлений наполнения желудочков
сердца, после чего начинают инфу-
зию вазодилататоров (см. раздел
3.9.2.4).
В ряде клинических ситуаций
встречается относительная гипово-
лемия или сосудистая недостаточ-
ность. При этом для нормализации
АД и СИ применяют препараты с
вазопрессорным эффектом.
Падение производительности сер-
дца может развиваться на фоне бра-
диаритмий (синусовая, узловая бра-
дикардия, атриовентрикулярная
блокада II—III степени), а также та-
хиаритмий. Коррекцию этих нару-
шений осуществляют с помощью
электрокардиостимуляции, электро-
импульсной терапии или медика-
ментозной терапии.
Симпатомиметики. J.Wilson и со-
авт. (1999), опираясь на результаты
контролируемого рандомизирован-
ного исследования, пришли к за-
ключению, что периоперационное
применение инотропной поддерж-
ки и регуляция жидкостного балан-
са под контролем инвазивного мо-
ниторинга значительно снижают
число осложнений, летальность и
сроки пребывания в стационаре бо-
льных. При операциях на сердце и
магистральных сосудах частота ис-
пользования симпатомиметиков до-
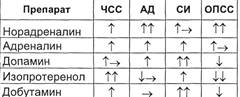
стигает 50 %. Основные гемодина-
мические эффекты наиболее часто
используемых симпатомиметиков
представлены в табл. 3.3.
Таблица 3.3. Гемодинамические эф-
фекты терапевтических доз симпато-
миметиков
Основными показаниями к ис-
пользованию симпатомиметиков
являются сердечная, сосудистая
недостаточность или их сочетание.
В связи с этим при выборе препа-
рата и подборе его оптимальной
дозы учитывают особенности их
влияния на гемодинамику и кисло-
родтранспортную функцию паци-
ентов. Гемодинамические эффекты
симпатомиметиков определяются
их дозой и индивидуальной чувст-
вительностью больного к препа-
рату.
Известно, что наиболее выражен-
ным хронотропным эффектом об-
ладает изопротеренол, поэтому он
является препаратом выбора у бо-
льных с брадикардией и нарушени-
ями проводимости сердца. Прове-
денные нами исследования показа-
ли, что изопротеренол снижает со-
противление большого и малого
круга кровообращения и увеличи-
вает показатели оксигенации арте-
риальной крови. Допамин при ис-
пользовании его в дозах свыше
5 мкг/(кг • мин) вызывал статисти-
чески значимое повышение сопро-
тивления сосудов малого круга кро-
вообращения и фракции внутриле-
гочного шунтирования. Эти эффек-
ты не характерны для добутамина,
поэтому ему следует отдавать пред-
почтение у больных с легочной ги-
пертензией и нарушениями оксиге-
нирующей функции легких. У па-
циентов, имеющих сочетание сер-
дечной недостаточности с наруше-
нием функции почек, оправдано
применение средних доз добутами-
на и небольших [до 2 мк/(кг • мин)]
доз допамина.
В ряде клинических ситуаций на-
блюдаются признаки высокой пост-
нагрузки сердца в сочетании с на-
рушением его инотропной функ-
ции. В подобных случаях сочетают
введение инотропных средств (до-
бутамин, допамин) с вазодилатато-
рами (нитропруссид натрия, адалат,
исрадипин).
Адреналин считается препаратом
выбора при анафилактических ре-
акциях, которые могут возникать во
время операции или в послеопера-
ционном периоде. Кроме того, в
ряде случаев, когда высокие дозы
добутамина или допамина не при-
водят к стабилизации гемоди-
намики, улучшить ситуацию уда-
ется путем подключения 300—
500 нг/(кг • мин) адреналина.
 В учебниках по сердечно-сосуди- В учебниках по сердечно-сосуди-
стой хурургии, издаваемых 20 лет
назад, звучал прямой запрет на ис-
пользование норадреналина [Кон-
стантинов Б.А., 1981]. В настоящее
время благодаря усовершенствова-
нию методов диагностики стало
возможным диагностировать изоли-
рованную сосудистую недостаточ-
ность, в результате чего норадрена-
лин был «реабилитирован» и нашел
свое место в послеоперационной
интенсивной терапии у данной ка-
тегории больных. Изолированная
сосудистая недостаточность в по-
слеоперационном периоде может
наблюдаться при выраженной ги-
пертермии, интоксикации после ре-
васкуляризации нижних конечно-
стей на фоне выраженных доопера-
ционных трофических нарушений,
при сепсисе и синдроме полиорган-
ной недостаточности. В этих случа-
ях удается добиться улучшения ге-
модинамики на фоне введения
50—500 нг/(кг-мин) норадреналина.
Препарат также может применяться
в сочетании с инотропными средст-
вами при комбинации сердечной и
сосудистой недостаточности.
В течение последнего десятиле-
тия существенно изменилась такти-
ка назначения симпатомиметиков
при интенсивной терапии. Это по-
ложение иллюстрирует табл. 3.4.
Проведенный нами сравнительный
анализ частоты использования раз-
личных симпатомиметиков в 1992 и
2001 гг. показал, что сейчас значи-
тельно сократилась частота исполь-
зования монотерапии допамином и
добутамином. Чаще всего данные
препараты применяют в небольших
[до 5 мкг/(кг-мин)] или средних
[5—10 мкг/(кг-мин)] дозах. Наблю-
давшееся 10 лет назад применение
этих препаратов в высоких дозах
[10—20 мкг/кг-мин)] встречается
крайне редко. В частности, высокие
дозы допамина используют в 4 раза
реже, а у 90 % пациентов применя-
ют небольшие и средние дозы пре-
парата.
Таблица 3.4. Частота использования
различных доз допамина (в процен-
тах) в раннем периоде после операций
на сердце и магистральных сосудах
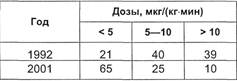
Аналогичная тенденция верна и
для добутамина (табл. 3.5). Помимо
того что данный препарат стал ли-
дировать по частоте применения,
высокие его дозы применяют лишь
у 2 % больных, получающих симпа-
томиметики.
Таблица 3.5. Частота использования
различных доз добутамина (в процен-
тах) в раннем периоде после операций
на сердце и магистральных сосудах
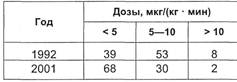
Полученные данные объясняют-
ся более активным использованием
комбинации различных симпатоми-
метиков, позволяющей оптимизи-
ровать интенсивную терапию за
счет дифференцированного учета
присущих каждому из них эффек-
тов. Известно, например, что как у
допамина, так и у добутамина при
высоких дозах инфузии превалиру-
ет вазопрессорный альфа-эффект.
В связи с этим их целесообразно
применять в умеренных дозах,
обеспечивая вазопрессорный эф-
фект за счет параллельной инфузии
норадреналина.
В последние годы в отделении
послеоперационной интенсивной
терапии кардиохирургического кор-
пуса РНЦХ РАМН наблюдается
следующая статистика: монотера-
пия добутамином осуществляется у
35 %, допамином — у 6 %, норадре-
налином — у 15 %, адреналином —
у 8 % пациентов. У остальных боль-
ных применяют рационально подо-
бранную комбинацию различных
препаратов. Во всех случаях подбор
симпатомиметика при выраженной
недостаточности кровообраще-
ния — кропотливая работа, кото-
рую осуществляют под контролем
инвазивного мониторинга с учетом
индивидуальной реакции пациента
на вводимые препараты.
Сердечные гликозиды. Обладая
положительным инотропным и от-
рицательным хронотропным эф-
фектом, сердечные гликозиды не
увеличивают потребление миокар-
дом кислорода [Константинов Б.А.,
1981]. Обычно препараты этой
группы неэффективны при выра-
женной ОНК, в частности при кар-
диогенном шоке. Спорным остает-
ся также вопрос об их назначении в
острой стадии инфаркта миокарда.
Вместе с тем сердечные гликозиды
остаются препаратами выбора у бо-
льных с застойной сердечной недо-
статочностью.
Сердечные гликозиды назначают
больным с распространенным кар-
диосклерозом, пациентам, которым
выполняют коррекцию клапанных
пороков сердца или вентрикулото-
мию, при мерцательной аритмии с
целью урежения частоты пульса и
восстановления синусового ритма.
Противопоказаниями к назначе-
нию сердечных гликозидов являют-
ся атриовентрикулярная блокада
II—III степени, слабость синусово-
го узла, узловой ритм, синоаурику-
лярная блокада.
В нашей практике мы применяем
сердечные гликозиды у больных с
нарушениями проводимости сердца
на фоне проведения ЭКС через
миокардиальные электроды. Чаще
применяют внутривенную форму
дигоксина, поскольку он выводится
почками и является таким образом
более управляемым препаратом.
Его средние суточные дозы состав-
ляют 0,12—0,4 мг/м2.
Инфузионно-трансфузионная те-
рапия. Принципы инфузионно-
трансфузионной терапии. Жидкост-
ные пространства организма. Об-
щее содержание воды в организме
составляет около 60 %, при этом
она распределяется в различных
жидкостных пространствах. Во
внутриклеточном пространстве на-
ходится 2/3воды и во внеклеточ-
ном - 1/3[Lewis R.T., 1980].
Внеклеточное пространство со-
стоит из интерстициального и внут-
рисосудистого секторов. Обычно
75 % внеклеточной жидкости нахо-
дится в интерстиции и 25 % — в со-
судистом русле. Имеются значите-
льные различия в электролитном
составе внутриклеточного и внекле-
точного жидкостного пространства.
В клетках преобладает содержание
ионов калия, а во внеклеточном
пространстве — ионов натрия и
хлора. Для поддержания электро-
литного градиента необходимо
функционирование натрий-калие-
вого насоса.
В норме мембрана клетки обла-
дает относительной проницаемо-
стью для ионов электролитов, но
она свободно проницаема для
воды. Например, снижение кон-
центрации натрия и осмолярности
во внеклеточном пространстве по-
сле инфузии 5 % раствора глюко-
зы сопровождается перемещением
воды в клетку, что может привести
к уравниванию осмотического дав-
ления в этих жидкостных секторах.
И наоборот, увеличение концент-
рации натрия и осмолярности во
внеклеточном пространстве, на-
пример в результате инфузии ги-
пертонического раствора на-
трия, сопровождается перемещени-
ем воды из внутриклеточного во
внеклеточное пространство. Инфу-
зия изотонических растворов элек-
тролитов не изменяет осмолярно-
сти внеклеточного пространства и
тем самым не приводит к переме-
щению воды.
Перемещение воды между двумя
компонентами внесосудистого про-
странства определяется прежде все-
го разностью концентрации белка.
Коллоидно-осмотическое давление
является основным фактором, бла-
годаря которому эндотелий непро-
ницаем для белков плазмы. При на-
рушениях белкового обмена в резу-
льтате осмотического дисбаланса
вода переходит из интерстициаль-
ного пространства в кровяное рус-
ло. Молекулы кристаллоидов не со-
здают градиента давления, посколь-
ку они свободно проходят через
мембрану капилляра. В норме 60 %
КОД обеспечивается за счет раз-
личных белков (из них 75 % — за
счет альбумина, остальное — за
счет глобулинов и фибриногена).
40 % КОД поддерживается за счет
концентрации катионов. У пациен-
тов отделения интенсивной тера-
пии нормальный КОД составляет
от 18 до 20 мм рт.ст. [Rackow E.C.
et al, 1977].
Показания к инфузионно-транс-
фузионной терапии:
• абсолютный дефицит объема
циркулирующей крови (абсолютная
гиповолемия при кровотечении,
недовосполненной кровопотере во
время и после операции; потеря
жидкости и электролитов при по-
лиурии и через желудочно-кишеч-
ный тракт, гипертермии);
• относительная гиповолемия
(вазодилатация, анафилактический
и септический шок, феномен депо-
нирования крови и жидкости);
• сердечная недостаточность в
комплексной терапии при необхо-
димости увеличения насосной фун-
кции сердца через механизм Фран-
ка—Старлинга;
• парентеральное питание;
• коррекция кислотно-щелочного
и электролитного баланса, регуля-
ция онкотического давления крови.
Препараты крови. Цельная донор-
ская кровь, эритроцитная масса. От-
рицательные последствия трансфу-
зии донорской крови хорошо изве-
стны [Константинов Б.А. и др.,
2000], поэтому показания к ее ис-
пользованию в хирургии стараются
максимально сузить.
Большинство авторов сходятся во
мнении, что у больных, перенес-
ших операцию на сосудах, оптима-
льный гематокрит составляет 30—
35 %. По нашему мнению, этот по-
казатель следует определять инди-
видуально с учетом величины арте-
риального транспорта кислорода и
основной его детерминанты — сер-
дечного индекса. Согласно прове-
денным исследованиям, у опериро-
ванных больных снижение гемо-
глобина на 1 г% должно сопро-
вождаться возрастанием СИ на
400 мл/(мин • м2]). В противном
случае наблюдаются признаки неа-
декватной тканевой оксигенации,
что требует трансфузии эритроцит-
ной массы или инотропной поддер-
жки с последующей гемотрансфу-
зией, которая не может быть вы-
полнена в срочном порядке. Таким
образом, показания к переливанию
цельной крови или эритроцитной
массы определяют индивидуально.
У большинства больных гемотранс-
фузия показана при снижении Ht <
< 30 %. У больных с низким кар-
диореспираторным резервом опти-
мальный гематокрит определяют с
учетом артериального транспорта
кислорода и состояния тканевой
оксигенации.
При интенсивной терапии у опе-
рированных больных широко испо-
льзуют кровесберегающие техноло-
гии. Для этого производят предопе-
рационную заготовку аутокрови и
аутоплазмы в предоперационном
периоде, забор и аутотрансфузию
крови во время операции и в ран-
нем послеоперационном периоде.
При операциях, протекающих с
планируемой массивной кровопоте-
рей, применяют селл-сейвер (cell-
saver) — сепаратор клеток кро-
ви, предназначенный для сбора и
трансфузии аутоэритроцитов. Ап-
парат транспортируют вместе с па-
циентом в отделение интенсивной
терапии и используют при про-
должающейся послеоперационной
кровопотере. У больных, опериро-
ванных в условиях ИК, дренажи
присоединяют к кардиотомному ре-
зервуару. При значительной крово-
потере в течение первых 8 ч со-
бранную в нем кровь после отмыва-
ния жидкой части используют для
гемотрансфузии. Поскольку при
кровотечении происходят травми-
рование и разрушение части эрит-
роцитов, трансфузия цельной кро-
ви, излившейся по дренажам, мо-
жет сопровождаться массивным
внутрисосудистым гемолизом.
Нашивная донорская плазма —
продукт обработки крови, поэтому
она содержит в готовом виде мно-
гие ценные вещества, однако ей
присущи и отрицательные свойства
крови: цитратная токсичность, аци-
доз, гиперкалиемия и др. При ин-
фузии нативной плазмы крови име-
ется риск таких осложнений, как
заражение вирусным гепатитом,
ВИЧ-инфекция; высока также ве-
роятность анафилактических реак-
ций. Наличие в ней чужеродных
лейкоцитов, когда не используются
лейкоцитарные фильтры, может
вызвать реакцию системного воспа-
лительного ответа, особенно при
введении больших объемов, поэто-
му ее использование у больных с
небольшой кровопотерей следует
ограничить, заменив растворами
кристаллоидных и синтетических
коллоидных растворов. Примене-
ние нативной плазмы оправдано
при острой гипо- и диспротеине-
мии и отсутствии синтетических
коллоидных растворов и растворов
альбумина.
Свежезамороженная плазма в от-
личие от нативной содержит факто-
ры свертывания: весь комплекс ста-
бильных факторов гемостаза, фиб-
ринолиза, системы комплемента
и пропердина, разномолекулярные
белковые комплексы, обеспечиваю-
щие онкотическое давление, анти-
тела, а также иммунологическую
составляющую крови. В этой связи
среди компонентов крови по объ-
ему применения в клинике этот
препарат занимает первое место
[Константинов Б.А. и др., 2000].
Показаниями к применению свеже-
замороженной плазмы являются
подготовка больных с дефицитом
факторов свертывания, острый
ДВС-синдром, послеоперационные
кровотечения, связанные с дефици-
том факторов свертывания.
Криопреципитат — концентриро-
ванная смесь плазменных факторов
свертывания крови, полученная из
свежезамороженной плазмы.
Основными показаниями к исполь-
зованию криопреципитата являют-
ся дефицит факторов свертывания
и послеоперационные кровотече-
ния.
Кристаллоидные растворы. Наи-
более часто в практике интенсив-
ной терапии используют изотони-
ческие растворы хлорида натрия и
лактата Рингера. Их способность к
увеличению ОЦК идентична. Они
легко проходят через сосудистую
мембрану и равномерно распреде-
ляются во внеклеточном простран-
стве. Исследования, проведенные у
пациентов, находящихся в критиче-
ском состоянии, показали, что че-
рез 1—2 ч после инфузии в сосуди-
стом русле остается менее 20 % вве-
денного объема кристаллоидов
[Lamke L.O. et al., 1976].
Несмотря на то что оба раствора
имеют низкий рН, для нейтрализа-
ции ацидоза обычно требуется вве-
дение небольших объемов щелоч-
ных растворов. Лактат натрия, со-
держащийся в растворе лактата
Рингера, не является кислотой, и
он метаболизируется в печени, пре-
вращаясь в бикарбонат, который
оказывает умеренный ощелачиваю-
щий эффект.
Растворы кристаллоидов неток-
сичны, их введение не приводит к
анафилактоидным реакциям. При
восполнении значительного дефи-
цита О ЦК только растворами крис-
таллоидов, когда вводят большие их
объемы, неизбежно возникновение
интерстициального отека, прежде
всего отека легких. Кроме того, не-
обходимо учитывать, что для вос-
полнения дефицита ОЦК раствора-
ми кристаллоидов объем инфузии
должен в 3—4 раза превышать объ-
ем кровопотери, поскольку они
равномерно распределяются во всех
жидкостных пространствах орга-
низма.
Гипертонический раствор хлорида
натрия. В результате инфузии ги-
пертонического раствора NaCl при-
рост объема внеклеточного про-
странства существенно превышает
объем введенного раствора, что
обусловлено перемещением воды
из внутриклеточного пространства.
Положительный гемодинамический
эффект гипертонического раствора
натрия объясняется не только уве-
личением ОЦК. Есть данные о том,
что он обладает положительным
инотропным эффектом и снижает
ОПСС и сопротивление легочных
сосудов за счет расширения прека-
пилляров [Wildenthal К. et al., 1969].
Его положительный терапевтиче-
ский эффект объясняют также по-
вышением венозного тонуса, кото-
рое обусловлено вагусным рефлек-
сом, запускаемым при попадании
гипертонического раствора в сосу-
ды малого круга кровообращения
[Gazitua et al., 1971]. Следует, одна-
ко, учитывать, что введение гипер-
тонического раствора натрия может
приводить к гиперосмолярности,
гипернатриемии, гиперхлоремиче-
скому ацидозу и гипокалиемии. В
результате дегидратации головного
мозга могут возникать такие клини-
ческие симптомы, как дезориента-
ция, оглушенность, судороги. У бо-
льных с низкими резервами произ-
водительности сердца может разви-
ться отек легких. В связи с этим не-
контролируемое введение гиперто-
нического раствора натрия хлорида
недопустимо. Данный препарат
можно вводить, пока сывороточная
концентрация натрия не превышает
150 ммоль/л, а осмолярность сыво-
ротки крови — 350 мосмоль/л.
Коллоидные растворы. Альбумин
является основным белком, кото-
рый образуется в печени и состав-
ляет около 50 % ее синтетической
функции. Альбумин занимает поч-
ти 50 % от общего состава белков
плазмы и обеспечивает от 2/3 до 2/4
КОД плазмы.
Увеличение КОД и объема цир-
кулирующей крови в результате ин-
фузии раствора альбумина зависит
от его концентрации. Выпускают
2,5 %, 5 %, 10 %, 20 % и 25 % рас-
творы альбумина. В 1 л 5 % раство-
ра содержится 50 г альбумина, что
создает КОД, составляющий 20 мм
рт.ст. Выпускается также 25 % рас-
твор, содержащий 12,5 г альбумина
в 50 мл раствора, что создает КОД,
составляющий около 100 мм рт.ст.
Инфузия альбумина приводит к эф-
фективному восполнению дефици-
та ОЦК и стабилизации гемодина-
мики. Инфузия 500 мл 5 % раствора
альбумина увеличивает ОЦК на
450—600 мл [Lamke L.O. et al.,
1976]. При нормальной капилляр-
ной проницаемости через 2 ч в со-
судистом русле остается 90 % вве-
денного раствора альбумина. При
острой гиповолемии предпочтение
отдают 5 % раствору альбумина, а
25 % раствор обычно используют у
больных с сочетанием гиповолемии
и повышенного объема внеклеточ-
ной жидкости.
Длительность гемодинамического
эффекта, обусловленного инфузией
раствора альбумина, различна при
разных патологических состояниях.
В некоторых случаях наблюдаются
значительный переход альбумина в
интерстициальный сектор и его на-
копление в коже или интерстициа-
льном пространстве легких.
Частота анафилактических реак-
ций, связанных с инфузией альбу-
мина, составляет примерно 0,11 %
[Ring J. et al., 1977]. Риск зараже-
ния гепатитом отсутствует, поско-
льку во время приготовления рас-
твора его держат при температуре
60 °С в течение 10 ч. Отсутствует
также риск передачи ВИЧ-инфек-
ции. Есть указания на то, что при
введении больших объемов раство-
ров альбумина может понижаться
сывороточная концентрация иони-
зированного кальция, что приводит
к отрицательному инотропному эф-
фекту.
Альбумин обладает некоторыми
уникальными эффектами, отличаю-
щими его от синтетических коллои-
дов и кристаллоидов: способностью
регулировать содержание во вне-
клеточном пространстве различных
веществ, таких как железо и били-
рубин, блокировать свободные ра-
дикалы, что сопровождается подав-
лением перекисного окисления
липидов, связывать различные
токсичные вещества, образующиеся
при воспалительном процессе, вли-
ять на проницаемость микрососу-
дов для молекул других белков.
Восполнение уровня альбумина со-
провождается нормализацией про-
ницаемости эндотелия. Благода-
ря вышеперечисленным свойствам
альбумина многие врачи отдают
ему предпочтение перед другими
плазмозамещающими растворами.
Существенным фактором, ограни-
чивающим широкое применение
растворов альбумина, является их
высокая стоимость.
Декстраны представляют собой
смесь полимеров глюкозы различ-
ной величины и молекулярной мас-
сы. Чаще всего в клинической
практике используют декстран-70
(макродекс, полиглюкин) и декст-
ран-40 (реомакродекс или реопо-
лиглюкин).
Инфузия декстрана приводит к
увеличению объема плазмы. Длите-
льность и степень этого увеличения
определяются общим объемом ин-
фузии, скоростью инфузии, моле-
кулярной массой и клиренсом пре-
парата из плазмы. Мелкие молеку-
лы декстрана очень быстро филь-
труются почками, приводя к уме-
ренному диуретическому эффекту,
или проходят через эндотелий в ин-
терстициальное пространство, от-
куда в последующем возвращаются
в кровоток по лимфатическим пу-
тям. Крупные молекулы декстрана
недолго хранятся в гепатоцитах,
клетках почечных канальцев и
ретикулоэндотелиальной системы.
Они не обладают токсическим эф-
фектом и постепенно метаболизи-
руются в углекислоту и воду.
Инфузия декстрана-70 сопровож-
дается более продолжительным эф-
фектом, чем декстана-40. Через 3 ч
в плазме остается 70 % введенного
декстрана-70, а через 24 ч — 30 %
[Thompson W.L. et al., 1975]. После
введения 1 л декстрана-70 больным
в раннем послеоперационном пери-
оде в среднем объем плазмы увели-
чивается на 790 мл. Это сравнимо с
эффектом от введения аналогично-
го объема 6 % гидроксиэтилкрахма-
ла и больше, прироста ОЦК в резу-
льтате введения аналогичного объе-
ма 5 % альбумина.
У декстрана-40 онкотическое
давление выше, чем у 6 % декстра-
на-70, однако вследствие его очень
быстрого выведения почками уве-
личение объема плазмы непродол-
жительно. У пациентов с нормаль-
ной функцией почек уже через 6 ч
60 % декстрана-40 выводится с мо-
чой [Arturson G. et al., 1964]. У па-
циентов, находящихся в критиче-
ских состояниях, помимо увеличе-
ния объема плазмы, наблюдается
улучшение микроциркуляции. Оба
препарата снижают вязкость крови
и, таким образом, за счет улучше-
ния периферического кровотока
приводят к улучшению тканевой
оксигенации. У пациентов с нару-
шенной микроциркуляцией и рео-
логией крови эти эффекты декстра-
на-40 имеют большое значение и
используются для профилактики
тромботических осложнений в ран-
нем послеоперационном периоде.
Значительный объем декстрана-
40 фильтруется в почках и поступа-
ет в почечные канальцы. Это суще-
ственно повышает вязкость мочи.
В связи с тем что канальцевая реаб-
сорбция воды при этом не прекра-
щается, декстран может приводить
к необратимой закупорке почечных
канальцев и острой почечной недо-
статочности [Mailloux L. et al.,
1967]. Вероятность повреждения
почек повышается при нарушении
их функции или обезвоживании ор-
ганизма, поэтому следует избегать
введения декстрана-40 больным с
почечной недостаточностью.
Декстран-70 реже вызывает раз-
витие острой почечной недостаточ-
ности, возможно, потому, что зна-
чительно меньшая часть его моле-
кул фильтруется гломерулами почек
[Feest T.G. et al., 1976].
Частота анафилактоидных реак-
ций на декстраны составляет около
0,032 % [Ring J. et al., 1977]. Тяже-
лые реакции возникают приблизи-
тельно в 0,008 % случаев; обычно
они развиваются в течение 5 мин
после начала инфузии декстрана.
К побочным эффектам декстра-
нов относят также снижение факто-
ров свертывания за счет гемодилю-
ции, покрытия внутренней стенки
сосудов и клеточных элементов, а
также нарушения образования фиб-
ринового сгустка. Декстран-40 при-
водит к нарушениям свертывающей
системы крови в большей степени,
чем декстран-70. В целях снижения
риска кровотечений объем инфузи-
руемого декстрана должен быть
ограничен до 20 или 1,5 г/(кг • сут)
[Alik M. et al., 1967]. Нельзя забы-
вать, что геморрагические осложне-
ния могут возникать у пациентов с
предрасположенностью к ним, на-
пример с тромбоцитопенией. Паци-
ентами высокого риска считают бо-
льных с почечной недостаточно-
стью, поскольку у них возможны
сочетание уремической дисфунк-
ции тромбоцитов и значительное
увеличение периода полувыведения
декстрана.
Растворы гидроксиэтилкрахмала.
В клинической практике использу-
ют 6 % и 10 % растворы гидрокси-
этилкрахмала (ГЭК) в изотониче-
ском растворе натрия хлорида.
Наиболее часто применяют следую-
щие формы растворов ГЭК: гемохес
(B.Braun), HAES-стерил, плазма
стерил (Фрезениус), инфукол (Зе-
рум-Верк) и др. Фармакокинетика
их сложна вследствие неоднородно-
сти молекулярной массы и различ-
ной степени гидроксиэтилирования
вещества, содержащегося в рас-
творе. Молекулы с мол.м. менее
50 000 Да очень быстро экскретиру-
ются почками и распределяются в
различных тканях организма. Мо-
лекулы с большей массой могут
также попадать в различные ткани
организма, а также захватываться
клетками ретикулоэндотелиальной
системы или разрушаться амилазой
крови с последующим выведением
с мочой или желчью. У нормальных
индивидуумов 46 % из 500 мл вве-
денного 6 % раствора ГЭК выво-
дится с мочой в течение 2 сут, а
остальные 54 % — в течение 6 сут
[Yacobi A. et al., 1982]. Ткани с от-
носительно высокой активностью
макрофагов, например печень и се-
лезенка, захватывают небольшое
количество гидроксиэтилкрахмала
и задерживают его на довольно
длительный период времени. Нали-
чие молекул ГЭК в клетках ретику-
лоэндотелиальной системы не угне-
тает их функцию [Shatney C.H.,
1984]. Несмотря на то что его моле-
кулы попадают также в клетки эпи-
телия почечных канальцев, появля-
ющиеся морфологические измене-
ния не сопровождаются функцио-
нальными нарушениями [Shat-
ney С.Н. et al., 1984].
ГЭК является очень эффектив-
ным плазмозамещающим препара-
том. Прирост объема плазмы зна-
чительно больше объема инфузиру-
емого раствора. Через 24 ч после
введения 1000 мл препарата объем
плазмы в среднем превышает ис-
ходный на 285 мл, причем эф-
фективность гидроксиэтилкрахмала
сравнима с альбумином или даже
выше, что объясняется более высо-
ким КОД 6 % раствора ГЭК.
Объем вводимого раствора ГЭК
обычно подбирают индивидуально.
Обычно для ликвидации гиповоле-
мии достаточно введения 500—1000
мл, однако у больных с продолжаю-
щимся кровотечением или септиче-
ским шоком для стабилизации ге-
модинамики могут потребоваться
значительно большие объемы. Не-
смотря на высокие вводимые объ-
емы, препарат не оказывает отри-
цательного влияния на функцию
почек, печени или легких. Изуче-
ние влияния раствора ГЭК на свер-
тывающую систему крови в услови-
ях клиники свидетельствует об от-
сутствии значительных коагулоло-
гических изменений, а имеющиеся
сдвиги в состоянии свертывающей
системы крови объясняются эф-
фектом гемодилюции. Несмотря на
это, не рекомендуется превышать
дозу 20 мл/(кг • сут). Частота ана-
филактоидных реакций на ГЭК не-
высока. Сообщается о 14 реакциях
на 16 405 инфузий, что составляет
0,085 % [Ring J. et al., 1977].
После введения ГЭК нередко по-
вышается уровень сывороточной
амилазы. Гиперамилаземия может
привести к ошибочной постановке
диагноза панкреатита. Вместе с тем
данных об отрицательном влиянии
препарата на поджелудочную желе-
зу нет. При подозрении на наличие
панкреатита у больных, получав-
ших гидроксиэтилкрахмал, реко-
мендуют ориентироваться на сыво-
роточную концентрацию липазы
или динамику уровня амилазы
[Mishler J.M. et al., 1977].
Препараты желатина. В послед-
ние годы разработаны новые препа-
раты из желатина; одной из раз-
новидностей модифицированного
жидкого желатина является гелофу-
зин (B-Braun). Отечественный ана-
лог — модежель.
Гелофузин — 4 % раствор жела-
тина (модифицированный жидкий
желатин) в растворе хлорида на-
трия. Желатин получают из колла-
геновой ткани (хрящей) крупного
рогатого скота методом термиче-
ской деградации, гидролиза и сук-
цинирования. Это плазмозамещаю-
щий раствор с периодом полувыве-
дения около 9 ч, имеющий сред-
нюю мол.м. около 30 000 Да, колло-
идно-осмотическое давление (КОД)
453 мм вод.ст., или 33,3 мм рт.ст., и
осмолярность 274 мосм/л.
В проспективном рандомизиро-
ванном исследовании [Beards S.C.
et al., 1994] сравнивали инфузию
500 мл гелофузина и гидроксиэтил-
крахмала Hespan, которые вводили
в течение 10 мин пациентам с гипо-
волемическим шоком. Положитель-
ный гемодинамический эффект, за-
ключавшийся в возрастании произ-
водительности сердца и артериаль-
ного транспорта кислорода при не-
котором снижении концентрации
гемоглобина, отмечен в обеих груп-
пах. Авторами не получено стати-
стически достоверных различий
между гемодинамическими реакци-
ями на введение сравниваемых пре-
паратов.
Согласно данным Марютина и
соавт. (1997), у пациентов с продол-
жающейся кровопотерей, получав-
ших гелофузин, полиглюкин или
гидроксиэтилкрахмал, наибольший
волемический эффект наблюдался
при использовании гидроксиэтил-
крахмала, однако при анализе по-
казателей гемостаза и количества
геморрагических рецидивов выяв-
лено несомненное преимущество
гелофузина. Раствор модифициро-
ванного жидкого желатина не влия-
ет на свертывающую систему кро-
ви, даже если объем инфузий пре-
вышает 4 л за 24 ч [Edwards J.D. et
al., 1987]. Есть указания на особые
его преимущества при исходной ги-
покоагуляции и/или тромбоцитопе-
нии, а также в ситуациях с высоким
риском развития ДВС-синдрома
[Марютин и др., 1998]. Считается,
что гелофузин при инфузионной
терапии гиповолемических состоя-
ний различного генеза у больных
хирургического профиля оказывает
стойкий волемический и гемодина-
мический эффект, устраняет мик-
роциркуляторные нарушения и
улучшает газотранспортную функ-
цию крови [Beards S.C. et al., 1994].
Особого внимания заслуживает
преимущество препаратов желати-
на по сравнению с другими синте-
тическими коллоидами у больных с
почечной недостаточностью. В ра-
боте H.Kohler (1979) показано, что
при снижении уровня клубочковой
фильтрации с 90 до 0,5 мл/мин пе-
риод полувыведения препаратов
желатина увеличивается менее чем
в 2 раза, гидроксиэтилкрахмала —
в 2,5 раза, а декстрана-40 — в
7,5 раза. Более того, имеются ука-
зания на то, что у больных с ану-
рией усиление элиминации ГЭК в
печени может приводить к разви-
тию портальной гипертензии и ас-
цита.
Поскольку концентрация натрия
в растворе гелофузина составляет
154 ммоль/л, нельзя забывать о воз-
можности избыточного накопления
этого электролита в организме па-
циентов с почечной недостаточно-
стью.
Частота анафилактических реак-
ций на препараты модифицирован-
ного жидкого желатина составляет
от 1 на 6000 до 1 на 13 000 случаев.
Такие реакции являются результа-
том выброса большого количества
вазоактивных субстанций и чаще
наблюдаются у лиц, предрасполо-
женных к аллергии [Ring J. et al.,
1977].
Имеются публикации о возмож-
ном негати
Дата добавления: 2015-02-06 | Просмотры: 908 | Нарушение авторских прав
1 | 2 | 3 |
|



 В учебниках по сердечно-сосуди-
В учебниках по сердечно-сосуди-
