|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
БРОЖЕНИЕ И ДЫХАНИЕ РАСТЕНИЙ
6.1. Брожение
Первый этап, то есть гликолиз, одинаков при брожении и дыхании. Поворотным моментом является образование пировиноградной кислоты. Впервые Л. Пастер показал, что в присутствии кислорода брожение у дрожжей заменяется дыханием. Дело в том, что для брожения необходим НАДН, который в аэробных условиях окисляется. Это явление характерно и для высших растений и получило название эффекта Пастера. В зависимости от конечного продукта различают разные типы брожения: спиртовое и молочнокислое. В присутствии кислорода может происходить уксуснокислое брожение.
6.2. Дыхание
Дыхание – это окислительный распад органических веществ при участии кислорода с образованием воды, углекислого газа и макроэргических соединений, которые используются клетками.
6.2.1. Субстраты дыхания Дыхательный коэффициент – это объемное или молярное отношение СО2, выделившегося в процессе дыхания, к поглощенному за это же время О2. При нормальном доступе кислорода величина коэффициента зависит от субстрата дыхания. Если используются углеводы, то коэффициент равен 1. Если разложению подвергаются более окисленные соединения, например, органические кислоты, то поглощение кислорода уменьшается и коэффициент становится больше 1. Так, при использовании яблочной кислоты он равен 1,33. При окислении более восстановленных соединений (жиры, белки) требуется больше кислорода и коэффициент становится меньше 1. Например, при использовании жиров коэффициент равен 0,7. При недостатке углеводов используются другие субстраты. Особенно это проявляется при прорастании семян, в которых запасными питательными веществами являются белки и жиры. Белки предварительно расщепляются до аминокислот. Затем аминокислоты окисляются до ацетилкоэнзима А и кетокислот, которые участвуют в цикле Кребса. Жиры гидролизуются липазой до глицерина и жирных кислот. Глицерин фосфорилируется и затем окисляется до 3-фосфоглицеринового альдегида, который включается в обмен углеводов. Жирные кислоты окисляются с образованием ацетилкоэнзима А.
6.2.2. Оксиредуктазы Окисление дыхательных субстратов в ходе дыхания осуществляется с участием ферментов. Они называются оксиредуктазами, так как окисление одного вещества (донора электронов и протонов) сопряжено с восстановлением другого вещества (акцептора). Различают следующие группы ферментов. Анаэробные или пиридиновые дегидрогеназы. Это двухкомпонентные ферменты, коферментом которых является НАД или НАДФ. Они передают электроны различным акцепторам, но не кислороду и отнимают два протона от субстрата. Один протон присоединяется к коферменту, а другой выделяется в среду. В зависимости от белковой части различают более 150 ферментов. Аэробные или флавиновые дегидрогеназы. Они катализируют отнятие двух протонов от субстратов и передают электроны от анаэробных дегидрогеназ разным акцепторам (хиноны, цитохромы), в том числе и кислороду. Простетической группой служат производные витамина В2 – флавинадениндинуклеотид и флавинмононуклеотид. Оксидазы. Эти ферменты передают электроны от субстрата только на кислород. При этом образуются вода (переносятся на О2 4 электрона), перекись водорода (Н2О2) или супероксидный анион кислорода (О-2). Н2О2 и О-2 весьма токсичны и поэтому быстро превращаются в воду и кислород под действием каталазы и супероксиддисмутазы, соответственно. Оксигеназы. Они активируют кислород и катализируют его присоединение к различным органическим соединениям (аминокислоты, фенолы, ненасыщенные жирные кислоты, ксенобиотики – чужеродные токсичные вещества).
6.2.3. Гликолитический путь Этот путь дыхательного обмена состоит из двух фаз – анаэробной (гликолиз) и аэробной (цикл Кребса).
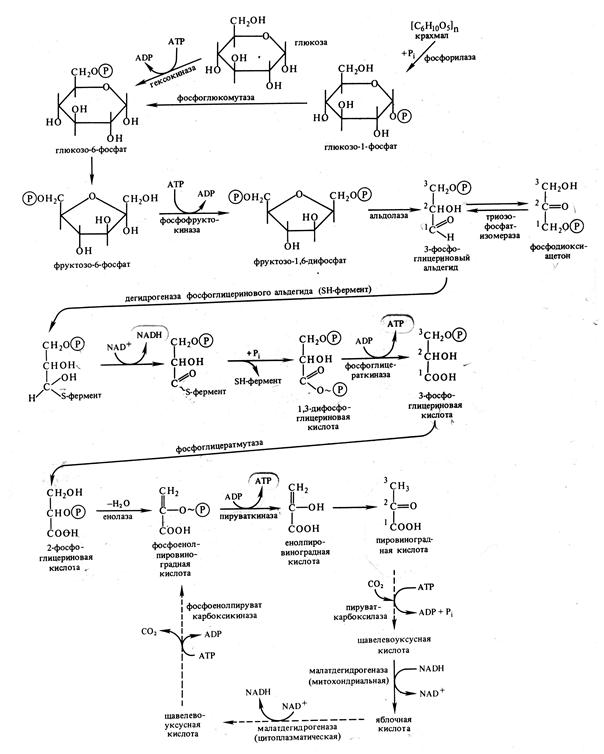
6.2.3.1. Гликолиз Реакции гликолиза идут в цитозоле и в хлоропластах. В результате гликолиза из одной молекулы глюкозы образуется 2 молекулы пировиноградной кислоты и 4 молекулы АТФ (рис. 6.1). Поскольку макроэргическая связь формируется прямо на окисляемом субстрате, такой процесс образования АТФ получил название субстратного фосфорилирования. Две молекулы АТФ покрывают расход на первоначальное активирование субстрата за счет фосфорилирования. Следовательно, накапливаются 2 молекулы АТФ. Кроме того, в ходе гликолиза восстанавливаются 2 молекулы НАД до НАДН, окисление которых в электронтранспортной цепи митохондрий приводит к синтезу 6 молекул АТФ. Итого образуются 8 молекул АТФ. Образовавшиеся 2 молекулы пировиноградной кислоты вступают в аэробную фазу дыхания.
Рис. 6.1. Этапы гликолиза. Пунктиром обозначены обходные пути при обращении гликолиза (по В. В. Полевому).
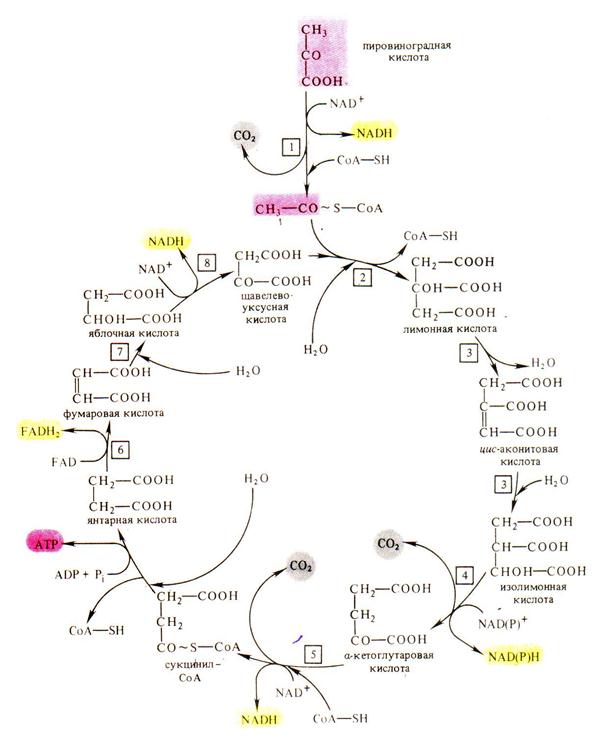
6.2.3.2. Цикл ди- и трикарбоновых кислот (цикл Кребса) Аэробная фаза дыхания локализована в митохондриях. Пировиноградная кислота окисляется до воды и углекислого газа в дыхательном цикле, получившем название цикла ди- и трикарбоновых кислот или цикла Кребса в честь английского биохимика Г. Кребса, описавшего этот путь (рис 6.2.). В этом цикле окисляется не сама пировиноградная кислота, а ее производное – ацетилкоэнзим А. Он образуется в результате окислительного декарбоксилирования пировиноградной кислоты. Процесс этот состоит из ряда реакций и катализируется сложной мультиферментной системой, состоящей из трех ферментов и пяти коферментов, и названной пируваткарбоксилазой.
Рис. 6.2. Цикл Кребса (цикл ди- и трикарбоновых кислот). 1 – мультиэнзимный комплекс окислительного декарбоксилирования пировиноградной кислоты, 2 – цитратсинтаза, 3 – аконитатгидратаза, 4 – изоцитратдегидрогеназа, 5 – мультиэнзимный комплекс окислительного декарбоксилирования α-кетоглутаровой кислоты, 6 – сукцинатдегидрогеназа, 7 – фумаратгидратаза, 8 – малатдегидрогеназа (по В. В. Полевому).
При окислении одной молекулы пировиноградной кислоты образуется 3 молекулы НАДН, 1 молекула НАДФН и 1 молекула ФАДН2, при окислении которых в дыхательной электронтранспортной цепи синтезируется 14 молекул АТФ. Кроме того, 1 молекула АТФ образуется в результате субстратного фосфорилирования.
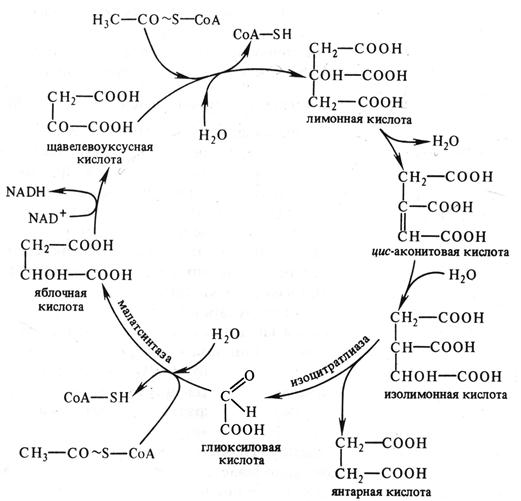
6.2.3.3. Глиоксилатный цикл Он является модификацией цикла Кребса и локализован не в митохондриях, а в глиоксисомах. В этих органеллах образуется изолимонная кислота, как и в цикле Кребса. Затем она под действием изоцитратлиазы распадается на глиоксиловую и янтарную кислоты. Глиоксиловая кислота реагирует со второй молекулой ацетилкоэнзима А с образованием яблочной кислоты, которая затем окисляется до щавелевоуксусной кислоты. Янтарная кислота выходит из глиоксисомы и превращается в щавелевоуксусную кислоту (рис. 6.3).
Рис. 6.3. Схема глиоксилатного цикла (по В. В. Полевому).
В ходе глиоксилатного цикла утилизируются две молекулы ацетилкоэнзима А, образовавшегося при распаде запасных жиров, и образуется одна молекула НАДН.
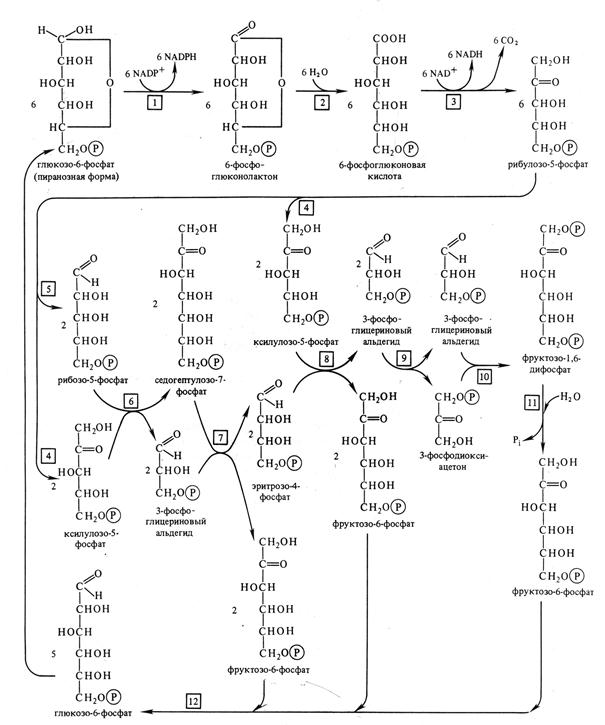
6.2.4. Апотомический путь Апотомический путь катаболизма гексоз (пентозофосфатный путь окисления глюкозы, гексозомонофосфатный цикл, пентозный шунт) происходит в цитоплазме и при отсутствии света в хлоропластах. Глюкоза фосфорилируется при участии гексокиназы до глюкозо-6-фосфата. Он окисляется глюкозо-6-фосфатдегидрогеназой. При этом образуются восстановленный НАДФН и лактон фосфоглюконовой кислоты. Лактон произвольно или при участии глюконолактозы гидролизуется до 6-фосфоглюконовой кислоты. Она под действием фосфоглюконатдегидрогеназы с коферментом НАДФ декарбоксилируется с образованием восстановленного НАДФН и пятиуглеродного сахара рибулозо-5-фосфата. Отсюда и название апотомический путь (апотомия – усекновение). Последующие реакции представляют цикл регенерации исходного субстрата – глюкозо-6-фосфата. Для прохождения полного цикла необходимы три молекулы глюкозо-6-фосфата. Как видно из рис. 6.4, из 6 молекул глюкозо-6-фосфата образуются 6 молекул СО2 и 6 молекул рибулозо-5-фосфата, из которых восстанавливается 5 молекул глюкозо-6-фосфата. При этом также образуется 12 молекул НАДФН, которые при окислении в дыхательной электронтранспортной цепи могут дать 36 молекул АТФ, что не уступает энергетическому выходу гликолитического пути. Продукты апотомического пути также участвуют в обмене веществ.
Рис. 6.4. Пентозофосфатный цикл. 1 – глюкозо-6-фосфатдегидрогеназа, 2 – глюконолактоназа, 3 - фосфоглюканатдегидрогеназа (декарбоксилирующая), 4 – фосфопентоэпимераза, 5 - фосфопентоизомераза, 6 – транскетолаза, 7 – трансальдолаза, 8 – транскетолаза, 9 - триозофосфатизомераза, 10 – альдолаза, 11 – фосфатаза, 12 – гексозофосфатизомераза (по В. В. Полевому).
6.2.5. Прямое окисление сахаров Некоторые бактерии, грибы и морские водоросли способны окислять нефосфорилированную глюкозу. Сначала a-глюкоза превращается в b-форму при участии мутаротазы. Затем флавинзависимая глюкооксидаза отнимает 2 атома водорода от группировки СНОН 1-го атома углерода глюкозы и переносит их на молекулярный кислород, образуя перекись водорода. Она разлагается каталазой и пероксидазой. Глюкоза при этом превращается в лактон глюконовой кислоты, который неферментативно гидратируется с образованием глюконовой кислоты. Глюконовая кислота после фосфорилирования распадается на пировиноградную кислоту и 3-фосфоглицериновый альдегид.
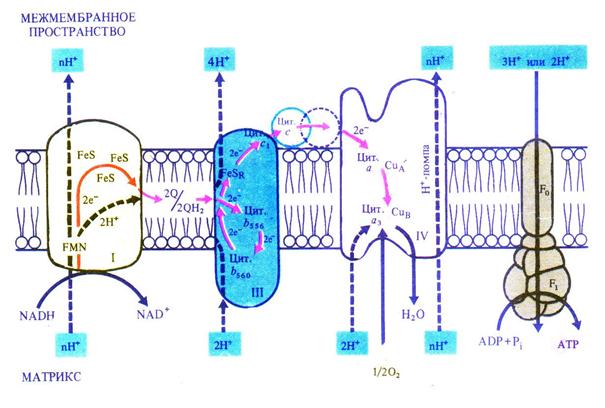
6.2.6. Дыхательная электронтранспортная цепь и окислительное фосфорилирование Дыхательная электронтранспортная цепь состоит из переносчиков электронов, которые передают электроны от субстратов на кислород. Расположение переносчиков определяется величиной их окислительно-восстановительного потенциала. Цепь начинается с НАДН, имеющего потенциал –0,32 В, и кончается кислородом с потенциалом +0,82 В. Переносчики расположены по обеим сторонам внутренней мембраны митохондрий и пересекают ее. На внутренней стороне мембраны, расположенной к матриксу митохондрии, два протона и два электрона от НАДН переходят на флавинмононуклеотид и железосерные белки. Флавинмононуклеотид, получив протоны, восстанавливается и переносит их на внешнюю сторону мембраны, где отдает протоны в межмембранное пространство. Железосерные белки, находящиеся внутри мембраны, передают электроны от НАДН окисленному убихинону Q. Он, присоединив еще два протона, диффундирует в мембране к цитохромам. Цитохром b 560 отдает два электрона убихинону, который, присоединив еще два протона из матрикса, передает два электрона цитохрому b 556 и два электрона цитохрому c 1, а протоны выходят в межмембранное пространство. На наружной стороне мембраны цитохром с, получив два электрона от цитохрома c 1, передает их цитохрому а, который переносит их через мембрану на цитохром а 3. Цитохром а 3, связывая кислород, отдает ему электроны. Кислород присоединяет два протона с образованием воды (рис. 6.5).
Рис. 6.5. Локализация электрон- и протонтранспортных реакций во внутренней мембране митохондрий (по В. В. Полевому).
Таким образом, транспорт электронов в дыхательной электронтранспортной цепи сопровождается трансмембранным переносом протонов. Возникающая разность потенциалов по обеим сторонам внутренней мембране митохондрий используется для синтеза АТФ (окислительное фосфорилирование), как это было показано в разделе 5.2.2. В результате прохождения двух электронов по цепи образуется 3 молекулы АТФ.
6.2.7. Влияние внешних и внутренних факторов на дыхание Температура. Дыхание у некоторых растений идет и при температуре ниже 0оС. Так, хвоя ели дышит при –25оС. Интенсивность дыхания, как всякой ферментативной реакции, возрастает при повышении температуры до определенного предела (35-40оС). Кислород необходим для осуществления дыхания, так как он является конечным акцептором электронов в дыхательной электронтранспортной цепи. Увеличение содержания кислорода в воздухе до 8-10 % сопровождается повышением интенсивности дыхания. Дальнейшее увеличение концентрации кислорода существенно не влияет на дыхание. Однако в атмосфере чистого кислорода дыхание растений снижается, а при длительном его действии растение погибает. Гибель растения обусловлена усилением в клетках свободнорадикальных реакций и повреждением мембран вследствие окисления их липидов. Углекислый газ является конечным продуктом дыхания. При высокой концентрации газа дыхание растений снижается по следующим причинам: 1) ингибируются дыхательные ферменты, 2) закрываются устьица, что препятствует доступу кислорода к клеткам. Содержание воды. Водный дефицит растущих тканей увеличивает интенсивность дыхания из-за активации распада сложных углеводов (например, крахмала) на более простые, которые являются субстратом дыхания. Однако при этом нарушается сопряжение окисления и фосфорилирования. Дыхание в этом случае представляет бесполезную трату вещества. Иная закономерность характерна для органов, находящихся в состоянии покоя. Повышение содержания воды в семенах приводит к резкому увеличению интенсивности дыхания. Свет. Трудно выявить влияние света на дыхание зеленых растений, так как одновременно с дыханием осуществляется противоположный процесс – фотосинтез. Освещенность, при которой интенсивность фотосинтеза равна интенсивности дыхания по уровню поглощенного и выделенного углекислого газа, называют компенсационным пунктом. Дыхание незеленых тканей активируется светом коротковолновой части спектра, так как максимумы поглощения флавинов и цитохромов расположены в области 380-600 нм. Минеральные вещества. Такие элементы как фосфор, сера, железо, медь, марганец необходимы для дыхания, являясь составной частью ферментов или как фосфор промежуточным продуктом. При повышении концентрации солей в питательном растворе, на котором выращивают проростки, их дыхание активируется (эффект «солевого дыхания»). Механическое повреждение усиливает дыхание из-за быстрого окисления фенольных и других соединений, которые выходят из поврежденных вакуолей и становятся доступными для оксидаз. Изменение интенсивности дыхания в онтогенезе. У с ветолюбивых растений более высокая интенсивность дыхания по сравнению с теневыносливыми. Растения северных широт дышат более интенсивно, чем южные, особенно при пониженной температуре. Наиболее высока интенсивность дыхания у молодых активно растущих тканей и органов. После окончания роста дыхание листьев снижается до уровня, равного половине максимального и затем долго не меняется. При пожелтении листьев и в период, предшествующий полному созреванию плодов, у этих органов наблюдается активация синтеза этилена с последующим кратковременным усилением дыхания, которое называют климактерическим подъемом дыхания. Этилен увеличивает проницаемость мембран и гидролиз белков, что приводит к повышению содержания субстратов дыхания. Однако это дыхание не сопровождается образованием АТФ.
6.2.8. Взаимосвязь дыхания с другими процессами обмена Для дыхания нужны в качестве субстратов углеводы, которые образуются в ходе фотосинтеза. Многие промежуточные продукты дыхания необходимы для биосинтеза важнейших соединений. Триозофосфат, превращаясь в глицерин, может использоваться при синтезе жиров. Пировиноградная, кетоглутаровая и щавелевоуксусная кислоты путем аминирования превращаются в аланин, глютаминовую и аспарагиновую аминокислоты. Они используются при синтезе белков. Янтарная кислота дает основу для формирования порфиринового ядра хлорофилла. Ацетилкоэнзим А является исходным материалом для образования жирных кислот. Пентозы, образующиеся в ходе апотомического пути окисления, входят в состав нуклеотидов, нуклеиновых кислот, никотинамидных и флавиновых коферментов. Эритрозо-4-фосфат, реагируя с фосфоэнолпировиноградной кислотой, образует шикимовую кислоту, которая необходима для образования ароматических аминокислот, например, триптофана. Триптофан участвует в синтезе белков и является предшественником фитогормона 3-индолилуксусной кислоты.
Дата добавления: 2015-02-02 | Просмотры: 1619 | Нарушение авторских прав |