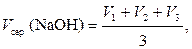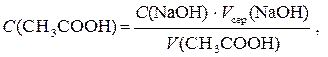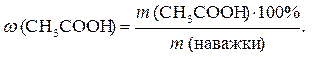|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Визначення масової частки оцтової кислотиЗа допомогою піпетки відібрати 10,0 мл розчину оцтової кислоти й перенести в конічну колбу ємністю 50 ̶ 100 мл, додати 2 ̶ 3 краплі фенолфталеїну й титрувати з бюретки робочим розчином натрій гідроксиду до появи блідо - рожевого забарвлення. Визначити (за шкалою бюретки) об'єм робочого розчину лугу, витраченого на титрування. Повторити титрування ще двічі та з одержаних результатів вирахувати середнє арифметичне значення об’єму NaOH V сер (NaOH):
де V 1, V 2, V 3 – об’єми розчину NaOH у паралельних титруваннях, мл.
Розрахунок масової частки оцтової кислоти:
1) знайти молярну концентрацію еквівалента оцтової кислоти в розчині:
де С (NaOH) – молярна концентрація розчину NaOH, моль/л, V (СН3СООН) – об’єм розчину оцтової кислоти, що був узятий для титрування, мл;
2) знайти масу оцтової кислоти в одному літрі розчину:
де М екв(СН3СООН) – молярна маса еквівалента СН3СООН, г/моль, V = 1л – об’єм розчину кислоти;
3) знайти масову частку оцтової кислоти в наважці (наважка – це певна маса концентрованої оцтової кислоти, з якої готувався 1 л розчину, що до-сліджувався):
Дата добавления: 2015-12-15 | Просмотры: 866 | Нарушение авторских прав 12 |