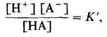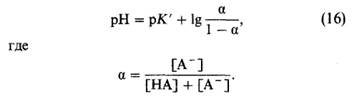|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Буферные системы крови, их характеристики и принцип действия.Общее понятие о буферных системах. Прежде всего необходимо вспомнить, что реакции диссоциации слабой кислоты НА на ионы водорода Н+ и сопряженное основание А- подчиняются закону действующих масс. Кинетику таких реакций описывает уравнение Подобное уравнение для буферных систем, выведенное из закона действующих масс, называется уравнением Гендерсона- Гассельбальха. Величина рK', так же как и К', -константа, характеризующая свойства системы (рК'= -lgK'). Уравнение можно представить в следующем виде:
Показателем способности системы, состоящей из слабой кислоты и сопряженного основания, создавать буферный эффект служит буферная емкость - величина, равная соотношению между количеством ионов Н+ или ОН+, добавленных в раствор, и изменением рН. Таким образом, буферная емкость раствора зависит от его концентрации и от разницы между рН и рК' этого раствора. Бикарбонатный буфер. Из имеющихся в крови буферных систем рассмотрим прежде всего бикарбонатную систему. Она включает относительно слабую угольную кислоту, образующуюся при гидратации СО2, и бикарбонат в качестве сопряженного основания. Регулируя напряжение СО2 в крови, дыхательная система обеспечивает высокое содержание компонентов буферной системы. Кроме того, органы дыхания вместе с бикарбонатным буфером образуют «открытую систему», в которой напряжение СО2 (а следовательно, и рН крови) может регулироваться путем изменения вентиляции легких. Фосфатный буфер. В фосфатной буферной системе, образованной неорганическими фосфатами крови, роль кислоты играет одноосновный фосфат H2PO4, а роль сопряженного основания-двухосновный фосфат НРО. Величина рК' фосфатного буфера (6,8) сравнительно близка к рН крови, однако емкость данного буфера невелика по причине низкого содержания фосфата в крови. Белковый буфер. Буферные свойства белков крови обусловлены способностью аминокислот ионизироваться. Концевые карбокси- и аминогруппы белковых цепей играют в этом отношении незначительную роль, так как таких групп мало и их рК' существенно отличаются от рН крови. Значительно больший вклад в создание буферной емкости белковой системы вносят боковые группы, способные ионизироваться, и особенно имидазольнов кольцо гистидина. К буферным белкам относятся как белки плазмы (в частности, альбумин), так и содержащийся в эритроцитах гемоглобин. На долю последнего приходится большая часть буферной емкости белковой системы, что связано как со значительной концентрацией гемоглобина, так и с относительно высоким содержанием в нем гистидина.
#72. Основные принципы классификации крови по системе AB0. Интерпретировать результаты с помощью синтетических цоликлонов. Группы крови. Совокупность эритроцитарных (агглютиногены) и плазменных (агглютинины) белков определяет разделение крови на группы. Из многочисленных типов классификации наиболее распространена Янского—Ландштейнера (АВО) и резус-принадлежность (Rh+ и Rh-). Открытие групп крови и Rh-фактора сделало возможным ее переливание от донора к реципиенту. Поддержание жидкого состояния крови является обязательным условием сохранения гомеостаза. Антисвертывающая система представлена совокупностью веществ, препятствующих образованию кровяного сгустка (тромб). Фибринолитическая система обеспечивает растворение уже образовавшегося тромба. Система классификации крови. Существуют разные виды классификации крови на группы. В основе разделения крови людей на группы в системе АВО лежит наличие в эритроцитах агглютиногенов (А, В), а в плазме крови агглютининов (α, β). При взаимодействии одноименных агглютиногенов и агглютининов происходит реакция гемагглютинации, т. е. склеивание эритроцитов. Изучение условий агглютинации эритроцитов привело к открытию групп крови и сделало возможным ее переливание. Агглютиногены возникают у человека еще в эмбриональном периоде развития. Агглютинины появляются позже, и титр их в сыворотке крови у детей первых недель после рождения очень низок. В зависимости от наличия или отсутствия в эритроцитах агглютиногенов А и В различают четыре группы крови: группу I, или 0 (α, β); группу II, или А (α); группу III, или В (β); группу IV, или АВ (в скобках указаны агглютинины). В сыворотке IV группы агглютининов α и β нет. Определение групп крови в системе АВО. Люди используют многие методы определения крови. Основными являются определение с помощью стандартных сывороток и с помощью синтетических цоликлонов. В настоящее время в клинике широко используют синтетические цоликлоны — растворы с аналогами агглютининов α и β. Этот метод более надежен и прост: агглютинация происходит прямо между одноименными агглютиногенами исследуемой крови и агглютининами цоликлонов. Эритротесты цоликлон анти-А (розовый цвет) и анти-В (синий цвет) предназначены для определения групп крови человека взамен стандартных изогемагглютинирующих сывороток. Для каждого определения группы крови достаточно применять по одной серии реагентов анти-А и анти-В.
#73. Возможные причины резус конфликта между матерью и плодом. Стандартные цоликлоны Резус-фактор. Кроме агглютиногенов, определяющих четыре названные группы крови (система АВО), эритроциты могут содержать в разных комбинациях и многие другие агглютиногены. Среди них особенно большое значение имеет резус-фактор. Причины резус конфликта между матерью и плодом. Rh-агглютиноген (резус-фактор) не имеет в плазме "врожденных" агглютининов. Они могут вырабатываться иммунной системой резус-отрицательного реципиента при переливании ему резус-положительной крови или организмом резус-отрицательной матери, беременной резус-положительным плодом, если плацента имеет дефекты, и вследствие нарушения ее барьерных функций кровь плода и матери смешиваются. В первом случае повторное переливание резус-несовместимой крови может привести к аутоиммунному гемолизу, так как резус-антитела являются сильнейшими гемолитическими ядрами. Во втором случае, если целостность плаценты нарушена, иммунная система матери вырабатывает резус-антитела к эритроцитам плода, что может привести к частичному, а при высоком титре антител к полному, гемолизу крови плода и его внутриутробной гибели. Метод определения резус-фактора крови. Классическая тепловая проба на водяной бане в настоящее время не проводится. В клинической лабораторной практике применяют экспресс-метод. Наденьте перчатки. Нанесите на тарелку по одной капле контрольной сыворотки (справа — К) и стандартной антирезус сыворотки (слева — Rh). Рядом с каждой сывороткой поместите по одной капле исследуемой крови (размер капли крови должен быть вдвое меньше, чем капля сыворотки). Последующие манипуляции должны начинаться с контрольной сыворотки, но не наоборот! (в противном случае пользоваться одним концом палочки нельзя). Стеклянной палочкой перемешайте каплю крови с каплей сыворотки (контрольной), образуя общую каплю размером с копеечную монету. Затем подобным же образом перемешайте кровь с антирезус-сывороткой. Покачивая тарелку, наблюдайте за реакцией. Для лучшего выявления наличия или отсутствия агглютинации можно добавить в обе пробы по капле физиологического раствора. Если исследуемая кровь резус-положительна, то в пробе со стандартной антирезус сывороткой наблюдается агглютинация эритроцитов (в контроле ее быть не должно). Если кровь резус-отрицательная, агглютинация отсутствует в обеих пробах. При возникновении агглютинации в пробе с контрольной сывороткой определение следует повторить либо проводить другими методами. Еще более прост метод определения Rh-фактра с помощью стандартных цоликлонов. Каплю стандартной сыворотки "цоли-клон анти-Д-супер" нанесите на сухое стекло. Добавьте 1 каплю исследуемой крови, смешайте. При наличии агглютинации кровь считают резус-положительной, а при отсутствии агглютинации — отрицательной.
#74. Физеологические основы переливания крови. Правила переливания. Гемотрансфузионные среды. Физиологические основы и правила переливания крови. 1. Прежде чем приступить к трансфузии, врач должен: а) Определить показания к трансфузии, выбрать трансфузионную среду. б) Определить групповую принадлежность крови больного с помощью стандартных сывороток или синтетических цоликлонов, независимо от того, имеются ли эти данные в выписке, истории болезни, паспорте и др. в) Определить групповую принадлежность крови донора из каждого флакона, предназначенного для переливания. г) Провести пробы на совместимость. 2. Во время трансфузии внимательно следят за: а) общим самочувствием больного; б) жалобами на боли в поясничной области; в) состоянием пульса, дыхания, артериального давления. 3. После трансфузии больному необходимо: а) соблюдать постельный режим в течение 2—3 ч; б) производить почасовое измерение температуры тела в течение 3 ч; в) сделать общий анализ крови; г) сделать общий анализ мочи; д) измерять диурез в течение суток (после массивных трансфузий и в тяжелых случаях реанимации и интенсивной терапии). 4. Подробно документировать в истории болезни и в журнале по форме № 9 операцию переливания крови, ее компонентов и кровезаменителей.
#75. Механизмы свертывания крови. Гемостаз — остановка кровотечения при повреждении стенки сосуда, которая является результатом спазма кровеносных сосудов и формирования кровяного сгустка. Система гемостаза включает в себя форменные элементы крови (главным образом тромбоциты), сосудистую стенку, плазменные факторы свертывания и противосвертывания. Важная роль в свертывании крови принадлежит биологически активным веществам, способствующим свертыванию крови, препятствующим свертыванию крови и разжижающим уже свернувшуюся кровь. Эти вещества содержатся в плазме и форменных элементах крови, а также в тканях, в том числе сосудистой стенки. В системе свертывания крови различают сосудисто-тромбоцитарный (первичный) и коагуляционный (вторичный) механизмы гемостаза. Cосудисто-тромбоцитарный гемостаз. Остановка кровотечения начинается с первичной реакции крови на травму ткани и сосуда, важнейшая роль в которой принадлежит тромбоцитам. Роль тромбоцитов в первичном гемостазе определяется их способностью прилипать к поверхности сосудистой стенки у места повреждения (адгезия), подвергаться биохимическим и структурным изменениям, высвобождать содержимое своих гранул (реакция освобождения) и склеиваться друг с другом (агрегация). Адгезия (прилипание) тромбоцитов происходит только к поврежденному эндотелию при контакте с соединительной тканью, главным образом с коллагеном. Механизм адгезии связан с дзета-потенциалом тромбоцитов: группы отрицательно заряженных сиаловых кислот на их мембране реагируют с положительно заряженными аминогруппами коллагена сосудистой стенки. Важную роль в адгезии тромбоцитов играют двухвалентные катионы и фактор Виллебранда (тканевый фактор, синтезируемый в эндотелии сосудов, для которого на тромбоцитах имеются специфические рецепторы). Агрегация и аккумуляция тромбоцитов являются следующим этапом образования гемостатической пробки. Главный стимулятор агрегации — АДФ, источником которой служат поврежденный эндотелий, разрушенные эритроциты и тромбоциты. Другим важным агрегирующим фактором является тромбин, вызывающий агрегацию в значительно меньших количествах, которые необходимы для свертывания крови. Следы тромбина, образовавшиеся при активации внешнего или внутреннего механизма гемостаза, резко усиливают освобождение АДФ и других пластиночных факторов, способствующих уплотнению тромбоцитарной пробки. Реакция освобождения является активным секреторным процессом, протекающим без повреждения мембраны и разрушения клеток. Освобождение может протекать в один или два этапа. Препятствуют агрегации: повышение уровня цАМФ в тромбоцитах; простагландины Ei и D2; простациклин (активный вазодилататор). Способствуют агрегации: снижение цАМФ в тромбоцитах; простагландины Е2, F2, тромбин, адреналин, эпинефрин. Формирование тромбоцитарной пробки (ретракция). Изменение формы тромбоцитов и ретракция (уплотнение) тромбоцитарной пробки происходят при обязательном участии актиномиозиноподобного сократительного белка — тромбостенина. Коагуляционный гемостаз и свёртывающая система крови. Свертывающая система крови — ферментативная система, обеспечивающая остановку кровотечения путем формирования фибриновых тромбов. А. Шмидт предложил двухфазную теорию свертывания, согласно которой в первой фазе образуется тромбин, а во второй под его влиянием фибриноген превращается в фибрин. А. Моравитц и соавт. открыли образование тромбопластинов в плазме и показали роль ионов кальция в превращении протромбина в тромбин. Это позволило сформулировать трехфазную теорию свертывания, согласно которой процесс протекает последовательно: в первой фазе образуется активная протромбиназа, во второй — тромбин, в третьей — появляется фибрин. Факторы свёртывания крови. Фибриноген - необходим для агрегации тромбоцитов; протромбин - образуется в печени с участием витамина К; тканевый тромбопластин - катализирует свертывание крови по внешнему механизму; кальций - участвует во всех фазах свертывания крови; АС-глобулин - белок, синтезируемый в печени и активируемый тромбином; проконвертин - гликопротеид, синтезируемый в печени при участии витамина К; фактор Кристмаса - способствует активации фактора Стюарта; фактор Стюарта—Прауэра - участвует в активации прототромбина; фактор Розенталя - способствует активации фактора Кристмаса; фактор Хагемана – активирует проконвертин и фактор Розенталя; фибринстабилизирующий фактор - стабилизирует фибрин; фактор Фитцджеральда - участвует в активации факторов Розенталя, Хагемана и плазминогена; фактор Флетчера —участвует в активации фактора Хагемана и плазминогена.
#76. Противосвертывающая система. Противосвёртывающая система крови. Одним из важнейших гомеостатических показателей является динамическое равновесие между свертывающей и противосвертывающей системами крови. В норме противосвертываюицие механизмы доминируют над свертывающими, что предотвращает спонтанное внутрисосудистое тромбо-образование. Процесс коагуляции ограничивается зоной повреждения сосудов и тканей и не распространяется на весь кровоток. Вместе с тем естественное минимальное тромбообразование компенсируется различными механизмами фибринолиза. Условно в организме человека выделяют первую и вторую противосвер-тывающие системы. Первая поддерживает кровь в жидком состоянии и препятствует спонтанному тромбообразованию (антитромбин III, гепарин, а2-макроглобулин, ai-антитрипсин). Вторая активируется в процессе свертывания крови, ограничивая его участком повреждения (нити фибрина, протеины S, С). Патологическая противосвертывающая система, представленная иммунными ингибиторами отдельных фаз свертывания (парапротеины, макро- и криоглобулины), появляется при некоторых заболеваниях и как осложнение лекарственной терапии. Фибринолитическая система крови. Фибринолиз— растворение фибрина — имеет огромное физиологическое значение. Благодаря ему из кровотока удаляется фибрин, рассасываются тромбы, образуются высокоактивные антикоагулянты и антиагреганты. Фибринолитической активностью обладают многие ткани и органы, в том числе легкие. Фибринолиз осуществляется протеолитической ферментной системой крови плазминоген — плазмин. Методы определения времени свертывания крови. Существует несколкьо методов определения времени свёртывания крови. Наиболее известные: Способ Мак-Магро, капельный способ, способ по Сухареву. Принцип двух последних заключается в определении времени спонтанного свёртывания крови и позволяет выявить грубый дефицит факторов свёртыванрия – фибриногена, антигемофильных глобулинов, протромбина. Методы определения времени кровотечения крови. Наиболее известный метод – это метод уколочной пробы по Дюке. В норме кровотечение должно длится 2-3 минуты.
#77 Какими методами можно проанализировать внешнее дыхание человека? Объясните, что позволяет врачу делать заключение об отклонении параметров внешнего дыхания от нормы. Изменение какого показателя внешнего дыхания будет свидетельствовать о сужении воздухоносных путей? Внешнее дыхание - газообмен между организмом и окружающим его атмосферным воздухом Внешнее дыхание представляет собой ритмический процесс, частота которого у здорового взрослого человека составляет 16-20 циклов в 1 мин. Основная задача внешнего дыхания заключается в поддержании постоянного состава альвеолярного воздуха — 14% кислорода и 5% углекислого газа. Дата добавления: 2015-12-15 | Просмотры: 1038 | Нарушение авторских прав |