|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Тромболитическая терапия и ангиопластика
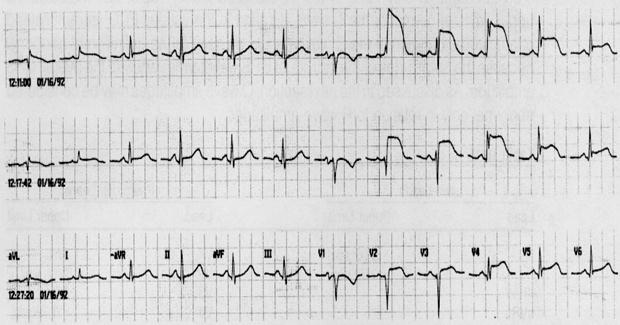
Тромболитическая терапия противопоказана больным с ОКС без подъемов сегмента ST, но она является наиболее распространенным в мире способом реперфузии при ИМ с подъемами сегмента ST. Тромболизис спасает 30 жизней на каждую 1000 пациентов, пролеченных в срок до 6 часов, и 20 жизней – в период 7-12 часов от возникновения боли в груди (Fibrinolytic Therapy Trialists’…, 1994). На этой статистике основываются рекомендации проводить тромболитическую терапию в отсутствие противопоказаний в пределах 12 часов от начала ИМ, предпочтительно в первые 6 часов. На рисунке 4 показана быстрая положительная динамика ЭКГ после применения тромболитика. Хотя вовремя проведенная тромболитическая терапия несомненно эффективна, она не восстанавливает коронарный кровоток примерно у 15% пациентов и, по меньшей мере, в 1% случаев вызывает внутрицеребральное кровотечение (The GUSTO Angiographic Investigators…, 1993; E.Keeley, C.Grines, 2004).
Рисунок 4. Быстрое уменьшение выраженности подъемов сегмента ST при проведении тромболитической терапии, указывающее на ее успешность.
Первичная ангиопластика существенно превосходит тромболизис в способности снижать смертность, частоту ИМ и инсульта независимо от применяемого фибринолитического препарата (E.Keeley, C.Grines, 2003). При выборе способа реперфузионной терапии при ИМ с подъемами сегмента ST следует помнить о преимуществах чрескожного коронарного вмешательства и недостатках тромболизиса. В сроки 6-12 ч от начала симптомов первичная ангиопластика (W.Wijns et al., 2010): · полнее устраняет симптомы ишемии; · чаще и лучше восстанавливает проходимость артерии; · реже сопровождается реокклюзией артерии; · лучше восстанавливает функцию левого желудочка; · обеспечивает лучшие клинические исходы. Кроме того, тромболизис нередко противопоказан, в ряде экономически развитых стран практически применяется только на догоспитальном этапе. К сожалению, доступность первичной ангиопластики в современном мире весьма ограничена. В этой ситуации возникла идея проводить простой и доступный тромболизис, а затем, при появлении возможности, ангиопластику. Результаты применения такой комбинированной терапии оказались разочаровывающими – частота смертельного исхода, ИМ, инсульта и больших кровотечений оказалась выше, чем при первичной ангиопластике (E.Keeley et al., 2006). Поэтому у пациентов, получавших тромботическую терапию, не проводится ангиопластика, если отсутствуют доказательства безуспешности тромболизиса. При получении таких доказательств возможно выполнение «ангиопластики спасения», которая улучшает выживаемость по сравнению с ограничением объема лечения только консервативными мероприятиями (A.Gershlick et al., 2005; T.Patel et al., 2006). В действующих Рекомендациях по реваскуляризации миокарда (W.Wijns et al., 2010) подчеркивается важность минимизации любых задержек на ранних этапах лечения ОКС c подъемами сегмента ST. 1. Если пациент госпитализирован (или находился в момент развития ОКС) в стационаре, в котором не выполняется первичная ангиопластика, а время до ее возможного проведения в другой клинике менее 2 часов, следует осуществить экстренную транспортировку. 2. Если время до ангиопластики превысит 2 часа, то следует ввести тромболитик и, все равно, при возможности организовать перевод больного в кардиохирургический центр. 3. В случаях стойкой элевации сегмента ST после тромболизиса более, чем наполовину от максимального начального повышения и/или сохраняющейся ангинозной боли в груди, следует немедленно рассмотреть возможность выполнения «ангиопластики спасения». 4. В случаях успешного тромболизиса пациент может быть подвергнут коронарной ангиопластике в течение 24 часов. 5. Более, чем через 3 дня от начала ОКС у больного с развившимся ИМ с Q-зубцом, реваскуляризация может выполняться при рецидивирующей стенокардии и/или документированной ишемией большой зоны жизнеспособного миокарда (более 10% массы левого желудочка). При выборе между ангиопластикой и коронарным шунтированием у больных с ОКС с подъемами сегмента ST следует учитывать следующие положения Рекомендаций (W.Wijns et al., 2010): · коронарное шунтирование показано при анатомических изменениях коронарных артерий, не позволяющих выполнить ангиопластику; · коронарное шунтирование показано при безуспешности попытки ангиопластики и угрозе некроза большой области сердца, должно выполняться в такой ситуации в срок до 3-4 часов; · в других случаях, когда нет персистирующих болей и нестабильности гемодинамики, оптимальный срок проведения коронарного шунтирования – через 3-7 дней от начала ИМ; · пожилой возраст, снижение фракции выброса левого желудочка и тяжелые сопутствующие заболевания ассоциируются с максимальным риском коронарного шунтирования. При острой сердечной недостаточности необходима эхокардиография для оценки функции левого желудочка и исключения опасных для жизни механических осложнений, которые требуют хирургической коррекции (митральная регургитация, разрыв межжелудочковой перегородки, разрыв свободной стенки и тампонада сердца). В таких случаях показана полная реваскуляризация методом ангиопластики всех критически стенозированных крупных коронарных артерий, при необходимости на фоне внутриаортальной балонной контрпульсации. При безуспешности ангиопластики показано экстренное коронарное шунтирование, но только при сохранении нестабильной гемодинамики или угрожающих жизни желудочковых аритмий на фоне распространенной ишемии (стеноз ствола левой коронарной артерии или трех основных ветвей) (W.Wijns et al., 2010).
Резюме
Реваскуляризация у больных с ОКС без подъемов сегмента ST и инвазивная или фармакологическая реперфузия у пациентов с ИМ и подъемами сегмента ST – эффективные способы сохранения жизни. Реваскуляризация превосходит консервативную терапию у пациентов с высоким и умеренным риском, однако при низком риске первоначально может проводиться оптимальное медикаментозное лечение. Тромболизис является основой реперфузионной терапии, а первичная ангиопластика предпочтительна, когда она реально доступна. Больные, у которых тромболитическая терапия оказалась успешной, должны в дальнейшем подвергаться риск-стратификации (определение толерантности к физической нагрузке, ограничиваемой ишемией, и эхокардиографическая оценка функции левого желудочка). Низкие показатели, полученные в результате такого обследования, указывают на потребность в дополнительной реваскуляризации. Пациенты, у которых попытка тромболизиса оказалась неудачной, нуждаются в быстром проведении ангиопластики.
Литература
Airoldi F, Colombo A, Morici N, et al. Incidence and predictors of drug-eluting stent thrombosis during and after discontinuation of thienopyridine treatment. Circulation 2007;116: 745–754. Anderson JL, Adams CD, Antman EM, et al. ACC/AHA 2007 Guidelines for the Management of Patients With Unstable Angina/Non–ST-Elevation Myocardial Infarction—Executive Summary. J Am Coll Cardiol 2007; 50: 652–726. Angiolillo DJ, Fernandez-Ortiz A, Bernardo E, et al. Identification of low responders to a 300-mg clopidogrel loading dose in patients undergoing coronary Stenting. Thromb Res 2005; 115: 101–108. Awata M, Kotani J, Uematsu M, et al. Serial angioscopic evidence of incomplete neointimal coverage after sirolimus-eluting stent implantation: comparison with bare-metal stents. Circulation 2007; 116: 910–916. Basalus MW, Ankone MJ, van Houwelingen GK, et al. Coating irregularities of durable polymer-based drug-eluting stents as assessed by scanning electron microscopy. EuroIntervention 2009; 5: 157–165. Bassand JP, Hamm CW, Ardissino D, et al. Guidelines for the diagnosis and treatment of non-ST-segment elevation acute coronary syndromes. The task force for the diagnosis and treatment of non-ST-segment elevation acute coronary syndromes of the European Society of Cardiology. Eur Heart J 2007; 28: 1598–1660. Bavry AA, Bhatt DL. Acute myocardial infarction and drug-eluting stents: a green light for their use or time for measured restraint? Am Heart J 2007; 153: 719–721. Bavry AA, Bhatt DL. Drug-eluting stents: dual antiplatelet therapy for every survivor? Circulation 2007; 116: 696–699. Bavry AA, Kumbhani DJ, Quiroz R, et al. Invasive therapy along with glycoprotein IIb/IIIa inhibitors and intracoronary stents improves survival in non-ST segment elevation acute coronary syndromes: a meta-analysis and review of the literature. Am J Cardiol 2004; 93: 830–835. Bavry AA, Kumbhani DJ, Rassi AN, et al. Benefit of early invasive therapy in acute coronary syndromes a meta-analysis of contemporary randomized clinical trials. J Am Coll Cardiol 2006; 48: 1319–1325. Beijk MA, Klomp M, Verouden N, et al. Genous endothelial progenitor cell capturing stent versus the Taxus Liberte stent in patients with de novo coronary lesions with a high-risk of coronary restenosis: a randomised, single-centre, pilot study. Eur Heart J 2010; 31: 1055–1064. Bhatt DL. To cath or not to cath: that is no longer the question. JAMA 2005; 293: 2935–2937. Bhatt DL, Roe MT, Peterson ED, et al. Utilization of early invasive management strategies for high-risk patients with non-ST-segment elevation acute coronary syndromes. Results from the CRUSADE quality improvement initiative. JAMA 2004; 292: 2096–2104. Boden WE, O’Rourke RA, Crawford MH, et al. Outcomes in patients with acute non-Q-wave myocardial infarction randomly assigned to an invasive as compared with a conservative management strategy. Veterans Affairs Non-Q-Wave Infarction Strategies in Hospital (VANQWISH) Trial Investigators. N Engl J Med 1998; 338: 1785–1792. Brodie BR, Stuckey T, Downey W, et al. Outcomes and complications with off-label use of drug-eluting stents: results from the STENT (Strategic Transcatheter Evaluation of New Therapies) group. J Am Coll Cardiol Intv 2008; 1: 405–414. Camenzind E, Steg PG, Wijns W. Stent thrombosis late after implantation of first-generation drug-eluting stents: a cause for concern. Circulation 2007; 115: 1440–1455. Cannon CP, Weintraub WS, Demopoulos LA, et al.; TACTICS (Treat Angina with Aggrastat and Determine Cost of Therapy with an Invasive or Conservative Strategy) – Thrombolysis in Myocardial Infarction 18 Investigators. Comparison of early invasive and conservative strategies in patients with unstable coronary syndromes treated with glycoprotein IIb/IIIa inhibitor tirofiban. N Engl J Med 2001; 344: 1879–1887. Clayton TC, Pocock SJ, Henderson RA, et al. Do men benefit more than women from an interventional strategy in patients with unstable angina or non-ST-elevation myocardial infarction? The impact of gender in the RITA 3 trial. Eur Heart J 2004; 25: 1641–1650. Daemen J, Keiichi T, Kristensen SD, et al. Two-year clinical follow-up of the unrestricted use of the paclitaxel-eluting stent compared with the sirolimus-eluting stent as part of the Taxus-Stent Evaluated at Rotterdam Cardiology Hospital (T-SEARCH) registry. Euro Intervention 2006; 2: 330–337. de Winter RJ, Windhausen F, Cornel JH, et al. Early invasive versus selectively invasive management for acute coronary syndromes. N Engl J Med 2005; 353: 1095–1104. Dotter CT, Judkins MP. Transluminal treatment of arteriosclerotic obstruction. Description of a new technic and a preliminary report of its application. Circulation 1964; 30: 654–670. Farb A, Boam AB. Stent thrombosis redux—the FDA perspective. N Engl J Med 2007; 356: 984–987. Ferguson JJ, Califf RM, Antman EM, et al. Enoxaparin vs unfractionated heparin in high-risk patients with non-ST-segment elevation acute coronary syndromes managed with an intended early invasive strategy: primary results of the SYNERGY randomized trial. JAMA 2004; 292: 45–54. Fibrinolytic Therapy Trialists’ Collaborative Group. Indications for fibrinolytic therapy in suspected acute myocardial infarction: collaborative overview of early mortality and major morbidity results from all randomized trials of more than 1,000 patients. Lancet 1994; 343: 311–322. Garg S, Serruys PW. Coronary stents. Current status. J Am Coll Cardiol 2010; 56: Suppl S: S1–S42. Garg S, Serruys PW. Coronary stents. Looking forward. J Am Coll Cardiol 2010; 56: Suppl S: S43–S78. Gershlick AH, Stephens-Lloyd A, Hughes S, et al. Rescue angioplasty after failed thrombolytic therapy for acute myocardial infarction. N Engl J Med 2005; 353: 2758–2768. Gruntzig A. Transluminal dilatation of coronary-artery stenosis. Lancet 1978; 1: 263. Guagliumi G, Musumeci G, Sirbu V, et al. Optical coherence tomography assessment of in vivo vascular response after implantation of overlapping bare-metal and drug-eluting stents. J Am Coll Cardiol Intv 2010; 3: 531–539. Hochman JS, McCabe CH, Stone PH, et al. Outcome and profile of women and men presenting with acute coronary syndromes: a report from TIMI IIIB. TIMI Investigators. Thrombolysis in Myocardial Infarction. J Am Coll Cardiol 1997; 30: 141–148. Hoffmann R, Mintz GS, Dussaillant GR, et al. Patterns and mechanisms of in-stent restenosis. A serial intravascular ultrasound study. Circulation 1996; 94: 1247–1254. Jabara R, Chronos N, Robinson K. Novel bioabsorbable salicylate-based polymer as a drug-eluting stent coating. Catheter Cardiovasc Interv 2008; 72: 186–194. James SK, Stenestrand U, Lindback J, et al. Long-term safety and efficacy of drug-eluting versus bare-metal stents in Sweden. N Engl J Med 2009; 360: 1933–1945. Jeremias A, Kirtane A. Balancing efficacy and safety of drug-eluting stents in patients undergoing percutaneous coronary intervention. Ann Intern Med 2008; 148: 234–238. Kandzari DE, Roe MT, Ohman EM, et al. Frequency, predictors, and outcomes of drug-eluting stent utilization in patients with high-risk non-ST-segment elevation acute coronary syndromes. Am J Cardiol 2005; 96: 750–755. Kedhi E, Joesoef KS, McFadden E, et al. Second-generation everolimus-eluting and paclitaxel-eluting stents in real-life practice (COMPARE): a randomised trial. Lancet 2010; 375: 201–209. Keeley EC, Boura JA, Grines CL. Comparison of primary and facilitated percutaneous coronary interventions for ST-elevation myocardial infarction: quantitative review of randomized trials. Lancet 2006; 367: 579–588. Keeley EC, Grines CL. Primary angioplasty versus intravenous thrombolytic therapy for acute myocardial infarction: a quantitative review of 23 randomised trials. Lancet 2003; 361: 13–20. Keeley EC, Grines CL. Primary coronary intervention for acute myocardial infarction. JAMA 2004; 291: 736–739. Kirtane AJ, Gupta A, Lyengar S, et al. Safety and efficacy of drug-eluting and bare metal stents: comprehensive meta-analysis of randomized trials and observational studies. Circulation 2009; 119: 3198–3206. Lagerqvist B, James SK, Stenestrand U, et al. Long-term outcomes with drug-eluting stents versus bare-metal stents in Sweden. N Engl J Med 2007; 356: 1009–1019. Lemesle G, Delhaye C, Sudre A, et al. Impact of high loading and maintenance dose of clopidogrel within the first 15 days after percutaneous coronary intervention on patient outcome. Am Heart J 2009; 157: 375–382. Marx SO, Marks AR. Bench to bedside: the development of rapamycin and its application to stent restenosis. Circulation 2001; 104: 852–855. Mehta SR, Cannon CP, Fox KA, et al. Routine vs selective invasive strategies in patients with acute coronary syndromes: a collaborative meta-analysis of randomized trials. JAMA 2005; 293: 2908–2917. Moliterno DJ. Healing Achilles—sirolimus versus paclitaxel. N Engl J Med 2005; 353: 724–727. Nordmann AJ, Briel M, Bucher HC. Mortality in randomized controlled trials comparing drug-eluting vs. bare metal stents in coronary artery disease: a meta-analysis. Eur Heart J 2006; 27: 2784–2814. Park SJ, Park DW, Kim YH, et al. Duration of dual antiplatelet therapy after implantation of drug-eluting stents. N Engl J Med 2010; 362: 1374–1382. Pasceri V, Patti G, Speciale G, et al. Meta-analysis of clinical trials on use of drug eluting stents for treatment of acute myocardial infarction. Am Heart J 2007; 153: 749–754. Patel TN, Bavry AA, Kumbhani DJ, et al. A meta-analysis of randomized trials of rescue percutaneous coronary intervention after failed fibrinolysis. Am J Cardiol 2006; 97: 1685–1690. Rensing BJ, Vos J, Smits PC, et al. Coronary restenosis elimination with a sirolimus eluting stent: first European human experience with 6-month angiographic and intravascular ultrasonic follow-up. Eur Heart J 2001; 22: 2125–2130. Rossini R, Capodanno D, Lettieri C, et al. Prevalence, predictors, and long-term prognosis of premature discontinuation of oral antiplatelet therapy after drug eluting stent implantation. Am J Cardiol 2011; 107: 186–194. Schomig A, Dibra A, Windecker S, et al. A meta-analysis of 16 randomized trials of sirolimus-eluting stents versus paclitaxel-eluting stents in patients with coronary artery disease. J Am Coll Cardiol 2007; 50: 1373–1380. Schulz S, Schuster T, Mehilli J, et al. Stent thrombosis after drug-eluting stent implantation: incidence, timing, and relation to discontinuation of clopidogrel therapy over a 4 year period. Eur Heart J 2009; 30: 2714–2721. Serruys PW, Daemen J. Late stent thrombosis: a nuisance in both bare metal and drug-eluting stents. Circulation 2007; 115: 1433–1439. Serruys PW, Onuma Y, Garg S, et al. 5-Year clinical outcomes of the ARTS II (Arterial Revascularization Therapies Study II) of the sirolimus-eluting stent in the treatment of patients with multivessel de novo coronary artery lesions. J Am Coll Cardiol 2010; 55: 1093–1101. Serruys PW, Strauss BH, Beatt KJ, et al. Angiographic follow-up after placement of a self-expanding coronary-artery stent. N Engl J Med 1991; 324: 13–17. Sigwart U, Fuel J, Mirkovitch V, Joffre F, Kappenberger L. Intra-vascular stents to prevent occlusion and restenosis after transluminal angioplasty. N Engl J Med 1987; 316: 701–706. Spertus JA, Kettelkamp R, Vance C, et al. Prevalence, predictors, and outcomes of premature discontinuation of thienopyridine therapy after drug-eluting stent placement: results from the PREMIER registry. Circulation 2006; 113: 2803–2809. Stettler C, Wandel S, Allemann S, et al. Outcomes associated with drug-eluting and bare-metal stents: a collaborative network meta-analysis. Lancet 2007; 370: 937–948. Stone GW, Rizvi A, Newman W, et al. Everolimus-eluting versus paclitaxel-eluting stents in coronary artery disease. N Engl J Med 2010; 362: 1663–1674. Tanzilli G, Greco C, Pelliccia F, et al. Effectiveness of two-year clopidogrel + aspirin in abolishing the risk of very late thrombosis after drug-eluting stent implantation (from the TYCOON [two-year ClOpidOgrel need] study). Am J Cardiol 2009; 104: 1357–1361. The GUSTO Angiographic Investigators. The effect of tissue plasminogen activator, streptokinase, or both on coronary-artery patency, ventricular function, and survival after acute myocardial infarction. N Engl J Med 1993; 329: 1615–1622. Turco MA. TCT-380: TAXUS ATLAS Small Vessel and TAXUS ATLAS Long Lesion trials. Long-term benefit of TAXUS Liberte versus TAXUS Express in small vessels and long lesions. Am J Cardiol 2009; 104: 141D. van Domburg RT, Foley DP, de Jaegere PP, et al. Long term outcome after coronary stent implantation: a 10 year single centre experience of 1000 patients. Heart 1999; 82: Suppl 2: 1127–1134. van Werkum JW, Heestermans AA, Zomer AC, et al. Predictors of coronary stent thrombosis: the Dutch Stent Thrombosis Registry. J Am Coll Cardiol 2009; 53: 1399–1409. Wallentin L, Becker RC, Budaj A, et al. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009; 361: 1045–1057. Wijns W, Kolh P, Danchin N, et al. Guidelines on myocardial revascularization. The Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Developed with the special contribution of the European Association for Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J 2010; 31: 2501–2555. Wiviott SD, Braunwald E, McCabe CH, et al. Intensive oral antiplatelet therapy for reduction of ischaemic events including stent thrombosis in patients with acute coronary syndromes treated with percutaneous coronary intervention and Stenting in the TRITON-TIMI 38 trial: a subanalysis of a randomised trial. Lancet 2008; 371: 1353–1363.
Дата добавления: 2015-02-06 | Просмотры: 764 | Нарушение авторских прав |