|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Патология кровеносных сосудов• Гомеометрическая • Повышение силы и скорости сокращений сердца при неменяющейся исходной длине мышечного волокна • Гетерометрическая • Повышение силы сокращений сердца при увеличении исходной (в диастолу) длины мышечного волокна Гомеометрическая компенсация (при увеличении сопротивления сердечному выбросу): • Феномен Анрепа. Увеличение перфузионного давления в коронарных артериях при наличии препятствия в сосудах большого круга кровообращения (эффект садового шланга) • Феномен Боудичи. Увеличение сократимости миокарда при блокаде K-Na-АТФазы (увеличение поступления Са) • Феномен Сарноффа-Митчелла. Увеличение сократимости миокарда при блокаде K-Na АТФаз Гетерометрическая компенсация (при повышении притока крови): • Механизм Франка-Старлинга. Повышение наполнения камер сердца ведет к увеличению растяжения мышечных волокон и более сильному сокращению в систолу • Тоногенная дилатация полостей сердца. Увеличение ударного объема за счет растяжения эластических волокон • Сокращение плеча доставки энергии к кардиомиоцитам феномен Фролова). Уменьшение расстояния от митохондрий до сократительных элементов Гипертрофия – последствия 1. Увеличение объема клетки Уменьшение клеточной поверхности по отношению к массе Снижение относительной площади мембраны Ухудшение условий для транспорта газов, питательных вещест.
2. Рост клетки Отставание нарастания эндоплазматического ретикулума и тубулярной системы Несоответствие метаболизма электролитов потребностям клетки Нарушение процессов сокращения и расслабления.
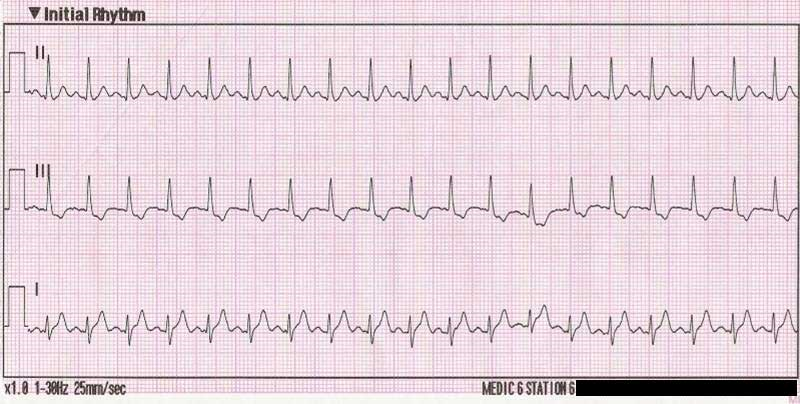
3. Увеличение объема цитоплазмы относительно ядра Ухудшение условий для синтеза белков Нарушение пластических процессов 4. Отставание роста числа митохондрий от объемов клетки Ухудшение энергетического обеспечения клетки 5. Рост клетки Отсутствие адекватного увеличения капиллярной сети и нервных окончаний Ухудшение нервно-сосудистого обеспечения Стадии развития компенсаторной гиперфункции и гипертрофии миокарда: • Аварийная • Завершившейся гипертрофии и устойчивой гиперфункции • Постепенного истощения и развития кардиосклероза Аварийная стадия Повышение нагрузки на сердце Мобилизация энергетических возможностей Усиление синтеза белка, наращивание субклеточных структур Приспособление к новым условиям Стадия устойчивой гиперфункции Завершен процесс адаптации Сердце работает с перегрузкой Энергетические процессы сбалансированы на более высоком уровне Стадия истощения и кардиосклероза Нарастание изменений в обменных процессах Структурные изменения Кардиодистрофия Гибель кардиомиоцитов Замещение соединительной тканью Нарушение проводимости. Хроническая сердечная недостаточность. Тахикардия
В начальных стадиях возникает только при физической нагрузки, приходя в норму не ранее чем через 10 минут. В дальнейшем наблюдается в покое. Развивается как компенсаторная реакция.
Отеки. Один из наиболее распространенных симптомов. На ранних стадиях возможны скрытые отеки. Задержка в организме до 5 литров жидкости может не сопровождаться видимыми проявлениями. Отеки распространяются снизу вверх: ноги – поясница – вся подкожная клетчатка. До появления периферических отёков застой крови прежде всего развивается в печени, которая набухает, увеличивается в размерах, что обуславливает появление чувства тяжести, а затем и тупых болей в области правого подреберья.
Цианоз. Изменение окраски (синюшность) кожи и слизистых. Уменьшение кислорода в крови и увеличение восстановительного гемоглобина.
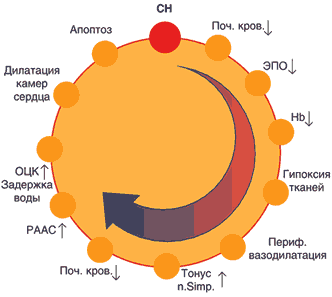
Одышка. Частый ранний симптом: учащение дыхания и вовлечение в дыхательные движения дополнительной мускулатуры. В начальной стадии связана с нагрузкой. В дальнейшем проявляется в покое. Схема взаимосвязи (порочный круг) сердечной недостаточности.
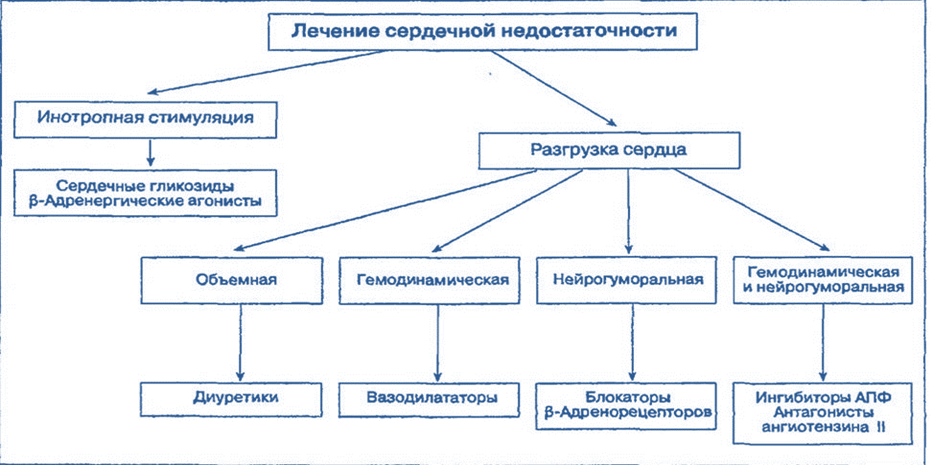
Патогенетические принципы лечения СН
Патология кровеносных сосудов Атеросклероз - системное поражение артерий вследствие хронической воспалительной реакции гиперчувствительности замедленного типа в сосудистой стенке. Одна из наиболее распространенных болезней и самая частая причина потери трудоспособности, инвалидизации и преждевременной смерти. Чаще поражает лиц старше 40 лет, в 3-4 раза больше мужчин. Обмен липидов Резервно-энергетическая функция – обеспечивается триглицеридами (ТГ) Мембранообразующая функция – связана с метаболизмом глицеро фосфолипидов Рецепторо-посредниковая функция – обеспечивается гликосфинголипидами (ФЛ) Регуляторно-сигнальная функция – связана с липидными спиртами (стероидами) из холестерина (ХН) – циклопентанпергидрофенантрен ХН хиломикроны (ТГ) ЛПОНП (ТГ) ЛППП (ХН) ЛПНП (ХН) ЛПВП (ФЛ) липопротеиды превращаются друг в друга при метаболизме с участием липопротеиновой липазы образующейся в эндотелии. Типы гиперлипопротеинемий связаны с нарушением образования, транспорта, и утилизации липопротеинов I - XM IIa - ЛПНП IIb - (ЛПНП + ЛПОНП) III - ЛППП IV - ЛПОНП V - (ХМ + ЛПОНП) Наиболее атерогенны II, III, IV типы гиперлипопротеинемий Альфа-липопротеиды - прочные соединения холестерина + триглицеридов + белков. Непрочные соединения: бета-липопротеиды и пребета-липопротеиды. Этиология. Нарушение обмена липидов (холестерин и b-липопротеиды) и повреждение эндотелия сосудов. Факторы риска: артериальные гипертензии, сахарный диабет, психоэмоциональные перенапряжения, ожирение, гиподинамия, нерациональное питание, наследственность, курение. Некоторые из них не подлежат профилактической коррекции или отмене. Главными факторами, повреждающими эндотелий, являются факторы риска атеросклероза. В настоящее время их насчитывают более 200. Однако основными из них являются гипертензия, курение и повышенный уровень холестерина в плазме крови. При этом курение увеличивает риск возникновения коронарных событий в 1,6 раза, гипертензия (систолическое артериальное давление (АД) выше 195 мм рт. ст.) – в 3 раза, гиперхолестеринемия (8,5 ммоль/л, 330 мг/дцл и более) – в 4 раза, а сочетание трех перечисленных факторов риска – в 16 раз. Каким же образом столь различные факторы риска оказывают подобное повреждающее действие на эндотелиальную выстилку сосудов? Как показали исследования последних лет, факторы риска реализуют свое повреждающее действие через усиление процессов оксидативного стресса, интенсивная продукция перекисных радикалов нарушает баланс между защитными и повреждающими воздействиями на стенку сосуда. В процессе атерогенеза трудно переоценить роль эндотелия, который является полуселективным барьером для диффузии макромолекул из просвета сосуда в интерстициальное пространство. Являясь высокоактивным эндокринным органом, эндотелий обеспечивает регуляцию тонуса сосудов, процессы гипертрофии и пролиферации гладкомышечных клеток (ГМК), модуляцию свертывания крови и фибринолиза, а также процесса воспаления. При атеросклерозе нарушается баланс между гуморальными факторами, оказывающими потенциальное защитное действие (NO, эндотелиальный фактор гиперполяризации, простагландин – PGI), и факторами, повреждающими стенку сосуда (эндотелин-1, тромбоксан А2, супероксид-анион). Основная защитная роль в интактном эндотелии отведена NO, обеспечивающему вазодилатацию, торможение экспрессии молекул адгезии, а также агрегации тромбоцитов, антипролиферативное, антиапоптотическое и антитромботическое действие. Холестерин в организме находится в составе белково-липидных комплексов – липопротеидов (ЛП) циркулирующих в крови. Модифицированные в результате перекисного окисления ЛП низкой плотности (мЛПНП) являются антигенами и именно они ответственны за формирование атеросклеротических поражений артерий. Преодоление ЛП эндотелиального барьера, осуществляется за счет количественного накопления везикул содержащих мЛПНП, которые постепенно сливаются между собой передвигаясь к базальной мембране и далее в субэндетелиальный слой интимы. Крайней степенью активации неспецифического эндоцитоза является заполнение всей цитоплазмы эндотелиальной клетки везикулами (пенистые клетки) с образованием внутриклеточных каналов и расширением межэндотелиальных пространств. Прямой контакт между плазмой крови и субэндотелиальным слоем приводит к серозно-фиброзному отеку, дополнительному отложению мЛПНП, с фиксацией белковых компонентов плазмы. Эти вещества подвергаются ферментной модификации с приобретением аутоантигенных свойств. Происходит очаговая адгезия негранулярных лейкоцитов на стенке эндотелия в зоне скопления в интиме мЛПНП, в местах продукции интерлейкинов. Таким образом, мЛПНП запускают синтез клетками эндотелия, макрофагами, Т-лимфоцитами медиаторов воспаления – цитокинов которые, в свою очередь, активируя ПОЛ усиливают образование мЛПНП. Возникает замкнутый круг. В склеротических бляшках создается взаимоактивирующий и взаиморегулируемый процесс между макрофагами и Т- лимфоцитами. Воздействие на макрофаги интерферона (IFN-g) вырабатываемого активированными Т-лимфоцитами стимулирует мононуклеары продуцирующие фактор некроза опухолей (TNFa), который в свою очередь активирует выработку в эндотелиоцитах интерлейкина (IL-1b). Происходит цитотоксическое действие на окружающие клетки. Патогенез. Развитие хронической воспалительной реакции гиперчевствительности замедленного типа сосудистой стенки пусковым моментом которой является накопление мЛПНП в интиме артерий. Нарушение соотношения между холестерином, фосфолипидами и белками Þ избыточное образование b-липопротеидов являщихся аутоантигенами Þ образование аутоантител (Т-лимфоцитов) Þ формирование иммунных комплексов Þ отложение их в интиме артерий Þ повреждения сосудистой стенки Þ заполнение очагов поражения жиро-белковым детритом Þ разрастание соединительной ткани Þ формирование атеросклеротической бляшки суживающей просвет сосуда Þ нарушение питания сосудистой стенки Þ изъязвление фиброзных бляшек Þ тромбообразование вследствие чего закупорка сосудов и тромбэмболические осложнения Þ кальциноз с резкой деформацией и сужением сосудов. Клиника. В латентном периоде бессимптомное течение с увеличением содержания холестерина и b-липопротеидов. 1. стадия – ишемическая, проявляется нарушением кровоснабжения органов и тканей (ИБС-стенокардия) 2. стадия – тромбонекротическая, проявляется тромбозом или тромбэмболией артерий (инфаркты) 3. стадия – фиброзная, характеризуется развитием в органах соединительной ткани (кардиосклероз) Клиническая картина атеросклероза зависит от локализации поврежденных артерий (коронарные, аорта, головной мозг, конечности) поэтому признаки нарушений могут быть различны. Однако этиотропная и патогенетическая терапии будут одинаковы. Артериальная гипер- и гипотензия, их гемодинамические варианты. Этиология и патогенез артериальной гипертензии. Роль нервных факторов, нарушений эндокринной системы и почек в ее развитии. Гипертоническая болезнь. Этиология, патогенез, факторы риска. Отличие от симптоматических гипертензий. Дата добавления: 2014-05-16 | Просмотры: 1444 | Нарушение авторских прав |