|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Фосфорилювання моносахаридів.Вуглеводи Основні питання: 1. Вуглеводи. Функції. Класифікація. Поширення в природі. 2. Моносахариди: будова, класифікація, ізомерія, фізичні та хімічні властивості. 3. Дисахариди: будова і класифікація, фізичні і хімічні властивості. 4. Полісахариди: крохмаль, інулін, клітковина. Вуглеводи (цукри) – біоорганічні сполуки, що за своєю хімічною будовою є альдегідо- та кетопохідними багатоатомних спиртів. Термін був вперше запропонований у 1844р. К.Шмідтом. Вуглеводи містяться у всіх живих організмах. В рослинах близько 80 – 90% сухої маси, в організмах тварин 1 – 2% припадає на вуглеводи. Вуглеводи – продукти асиміляції вуглекислого газу зеленими рослинами і фото синтезуючими мікроорганізмами (фотосинтез). При фотосинтезі енергія Сонця перетворюється в енергію хімічних зв’язків. Фотосинтез відбувається за участю ферментних систем і поглинаючих променеву енергію рослинних пігментів – хлорофілів: 6СО2 + 6Н2О hν С6Н12О6 + 6О2
В основі фотосинтезу лежить окислювально-відновний процес, у якому електрони переносяться від донора-відновника (води, гідрогену) до акцептора (ацетату, СО2), з утворенням відновлених сполук (вуглеводів) і виділенням кисню. Фотосинтез – єдиний процес у біосфері, який приводить до збільшення вільної енергії за рахунок зовнішнього джерела ‑ Сонця і забезпечує існування на земній кулі всіх живих організмів. При цьому щорічно на землі утворюється більше 100млрд. т органічних речовин, живими організмами (зеленими рослинами) засвоюється приблизно 200млрд.т вуглекислого газу і виділяється приблизно 145 млрд. т вільного кисню. Виникнення в існуванні Землі явища фотосинтезу стало стимулом біологічної еволюції різних форм життя. У ході еволюції біохімічних процесів значна частина простих вуглеводів, що утворилась внаслідок фотосинтезу, під впливом відповідних ферментних систем полімеризується в більш складні і стійкі вуглеводи: С6Н12О6 + С6Н12О6 → С12Н22О11 + Н2О моносахарид + моносахарид = дисахарид С12Н22О11 + С6Н12О6 → С18Н32О16 + Н2О дисахарид + моносахарид = трисахарид n С6Н12О6 → (C6H10O5)n + n Н2О
Функції вуглеводів: þ Пластична (синтезуються нуклеїнові та органічні кислоти); þ Опорна (у комплексі з білками входять до складу хрящових тканин); þ Регуляторна (регулюють осмотичні процеси); þ Захисна (утворюють клітинну мембрану у вигляді комплексів з білками); þ Енергетична (при окисленні 1г виділяється 16,9кДж енергії). Класифікація вуглеводів: 1. Моносахариди ‑ найпростіші вуглеводи, молекули яких не здатні розщеплюватися при гідролізі на простіші речовини. 2. Дисахариди ‑ вуглеводи, молекула яких під час гідролізу розщеплюється на дві молекули моносахаридів. 3. Полісахариди – складні вуглеводи, молекули яких мають більше 10 моносахаридних залишків, сполучених між собою О-глікозидними зв’язками і утворюючих лінійні або розгалужені ланцюги.
1. Залежно від кількості атомів карбону розрізняють: тріози (С3Н6О3), тетрози (С4Н8О4), пентози (С5Н10О5), гексози (С6Н12О6), гептози (С7Н14О7), октози (С8Н16О8), нонози (С9Н18О9) і декози (С10Н20О10). 2. Кожна група моносахаридів поділяється на альдози і кетози: глюкоза – альдоз, фруктоза – кетоза.
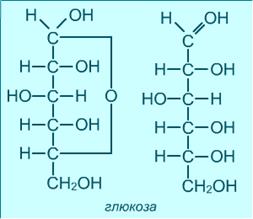
3. Моносахариди існують у відкритій (ациклічній) і напівацетальній (циклічній) формах.
Фруктоза – плодовий цукор є представником кетоз, невідновлюючий цукор. У розчині фруктози містяться з відкритою кетоформою дві циклічні форми – п’яти та шестичленна. Слід пам’ятати, що букви D та L позначають лише розміщення атомів водню та гідроксильних груп у молекулі моносахариду (порівнюють з гліцериновим альдегідом).
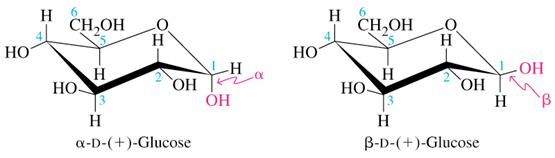
4. Залежно від розміщення (по відношенню до площини кільця молекули) гідроксильної групи при першому асиметричному вуглецевому атомі (1) циклічної форми, моносахариди поділяються на α та β-форми.
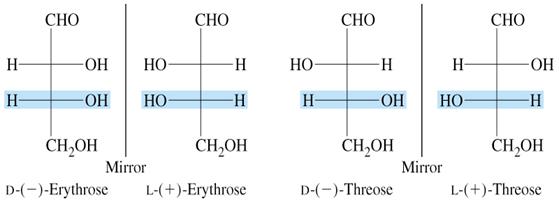
Наприклад, якщо у циклічній формі фруктози гідроксильні групи при першому та другому асиметричних атомах вуглецю направлені по одну сторону по відношенню до площини кільця молекули, то це буде α-форма; якщо по різні сторони – β-форма. 5. Залежно від величини кута оберту площини поляризованого світла ‑ оптичної активності ‑ розрізняють право- (+) й ліво (‑) - обертаючі форми. n Розчини моносахаридів, здатних переходити в циклічну форму, виявляють оптичну активність, яка по мірі стояння цих розчинів змінюється до тих пір, поки не досягне певної величини. n Явище зміни оптичної активності свіжо виготовленого розчину моносахариду називається мутаротація. n Мутаротація пояснюється тим, що в розчині одна форма моносахариду поступово переходить у другу форму. В результаті в розчині будуть знаходитися обидві форми моносахариду (α- та β-) і між ними встановиться певна рівновага. Речовини, які здатні обертати площину поляризації світлового променя, називаються оптично активними. Теорія оптичної (дзеркальної ізомерії) Вант-Гоффа і Ле-Беля (1847р.): органічні речовини, що містять асиметричний атом вуглецю, зв’язаний з чотирма атомами або групами атомів, виявляють оптичну активність. М’ясомолочна кислота та молочна кислота, що утворюється при зброджуванні сахаридів, є дзеркальними ізомерами. Це виявляється в їх різній оптичній активності: м’ясомолочна кислота обертає площину поляризації світла праворуч, а молочна кислота, що утворюється внаслідок бродіння сахаридів – ізомер, що обертає площину поляризації світла ліворуч.
| | Н ¾* С ¾ ОН НО ¾ С*¾ Н (проекційні формули дзеркальних ізомерів молочної | | кислоти ‑ антиподів) СООН СООН Ä Оптично неактивні речовини, що складаються з однакових кількостей оптичних антиподів, називаються рацемічними сполуками (рацематами). Оптично неактивною речовиною є молочна кислота бродіння. Це пояснюється тим, що молочна кислота бродіння є сумішшю однакових кількостей двох оптичних ізомерів проавообертаючого та лівообертаючого, тому результати їх оптичної активності взаємно знищуються. Ä Оптична (дзеркальна) ізомерія – це вид просторової ізомерії (стереоізомерії), що залежить від асиметрії молекули, в даному випадку від просторового розміщення чотирьох різних атомів або груп атомів навколо асиметричного атома вуглецю, причому оптичні ізомери (стереоізомери) відносяться один до одного, як предмет до його дзеркального відображення. Фізичні властивості моносахаридів: Моносахариди – тверді кристалічні речовини, солодкі на смак (фруктоза у 2,5 рази солодша за глюкозу), добре розчиняються у воді, мають відносно високу температуру плавлення. Розчини моносахаридів (крім рацематів) оптично активні. Хімічні властивості моносахаридів: 1. Карамелізація ‑ процес відщеплення молекул води від сахаридів, що приводить до утворення ангідридів, продуктами конденсації яких є забарвлені сполуки: кармелан (жовтий колір) → кармелен (коричневий) → кармелін (майже чорний). Від кармелану до кармеліну зменшується розчинність сполук у воді. Відбувається при температурі 135-1400С при перегріванні сиропів, виготовленні повидла, джемів, утворення паленого цукру. Окислення При дії окислювачів утворюються відповідні кислоти: Ä при окисленні альдегідної групи глюкози утворюється глюконова кислота: СН2ОН ‑ (СНОН)4 – СОН + [O] → СН2ОН (СНОН)4 – СООН (глюконова кислота) Ä дія Сu(ОН)2 при нагріванні, або реакція «срібного дзеркала»: СН2ОН ‑ (СНОН)4 – СОН + Ag2O → 2Ag↓ + СН2ОН ‑ (СНОН)4 – СООН СН2ОН (СНОН)4 – СОН + 2Cu(OH)2 → Cu2O↓ + СН2ОН (СНОН)4 – СООН + 2Н2О Ä енергійне окислення в кислому середовищі (HNO3):
HNO3 COOH ‑ (СНОН)4 – СООН (сахарна кислота)
3. Відновлення моносахаридів. Реакція відбувається при наявності водню і у присутності каталізаторів (Ni, амальгам натрію), утворюються спирти: СН2ОН ‑ (СНОН)4 – СОН + Н2 → СН2ОН ‑ (СНОН)4 – СН2ОН глюкоза сорбіт 4. Бродіння відбувається при наявності мікроорганізмів (дріжджі, плісняві грибки, деякі бактерії) або їх певних ферментів. · Спиртове бродіння відбувається під дією дріжджів при виготовленні тіста: С6Н12О6 → 2С2Н5ОН + 2СО2 (вуглекислий газ розпушує тісто) · Молочнокисле (лактатне) бродіння. Відбувається при дії молочнокислих бактерій при скисанні молока, заквашуванні овочів, при виготовленні тіста: С6Н12О6 → 2СН3СН(ОН)СООН (молочна кислота сприяє набуханню клітковини у борошні, затримує розвиток патогенних мікроорганізмів). · Лимонокисле (цитратне) бродіння спричиняється пліснявими грибами Citromyces graber, Aspergi lus niger: С6Н12О6 → НООС – СН2 – С (ОН) – СН2 – СООН + 2Н2О │ СООН Лимонна (цитратна) кислота · Маслянокисле бродіння С12Н22О11 → СН3 – (СН2)2 ‑ СООН + 2СО2 + 2Н2, Відбувається при потраплянні в молоко, а звідти ‑ і в сир газоутворюючих бактерій групи «колі» (молочнокислих бактерій), які спричиняють бродіння молочного цукру, з утворенням дуже великої кількості вуглекислого газу і водню, що спричиняє здимання, спучування сиру. Зв’язаність сирної маси порушується, і він тріскається. Молоко, забруднене маслянокислими бактеріями, є несиропридатним, тому спучування сирів на пізніх стадіях дозрівання свідчить про неякісну сировину. 5. Взаємодія з гідроксидом купруму(ІІ). Аналогічно багатоатомними спиртам моносахариди розчиняють голубий осад, утворюючи сполуку типу гліколяту купруму синього кольору: Н – С = О Н – С = О │ │ Н – С – ОН Н – С – ОН │ │
│ │
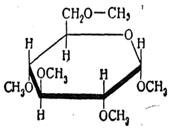
Н – С – ОН Н – С – О │ │ СН2ОН СН2ОН 6. Реакції алкілування. При взаємодії моносахаридів із спиртами (каталізатор Аg2O) або галогеналкілами (каталізатор НСІ) утворюються повні етери:
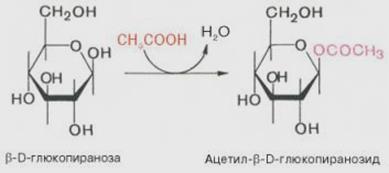
7. Реакції ацилювання. При дії на моносахариди ангідридів кислот утворюються естери циклічних форм моносахаридів.
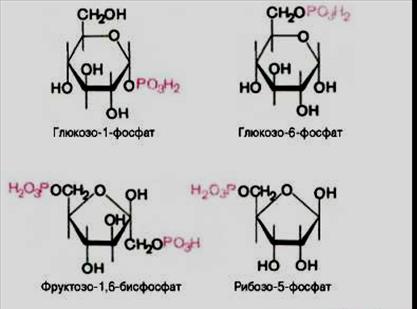
Фосфорилювання моносахаридів. Дана реакція приводить до утворення моно- і дифосфорних естерів, що мають надзвичайно велике значення в багатьох реакціях обміну, особливо в анаеробному гліколізі і глікенолізі, дає можливість клітинам живих організмів одержувати макроергічні сполуки (АТФ і АДФ і їх аналоги).
Дата добавления: 2015-11-25 | Просмотры: 2501 | Нарушение авторских прав |

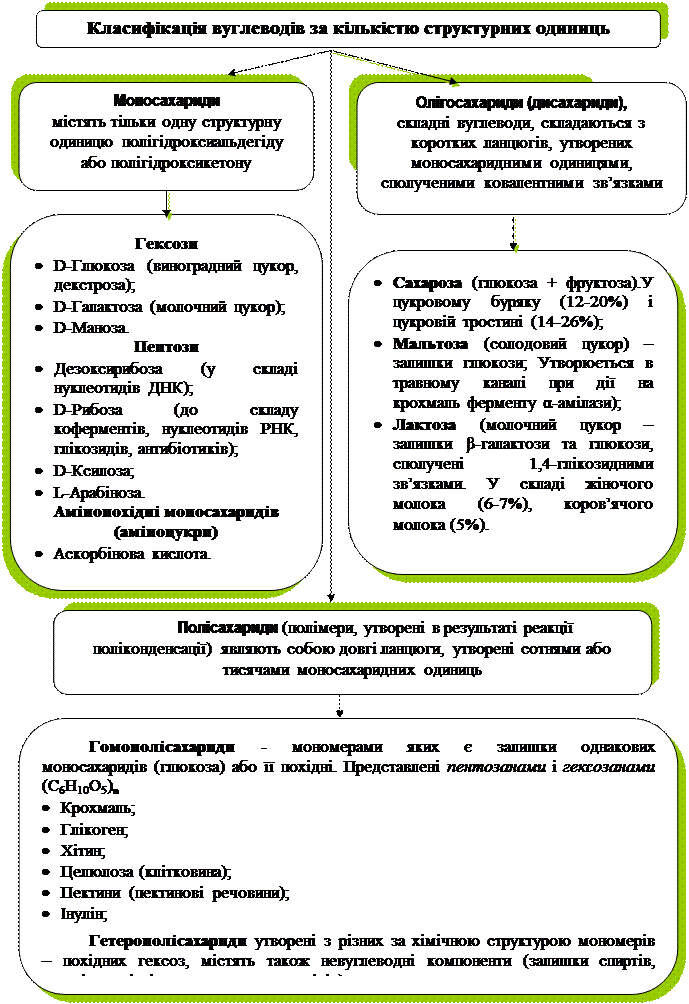
 Класифікація моносахаридів:
Класифікація моносахаридів: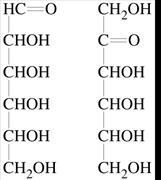



 СН3 СН3
СН3 СН3 СН2ОН ‑ (СНОН)4 – СОН HNO3 COH ‑ (СНОН)4 – СООН (глюкуронова кислота )
СН2ОН ‑ (СНОН)4 – СОН HNO3 COH ‑ (СНОН)4 – СООН (глюкуронова кислота ) Глюкоза, галактоза – відновлювальні сахариди (дають реакцію „срібного дзеркала”), фруктоза – невідновний цукор (не вступає в реакції окислення Аg2O, Cu(OH)2).
Глюкоза, галактоза – відновлювальні сахариди (дають реакцію „срібного дзеркала”), фруктоза – невідновний цукор (не вступає в реакції окислення Аg2O, Cu(OH)2).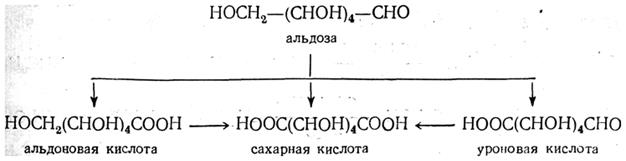
 Н – С – ОН + Cu(OH)2 Н – С – ОН + 2H2O
Н – С – ОН + Cu(OH)2 Н – С – ОН + 2H2O Н – С – ОН Н – С – О
Н – С – ОН Н – С – О │ │ Cu
│ │ Cu