|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
КОРА НАДПОЧЕЧНИКОВ
Кора надпочечников состоит из трех слоев (зон): клубочковой, пучковой и сетчатой (рис. 5.2.1). Клубочковая зона в виде узкого наружного слоя расположена под капсулой надпочечника. Клетки этого слоя соединены между собой в виде клубочков. Пучковая зона является самым большим слоем коры, и его клетки располагаются в виде пучков. Сетчатая зона окружает мозговой слой надпочечника, и ее клетки располагаются в виде сетки. В коре надпочечников синтезируются три группы гормонов. В клубочковой зоне синтезируются минералокортикоиды, главным представителем которых является альдостерон. В пучковой и сетчатой зонах синтезируются глюкокортикоиды, главным представителем которых является кортизол, и надпочечниковые андрогены. Химическая природа гормонов. По своей химической природе гормоны коры надпочечников являются стероидными гормонами. Это очень важная группа биологически активных веществ. Они представляют собой производные холестерина – кортизол, альдостерон, мужские и женские половые гормоны. Для всех этих гормонов характерна гидрофобность. Поэтому они хорошо проходят из мест своего синтеза через клеточную мембрану и попадают беспрепятственно в другие среды (кровь, межклеточное пространство). В крови они требуют специальных носителей, так как гидрофобны. Транспорт глюкокортикоидов
Кортизол и надпочечниковые андрогены секретируются в кровь в свободном состоянии, однако, сразу же связываются белками сыворотки крови. Большая часть кортизола связана с кортизолсвязывающим глобулином или транскортином. С ним связано 75-80% кортизола и с альбумином – 15%. В норме в транскортине содержится 700 нмоль/л (25 мкг/дл) кортизола. При гиперсекреции кортизола увеличивается общий кортизол (за счет связанного и за счет свободного). Общий кортизол в сыворотке может увеличиваться при избытке эстрогенов (беременность, лечение эстрогенами, прием контрацептивов), тиреотоксикозе, диабете, но только за счет связанного с белком. Свободный кортизол не увеличивается. Это связано с тем, что эти состояния увеличивают синтез транскортина в печени и связывание им кортизола. Большинство синтетических аналогов кортизола находится в меньшей связи с белком, чем кортизол. Это объясняет тот факт, что они в значительно меньших дозах и быстрее чем кортизол могут привести к проявлениям, подобным синдрому Кушинга как побочных эффектов лечения.
Механизм действия кортикостероидов
Кортизол, как и другие стероидные гормоны, свободно проходит через клеточные мембраны в клетки, где соединяется с соответствующим для него внутриклеточным рецептором. Далее в ядре клетки они связываются с определенной ДНК (геномом) и активируют ее. В результате увеличивается образование мРНК, которая стимулирует в клетке синтез белковых медиаторов ответа, специфических для каждого гормона.
Физиологические эффекты глюкокортикоидов К глюкокортикоидным гормонам относятся кортизол, кортизон, кортикостерон, 11-дезоксикортизол, 11-дегидрокортикостерон. У человека наиболее важным глюкокортикоидом является кортизол, который секретируется со скоростью 20-25 мг/сут, и концентрация его в течение суток колеблется от 4 до 16 мкГ%. Физиологические эффекты глюкокортикоидов весьма разнообразны, они прямо или опосредованно регулируют практически все физиологические и биохимические процессы. Часть из них представляют собой полезный для организма эффект, позволяющий организму выживать в условиях критических ситуаций. Часть эффектов глюкокортикоидов является своеобразной платой за спасение. Итак: 1.
2. Глюкокортикоиды изменяют белковый обмен: углеводный обмен – гипергликемия, глюконеогенез, подавление транспорта глюкозы в мышечной и жировой ткани, подавление гликолиза и гликолитических ферментов, компенсаторная гиперинсулинемия при гипергликемии, синтез гликогена; белковый обмен – катаболический эффект: катаболизм белков мышечной, эпителиальной и лимфоидной тканей, поступление аминокислот в кровь и печень, повышение образования мочевины и экскреции азота, отрицательный азотистый баланс; анаболический эффект: синтез ферментов и некоторых белков в печени; антианаболический эффект: подавление синтеза белков de novo в печени на уровне трансляции. Одновременно в других органах и тканях, в частности, в скелетных мышцах глюкокортикоиды тормозят синтез белков для того, что бы создать депо аминокислот, необходимых для глюконеогенеза. Изменяют липидный обмен: липолитический эффект в тканях, гиперлипидемия и гиперхолестеринемия, активация кетогенеза в печени, угнетение липогенеза в печени, стимуляция липогенеза и перераспределения жира в жировой ткани центральной оси туловища и лица, стимуляция аппетита и потребления жира. 3. Глюкокортикоиды вызывают активацию липолиза для появления еще одного источника энергии – жирных кислот. Итак, главный эффект глюкокортикоидов – это мобилизация энергетических ресурсов организма. 4. Глюкокортикоиды угнетают все компоненты воспалительной реакции – уменьшают проницаемость капилляров, тормозят экссудацию, снижают интенсивность фагоцитоза. Это свойство используется в клинической практике – для снятия воспалительных реакций, например, после проведения операции на глазу по поводу катаракты больному рекомендуется ежедневно вводить глазные капли, содержащие глюкокортикоиды (кортизон, гидрокортизон). 5. Глюкокортикоиды резко снижают продукцию лимфоцитов (Т- и В-) в лимфоидной ткани – при массивном повышении уровня в крови глюкокортикоидов наблюдается опустошение тимуса, лимфатических узлов, снижение в крови уровня лимфоцитов. Под влиянием глюкокортикоидов снижается продукция антител, уменьшается активность Т-киллеров, снижается интенсивность иммунологического надзора, снижается гиперчувствительность и сенсибилизация организма. Все это позволяет рассматривать глюкокортикоиды как активные иммунодепрессанты. 6. Глюкокортикоиды, вероятно, повышают чувствительность гладких мышц сосудов к катехоламинам, поэтому на фоне глюкокортикоидов повышается спазм сосудов, особенно мелкого калибра, и возрастает артериальное давление. Это свойство глюкокортикоидов, вероятно, лежит в основе таких явлений, как язвы желудка в двенадцатиперстной кишки, нарушение микроциркуляции в сосудах миокарда и как следствие – развитие аритмии, нарушение физиологического состояния кожных покровов – экземы, псориаз. Все эти явления наблюдаются в условиях повышенного содержания эндогенных глюкокортикоидов (при стресс-реакции) или в условиях длительного введения глюкокортикоидов с лечебной целью. 7. В низких концентрациях глюкокортикоиды вызывают повышение диуреза – за счет увеличения скорости клубочковой фильтрации и, возможно, за счет угнетения выброса АДГ. Но при высоких концентрациях глюкокортикоиды ведут себя как альдостерон – вызывают задержку натрия и воды в организме. 8. Глюкокортикоиды повышают секрецию соляной кислоты и пепсина в желудке, что вместе с сосудосуживающим эффектом приводит к появлению язв желудка. 9. При избыточном количестве глюкокортикоиды вызывают деминерализацию костей, остеопороз, потерю кальция с мочой, снижают всасывание кальция в кишечнике, ведут себя как антагонист витамина Д3. В этих же условиях вследствие торможения синтеза белка в скелетных мышцах наблюдается у человека мышечная слабость. 10. За счет активации липолиза при действии глюкокортикоидов повышается интенсивность перекисного окисления липидов (ПОЛ), что приводит к накоплению в клетках продуктов этого окисления, существенно нарушающих функцию плазматической мембраны. 11. Глюкокортикоиды влияют и на деятельность ЦНС, на функцию ВНД – они повышают обработку информации, улучшают восприятие внешних сигналов, действующих на многие рецепторы – вкусовые, обонятельные и т.п. Однако при недостатке и особенно при избыточном содержании глюкокортикоидов наблюдаются существенные изменения в состоянии ВНД – вплоть до возникновения шизофрении (при длительном стрессе!). 12. Участие в развитии общего адаптационного синдрома – стресс-реакции. Регуляция секреции глюкокортикоидов Глюкокортикоиды принадлежат к той группе гормонов, концентрация которых в плазме поддерживается на постоянном уровне за счет регуляторных механизмовв течение более или менее длительных периодов времени. Циркадианные колебания (более низкие концентрации наблюдаются в ночное время по сравнению с дневным) можно рассматривать как результат сдвига заданного значения в ходе 24-часового ритма. Самое высокое содержание глюкокортикоидов в крови в 6-8 часов утра. Необходимо помнить, что значительная часть кортизола в плазме связана с α-глобулином (транскортином), а другая фракция связана с альбуминами плазмы. Однако несущественно, какая из концентраций регулируется, потому что относительные концентрации свободных и связанных кортикоидов в плазме и клеточных кортикоидов определяются исключительно физическими законами (действия массы и диффузии). Регуляция концентрации кортизола осуществляется следующим образом: рилизинг-гормон КРГ, образованный в гипофизотропной зоне гипоталамуса, достигает аденогипофиза по воротным сосудам и там вызывает выделение АКТГ (рис. 5.2.2); АКТГ доставляется кровью к коре надпочечника, где он стимулирует выделение глюкокортикоидов. Эта последовательность событий установлена двумя основными группами экспериментов. · Демонстрацией того, что секреция АКТГ и глюкокортикоидов усиливается после электрической стимуляции срединного возвышения. · Демонстрацией того, что усиление секреции АКТГ и кортизола, в норме индуцируемое стрессорными факторами, не определяется после электрокоагуляции ограниченных участков срединного возвышения.
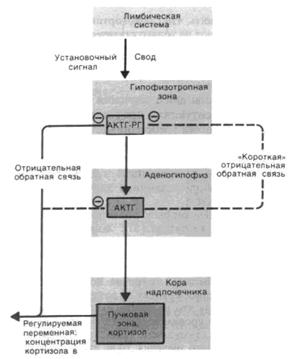
Рис. 5.2.2. Схема регуляции секреции глюкокортикоидов в коре надпочечника посредством КРФ и АКТГ; отрицательная обратная связь тормозит в первую очередь секрецию КРФ (влияя на АКТГ лишь незначительно).
Данные, полученные во 2-й серии экспериментов, показали также, что образование рилизинг-фактора в гипофизотропной зоне находится под контролем высших центров ЦНС, которые получают и перерабатывают сигналы, поступающие с периферии организма (некоторые – от органов чувств). Результаты этих опытов дают также основание к трактовке наблюдений о том, что эмоциональное состояние и поведение отражаются на секреторной активности коры надпочечников. Отрицательная обратная связь. Микроинъекция глюкокортикоидов в гипофизотропную зону вызывает заметное снижение секреции АКТГ. Секреция АКТГ изменяется также при их же инъекции в аденогипофиз. Эти эффекты указывают на то, что рецепторы глюкокортикоидов, которые оказывают влияние на секрецию АКТГ через цепь отрицательной обратной связи, располагаются как в гипофизотропной зоне, так и в самом гипофизе (рис. 5.2.2.). В гипофизотропной зоне кортикоиды влияют на выделение КРГ, а в аденогипофизе они модулируют влияние КРГ на выделение АКТГ. Недавно было показано, что АКТГ способен непосредственно ингибировать свою собственную выработку через так называемую короткую цепь обратной связи; местом его действия, как предполагается, являются нейросекреторные клетки гипофизотропной зоны. Эффекты альдостерона Альдостерон увеличивает активный транспорт Na+ через клеточные мембраны. В почке эффект заключается в повышении реабсорбции Na+ в канальцах и, вследствие осмотических явлений, реабсорбции воды. Кроме того, А стимулирует секрецию К+ и Н+. Альдостерон сходным образом влияет на потовые, слюнные и кишечные железы. Это внепочечные эффекты альдостерона. Содержание NaCl в секрете потовых желез, которое в норме значительно ниже, чем в плазме, при недостаточности альдостерона резко возрастает. Поэтому в случаях недостаточности альдостерона потоотделение, вызванное повышенной температурой окружающей среды, способно быстро привести к опасной потере NaCl. Одним из факторов адаптации к теплу является усиление секреции альдостерона, в результате чего содержание NaCl в поту снижается. Латентный период действия альдостерона на почки составляет около 30 мин; это время достаточно для индукции ферментов, которая, как предполагают, является основой действия альдостерона. При избытке альдостерона – гиперволемия: активация канальцевой реабсорбции Na+ и секреции К+; поддержание осмотического давления, возбудимости клеток, артериального давления; регуляция ионного транспорта в потовых и слюнных железах и желудочно – кишечном тракте; при избытке – гиперволемия, гипертензия, отеки, гипокалиемия, алкалоз, нарушения сердечного ритма, повышение экскреции магния и кальция; при недостатке – гиповолемия, гипотензия, гиперкалиемия, ацидоз, нарушения сердечного ритма, мозговые нарушения, избыток вазопрессина, нарушения пищеварения.
Регуляция секреции альдостерона В очень большом количестве исследований показано, что к увеличению секреции альдостерона приводят три основных состояния: 1) усиленное потребление калия, 2) отрицательный баланс натрия (например, сниженное содержание соли в пище или значительные потери NaCl с потом) и 3) уменьшение объема плазмы (например, при кровопотере или неадекватном потреблении жидкости). Увеличение скорости секреции альдостерона под влиянием этих факторов осуществляется следующими механизмами.
Ренин секретируется в юкстагломерулярном аппарате (ЮГА) почек. ЮГА образован специальными клетками, окружающими капиллярный клубочек. Секреция ренина в ЮГК регулируется четырьмя основными влияниями. Во-первых, величиной давления крови в приносящей артериоле, т.е. степенью ее растяжения. Снижение растяжения активирует, а увеличение – подавляет секрецию ренина. Во-вторых, регуляция секреции ренина зависит от концентрации натрия в моче дистального канальца, которая воспринимается клетками – своеобразным Na-рецептором клеток ЮГА. Чем больше натрия оказывается в моче канальца, тем выше уровень секреции ренина. В-третьих, секреция ренина регулируется симпатическими нервами, ветви которых заканчиваются на ЮГК, медиатор норадреналин через β-адренорецепторы стимулирует секрецию ренина. В-четвертых, регуляция осуществляется по механизму отрицательной обратной связи, включаемой уровнем в крови других компонентов системы – ангиотензина и альдостерона, а также их эффектами – содержанием в крови натрия, калия, артериальным давлением, концентрацией простагландинов в почке, образующихся под влиянием ангиотензина (рис.5.2.3.).
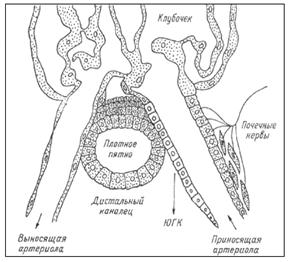
Рис. 5.2.3. Структура юкстагломерулярного аппарата. ЮКГ – юкстагломерулярные клетки.
Кроме почек образование ренина происходит в стенках кровеносных сосудов многих тканей, головном мозге, слюнных железах. Ренин является ферментом, приводящим к расщеплению α-глобулина плазмы крови - ангиотензиногена, образующегося в печени. При этом в крови образуется малоактивный декапептид ангиотензин-I, который в сосудах почек, легких и других тканей подвергается действию ангиотензин-превращающего фермента (АПФ), отщепляющего от ангиотензина-I две аминокислоты. Образующийся октапептид ангиотензин-II обладает большим числом различных физиологических эффектов, в том числе стимуляцией клубочковой зоны коры надпочечников, секретирующей альдостерон, что и дало основание называть эту систему ренин-ангиотензин-алъдостероновой (рис. 5.2.4.).
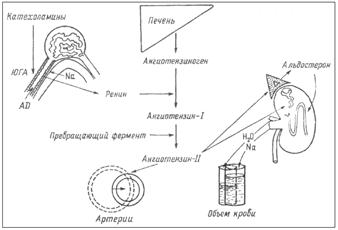
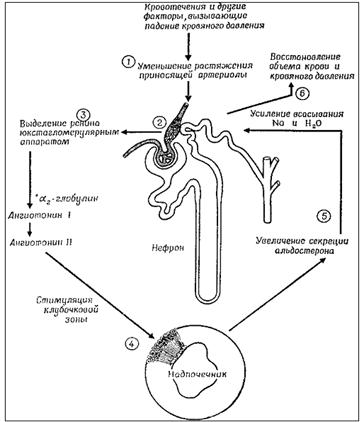
Рис. 5.2.4. Ренин-ангиотензивная-альдостероновая система. Ангиотензин-II кроме стимуляции продукции альдостерона, вызывает мощный спазм артериальных сосудов, увеличивает реабсорбцию натрия и ослабляет клубочковую фильтрацию в почках, способствует формированию чувства жажды и питьевого поведения. Таким образом, ренин-ангиотензин-альдостероновая система участвует в регуляции почечного кровообращения, объема циркулирующей крови, осмотического давления, водно-солевого обмена и поведения (рис. 5.2.5.).
Рис. 5.2.5. Регуляторная роль почек в секреции альдостерона. Ангиотензин-II кроме стимуляции продукции альдостерона, вызывает мощный спазм артериальных сосудов, увеличивает реабсорбцию натрия и ослабляет клубочковую фильтрацию в почках, способствует формированию чувства жажды и питьевого поведения. Таким образом, ренин-ангиотензин-альдостероновая система участвует в регуляции почечного кровообращения, объема циркулирующей крови, осмотического давления, водно-солевого обмена и поведения (рис. 5.2.5.). Эти три регуляторных механизма достаточно эффективно компенсируют воздействия, приводящие к нарушению водно-солевого равновесия. Благодаря этим взаимосвязанным функциям альдостерониграет существенную роль в цепях регуляции, поддерживающих постоянство концентрацииNa/K в плазме иособенно объема жидкости в организме. С кибернетической точки зрения альдостерон является контролирующим элементом в нескольких переплетающихся биологических регуляторных цепях.
Эффекты надпочечниковых андрогенов
Основные надпочечниковые андрогены дегидроэпиандростерон (ДГЭАС), дегидроэпиандростерон-сульфат (ДГЭАС-сульфат) и андростендион обладают анаболическим эффектом. Они стимулируют синтез белка, увеличивают мышечную массу и сократительную способность мышц. Действие надпочечниковых андрогенов как половых гормонов очень слабое. Андростендион может превращаться в периферических тканях в тестостерон и в условиях его избытка у женщин может развиться гирсутизм и вирилизм. Синтезированы и нашли широкое применение в клинике аналоги андрогенов, активирующие синтез белка и обладающие минимальным вирилизирующим действием (анаболические стероиды). Физиологическая роль андрогенов в женском организме заключается в основном в воздействии на белковый обмен. Значение эстрогенов у мужчин не ясно. Физиологическое значение надпочечниковых андрогенов у мужчин аналогично роли полового гормона тестостерона. Но после кастрации увеличивается толщина сетчатой зоны, но компенсировать недостаток андрогенов и играть роль «третьей гонады» надпочечники не в состоянии.
Заболевания надпочечников Аддисонова болезнь. В 1855 г. Addison опубликовал первое исчерпывающее сообщение о клинике и причине этого заболевания. Это сравнительно редкое заболевание возникает в результате поражения обоих надпочечников. Симптомы: сильная пигментация кожи, преобладающий дымчато-серый, бронзовый оттенок особенно на лице, тыльных поверхностях кистей и участках тела, подвергающихся трению одеждой; слизистая рта, десен, языка также пигментирована; наблюдается прогрессирующая мышечная слабость, быстрая утомляемость; гипотония; память слабеет; рвота, поносы; резкое ухудшение; гипонитриемия, гиперкалиемия. Адрено-генитальный синдром – избыточная продукция андрогенов надпочечников, вследствие гиперплазии или опухоли коры надпочечников. У женщин встречается в 5 раз чаще, чем у мужчин. Если гиперпродукция андрогенов коры надпочечников начинается у девочек еще во время внутриутробного развития, то возникает аномалии строения внутренних и наружных половых органов – ложный гермафродизм. Половые органы недоразвиты. Если заболевают мальчики – преждевременное развитие вторичных половых признаков. У детей обоего пола при адрено-генитальном синдроме наступает усиленный рост скелета и сильное развитие мускулатуры, что сопровождается значительным увеличением мышечной силы. У взрослых женщин развивается вирилизм и гирсутизм. Вирилизм – появление у женщин ряда типичных мужских черт и ослабление женских вторичных половых признаков. Развивается мужской облик лица, типичное для мужского строения туловище, огрубение голоса, уменьшение размера молочных желез, изменение наружных половых органов. На лице растут борода и усы, волосистость на теле распределяется по мужскому типу. Гирсутизм – усиленное развитие у женщин волосяного покрова на лице, туловище и конечностях, не сопровождающееся изменениями в половом аппарате, строении тела, вторичных половых признаков. Синдром Конна (первичный альдостеронизм) – причина – опухоль или гиперплазия клубочковой зоны коры надпочечников. Основные симптомы: периодически повторяющиеся приступы мышечной слабости, изменение кожной чувствительности, судорожные приступы и параличи. Гипокалиемия, что ведет к изменению миокарда. Синдром Кушинга – полиэтиологичное заболевание, подавляющее большинство клинических проявлений которого является следствием хронического избытка кортизола в организме и избыточного его действия на органы и ткани. Осложнения: компрессионные переломы позвоночника; переломы шейки бедра. Образование камней в почках - нефролитиаз, на фоне которого часто развивается пиелонефрит. Кальций может откладываться в паренхиме почек с развитием нефрокальциноза и, в конечном итоге, хронической почечной недостаточности. Артериальная гипертензия может осложниться мозговыми инсультами и в сочетании с гиперлипидемией и гиперинсулинемией способствует раннему развитию и тяжелому течению атеросклероза, в частности коронарных артерий. Кроме того, катаболические процессы, затрагивающие и сердечную мышцу, приводят к развитию кардиодистрофии, которая может проявляться сердечной недостаточностью и нарушениями ритма сердца. Больные могут умереть от инфаркта миокарда, мозгового инсульта и сердечной недостаточности.
Препараты гормонов коры надпочечников
Первый активный препарат коры надпочечников был получен в 1927 г. Это кортин. В 30-40-е годы были открыты и выделены кортизол, кортизон, ДОК. Далее синтезированы преднизолон (аналог кортизола (гидрокортизола), преднизон (аналог кортизона)). Получены кортикостероиды (КС) с избирательным действием подобные глюкокортикоидам (ГК) без минералокортикоидного (МК) эффекта – триамсинолон, дексаметазон. Толчком к интенсивным исследованиям и синтезу синтетических аналогов КС послужили результаты Hench c соавт. (1948) о высокой эффективности кортизона при лечении больных ревмотоидным полиартритом. Филип Хенч обратил внимание на то, что у больных ревматическими заболеваниями при беременности или желтухе наступает выраженное облегчение состояния. Он предположил, что улучшение самочувствия может быть обусловлено появлением в организме больных какого-то стероидного вещества, подобного либо половым гормонам, выделяемым при беременности в повышенных количествах, или желчным кислотам, накапливающиеся при желтухе. 21 сентября 1948 года была сделана первая попытка лечения кортизоном больного, страдавшего тяжелым хроническим суставным ревматизмом. Через несколько дней больной, который в течение 6 лет не мог подняться с постели из-за мучительных болей, самостоятельно встал. Таким образом, в 1948 году получила права гражданства кортикостероидная терапия, которая открыла новую эру в лечении ревматизма и спасла миллионы человеческих жизней. Научный мир по достоинству оценил это открытие. Кевдэлл, Хенч и Рейхштейн в 1950 году были удостоены Нобелевской премии. В дальнейшем началось широкое и во многих случаях очень эффективное применение КС при различных заболеваниях неэндокринной природы. Таким образом, терапию КС и их синтетическими аналогами используют в двух планах: 1) заместительная при гипокортицизме; 2) фармакологическую – используют их противовоспалительное и иммуносупрессивное действие. Угнетение иммунологических свойств связано с инволюцией тимико-лимфотической системы, а также с катаболическим действием (угнетается синтез антител). Возможные осложнения терапии кортикостероидами: 1) отложение жира в верхней половине туловища и лица (паукообразное ожирение); 2) стероидный диабет; 3) остеопороз и патологические переломы; 4) задержка роста детей; 5) стрии; 6) гирсудизм; 7) нарушение заживления ран; 8) мышечная слабость и миопатии; 9) отеки; 10) язвы ЖКТ; 11) гипертония; 12) изменение функционального состояния ЦНС; 13) нарушение mensis; 14) генерализация инфекций. Атрофия НП и синдром отмены.
Заболевания надпочечников (хронические недостатки коры надпочечников) Аддисонова болезнь. В 1855 Addison опубликовал первое исчерпывающее сообщение о клинике и причине этого заболевания. Это сравнительно редкое заболевание, возникает в результате поражения обоих надпочечников, реже другое заболевание. Симптомы. Сильная пигментация кожи, приобретающей дымчато-серый, бронзовый оттенок. Глюкокортикоиды применяются с лечебной целью как мощное противовоспалительное, десенсибилизирующее средство. Впервые с этой целью их применил Хенч. Филип Хенч обратил внимание на то, что у больных ревматическими заболеваниями при беременности или желтухе наступает выраженное облегчение состояния. Ученый совершенно правильно предположил, что улучшение самочувствия может быть обусловлено появлением в организме больных какого-то стероидного вещества, подобного либо половым гормонам, выделяемым при беременности в повышенных количествах, или желчным кислотам, накапливающиеся при желтухе. 21 сентября 1948 года была сделана первая попытка лечения кортизоном больного, страдавшего тяжелым хроническим суставным ревматизмом. Ученые не скрывали своих планов, и вся клиника с волнением следила за результатами эксперимента. Через несколько дней случилось чудо. Больной, который в течение 6 лет не мог подняться с постели из-за мучительных болей, самостоятельно встал. Попробовали новый метод лечения на другом больном – результат опять превзошел все ожидания. И пусть потом при детальных исследованиях ажиотаж первоначального восторга спал, обнаружились побочные эффекты действия гормонов коры надпочечников, и пришлось ограничить их применение, это уже неважно, с этим врачи научились справляться. Главное, что в 1948 году получила права гражданства кортикостероидная терапия, которая открыла новую эру в лечении ревматизма и спасла миллионы человеческих жизней. Научный мир по достоинству оценил это открытие. Кевдэлл, Хенч и Рейхштейн в 1950 году были удостоены Нобелевской премии.
Дата добавления: 2015-02-06 | Просмотры: 1936 | Нарушение авторских прав |
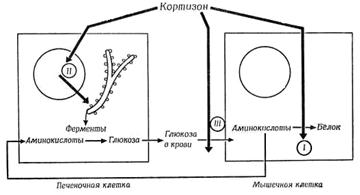
 Глюкокортикоиды участвуют в регуляции углеводного обмена, вызывают повышение содержания в крови глюкозы (поэтому – соответствующее название). Это повышение происходит за счет того, что гормоны вызывают активацию глюконеогенеза – образование глюкозы из аминокислот и жирных кислот (рис. 5.2.1).
Глюкокортикоиды участвуют в регуляции углеводного обмена, вызывают повышение содержания в крови глюкозы (поэтому – соответствующее название). Это повышение происходит за счет того, что гормоны вызывают активацию глюконеогенеза – образование глюкозы из аминокислот и жирных кислот (рис. 5.2.1).