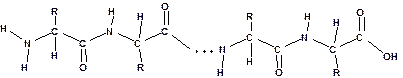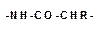|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Классификация. Определение: Белки – это сложные высокомолекулярные органические соединения , построенные из остатков аминокислотОпределение: Белки – это сложные высокомолекулярные органические соединения, построенные из остатков аминокислот, соединенных между собой амидными связями. Белки разделяются на протеины (простые белки), в состав которых входят только остатки аминокислот и протеиды (сложные белки). Это белки построенные не только из аминокислот, но и из других веществ: сахаридов или остатков фосфорной кислоты и нуклеиновые кислоты. Протеины классифицируются по трем группам. 1. По растворимости в воде: Альбумины - растворимые в воде и разбавленных растворах солей. Глобулины – мало растворимые в воде и растворимые в разбавленных растворах солей. Проламины – нерастворимые в воде и растворимые в водном спирте. Глютелины - нерастворимые в воде, в разбавленных растворах солей и водном спирте, растворимы в растворах кислот и щелочей. Склеропротеины - нерастворимые в воде, в разбавленных растворах солей, водном спирте и в растворах кислот и щелочей.
2. Протеиды классифицируются по продуктам гидролиза: Нуклеопротеиды – гидролизуются на протеины и нуклеиновые кислоты. Фосфопротеиды - гидролизуются на протеины и фосфорную кислоту. Глюкопротеиды - гидролизуются на протеины и углевод. Хромопротеиды - гидролизуются на протеины и красящие вещества.
3. Все белки классифицируются по функциям в организме: Резервные белки Структурные белки Белки, управляющие метаболизмом.
Как и аминокислоты, белки обладают амфотерным характером и изоэлектрической точкой. Положение изоэлектрической точки для белков может колебаться в широких пределах от кислой до сильнощелочной. Все белки оптически активны. Большинство из них обладает левым вращением.
Существует ряд качественных цветных реакций на белки: 1. Ксантопротеиновая с азотной кислотой. Белки обработанные азотной кислотой дают желтое окрашивание. 2. Биуретовая с солями меди в присутствии щелочи. Белки дают фиолетовую окраску за счет образования комплексной соли. 3. Реакция Миллона. С раствором нитрата ртути в азотистой кислоте белки дают красное окрашивание. 4. Сульфгидрильная. При нагревании белков с раствором плюмбита натрия выделяется черный осадок сульфида свинца.
Белки построены из остатков 26 аминокислот. Аминокислоты делятся на заменимые, которые могут быть синтезированы организмом и незаменимые, которые человеческим организмом не синтезируются. Например, изолейцин и треонин. Остатки аминокислот связаны в белковой молекуле амидными связями. Амидная связь в белках называется пептидной связью:
Карбоксильная группа одной молекулы аминокислоты образует амид, взаимодействуя с аминогруппой соседней молекулы аминокислоты. Отдельные пептидные звенья:
отличаются друг от друга только радикалами «R» при α-углеродном атоме.
Соединения, содержащие несколько аминокислотных остатков, называются пептидами. Соединения с большим количеством пептидных звеньев называются полипептидами.
При исследовании полипептидов в первую очередь выясняют из каких аминокислот построена макромолекула, а также какая аминокислота является N-концевой (свободная аминогруппа), а какая является С-концевой (свободная корбоксильная группа). Белки нацело гидролизуются в аминокислоты концентрированной соляной кислотой или 2% соляной кислотой при нагревании и при повышенном давлении. Гидролиз белков можно провести под действием щелочи. Выбор реагента зависит от того, какие конкретно аминокислоты необходимо получить из молекулы белка.
Дата добавления: 2015-12-15 | Просмотры: 692 | Нарушение авторских прав |