|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Місце розташування, розмір і структура підшлункової залозиПідшлункова залоза є органом і зовнішньої і внутрішньої секреції. Ендокринна частина залози представлена окремими клітинними групами, що утворять невеликі острівці в масі всієї іншої її тканини. Ці групи клітин називають острівцями Лангерганса. Число острівців найбільше в хвостовій частині залози. Розмір одного острівця складає 0,1–0,3 мм, число їх від 200 тис. до 1,8 млн. Деякі острівці відділені від оточуючих їх тканин тонкою сполучнотканинною оболонкою. В острівцях Лангерганса розрізняють чотири групи клітин: α, β, γ і δ. Вони неоднаково забарвлюються і виконують різні функції. Більше всього зустрічається β-клітин (70%), примерно 20% від числа всіх клітин приходиться на а α -клітини і приблизно по 5% складають γ – і δ -клітини. Гормони підшлункової залози. В острівцях Лангерганса утворюються три гормони: інсулін, глюкагон і ліпокаїн. Значення інсуліну було виявлено ще в 1889 р., коли дослідники Меринг і Мінковский, видаливши в собаки підшлункову залозу, знайшли в її сечі цукор. Звідси ними був зроблений висновок, що підшлункова залоза регулює кількість цукру в організмі. Росіянин учений Л. В. Соболєв у 1902р. показав, що підшлункова залоза поряд з екзокринною виконує й ендокринну функцію. Він перев’язав вивідну протоку підшлункової залози, після чого відзначав загибель клітин, у яких утвориться секрет, що виділяється в дванадцятипалу кишку, у той час як острівкова тканина не піддавалася зміні і збудження обміну вуглеводів не відзначалося. У 1921 р. ученые Бантиг і Бест виділили з острівців гормон, названий ними інсуліном (insula –острівець). В даний час цілком вивчена структура інсуліну і він штучно синтезований. Молекула інсуліну складається з двох ланцюгів: А и В. Ланцюг А включає 21 амінокислотний залишок, а ланцюг В – 13-30. Встановлено, що інсулін утворюється в β-клітинах. Для його зв’язування з білком гранул і наступного звільнення необхідний цинк. Інсулін стимулює синтез глікогену в печінці і м’язах, гальмує його перетворення в цукор і сприяє окислюванню цукру в м’язах. Тому після вимикання функції острівців Лангерганса (є лікарські препарати, що вибірково їх ушкоджують), у крові різко збільшується вміст цукру, що називається гіперглікемією, і він починає з’являтися в сечі. Наявність цукру в сечі називають глюкозурією. При введенні інсуліну різко зменшується кількість цукру в крові з 80-120 до 30-45 мг%. Зменшення кількості цукру в крові називають гіпоглікемією.
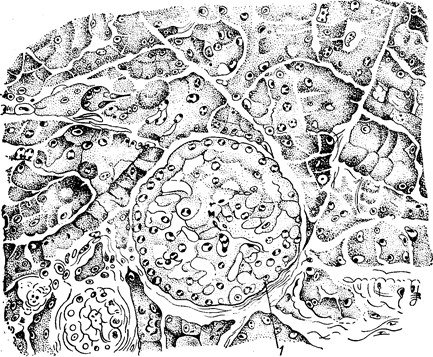
Рис. 62 Мікроструктура підшлункової залози. Глюкагон утворюється в α-клітинах, складається з 29 амінокислотних залишків і діє протилежно інсуліну. Він викликає гіперглікемію і зменшує вміст глікогену в печінці. Ліпокаїн сприяє виходу жирів з печінки, окисленню їх у ній і гальмує перетворення вуглеводів у жири. Секреція гормонів острівцями Лангерганса регулюється вмістом цукру в крові, α-и β-клітини сприймають зміни концентрації цукру в крові, і за принципом негативного зворотного зв’язку міняється активність цих клітин. Гіперглікемія активує β-клетки і гальмує α-клітини, а гіпоглікемія активує α-клітини і гальмує β-клітини. Механізм дії гормонів підшлункової залози. Вважають, що є кілька шляхів впливу гормонів підшлункової залози на вуглеводний обмін. Інсулін сприяє проникненню глюкози через мембрану клітини і її внутрішньоклітинному нагромадженню. Крім того, інсулін індукує синтез ферментів, що сприяє синтезу глікогену й окисленню глюкози. Глюкагон збільшує вміст ферменту, що викликає розщеплення глікогену. Гіпер- і гіпофункція підшлункової залози. Гіперфункція підшлункової залози – дуже рідке захворювання. Воно виявляється в гіпоглікемії й у зв’язаному з цим порушенні діяльності центральної нервової системи, що надзвичайно чутлива до нестачі глюкози. Виникають слабість, судороги, втрата свідомості. Уведення глюкози знімає всі ці явища. При гіпофункції підшлункової залози виникає цукровий діабет. Він характеризується цілим рядом симптомів, виникнення яких пов’язане зі збільшенням вмісту цукру в крові. Кількість його може підвищуватися до 200-500 мг%. При цьому в кров переходить рідина з тканин, що приводить до їх зневоднювання. Хворий постійно відчуває спрагу. Він випиває близько 10 л води, велика частина якої надходить у кров і виділяється нирками. За добу в таких хворих виділяється від 3 до 12, а в рідких випадках до 25 л. Ослаблення процесів окислювання глюкози приводить до збудження обміну жирів. Утворюються продукти неповного окислення жирів – кетонові тіла, що приводить до зрушення реакції крові в кислу сторону – до ацидозу. Інсулін – ефективний засіб лікування діабету. Він дає можливість протягом десятиліть зберігати працездатність хворих. РОЗДІЛ VІІІ ВІКОВІ ОСОБЛИВОСТІ ВІКОВІ ОСОБЛИВОСТІ ГІПОФІЗА Гіпофіз має ектодермальне походження. Аденогіпофіз (разом із проміжною часткою) формується з епітелію ротової порожнини, а нейрогіпофіз – із проміжного мозку. У дітей між передньою і проміжною частками є щілина. У дорослих ця щілина заростає й обидві частки тісно прилягають один до одного. Маса гіпофіза немовляти складає 100-150 мг. На другому році життя починається його збільшення, що виявляється особливо різким у 4-5 років, після чого до 11 років настає період уповільненого росту гіпофіза. З 11 років знову швидкість його росту збільшується. До періоду статевого дозрівання маса гіпофіза в середньому складає 200-350 мг, а до 18-20 років – 500-650 мг. Ацидофільні клітини гіпофіза з’являються на 13-15-й тиждень внутрішньоутробного розвитку. Після народження дитини число їх росте до 20 років, з 20 до 50 років залишається без зміни, а потім зменшується. Функція ацидофільних клітин починається уже в період внутрішньоутробного розвитку: її відзначали у плодів довжиною 50 мм. Кількість соматотропного гормону, виділюваного цими клітинами, у дітей до 3-5 років більше, ніж у дорослих. З 3-5 років установлюється норма виділення соматотропного гормону, характерна для дорослого. Кількість виділюваного соматотропного гормону (СТГ) відповідає дозріванням відповідних клітин гіпоталамуса. Показано, що з віком зменшується кількість релизинг-факторов, що викликають виділення соматотропного гормону гіпофіза. Чутливість різних тканин до дії СТГ із віком збільшується. Це виявляється в збільшенні інтенсивності клітинного розподілу, синтезу білка і РНК під впливом СТГ.
 СТГ у більшості випадків виділяється протягом усього життя. Припинення росту, незважаючи на наявність СТГ, залежить від збільшення в період статевого дозрівання кількості естрогенів, що зменшують його активність. СТГ у більшості випадків виділяється протягом усього життя. Припинення росту, незважаючи на наявність СТГ, залежить від збільшення в період статевого дозрівання кількості естрогенів, що зменшують його активність.
Сліди адренокортикотропного гормону (АКТГ) уперше виявляються в гіпофізі на 9–10-й тиждень внутрішньоутробного періоду. У гіпофізі немовлят відзначається така ж кількість АКТГ, як і в гіпофізі дорослих. Разом з тим комплекс адаптаційних реакцій, що розвиваються при дії стрес-факторів, у немовлят або зовсім відсутній, або виражений у дуже слабко. Це пов’язано з віковими особливостями функцій гіпоталамічних структур. Їх чутливість до імпульсів, що несуть інформацію про зміни, що відбуваються у внутрішньому і зовнішньому середовищі організму, збільшується з віком. Відповідно, підсилюється вплив ядер гіпоталамуса на функцію аденогіпофіза, що в умовах стресу супроводжуємося збільшенням секреції АКТГ. У старості чутливість ядер гіпоталамуса до інформації, що приходить по нервових шляхах, знову падає, з чим зв’язана менша виразність у літньому віці адаптаційного синдрому. Зниження чутливості гіпоталамічних ядер пов’язують зі зменшенням числа їх нейросекреторних клітин. Тиреотропний гормон (ТТГ) гіпофіза також починає виділятися ще у внутрішньоутробний період розвитку. Однак, відповідно малому числу базофільних клітин, кількість його невелика. На першому році життя збільшується число базофильных клітин гіпофіза і разом з тим росте кількість виділюваного ТТГ. Найбільш різке збільшення виділення ТТГ відзначається відразу після народження і перед початком періоду статевого дозрівання. В наступні роки аж до кінця періоду статевого дозрівання продовжується збільшення його секреції, максимум якої досягається у віці від 21 до 30 років. У віці 51-85 років величина її стає в два рази меншою, чим у 21-30 років. Антидіуретичний гормон гіпофіза починає виділятися на четвертому місяці ембріонального розвитку, максимум його виділення відзначається до одного року після народження, потім антидіуретична активність нейрогіпофіза починає падати до досить низьких величин і у віці 55 років вона приблизно в 2 рази менше, ніж у віці 1 року. Для клітин, зв’язаних із секрецією гонадотропних гормонів, характерна циклічність їх функції. Так, найбільша інтенсивність секреції відзначається в 4-4,5 місяці ембріонального розвитку, у дітей – у період статевого дозрівання й у дорослих – у період згасання статевої функції, коли зменшується кількість естрогенів і, відповідно, знімається їх гальмуюча дія на підгорбкову область. ВІКОВІ ОСОБЛИВОСТІ ЩИТОВИДНОЇ ЗАЛОЗИ Щитовидна залоза є одним з перших органів, що вдається розрізнити в людського ембріона. Зачаток її з’являється на 3-й тиждень ембріонального розвитку у виді стовщення ентодерми, що вистілає дно глотки. У зародка довжиною 23мм щитовидна залоза втрачає свій зв’язок із глоткою. У немовляти маса щитовидної залози коливається від 1 до 5 г. Вона трохи зменшується до 6 місяців, а потім починається період швидкого її збільшення, що продовжується до 5 років. З 6-7 років період швидкого збільшення маси щитовидної залози змінюється повільним. У період статевого дозрівання знову відзначається швидке збільшення маси щитовидної залози, що досягає маси залози дорослої людини.
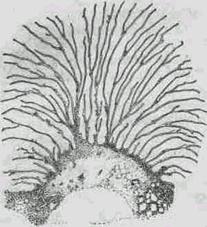
Уже на другому-третьому місяцях внутрішньоутробного розвитку в центрі фолікула з’являється колоїд. На 14-15-й тиждень щитовидна залоза починає Рис. 64 Розріз щитовидної залози на рівні перешийка:у горі – у немовляти; внизу – у дорослого. 1 – стравохід; 2 – трахея; 3 – щитовидна залоза. виявляти свою секреторну активність. Здатність до концентрації йоду в щитовидній залозі з’являється на 14-й тиждень, а зв’язування його в органічну форму відзначається від 15-го до 19-го тижня ембріонального розвитку. До моменту народження щитовидна залоза є функціонально активною, однак і в постнатальному розвитку відповідно до триваючого морфологічного дозрівання відбувається удосконаленняїїфункції. Обивдва цих процеси, і морфологічне і функціональне дозрівання, направляються ТТГ гіпофіза. Тому коливання в інтенсивності виділення гормонів щитовидною залозою цілком відповідають коливанням у секреції ТТГ гіпофіза. Найбільше збільшення секреції відзначається в періоди раннього дитинства і статевого дозрівання. Максимум активності щитовидної залози досягається в 21-30 років, після чого починається поступове зменшення інтенсивності її функціонування. Воно обумовлюється не тільки падінням кількості ТТГ гіпофіза, але і зниженням з віком чутливості до нього щитовидної залози. Чутливість тканин до граничної величини гормону щитовидної залози з віком збільшується. У той же час інтенсивність уже виниклої реакції в дітей більше, ніж у дорослих, що говорить про більшу реактивність їх тканин по відношенню до гормонів щитовидної залози. ВІКОВІ ОСОБЛИВОСТІ НАДНИРНИКІВ Наднирники починають формуватися в ранньому онтогенезі. У людини зачатки кори наднирників уперше виявляються на початку 4-й тижня внутрішньоутробного життя. В ембріона в 10 смв епітеліальний зачаток проникають нервові клітини, що формують мозковий шар наднирників. Уже в місячного ембріона людини маса наднирників дорівнює, а іноді і перевершує масу нирок. У немовляти маса наднирників складає близько 7 г. До шести місяців вона дещо зменшується, після чого починає збільшуватися. Темпи росту наднирників неоднакові в різні вікові періоди. Особливо різке збільшення наднирників відзначається в 6-8 місяців і в 2-4 роки. Відношення маси наднирників до маси всього тіла найбільше в немовляти: маса наднирників у них складає 0,3% від маси тіла, у дорослої ж людини – 0,03%. Збільшення маси наднирників продовжується до 30 років. Структура наднирників, характерна для ембріонального періоду, змінюється після народження дитини. У постнатальный період розвитку перероджується центральна частина їх кіркової речовини і відбувається заміна його знову утвореною тканиною, відновлення якої йде від периферії до центра. У немовляти кіркова речовина складається з двох неоднорідних частин. На периферії розташовані клітини, здатні посилено розмножуватися,– це проліферативний шар, що має вид вузької жовтої смужки.
Ближче до центра розташований широкий шар, що має червоне забарвлення. У процесі наступного розвитку товщина червоного шару зменшується, так що до одного року він перетворюється у вузьку смужку, а жовтий шар, навпаки, розширюється. Жовтий шар відповідає клубочковій і пучковій зонам наднирників, а червоний – сітчастій. На границі коркової і мозкової речовини наднирників з’являється тонка сполучнотканинна мембрана. Раніш за все формується пучкова зона, що зберігає свою високу функціональну активність до старості. Вже в ембріональний період розвитку починається секреція глюкокортикоїдів. Відсутність у немовлят адаптивного синдрому, незважаючи на гарний розвиток у них пучкової зони, зв’язано з недостатнім виділенням АКТГ. Клубочковая зона досягає максимального розвитку в період статевого дозрівання. До старості клубочкова і сітчаста зони різко зменшуються. Про кількість гормонів кори наднирників судять по кількості стероїдів, виведених із сечею. Виявилося, що в немовлят їх виділяється в добу менш 1 мг, у 12 років – 5 мг, у період статевого дозрівання – 14 мг. Після 30 років кількість гормонів кори наднирників починає зменшуватися. Інтенсивність реакції тканин на введення гормонів кори наднирників тим більше, чим менше вік. Мозкова речовина наднирників з’являється пізніше кіркової. Лише на 4-му місяці внутрішньоутробного розвитку відзначається вростання адреналової тканини в інтерреналову. На 5-6-му місяці виявляється секреторна функція хромофінних клітин. ВІКОВІ ОСОБЛИВОСТІ СТАТЕВИХ ЗАЛОЗ Чоловічі і жіночі статеві залози (насінники і яєчники), сформувавши в період внутрішньоутробного розвитку, піддаються повільному морфологічному і функціональному дозріванню уже після народження. Маса яєчка в немовлят складає 0,3 г, у 1 рік – 1 г, у 14 років – 2 г, у 15-16 років – 8 г, у 19 років – 20 г. Насінні канальці у новонароджених вузькі, за весь період розвитку їх діаметр збільшується в 3 рази. Яєчники закладаються вище порожнини малого таза, і у новонароджених процес їх опускання ще не закінчений. Вони досягають порожнини малого таза в перші 3 тижні після народження, але лише до 1-4 років остаточно встановлюється їх положення, характерне для дорослого. Маса яєчника у немовляти складає 5-6 г, і вона мало міняється протягом наступного розвитку: у дорослого маса яєчника дорівнює 6-8 г. У старості маса яєчника зменшується до 2 г. У період дитинства в яєчнику дівчаток дуже повільно ростуть примордіальні фолікули, у яких у більшості випадків оболонка ще відсутня. У хлопчиків насінні канальці в насінниках мало звиті. У сечі поза залежністю від статі міститься невелика кількість андрогенів і естрогенів, що утворюються в цей період у корі наднирників. Вміст андрогену у плазмі крові дітей обох статей відразу ж після народження такий же, як і в молодих жінок. Потім він знижується до дуже низьких цифр (іноді до 0) і залишається на такому рівні до 5-7 років. У період отроцтва в яєчниках з’являються граафові пухирці, фолікули швидко ростуть. Насінні канальці в насінниках збільшуються в розмірах, поряд зі сперматогоніямі з’являються сперматоцити. У цей период у хлопчиків зростає в плазмі крові й у сечі кількість андрогенів; у дівчаток – естрогенів. Їх кількість ще більше збільшується в юнацький період, що обумовлює розвиток вторинних статевих ознак. У цей період з’являється властива жіночому організму періодичність у кількості секретованих естрогенів, що забезпечує жіночий статевий цикл. Різке підвищення секреції естрогенів збігається за часом з овуляцією, після чого при відсутності запліднення настає менструація, якою називають виділення назовні слтзової оболонки матки разом із вмістом маткових залоз і кров’ю із судин, що розкриваються при цьому. Сувора циклічність у кількості естрогенів, що виділяються, і, відповідно, у змінах, що мають місце в яєчнику і матці,установлюється не відразу. Перші місяці статеві цикли можуть бути нерегулярними. З установленням регулярних статевих циклів починається період статевої зрілості, що продовжується в жінок до 45-50 років, а в чоловіків у середньому до 60 років. Період статевої зрілості в жінок характеризується наявністю регулярних статевих циклів: яєчникового і маткового.
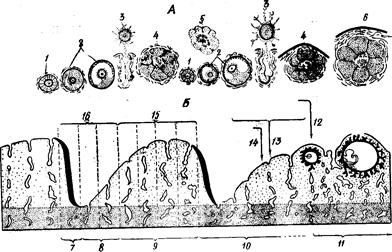
Рис. 66 Зіставлення циклічних змін Яєчниковий цикл продовжується в середньому 28 днів і складається з фолікулярної фази, овуляції і лютеїнової фази. Фолікулярна фаза характеризується розвитком фолікула, що розривається під час овуляції. У лютеїнову фазу на місці фолікула, що лопнув, утворюється жовте тіло. Поки функціонує жовте тіло, що секретує прогестерон, чергової овуляції відбутися не може, хоча фолікули при цьому розвиваються. За кілька днів перед овуляцією жовте тіло попередньої овуляції гине. Прогестерон з’являється в сечі через 2-3 дні після овуляції і зникає за 2-3 дні до настання чергової менструації. Найбільші кількості естрогенів відзначаються в період перед овуляцією і менструацією. Установлено, що великі кількості естрогенів у середині циклу, тобто перед овуляцією, викликають посилену секрецію лютеинизирующего гормону гіпофіза, під впливом якого відбувається овуляція. Прогестерон гальмує секрецію лютеїнізуючого гормону, що перешкоджає овуляції. Яєчниковому циклу відповідає матковий цикл. Він складається з фази десквамації, чи менструальної кровотечі, що продовжується 3-5 днів, фази регенерації – відновлення слтзової, що закінчується до 5-6-го дня від початку менструації, фази проліферації, що характеризується стовщенням слтзової оболонки матки, і фази секреції, коли починається секреція її залоз, збільшення розмірів клітин, відкладення в слтзової глікогену, фосфору, кальцію й інших речовин. Перші три фази збігаються за часом з фолікулярною фазою яєчникового циклу і продовжуються до 14 дня від початку менструації. Фаза секреції приходиться на другу половину яєчникового циклу і збігається з лютеїновою фазою. Фаза проліферації здійснюється під впливом естрогенного гормону, а фаза секреції – прогестерону. Якщо не відбувається запліднення яйлеклітини, жовте тіло гине, що викликає припинення секреції яєчників – прогестерону. При цьому знімається його гальмуюча дія на нейрогіпофіз, у результаті чого в крові наростає кількість окситоцина, що супроводжується появою менструації, тому що він викликає скорочення мускулатури стінки матки. Збільшенню кількості окситоцина сприяє також збільшення перед менструацією кількості секретованих естрогенів. У чоловіків період полової зрілості характеризується формуванням зрілих, здатних до запліднення сперматозоїдів, що виділяються назовні в момент еякуляції – виділення сперми, що відбувається під час статевого акту. Клімакс у жінки виявляється в нерегулярних статевих циклах, що пов’язано із загибеллю фолікулів і зменшенням виділення естрогенів. Це ж є причиною цілого ряду вегетативних розладів в організмі, що спостерігаються в цей період: змін кров’яного тиску, терморегуляції, інтенсивності обмінних процесів і т.д. У чоловіків у період угасання статевої функції втрачається рухливість сперматозоїдів, здатність до еякуляції і здійснення статевого акту, відбувається поступова атрофія насінників. ВІКОВІ ОСОБЛИВОСТІ ПАРАЩИТОВИДНИХ ЗАЛОЗ Паращитовидні залози виявляються на 6-й тиждень ембріонального розвитку. Уже у зародка довжиною 0,9 см відзначається диференціювання клітинних елементів цих залоз, у результаті якої у зародка довжиною 16 см виділяються п’ять груп різних клітин. Вважають, що на цій стадії розвитку починається секреція паратгормона. Після народження дітей продовжується дозрівання паращитовидних залоз, що знаходить висвітлення в збільшенні з віком кількості виділюваного гормону. Найбільша активність паращитовидних залоз відзначається в перші 4-7 років життя. ВІКОВІ ОСОБЛИВОСТІ ВИЛОЧКОВОЇ ЗАЛОЗИ Й ЕПІФІЗА Вилочкова залоза починає формуватися на 6-й тиждень ембріонального розвитку. Її маса в немовляти дорівнює 10-14 г. Приріст маси в перші роки життя складає 4-5 г, у 6-10 років – 26 г. До 11-15 років її маса збільшується до 37-38 г, після чого вона починає зменшуватися й у 15-20 років стає рівною 21 г, у 20-25 років – 18-20 г, у 40 років – 15 г и в 75 років – 4-5 г. У ранньому дитячому віці в зобній залозі переважає кіркова речовина, кількість сполучної тканини невелика. У період статевого дозрівання в ній збільшується кількість сполучної тканини, а кіркова і мозкова речовина зменшується. У зрілому віці відзначається сильне розростання сполучної і жирової тканини і майже повна відсутність кіркової і мозкової речовини. У старечому віці зобна залоза являє собою однорідний сполучнотканиный тяж. Епіфіз з’являється на 6-7-й тиждень внутрішньоутробного розвитку. Його маса при народженні складає 7 мг, а в дорослого – 100-200 мг. Збільшення розмірів епіфіза і його маси продовжується до 4–7 років, після чого він піддається зворотному розвитку – інволюції. Диференціювання клітинних елементів починається на першому році життя і продовжується протягом декількох років. В міру диференціювання клітинних елементів росте кількість виділюваного гормону. Незважаючи на інволюцію епіфіза, аж до старечого віку зберігаються окремі діяльні клітини, для яких характерна секреторна активність. ВІКОВІ ОСОБЛИВОСТІ ПІДШЛУНКОВОЇ ЗАЛОЗИ Ендокринна частина підшлункової залози починає формуватися на 5–6-й тиждень внутрішньоутробного розвитку, коли відбувається поділ її клітин на екзо- і ендокринні. При диференціюванні клітинних елементів спочатку виділяються b-клітини (на 3-му місяці ембріонального розвитку), а потім стають видимимі a-клітини. До кінця 5-го місяця в підшлунковій залозі плоду виявляються добре сформованими острівці Лангерганса. У дітей перших двох місяців життя відносне число їх більше,ніжу наступні періоди розвитку. Вони складають 6% від маси всієї залози. Наприкінці першого року життя на їх частку приходиться 1-0,8%, і таке співвідношення ендокринної і екзокринної частин підшлункової залози зберігається до 40-50 років. До старості процентний вміст острівцевої частини залози дещо збільшується (до 2-3%). З віком збільшуються розміри острівців від 50 мкм у період новонародженості до 100-200 мкм у віці від 10 до 50 років. Після 50 років розмір острівців знову зменшується. Характерні вікові зміни спостерігаються у вмісті цинку, що входить до складу гормонів підшлункової залози. Гранули цинку в клітинах підшлункової залози з’являються вже на 6-й тиждень ембріонального розвитку. У перші місяці після народження відзначається максимальний вміст цинку, що зберігається протягом періоду зрілості. У старості кількість цинку в гормонах різко знижується, відбувається розростання сполучної тканини і відносне збільшення числа клітин, що синтезують глюкагон за рахунок зменшення числа клітин, секретуючих інсулін. Цими змінами структури обумовлюються функціональні вікові особливості. У дітей перших шести місяців життя інсуліну виділяється в два рази більше, ніж у дорослих. Після сорока років падає активність ендокринного апарату підшлункової залози і зменшується відповідно до цього кількість секретованого нею гормону. Зменшення секреції інсуліну з одночасним відносним збільшенням у старості кількості глюкагона створює несприятливі умови для обміну вуглеводів і може послужити причиною розвитку цукрового діабету. РОЗДІЛ ІХ КРОВ Кров являє собою рідку тканину, що складається з плазми і формених елементів. Усього в організмі людини міститься 4,5–6 л крові, що складає 1/13 маси тіла. На долю плазми приходиться 54% об`єму крові, а на частку формених елементів – 46%. Кров, що циркулює в судинах, входить у поняття системи крові, що включає ще органи кровотворення, кроворуйнування та апарат регуляції складу крові. ЗНАЧЕННЯ КРОВІ Гомеостаз. Кров, лімфа і міжтканева рідину складають внутрішнє середовище організму. Однією з характерних її особливостей є гомеостаз – відносна сталість складу, фізичних і хімічних властивостей. Гомеостаз забезпечує життєдіяльність усіх клітин і тканин організму. Він необхідний для їх нормального функціонування. Межі коливань різних факторів зовнішнього середовища можуть бути значно більше тих, котрі сумісні з можливістю збереження функції клітин. Однак, завдяки тому що безпосереднім середовищем, у якім клітини знаходяться, є внутрішнє середовище організму, що характеризується відносною сталістю складу і властивостей, підтримується їх діяльність навіть при різких коливаннях зовнішніх умов. У цьому полягає одне зі значень крові для організму. Транспортна функція. Кров, знаходячись у постійному русі, виконує в організмі транспортну функцію. З кров’ю переноситься кисень від легень до всіх тканин організму, у зворотному напрямку переноситься вуглекислий газ (CO2). Здійснюючи перенос газів, кров бере участь у дихальній функції організму і сприяє підтримці кислотно-лужної рівноваги, тому що звільняє тканини від надлишку вуглекислого газу, що постійно в них утворюється. З кров’ю переносяться від органів травлення до тканин різні живильні речовини: амінокислоти, глюкоза, жири, мінеральні речовини, вітаміни. Усі вони утилізуються різними тканинами організму, а надлишок їх відкладається в депо, звідкіля вони переносяться знов-таки кров’ю до ділянки організму, що потребує їх. Таким чином, кров, транспортуючи живильні речовини, бере участь у живильній функції організму. Кров переносить продукти обміну речовин (сечовина, сечова кислота й ін.) від місця їх утворення до місця їх виділення, беручи участь у екскреторній функції організму. Транспортуючи гормони і усілякі фізіологічно активні речовини, кров здійснює гуморальну регуляцію функцій організму. Роль крові в теплорегуляції. В організмі є механізми, що забезпечують швидке звуження судин шкіри при зниженні температури навколишнього повітря і розширення судин при її підвищенні. Це приведе до зменшення чи збільшення віддачі тепла, тому що плазма складається на 90–92% з води і має внаслідок цього високу теплопровідність і питому теплоємність. Захисна функція. Захисна функція крові – це дуже широке поняття, тому що усе, що зв’язано з діяльністю системи крові, має захисне для організму значення. Кров захищає клітини живого організму від шкідливого впливу надмірно сильних коливань умов зовнішнього середовища. Згортання крові, обумовлена білками її плазми, захищає організм від крововтрат. Переносячи вуглекислий газ і кисень, кров захищає клітини від загибелі внаслідок недостатності кисню чи надлишку вуглекислого газу і т.д. Однак звичайно говорять про захисну функцію крові в більш вузькому значенні цього слова, розуміючи під захисною функцією захист організму від чужорідних для нього макромолекул, якими є білкові макромолекули бактеріальної клітини, вірусів, різні токсини. Проти цих чужорідних елементів у крові виробляються антитіла, з наявністю яких зв’язана захисна функція крові. Остання залежить також від активності лейкоцитів – білих кров’яних тілець. Лейкоцити мають здатність до поглинання і наступного перетравлення чужорідних елементів. В даний час встановлено, що лейкоцити беруть участь у виробленні антитіл. СКЛАД І ВЛАСТИВОСТІ ПЛАЗМИ КРОВІ Склад плазми. На частку сухої речовини плазми приходиться 8–10%. З них 6,5–8,2% складають білки. У значно меншій кількості в крові містяться небілкові азотисті з’єднання: поліпептиди, амінокислоти, сечовина, сечова кислота, креатин, креатинин, білірубін, індикан. Поліпептидів і амінокислот, що представляють собою продукти розщеплення білка, знаходиться в крові приблизно 4–10 мг% (4–10 мг у 100 м крові). Сечовини в плазмі міститься 10–24 мг%. Кількість її може незначно підвищитися при прийнятті багатої білками їжі чи при значній утраті води організмом, коли концентрация її в плазмі збільшується. Однак у здоровому організмі зрушення у вмісті сечовини в крові бувають короткочасними. Тривале збільшення кількості сечовини в крові, що відмічається при захворюваннях нирок, викликає важкі отруєння. У плазмі крові міститься 2,7 мг% сечової кислоти.Призахворюваннях, що супроводжуються порушенням обміну, кількість її може зростати до 6–8 мг%. Креатин і креатинин містяться в плазмі в незначній кількості: креатинина – 1–2 мг%, креатину – 3–5 мг%. Білірубін, що є продуктом розпаду гемоглобіну, міститься в плазмі ще в меншій кількості – 0,2–1,0 мг%. Усі ці продукти білкового обміну називають залишковим азотом. У плазмі крові його знаходиться від20до 40 мг%. Крім азотистих речовин у плазмі крові є ще цілий ряд безазотистих органічних сполук: глюкоза (100–120л(м%), жири (400–800 мг%), холестерин (100–250 мг%) і ін., а також різні мінеральні речовини, на частку яких приходиться 1 % від сухої речовини плазми. У плазмі містяться катіони Na+, К+, Са++, Mg++ і аніони С1-, НСОз-, НРО4-, Н2РО4-. Особливо великий вміст Na+ (280–350 мг%) і С1- (320–360 мг%). У менших кількостях у плазмі міститься K+ (19,8–20,6 мг%), Са++ (9–11 мг%), Mg++ (1–3 мг%). Йод, бром і залізо містяться в плазмі в дуже малій концентрації (тисячні частки мг%). У плазмі крові містяться різні ферменти. Однизних необхідні в процесі згортання крові. Інші розщеплюють живильні речовини. Наприклад, плазма містить амілазу, що діє на вуглеводи, і ліпазу, що розщеплює жири. Завжди в плазмі крові здорової людини присутні різні вітаміни. Білки плазми. Білки плазми в залежності від їх структури, властивостей і особливостей біологічної дії поділяють на декілька груп: альбуміни, глобуліни, фібриноген і протромбін. Крім цих видів білків, у плазмі розрізняють з’єднання білків з жирами – ліпопротеіни – і складне комплексне з’єднання пропердин. На долю альбумінів приходиться 50–60% усіх білків плазми. Вони володіють найменшої з усіх білків плазми молекулярною масою. Їх синтез відбувається в печінці. Глобуліни складають 35–40% від усіх білків плазми. Вони різні за будовою і властивостям, у зв’язку з чим їх поділяють на α1, α2, β і γ-глобуліни. Синтезуються глобуліни в печінці іувсіх елементах ретикуло-ендотеліальної системи. Фібриногену міститься в плазмі 4% від усіх її білків. Утворюється він у печінці. Молекулярна маса його велика. Він більш чим у два рази важче глобулінів. Протромбін, що синтезується також у печінці, має меншу, чим фібриноген, але більшу, чим альбумін, молекулярну масу. Його міститься в плазмі 10–20 мг%. Рис. 66. Згортання крові:
Жири у вільному виді містяться в плазмі тільки після прийому дуже жирної їжі. Звичайно вони знаходяться в комплексі з білками й у вигляді цих з’єднань – ліпопротеінів – транспортуються кров’ю. Ще більш складним за структурою, чим ліпопротеіни, є пропердин. Він складається з білка, жирів, полісахаридів і іонів магнію. Білки крові виконують в організмі різноманітні функцій. Вони регулюють розподіл води між судинною системою і тканинами організму; за рахунок властивих їм буферних властивостей сприяють збереженню на тому самому рівні активної реакції крові; беруть участь у транспорті гормонів, вітамінів, продуктів обміну речовин; виконують захисну функцію. Установлено, що особливо велику роль у боротьбі з чужорідним білком мають глобуліни, які мають назву γ-глобуліни, і пропердин. Глобуліни в плазмі є носіями антитіл. Пропердин відносять до систем, що створюють в організмі природний імунітет. Він нейтралізує в організмі бактерії і віруси. Білки плазми забезпечують процес згортання крові. Згортання крові. Згортанням крові називають процес утворення згустку – тромбу – крові, що складається з плазми і формених елементів. В основі згортання лежить утворення ниток фібрину з білка плазми фібриногену. Здатність крові до згортання є необхідною захисною реакцією, що охороняє організм від крововтрат. У плазмі здорової людини є усі компоненти, необхідні для її здійснення. Вони формують згортаючу систему крові. Однак у нормі в судинній системі процес тромбоутворення не повинний протікати, тому що це привело б до порушення циркуляції крові. У плазмі крові є ряд факторів, що утворюють протизгортаючу систему. Активність однієї та другої системи регулюється рефлекторно і гуморально, що забезпечує тонке пристосування діяльності систем до змін, що відбувають в організмі. В даний час відоме велике число з’єднань, що відносяться до згортаючої системи. Плазміні фактори згортання крові позначають римськими цифрами, а тромбоцитарні – арабськими. Виділяють тринадцять таких факторів: I фактор – фібриноген; II – протромбін; III – тромбопластин; IV– кальцій; V-VIII – фактори, представлені різними глобулінами плазми. При ушкодженні тканин і розташованих в них судин утворюються плазміний і тканинний тромбопластини. При утворенні плазменного тромбопластина необхідні фактори IV, V, VIII, IX, X, XI, XII і особливий фактор 3, що знаходиться в тромбоцитах. У формуванні тканинного тромбопластина беруть участь фактори IV, V, VII, Х та деякі з’єднання тканин. Під впливом тромбопластина і при участі факторів IV, VII, Х і фактора тромбоцитів 1 протромбін перетворюється в тромбін. Тромбін діє на фібриноген, перетворюючи його у фібрин. Для цієї фази необхідна участь кальцію і тромбоцитарних факторів 2 і 4. Згусток, що утворився, стабілізується фактором XIII. Після утворення згустку відбувається його ущільнення – ретракція – і наступне розщеплення фібрину – фібриноліз. Обидва процеси відбуваються під впливом спеціальних речовин, наявних у крові. Фібриноліз відбувається під впливом плазміну, що утворюється з плазміногену плазми при впливі стрептокінази, що також міститься в плазмі. Плазміноген, плазмін, стрептокіназа відносяться до протизгортаючої системи крові. До неї відносять також гепарин, що утворюється в печінці, і цілий ряд різних з’єднань, що відносяться до антитромбінів. При недостатності якого-небудь з факторів згортання і протизгортаючої системи крові чи при порушенні їх регуляції виникають різні патологічні явища, що можуть виявлятися в зменшенні чи в збільшенні здатності згортання крові. Наприклад, відсутність фактора XIII – антигемофільного глобуліну – викликає захворювання гемофілію, що характеризується порушенням процесу згортання крові і виявляється в кровоточивості. Посилена кровоточивість відзначається при недостатності кальцію в організмі. Вивчення факторів згортання і протизгортаючої системи має велике практичне значення. В даний час отримані високо очищенні препарати багатьох з’єднань цих систем, вивчені їх структура і налагоджений серійний випуск. Фізико-хімічні властивості плазми. Щільність плазми крові дорівнює 1025–1034 кг/м3. Щільність цільної крові більше і складає В’язкість плазми у1,7–2,2, а цільної крові в5,0 разів більше в’язкості води. Щільність крові і в’язкість її визначається кількістю еритроцитів і білковим складом плазми. Осмотичний тиск плазми. Якщо відокремити напівпроникною перетинкою дві судини, що містять розчини різної концентрації, то молекули розчинника проходять через цю перегородку в обох напрямках. Однак убік розчину з більш високою концентрацією розчиненої речовини переходить більше число молекул розчинника, чим у зворотному напрямку. Дифузію розчинника через перетинку, що розділяє розчини різної концентрації, називають осмосом. Тиск, який потрібно прикласти до розчину більшої концентрації, щоб процес осмосу припинився, називають осмотичним тиском. Він залежить від концентрації розчиненої речовини. Чим вона вище, тим вищу силу треба прикласти до розчину для припинення дифузії молекул розчинника і тим більше осмотичний тиск даного розчину. В організмі стінка кровоносної судини являє собою напівпроникну оболонку, по один бік якої знаходиться кров, по інший – тканинна рідина. Осмотичний тиск плазми крові залежить від кількості іонів електролітів, що знаходяться в ній, молекул білка й інших органічних речовин. Він відповідає приблизно 7,6 атм. Розчини, що мають однаковий осмотичний тиск, називають ізотонічними. Нормальна життєдіяльність клітин може здійснюватися тільки в ізотонічному середовищі. 0,9-відсотковий розчин хлористого натрію ізотонічний крові, тому його називають фізіологічним. Розчини з більшою концентрацією іонів і великим осмотичним тиском називають гіпертонічними, а з меншою концентрацією і меншим тиском – гіпотонічними. Глюкоза, сечовина й інші органічні сполуки відіграють незначну роль у створенні осмотичного тиску крові, тому що знаходяться в плазмі в меншій кількості, чим солі, і мають у порівнянні з ними дуже велику молекулярну масу. Виключення складають білки плазми, хоча вони обумовлюють менш 1% загальної величини осмотичного тиску крові. Стінки судин легко проникні для електролітів, тому вони знаходяться в крові і тканинній лімфі в однаковій концентрації і не можуть бути причиною осмотичних явищ. Для білків стінки непроникні, і від співвідношення їх концентрації по обидва боки стінки i судини залежить рух води з крові в тканину чи в зворотному напрямку. Якщо вміст білка в крові знижується, як це буває, наприклад, при голодуванні, рідина направляється переважно із судин у тканинну лімфу, і виникають набряки. Осмотичний тиск, який створюється білками крові, одержало назву онкотичного. При тій самій загальній кількості білків воно виявляється більш високим, якщо переважають відносно низькомолекулярні альбуміни, і менш високим, якщо переважають глобуліни, молекулярна маса яких значно більша. Активна реакція крові визначається співвідношенням гідроксильних і водневих іонів. У практиці кількість останніх, чи водневе число, прийнято виражати логарифмом їх концентрації зі зворотним знаком. Це число називають водневим показником (рН): У середньому рН крові дорівнює 7,36. Зрушення рн нижче 7 і вище 8 небезпечні для життя. Суміші речовин (наприклад, слабка кислота і її сіль), що охороняють реакцію середовища від змін, тобто підтримуючі сталість рН, одержали назву буферних систем. Найважливіша з них у крові – карбонатна система – складається з вугільної кислоти і її двовуглекислої солі. В організмі постійно утворюється молочна кислота й інші кислі продукти. Надходячи з клітин у кров, вони витісняють іони натрію і калію з бікарбонатів; в результаті утворюються солі молочної і інших кислот і вільна вугільна кислота, надлишок якої виводиться з організму. Таким чином, відбувається компенсація кислотного зрушення. Істотне значення в підтримці рН крові має фосфатна буферна система, наведена одно- і двозаміщенним фосфорнокислим натрієм. Кислоти, взаємодіючи з двозаміщенним фосфорнокислим натрієм, утворюють відповідні солі й однозаміщений фосфорнокислий натрій, що видаляється із сечею. Na2HPO4 + Н2СОз = NaHCO3 + NaН2PO4 Буферними властивостями володіють і білки крові, що дають амфотерні реакції внаслідок наявності в їхньому складі кислотних і лужних груп. У кислому середовищі білки зв’язують водневі іони, дисоціюють як основи, а в лужній зв’язують гідроксильні іони, диссоціюють як кислоти. З білків крові найбільшими буферними властивостями володіє гемоглобін. Усі буферні системи крові створюють її лужний резерв. ЕРИТРОЦИТИ Розмір, кількість і форма еритроцитів. Еритроцити – червоні кров’яні тільця – несуть в організмі дихальну функцію. До її виконання добре пристосовані розмір, кількість і форма еритроцитів. Еритроцити людини – дрібні клітини, діаметр яких дорівнює 7,5 мкм. Кількістьїх велика: усього в крові людини циркулює близько 25·1012 еритроцитів. Звичайно визначають число еритроцитів у 1 мм3 крові. Воно складає 5 000 000 у чоловіків і 4 500 000 у жінок. Загальна поверхня еритроцитів – 3200 м², що в 1500 разів перевищує поверхню людського тіла. Еритроцит має форму двоввігнутого диску. Така форма еритроцита сприяє кращому насиченню його киснем, тому що будь-яка точка його відстоїть від поверхні не більше чим на 0,85 мкм.
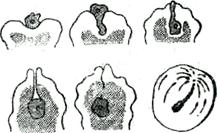
.Рис. 67. Модель молекули гемоглобіну Еритроцит вкритий білково-ліпідною мембраною. Остов еритроцита називають стромою, що складає 10% його обсягу. Особливістю еритроцитів є відсутність ендоплазматичної мережі, 71% еритроцита складає вода. Ядро в еритроцитах людини відсутнє. Ця виникла в процесі еволюції особливість його (у риб, амфібій, птахів еритроцити мають ядро) також спрямована на поліпшення дихальної функції: при відсутності ядра еритроцит може містити більшу кількість гемоглобіну, що переносить кисень. З відсутністю ядра зв’язана неможливість синтезу білка й інших речовин у зрілих еритроцитах. У крові (близько 1%) зустрічаються попередники зрілих еритроцитів – ретикулоцити. Вони відрізняються великим розміром і наявністю сітківково-ниткової субстанції, до складу якої входять рибонуклеїнова кислота, жири і деякі інші з’єднання. У ретикулоцитах можливий синтез гемоглобіну, білків і жирів. Гемоглобін, його будова і властивості. Гемоглобін (Hb) – дихальний пігмент крові людини – складається з активної групи, що включає чотири молекули гема, і білкового носія – глобіну. До складу гема входить двовалентне залізо, чим і обумовлюється здатність гемоглобіну переносити кисень. Один грам гемоглобіну містить 3,2–3,3 мг заліза. Глобин складається з α- і β-поліпептидних ланцюгів, що включають по 141 амінокислоті. Молекули гемоглобіну дуже щільно упаковані в еритроциті, завдяки чому загальна кількість гемоглобіну в крові досить велика: 700–800 г. У 100 мл крові в чоловіків міститься близько 16% гемоглобіну, у жінок біля 14%. Встановлено, що в крові людини не всі молекули гемоглобіну ідентичні. Розрізняють гемоглобін А1, на частку якого приходиться до 90% від усього гемоглобіну крові, гемоглобін А2 (2–3%) і А3. Різні види гемоглобіну відрізняються послідовністю розташування амінокислот у глобині. При впливі на гемоглобін різними реактивами глобін відщеплюється і утворюються різні похідні гема.Під впливом слабких мінеральних кислот чи лугів гем гемоглобіну перетворюється в гематин. При впливі на гем концентрованої оцтової кислоти в присутності NaCI утвориться кристалічна речовина, яка називається геміном. У зв’язку з тим, що кристали геміна мають характерну форму, визначення їх має дуже велике значення в практиці судової медицини для виявлення кров’яних плям на будь-якому предметі. Надзвичайно важливою властивістю гемоглобіну, що визначає його значення в організмі, є здатність з’єднуватися з киснем. З’єднання гемоглобіну з киснем одержало назву оксигемоглобіну (НвО2). Одна молекула гемоглобіну може зв’язати 4 молекули кисню. Оксигемоглобін – з’єднання неміцне, що легко дисоціює на гемоглобін і кисень. Завдяки властивісті гемоглобіну легко з’єднуватися з киснем і також легко його віддавати здійснюється постачання тканин киснем. У капілярах легень утворюється оксигемоглобін, у капілярах тканин він дисоціює з утворенням знову гемоглобіну і кисню, що споживається клітинами. У постачанні клітин киснем полягає основне значення геомглобина, а разом з ним і еритроцитів. Здатність гемоглобіну переходити в оксигемоглобін і навпаки має велике значення в підтримці сталості рН крові. Система гемоглобін – оксигемоглобін є буферною системою крові. З’єднання гемоглобіну з окисом вуглецю (чадним газом) називають карбоксигемоглобином. На відміну від оксигемоглобіну, що легко дисоціює на гемоглобін і кисень, карбоксигемоглобин дуже слабо дисоціює. Завдяки цьому при наявності в повітрі чадного газу велика частина гемоглобіну зв’язується з ним, втрачаючи при цьому здатність до переносу кисню. Це веде до збудження тканинного дихання, що може викликати смерть. При впливі на гемоглобін окислів азоту й інших окислювачів утворюється метгемоглобін, що, також як і карбоксигемоглобин, не може служити переносником кисню. Резистентність еритроцитів. Еритроцити зберігають свою функцію тільки в ізотонічних розчинах. У гіпертонічних розчинах вода з еритроцитів виходить у плазму, що веде до зморщуванню їх і втрати ними їх функції. У гіпотонічних розчинах вода з плазми спрямовується в еритроцити, які при цьому набухають, лопаються, і гемоглобін виходить у плазму. Руйнування еритроцитів у гіпотонічних розчинах називають гемолізом, а гемолізовану кров за її характерний колір називають лаковою. Інтенсивність гемолізу залежить від резистентності еритроцитів. Резистентність еритроцитів визначається тією концентрацією розчину NaCI, при якій відбувається їх гемоліз. Найбільша концентрація розчину, при якій починається гемоліз, характеризує мінімальну резистентність. Концентрація розчину, при якій всі еритроцити виявляються зруйнованими, визначає максимальну резистентність. У здорових людей мінімальна резистентність визначається концентрацією повареної солі 0,30– 0,32%, максимальна–0,42–0,50%. Резистентність еритроцитів неоднакова при різних функціональних станах організму. Реакція осідання еритроцитів – (РОЕ). Кров представляє собою стійку суспензію формених елементів. Ця властивість крові зв’язана з негативним зарядом еритроцитів, що заважає процесу їх склеювання – агрегації. Цей процес у крові, що рухається, дуже слабко виражений. Скупчення еритроцитів у виді монетних стовпчиків, які можна бачити у свіжій крові, є наслідок цього процесу. Якщо кров, яку змішали з розчином, що попереджає її згортання, помістити в градуйований капіляр, то еритроцити, що піддаються агрегації, осідають на дно капіляра. Верхній шар крові, що позбавляється еритроцитів, стає прозорим. Висотою цього незабарвленого стовпчика плазми визначають реакцію осідання еритроцитів (РОЕ). Величина РОЕ в чоловіків дорівнює від 3 до 9 мм1ч, у жінок – від 7 до 12 мм1ч. У вагітних жінок РОЕ може збільшуватися до 50 мм1ч. Процес агрегації різко підсилюється при зміні білкового складу плазми. Збільшення кількості глобулінів у крові при запальних захворюваннях супроводжується внаслідок адсорбції їх еритроцитами, зниженням електричного заряду останніх і зміною властивостей їх поверхні. Це підсилює процес агрегації еритроцитів, що супроводжується збільшенням РОЕ. ЛЕЙКОЦИТИ Види лейкоцитів, їх кількість. Лейкоцитами називають білі кров’яні тільця. Їх поділяють на дві великі групи: зернисті лейкоцити, чи гранулоцити, і незернисті, агранулоцити. Зернисті лейкоцити одержали свою назву через наявність у їх цитоплазмі характерної зернистості. У залежності від здатності сприймати ті чи інші барвники, гранулоцити поділяють на нейтрофіли, еозинофіли і базофіли. Нейтрофіли складають 60– 70% від усіх білих кров’яних тілець, еозинофіли – 1–4%, базофіли 0–0,5%. Агранулоцити представлені лімфоцитами і моноцитами. Лімфоцити складають 25– 30% від усіх лейкоцитів, моноцити – 6–8%. Усього в 1 мм3 крові міститься 6000–8000 лейкоцитів. Збільшення їх числа в крові називають лейкоцитозом. Він відзначається при гострих інфекційних захворюваннях, запальних процесах, при різних інтоксикаціях, після прийому їжі. Зменшення кількості лейкоцитів називають лейкопенією. Вона може спостерігатися при гнобленні функції кісткового мозку. Будова і функції різних видів лейкоцитів. Нейтрофіли мають округлу форму, діаметр їх 12 мкм. Цитоплазма в пофарбованому препараті рожевого кольору, гранули її зафарбовуються в синювато-рожевий колір. До складу зернистості входять самі різні ферменти, що забезпечують синтез і розщеплення речовин, амінокислоти, глікоген, ліпіди, РНК. Ядро, як правило, складається з 3–4 сегментів. Ядра мають відростки – ядерні придатки. Нейтрофіли мають яскраво виражену здатність до фагоцитозу. Фагоцитозом називають здатність клітини захоплювати і переварювати всілякі речовини (мікробів, фарбу, уламки клітин і т.д.). Рис. 68. Часткове поглинання еритроцита нейтрофілом людини:
Рис. 69. Послідовні стадія фагоцитозу.
Рис. 70. Псевдоподії лейкоцитів Рис. 71. Псевдоподії лейкоцита при розгляданні його в електронний мікроскоп. Явище фагоцитозу було відкритоІ.І. Мечниковим, що показав, що рухливі клітини – лейкоцити – здатні до захоплення і перетравлення твердих часток, завдяки чому вони виконують в організмі захисну функцію. Клітини, здатні до захоплювання і перетравлення чужорідних речовин, були названі ним фагоцитами, що означає «пожирателі клітин». Мечниковим були виділені основні фази фагоцитозу: зближення фагоцита з об’єктом, атракція, під якою розуміють поглинання, і перетравлення. Зближення фагоцитів з об’єктом можливо тому, що вони здатні до пересування. Для нейтрофилів характерно амебоподібне пересування. На кінці клітини, протилежної напрямку руху, з’являється псевдоподія. Вона збільшується в розмірах, і в неї переміщається цитоплазма. Швидкість руху нейтрофилів людини складає в середньому 28 мкм/хв. Швидкість руху залежить від температури середовища. Максимальна швидкість відзначається при температурі 38–39°С. Швидкість залежить також від різних речовин, які містяться в плазмі і тканинах, що піддаються ушкодженню. Для здійснення рухової активності необхідна енергія, що доставляє АТФ. У нейтрофилах ресинтез АТФ може відбуватися й у безкисневому середовищі, тобто в анаеробних умовах, за рахунок того, що процес розщеплення глюкози, що дає енергію для цього ресинтеза, може відбуватися в них анаеробно. Мечниковим була запропонована теорія запалення, відповідно до якої запалення варто розглядати як захисну реакцію організму, спрямовану на боротьбу зі шкідливим агентом. Лейкоцити-фагоцити, що скупчуються у вогнищі запалення, сприяють його ліквідації. Один лейкоцит може захопити 15–20 мікробів. При цьому велика кількість лейкоцитів гине у вогнищі запалення. Ця теорія Мечникова була надалі підтверджена. Зараз відомо, що інтенсивність фагоцитозу залежить від активності антитіл і пропердинової системи, від наявності вітамінів, від впливів нервових і гуморальних факторів. Гальмують фагоцитоз ацетилхолін, глюкокортикоїди. Нейтрофіли недовговічні: тривалість їх життя 8–12 діб. Крім фагоцитарної нейтрофіли виконують і транспортну функцію. Вони переносять антитіла, що адсорбують їхна своїй поверхні. Нейтрофіли підсилюють також мітотичну активність, сприяючи відновленню – регенерації – ушкоджених тканин. Еозинофіли мають діаметр 12–15 мкм. У їх цитоплазмі містяться гранули сферичної чи овальної форми, що офарблюються в жовто-рожевий колір. Інша цитоплазма забарвлюється в блакитний колір. Гранули містять ферменти, але в них відсутній глікоген. Ядро складається з двох сегментів. Еозинофіли володіють слабкою фагоцитарною активністю. Основна їх функція полягає в інактивуванні гістаміна, що особливо у великих кількостях утворюється при захворюваннях, зв’язаних з підвищеною чутливістю до чужорідних елементів. Еозинофіли містять фермент, що розщеплює гістамін. Крім того, адсорбуя останній, вони переносять його до легень і кишкивнику, де і відбувається його виділення. Зрозуміло, що у випадку підвищеного утворення гістаміна в організмі збільшується число еозинофілів. Базофіли – клітини діаметром 10 мкм. Гранули їх цитоплазми зафарблюються в темно-фіолетовий колір. Вони містять РНК, глікоген, ферменти, гепарини, гістамін. Цитоплазма забарвлюється в рожевий колір. Ядро лапчастої форми. Основна функція базофілів полягає в синтезі гістаміна, гепарина. Половина гістаміна крові знаходиться в базофілах. Лімфоцити в залежності від їх розмірів поділяють на три групи: великі (15–18 мкм), середні (10–14 мкм) і малі (6– 9 мкм). Більше всього в крові малих лімфоцитів. Форма лімфоцитів – кругла чи овальна. Ядро їх забарвлюється в темно-синій колір. Воно займає майже всю клітину. Цитоплазма фарбується основними фарбами. У ній містяться ферменти, нуклеїнові кислоти, АТФ. Глікоген є не у всіх лімфоцитах. Функція лімфоцитів зв’язана з виробленням γ-глобулінів. Чим більше цитоплазма містить РНК, тим сильніше виражена її здатність до вироблення антитіл. Так само як і нейтрофіли, лімфоцити можуть адсорбувати антитіла і транспортувати їх до вогнища запалення. Лімфоцити нейтралізують різні токсини. Моноцити – самі великі клітини крові. Їх діаметр досягає 13–25 мкм. Ядро неправильної, овальної чи бобоподібної форми, із вдавленнями і витягуваннями. Цитоплазма забарвлюється в блакитнувато-сірий чи сіро-синій колір. У цитоплазмі містяться РНК, полісахариди і ферменти. Моноцити мають більшу здатність до амебоподібного руху, чим лімфоцити, у зв’язку з чим для них характерна фагоцитарна функція. Вона здійснюється, на відміну від нейтрофілів, і в кислому середовищі. Тому моноцити активно беруть участь у боротьбі з інфекцією у вогнищах запалення. ТРОМБОЦИТИ Тромбоцити – кров’яні пластівці. У 1 мм3 крові їх міститься 250 000–400 000. Значна їх частина знаходиться в депо: печінці, селезінці, легенях. Звідти вони надходять у кров (при виникненні необхідності в цьому). У цитоплазмі пластівок маються зернятка – г р а н у л о м е р, що забарвлюється в темно-фіолетовий колір. Сама цитоплазма – г и а л о м е р – забарвлюється в блідо-синій колір. Діаметр тромбоцита 2–4 ммк. Тромбоцити здатні утворювати псевдоподії, розмір яких може в кілька разів перевищувати їх діаметр. У тромбоцитах маються АТФ, АДФ, РНК, актоміозин, різні ферменти. Ядро відсутнє. Тривалість життя тромбоцитів 8–10 днів. Функція тромбоцитів – участь у згортанні крові. Вони можуть прилипати до чужорідної поверхні і склеюватися, завдяки чому при ушкодженні судин утвориться білий тромб із тромбоцитів, що закупорює судину. В подальшому на ньому випадають нитки фібрину. У гиаломері утворюється речовина, що викликає ретракцию – ущільнення. У тромбоцитах міститься 9 різних факторів, що беруть участь у згортанні крові. При зменшенні кількості тромбоцитів різко збільшується час кровотечі. ІМУННІ ВЛАСТИВОСТІ КРОВІ Поняття про імунологію, антигени й антитіла. Імунологія – наука про механізми захисних реакцій організму – стала особливо інтенсивно розвиватися в другій половині XIX в. Одним з основоположників імунології як науки вважають французького вченого Луї Пастера, що розробив і ввів у практику ефективний метод боротьби з інфекційними хворобами – вакцинацію. У той час під імунітетом розуміли несприйнятливість до інфекційного агента і, відповідно, вся увага вчених була звернена на вивчення механізмів цієї несприйнятливості. І. І. Мечников розвив теорію імунітету, відповідно до якої несприйнятливість організму визначається фагоцитарною активністю лейкоцитів. Німецький вчений Пауль Ерлих створив гуморальну теорію імунітету, що пояснювала несприйнятливість організму виробленням у крові захисних гуморальних речовин – антитіл. У 1908 р. Мечников і Ерліх одержали за розробку теорії імунітету Нобелівську премію. Основні положення їх вчення збереглися і дотепер. Вони витримали перевірку часом, експериментальними фактами і клінічними спостереженнями. Однак у даний час, коли з’явилася можливість вивчати клітину на молекулярному рівні, коли розшифрований генетичний код, імунологія перетерпіла значні зміни. Вона збагатилася новими фактами, що привели навіть до зміни самого визначення імунології й імунітету. Імунітетом перестали називати тільки несприйнятливість до інфекційного агента. Це поняття стало більш широким, і, відповідно, набагато розширилося коло питань, якими займається імунологія. У новому розумінні імунітет – це збереження генетичної сталості клітинних утворень, захист організму від усього, що генетично для нього чужерідно: від мікробів, від чужих клітин і тканин, від власних, але змінених клітин (наприклад, ракових клітин). Чужорідні для організму макромолекули називають антигенами. Вони викликають в організмі утворення антитіл, що специфічно реагують на ці антигени. Розрізняють природні й імунні антитіла. У сироватці крові людини маються як ті, так і інші. Природні антитіла. Групи крові. Природні антитіла являють собою спадкоємну ознаку крові людини. Так, у плазмі крові маються аглютиніни α і β, що специфічно реагують на природні аглютиногени А и В, розташовані в еритроцитах. Антигени, що не надходять ззовні, а властиві самому організму, називають ізоантигенами. Отже, аглютиногени А і В є ізоантигенами. При зустрічі однойменних аглютиногенів і аглютинінів, наприклад А і α чи В і β, відбувається склеювання еритроцитів – аглютинація. У залежності від наявності чи відсутності в еритроцитах крові людини аглютиногена А чи В кров відносять до тієї чи іншої групи. По цьому принципі виділяють чотири групи крові. По Міжнародній номенклатурі ці групи позначають: О – при відсутності в еритроцитах аглютиногенів, А-при наявності аглютиногена А, В – у випадку присутності В-аглютиногена та АВ – у випадку наявності обох аглютиногенів. По Янсному, ці групи, відповідно, позначаються як I, II, III і IV. Групи крові відрізняються і по змісту аглютинінів. У плазмі крові першої групи містяться аглютиніни α і β, у плазмі другої групи – аглютинін β, у плазмі третьої групи – α й в плазмі четвертої відсутні обидва аглютиніни. Для попередження аглютинації необхідно усунути можливість зустрічі аглютинінів реципієнта, тобто людини, якому переливають кров, з відповідними аглютиногенами донора – людини, що дає кров для переливання. Зустріч аглютинінів донора з відповідними аглютиногенами реципієнта не має істотного значення в силу великого розведення аглютинінів у плазмі реципієнта. Людині, що має I групу крові, можна переливати кров тільки першої групи. У той же час, завдяки тому що вона не містить аглютиногенів, її можна переливати людині, що має кров будь-якої групи. Людям з IV групою крові можна перелити кров будь-якої групи. У той же час кров цієї групи можна перелити тільки людям, що мають ту ж групу. У зв’язку з цим людей, що мають першу групу крові, називають універсальними донорами, а четверту – універсальними реципієнтами. У крові II і III груп не виникає при переливанні аглютинації тільки в тому випадку, якщо кров, що вливається, буде або тієї ж групи, або I. Перелити кров цих груп можна людям з тією же групою крові і з IV.
Наявність (+) чи відсутність (–) аглютинації
|
При использовании материала ссылка на сайт medlec.org обязательна! (4.122 сек.) |

 Кількість фолікулів, що формують щитовидну залозу, і їх розмір з віком збільшуються. Так, у новонароджених діаметр фолікула складає 60-70 мкм, у віці одного року – 100 мкм, 3 років – 120-150 мкм, 6 років – 200 мкм, 12-15 років – 250 мкм. Збільшення кількості фолікулів відбувається шляхом їх брунькування. За рахунок розподілу клітин стінка фолікула товщає в якійсь її ділянці, у місці стовщення утвориться порожнина, і сформований у такий спосіб новий дочірній фолікул відокремлюється від основного. Після відділення фолікул покривається сполучнотканинною капсулою. Фолікулярний епітелій щитовидної залози у немовляти кубічний чи циліндричний. В міру росту організму він заміняється на кубічний і плоский, котрий характерний для фолікулів щитовидної залози дорослої людини. До 15 років маса і структура щитовидної залози стають такими ж, як у дорослої людини.
Кількість фолікулів, що формують щитовидну залозу, і їх розмір з віком збільшуються. Так, у новонароджених діаметр фолікула складає 60-70 мкм, у віці одного року – 100 мкм, 3 років – 120-150 мкм, 6 років – 200 мкм, 12-15 років – 250 мкм. Збільшення кількості фолікулів відбувається шляхом їх брунькування. За рахунок розподілу клітин стінка фолікула товщає в якійсь її ділянці, у місці стовщення утвориться порожнина, і сформований у такий спосіб новий дочірній фолікул відокремлюється від основного. Після відділення фолікул покривається сполучнотканинною капсулою. Фолікулярний епітелій щитовидної залози у немовляти кубічний чи циліндричний. В міру росту організму він заміняється на кубічний і плоский, котрий характерний для фолікулів щитовидної залози дорослої людини. До 15 років маса і структура щитовидної залози стають такими ж, як у дорослої людини.