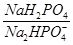|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Гуморальная регуляция. 51.Гуморальная регуляция, ее отличия от нервной51.Гуморальная регуляция, ее отличия от нервной. Харектеристика факторов гуморальной регуляции. Классификация гормонов. Гуморальна (рідинна) регуляція здійснюється за допомогою виділення біологічно активних речовин – справжніх та тканинних гормонів, метаболітів в рідкі середовища організму (кров, лімфа, тканинна рідина). З током цих рідин біологічно активні речовини надходять у тканини та органи, змінюючи їх функції та метаболізм.
В силу вказаних відмінностей нервова регуляція використовується для регуляції швидких процесів, що потребують більш тонкої регуляції (скорочення скелетних м’язів), гуморальна регуляція впливає на повільні, тривалі процеси (ріст, обмін речовин).
Порівняльна характеристика факторів гум факторів гуморальної регуляції
Гормони, що виділяються спеціалізованими чи неспеціалізованими ендокринними клітинами характеризуються дистантністю дії (діють на великій відстані від місця виділення), високою біологічною активністю (здійснюють регуляторний вплив у малих концентраціях), високою специфічністю (мають специфічну структуру, високоспецифічний характер дії на функції організму, їх дія не може бути замінена дією інших БАР).
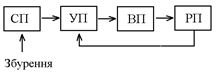
52. Контур гуморальної регуляції має такий вигляд: Отже, на відміну від контура нервової регуляції, в ланцюжку зворотнього зв’язку відсутній СП – рецептор, який контролює рівень РП (хоча він може і бути). КП в схемі контура – ендокринна залоза (чи клітина); ВП – орган-мішень, стрілочка між ними – гормон чи інша БАР (біологічно-активна речовина) – носій інформації; КПЗ – канал прямого зв’язку; КЗЗ1 – канал зовнішнього зв’язку; КЗЗ2 – канал зворотнього зв’язку. З схеми видно, що регуляція діяльності ендокринних залоз може відбуватися: - за відхиленням, у відповідь на зміну РП залоза змінює свою активність так, щоб це відхилення усунути; - за збуренням, при цьому інформація до залози (клітини) надходить по каналу зовнішнього зв’язку, найчастіше по нервовим волокнам, які її інервують. Регуляція діяльності будь-якої залози відбувається як за збуренням так і за відхиленням. За домінуючим (головним) механізмом в регуляції діяльності всі ендокринні залози можна поділити на 3 групи: 1. За відхиленням (на основі негативного зворотнього зв’язку, саморегуляції) рівня тих чи інших параметрів гомеостазу (РП). Секреція таких залоз вмикається (чи вимикається) в залежності від зміни даного параметра гомеостазу. Таким чином регулюється секреція:
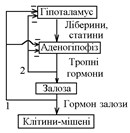
2. За відхиленням у відповідь на зміну концентрації гормону в крові. Так регулюється секреція залоз, гормони яких не регулюють рівень параметрів гомеостазу, а саме залоз, які знаходяться під контролем гіпоталамо-гіпофізарної системи (ліберини та статини гіпоталамуса тропні гормони гіпофіза гормони відповідних залоз): - гормони щитовидної залози (трийодтиронін та тетрайодтиронін); - гормони кіркової речовини наднирників (глюкокортикоїди); - статеві гормони статевих залоз; - меланоцитостимулюючий гормон гіпофіза; - пролактин гіпофіза. Зі схеми видно, що даний вид регуляції може здійснюватись на основі: а) довгого негативного зворотнього зв’язку – у відповідь на зміну концентрації в плазмі крові гормона “периферичної” залози (схема 1); б) короткого зворотного зв’язку – у відповідь на зміну концентрації в крові тропних гормонів гіпофіза (схема 2). Секреція гормонів залозами, що перебувають під контролем гіпоталамо-гіпофізарної системи, регулюється за збуренням (нейросекреторні клітини гіпоталамуса отримують і переробляють інформацію від нервових клітин. Тому, секреція цих гормонів змінюється, наприклад, під час стресу). 3. Мозкова речовина наднирників є виключенням із загальних правил, так як регулюється за допомогою нервових механізмів регуляції. Вона отримує симпатичну іннервацію, тому секреція катехоламінів (адреналін, норадреналін) збільшуються при підвищеній активності симпатичного відділу вегетативної нервової системи вони разом забезпечують ерготропну перебудову функцій організму в стані напруження. Симпатична нервова система та мозкова речовина наднирників функціонують як єдине ціле, утворюючи симпато-адреналову систему адаптації організму до дії стресових ситуацій.
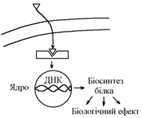
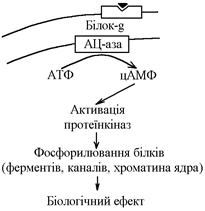
53.Свойства гормонов, их основные влияния. Механизм действия гормонов на клетки организма. За хімічною структурою гормони поділяються на: 1.Білково-пептидні (інсулін, глюкагон, всі гормони гіпоталамуса та гіпофіза). Вони водорозчинні, але погано розчиняються у ліпідах. 2.Стероїдні – гормони кіркової речовини наднирників, статеві гормони. Вони жиророзчинні, але погано розчинні у воді. 3.Похідні амінокислот: -тиреоїдні гормони (жиророзчинні); -катехоламіни (водорозчинні). Розчинність у воді чи в жирах визначає механізм дії гормонів на клітини- мішені: - жиророзчинні гормони легко проникають в клітину через її мембрану та діють через взаємодію з цитоплазматичними циторецепторами; - водорозчинні гормони не можуть проникнути в клітину через її мембрану, яка побудована переважно з ліпідів, тому їх дія на клітину пов’язана із взаємодією з мембранними циторецепторами вмикання мембранних механізмів утворення вторинних посередників (посланців, месенджерів). Зміна концентрації всередині клітини вторинних посередників змінює її функцію та метаболізм. Механізм дії на клітини жиророзчинних гормонів: Гормон через мембрану проникає в клітину та взаємодіє з цитоплазматичними циторецепторами комплекс гормон-рецептор транспортується до ядра клітини зв’язування гормона з ДНК збільшення швидкості синтезу І-РНК збільшення біосинтезу в клітині певних білків (ферментів, каналів і т.д.) зміна метаболізму, функції, будови клітини. Механізм дії жиророзчинних гормонів визначає наступні їх особливості: - великий латентний період (інтервал часу від виділення гормону до появи біологічного ефекту вплив через обмін нуклеїнових кислот ядра!!!); - довготривалість дії. При дії на клітини-мішені водорозчинних гормонів утворюються внутрішньоклітинні посередники: - цАМФ; цГМФ; - диацилгліцерол; - інозитол-3-фосфат; - іони Са2+, кальмодулін. Дія гормонів через мембранні циторецепторами характеризується відносно невеликим латентним періодом та відносно короткотривалим ефектом. 1. Механізм дії гормонів за участю цАМФ як внутрішньоклітинного посередника. Гормон взаємодіє з мембранним циторецептором за участю білка-g (Рrotein-G) активується мембранний фермент аденілатциклаза (АЦ-аза) перетворення АТФ в цАМФ активація цАМФ-залежних протеїнкіназ (ферменти, що фосфорилюють білки зміна їх властивостей): - фосфорилювання білків-ферментів зміна їх активності зміна метаболізму клітини; - фосфорилювання білків-каналів зміна проникності мембран для певних іонів; - фосфорилювання білків ядра зміна нуклеїнового обміну зміна біосинтезу білків в клітині. В результаті всіх цих змін змінюються обмін, функція та структура клітини.
При взаємодії гормона з мембранним циторецептором за участю білка-G активізується фосфоліпаза С (Ф-С), яка каталізує утворення з поліфосфатидилінозитолу (компонент мембрани) диацилгліцеролу (ДГ) та інозитол-3-фосфату (ІФ3), які надходять в клітину та виконують роль вторинних посередників. ІФ3 мобілізує іони Са2+ з внутрішньоклітинних депо біологічний ефект. ДГ активує залежні від нього протеїнкінази фосфорилювання білків біологічний ефект (зміна обміну, функції та структури клітини).
При взаємодії гормона з мембранними циторецепторами, за рахунок входу зовні та мобілізації з внутрішньоклітинних депо, збільшується концентрація в клітині іонів Са2+. Іони Са2+: - взаємодіють з білками клітини зміна їх властивостей; - взаємодіють з кальмодуліном його активація. Активний кальмодулін: - взаємодіє з білками клітини та змінює їх властивості; - активує залежні від нього протеїнкінази фосфорилювання білків біологічний ефект.
54.Роль гипоталамо-гипофизарной системы в регуляции функций эндокринных желез.Принцип обратной связи. Функція більшості залоз внутрішньої секреції регулюються гормонами передньої долі гіпофіза (аденогіпофіза). На вивільнення цих гормонів, у свою чергу впливають гормони, що продукуються нейронами гіпофізотропної долі гіпоталамуса (рилізинг-гормони). Останні здійснюють або стимулюючий, або пригнічуючий вплив на гіпофіз, відповідно до цього їх називають ліберинами (стимулюючі) чи статинами (пригнічуючі). Рилізинг-гормони виділяються у ділянці медіального підвищення і гіпоталамо-гіпофізарною портальною системою надходять в аденогіпофіз. Регулюється секреція гормонів гіпоталамуса вмістом гормонів периферичних ендокринних залоз. Принцип такої регуляції заключається в тому, що підвищення концентрації гормонів периферійних залоз у плазмі зумовлює зменшення викиду відповідних ліберинів, та навпаки. Ця регуляція (за принципом негативного зворотного зв’язку) функціонує навіть за відсутності низхідних впливів ЦНС. Роль ЦНС – у пристосуванні цієї регуляції до чинників внутрішнього і зовнішнього середовища.
55.Роль соматотропина Т3, Т4, инсулина в регуляции процессов роста и развития организма.
Дія соматотропного гормону і регуляція його соматоліберином та соматостатином. Гормор росту безпосередньо стимулює глікогеноліз і ліполіз, а також утворення соматомадинів у печінці. При дії за механізмом негативного зворотнього зв’язку, соматомедини замикають ланцюг. На периферії вони стимулюють ріст хрящів і кісток, а також синтез білка і поділ клітин. Тиреоїдні гормони підвищують рівень метаболізму у всьому організмі. В результаті впливу на процеси транскрипції та трансляції, вони стимулюють біосинтез білка. Також вони посилюють вихід з клітини Na+ і вхід до них K+. Окрім цього, вони активізують ферментні системи, що розщеплють вуглеводи – посилення вуглеводного обміну. У дітей тиреоїдні гормони стимулюють фізичний розвиток. Особливо цей процес важливий для нормального розвитку мозку у постнатальний період. Система гіпоталамус-гіпофіз-щитоподібна залоза. Нейрони гіпоталамуса секретують тиреоліберин, який ворітною системою надходить у гіпофіз, стимулюючи секрецію тиреотропного гормону (ТТГ). ТТГ індукує в щитоподібній залозі утворення тирозину (Т4) та трийодтироніну (Т3). Діючи за механізмом негативного зворотнього зв’язку на гіпофіз і на гіпоталамус, трийодтиронін пригнічуєсекрецію ТТГ. При дії інсуліну на інсулінові рецептори, посилюється транспорт клітини багатьох амінокислот, пригнічуються ферменти, що розщеплюють глікоген, активується надходження глюкози в клітини, стимулюється синтез жиру і жирних кислот.
56.Роль йодсодержащих гормонов щитовидной железы в регуляции функций организма. Тиреоїдні гормони Т3 і Т4 виконують такі життєво важливі функції: 1)стимулюють метаболізм у всьому організмі; 2)Т3 діє на геном зумовлюючи посилення транскрипції і трансляції стимуляція синтезу білка; 3)впливають на вихід із клітин Na+ і надходження до них К+; 4)підвищують активність багатьох ферментів, перш за все тих, які беруть участь в розщепленні вуглеводів підвищення їх метаболізму; 5)сприяють фізичному росту у дітей; 6)прияють нормальному розвитку мозку в постнатальний період (після народження).
57.Гуморальная регуляция уровня ионов кальция и фосфора в крови. Гипо- гиперсекреция паратгормона. Паратгормон (паратиреотропний гормон, ПТГ). Фізіологічним стимулом секреції ПТГ є зниження концентрації іонів Са2+ в крові (в свою чергу, підвищення їх концентрації зумовлює зменшення секреції ПТГ). ПТГ діє на кісткову тканину та активує остеокласти, які викликають резорбцію кісток і вивільнення Са2+ та фосфатів в кров. Одночасно ПТГ стимулює виділення фосфату нирками, перешкоджаючи цим самим зв’язуванню з ним Са2+. окрім того ПТГ активує в нирках фермент, що каталізує перетворення 25-гідроксикальциферола в 1,25-дигідрокальциферол (вітамін D3). Затримці Са2+ в організмі сприяє також пряма дія ПТГ на нирки, в результаті якого зменшується екскреція іонів Са2+. Кальцитонін. Стимулом його секреції С-клітинами щитовидної залози є підвищення концентрації Са2+ в крові (тобто, він є антагоністом ПТГ). Кальцитонін зменшує резорбцію кісток і підвищує концентрацію в них Са2+. Виділення кальцитоніну стимулюють також шлунково-кишкові гормони (при підвищенні їх концентрації в крові, що відбувається при прийомі їжі), такі як гастрин та холецистокінін, які стимулюють С-клітини. В результаті підвищеного виділення кальцитоніну, Са2+, що надходить з їжею швидко відкладається в кістках. Одночасно кальцитонін пригнічує процес травлення (сповільнює випорожнення шлунку, секрецію шлункового та панкреатичного соків), цим самим створюючи умови для рівномірного всмоктування Са2+ попередження різкого збільшення Са2+ в крові. Це має велике значення, тому що так чи інакше різке підвищення концентрації Са2+ в крові пригнічувало б секрецію ПТГ і Са2+ не затримувався б в нирках втрата Са2+ з сечею відразу ж після його надходження в організм.
58.Роль гормонов поджелудочной железы в регуляции функций организма. Підшлункова залоза (а точніше її острівці Лангерганса, які є скупченнями ендокринних альфа-, бета- та дельта-клітин) секретує гормони, які беруть участь в підтриманні постійного рівня цукру в крові – інсулін, глюкагон та соматостатин. Інсулін, що утворюється в бета-клітинах підшлункової залози здійснює: 1) зниження концентрації глюкози в крові (норма – 0,8-1,0г/л) шляхом підвищення проникності мембран клітин для глюкози поглинання клітинами глюкозами; 2) посилює перетворення в печінці глюкози в глікоген, що знижує її концентрацію в крові; 3) робить проникними для глюкози мембрани м’язових клітин, які в нормі для нього не проникні, що має значення при напруженій фізичній роботі; 4) забезпечує активний транспорт в клітини багатьох (хоча і не всіх) амінокислот; 5) стимулює синтез білка клітинами шляхом підвищення швидкості транскрипції ДНК в ядрі. 6) активує перетворення глюкози н а ліпіди; 7) стимулює утворення тригліцеролу з гліцеролу та жирних кислот. Глюкагон утворюється в альфа-клітинах підшлункової залози. Його можна назвати антагоністом інсуліну, тому що під його впливом здійснюється розщеплення глікогену в печінці (глікогеноліз) швидке підвищення концентрації глюкози в крові при гіпоглікемії. Соматостатин утворюється в дельта-клітинах підшлункової залози і спричиняє: 1) пригнічує синтез в гіпофізі гормона росту; 2) пригнічує секрецію інсуліна та глюкагона; 3) пригнічує перистальтику шлунково-кишкового тракту (ШКТ); 4) зменшує секрецію травного соку.
59.Роль гормонов коркового вещества надпочечниов в регуляции обменных процессов организма. Основні впливи глюкокортикоїдів на організм: - потенціюють вплив катехоламінів; - впливають на обмін речовин, а саме: а) вплив на білковий обмін – пригнічують біосинтез у багатьох тканинах (сполучна, м’язова), а у лімфоїдній тканині вони посилюють розпад білка; результатом таких впливів на білковий обмін є підвищення рівня амінокислот у плазмі крові; б) вплив на вуглеводний обмін – стимулюють процеси глюконеогенезу в печінці (утворення глюкози з амінокислот, котрі посилено надходять до печінки за рахунок впливу глюкокортикоїдів ни білковий обмін), утворена глюкоза витрачається у двох напрямках: - частина йде у кров – підтримання гіперглікемії; - частина йде на синтез глікогену – підтримання достатніх його запасів у організмі; в) посилюють ліполіз, який зумовлений дією катехоламінів; Таким чином, глюкокортикоїди підтримують гіперглікемію на фоні збереження запасів глікогену в організмі, що і є причиною тривалої адаптації, яка розвивається за рахунок активації гіпоталамо-наднирникової системи. Проте адаптація, що при цьому розвивається, потребує тривалого часу для своєї реалізації (система повільно активізується); механізм впливу глюкокортикоїдів на клітини мішені – через цитоплазматичні рецептори, за участю хроматину ядра, через зміну процесів біосинтезу білка у клітинах. Тому вплив цієї системи є довготривалим, але повільно розвивається. Роль мінералокортикоїдів в адаптації полягає в тому, що вони впливають на роботу нирок, внаслідок чого відбувається затримка Nа+ і води в організмі збільшення ОЦК посилення пресорної реакції. Окрім того, при збільшенні ОЦК, організм краще зможе перенести крововтрату, яка може виникнути в стресових ситуаціях.
60.Неспецифическая и специфическая адаптация организма к стрессовым воздействиям. Роль гормонов в неспецефической адаптации. Стресова ситуація (стрес, стан напруги) виникає в організмі кожен раз, коли на нього діє надзвичайний по силі подразник або, коли організм перебуває в стані емоційного напруження (емоційний стрес). Адаптація організму до дії надзвичайних подразників відбувається в двох напрямках: - специфічна адаптація – сукупність пристосувальних реакцій, що дозволяють організму адаптуватися до дії саме цього надзвичайного подразника. Наприклад, в умовах дії зовні на організм низької температури відбувається збільшення процесів теплоутворення та зниження тепловіддачі стабілізація температури ядра тіла, недивлячись на низьку температуру зовнішнього середовища. - неспецифічна адаптація – сукупність стереотипних (тих, що не залежать від природи діючого надзвичайного подразника) пристосувальних реакцій, які підвищують стійкість організму до дії будь-якого надзвичайного подразника (стресора). Неспецифічна адаптація проявляється в послідовній активації симпато-адреналової системи (САС) та гіпоталамо-гіпофізарно-наднирникової системи (ГГНС). Активація цих систем призводить до зміни функції органів та систем організму, до змін обміну речовин в ньому, які супроводжуються підвищенням фізичної та розумової діяльності покращення здатності адаптуватися до дії будь-якого стресора. Секреція вазопресину збільшується при будь-якому стресі. Діючи на нирки, він сприяє затриманню води в організмі збільшення ОЦК. Це, з однієї сторони, посилює пресорну реакцію (підвищення САД), з іншої сторони збільшує стійкіть організму до крововтрати, ймовірність якої в стані напруження завжди більша, ніж в стані відносного спокою. Секреція соматотропіну також збільшується при будь-якому стресі. Рахують, що основний адаптивний його вплив в цих умовах пов’язаний з посиленням ліполізу підвищення рівня жирних кислот в крові субстратне забезпечення скелетних м’язів та міокарда при їх посиленій роботі підвищення рівня фізичної працездатності.
61.Роль гипоталамо-гипофизарно-нанадпочечниковой системы в обеспечении неспецифической адаптации организма к стрессовым воздействиям. Основные эффекты кортикостероидов. Гіпофізарно-наднирникова система виділяє такі гормони, що забезпечують тривалу адаптацію організму до дії стресових чинників: - гормони гіпофіза соматотропін, вазопресин; - гормони кіркової речовини наднирників глюкокортикоїди та мінералокортикоїди. Основу цієї системи складають кортиколіберин гіпоталамуса, кортикотропін аденогіпофіза, глюкокортикоїди кори наднирників. Активація цієї системи відбувається за допомогою двох механізмів: - за рахунок отримання нейросекреторними клітинами гіпоталамуса інформації про дію стресора (за механізмом безумовних та умовних рефлексів); - за рахунок дії на ці клітини високих концентрацій катехоламінів – активація САС.
Основні впливи глюкокортикоїдів на організм: - потенціюють вплив катехоламінів; - впливають на обмін речовин, а саме: а) вплив на білковий обмін – пригнічують біосинтез у багатьох тканинах (сполучна, м’язова), а у лімфоїдній тканині вони посилюють розпад білка; результатом таких впливів на білковий обмін є підвищення рівня амінокислот у плазмі крові; б) вплив на вуглеводний обмін – стимулюють процеси глюконеогенезу в печінці (утворення глюкози з амінокислот, котрі посилено надходять до печінки за рахунок впливу глюкокортикоїдів ни білковий обмін), утворена глюкоза витрачається у двох напрямках: - частина йде у кров – підтримання гіперглікемії; - частина йде на синтез глікогену – підтримання достатніх його запасів у організмі; в) посилюють ліполіз, який зумовлений дією катехоламінів; Таким чином, глюкокортикоїди підтримують гіперглікемію на фоні збереження запасів глікогену в організмі, що і є причиною тривалої адаптації, яка розвивається за рахунок активації гіпоталамо-наднирникової системи. Проте адаптація, що при цьому розвивається, потребує тривалого часу для своєї реалізації (система повільно активізується); механізм впливу глюкокортикоїдів на клітини мішені – через цитоплазматичні рецептори, за участю хроматину ядра, через зміну процесів біосинтезу білка у клітинах. Тому вплив цієї системи є довготривалим, але повільно розвивається. Роль мінералокортикоїдів в адаптації полягає в тому, що вони впливають на роботу нирок, внаслідок чого відбувається затримка Nа+ і води в організмі Ù збільшення ОЦК Ù посилення пресорної реакції. Окрім того, при збільшенні ОЦК, організм краще зможе перенести крововтрату, яка може виникнути в стресових ситуаціях.
62.Структура и роль симпато-адреналовой системы в регуляции функций организма. До складу САС входять: - симпатичний відділ вегетативної нервової системи; - мозкова речовина наднирників. Активація САС в стресових ситуаціях відбувається дуже швидко. При дії стресора інформація швидко по нервовим шляхам (за механізмом умовних чи безумовних рефлексів) надходить в інтегративні центри гіпоталамуса Ù стовбурова сітчаста речовина Ù симпатичні центри спинного мозку Ù посилення впливу симпатичної нервової системи на органи та тканини. Так, як мозкова речовина наднирників отримує симпатичну інервацію, то швидко збільшується виділення в кров катехоламінів, що доповнює вплив симпатичного відділу вегетативної нервової системи. В результаті відбувається ерготропна перебудова функцій організму (збільшується частота та сила серцевих скорочень, збільшується тонус артеріальних та венозних судин) Ù розвиток пресорної реакції; розширюються бронхи; пригнічується секреторна та рухова активність органів системи травлення; збільшується збудливість рецепторів та структур ЦНС, підвищується працездатність клітин кори головного мозку; збільшується працездатність скелетних м’язів. Дуже важливим в забеспеченні адаптації є вплив САС на обмін речовин: 1 – активація глікогенолізу (розпад глікогену в печінці) Ù підвищення рівня глюкози в плазмі крові (гіперглікемія). 2 – активація ліполізу (розпад нейтрального жиру) в жировій тканині Ù підвищення рівня жирних кислот в крові. Такі зміни обміну речовин створюють субстратне забезпечення посиленої роботи клітин нервової системи та м’язів. Всі зміни в організмі при активації САС забезпечують високий рівень фізичної та розумової працездатності організму Ù адаптація до стресової ситуації. Адаптація, яку викликає активація САС відбувається швидко, але вона короткочасна. Це пов’язано з тим, що запаси глікогену в печінці невеликі (у дорослої людини 180-200 г), тому в умовах активації САС вони швидко виснажуються. Відповідно, гіперглікемія за рахунок лише активації САС не може зберігатися довгий час. Тому не може довготривало підтримувати високий рівень розумової та фізичної працездатності. Довготривала адаптація розвивається, якщо активація САС супроводжується активацією гіпоталамо-гіпофізарно-наднирникової системи. Кровь и ССС 63. Общая характеристика системы крови. Состав и функции. Понятие о гемостазе.
Кров циркулююча – знаходиться в стані активної циркуляції. Кров депонована – кров, яка перебуває в депо. Депо крові в організмі: – синуси селезінки та судини з низькою лінійною швидкістю кровотоку (венозні судини шкіри, ШКТ, легень і т.п.). Органи кровотворення – червоний кістковий мозок, тимус, лімфатичні вузли, селезінка, лімфатичні фолікули травного тракту. Органи руйнування елементів крові – макрофагоцитарна система організму. Нервові механізми регуляції забезпечують швидку зміну складу крові за рахунок перерозподілу її елементів (між депо і активною циркуляцією). Гуморальні механізми спрямовані на стимуляцію гемопоезу й викликають повільні, але надійні зміни складу крові. Ще раз підкреслемо, що діяльність системи крові спрямована на забезпечення двох результатів (див. вище схему).
Найважливішими параметрами фізико-хімічного гомеостазу є: 1. рН – від’ємний десятковий логарифм концентрації йонів водню (Н+). В артеріальній крові його величина складає 7,4, у венозній – 7,35. Сталість рН необхідна для нормального протікання процесів обміну речовин в клітинах (ферменти змінюють свою активність при зміні рН). 2. Осмотичний тиск (Росм.) – тиск розчинника на напівпроникну мембрану, якщо вона розділяє розчини з різною концентрацією осмотично активних речовин. Складає біля 7,6 атмосфер (1 атмосфера – 760 мм рт.ст.). Впливає на обмін між плазмою крові та міжклітинною рідиною. 3. Онкотичний тиск – частина осмотичного, що створюється білками. Його величина в крові складає 25-30 мм рт. ст. (1/200 від осмотичного тиску). Впливає на обмін води між плазмою крові та міжклітинною рідиною. 4. Ізойонія – постійний йонний склад плазми крові. Особливо велике значення має підтримання стійкості концентрації йонів Na+ та К+ в плазмі крові (концентрації йонів Na+ складає 142 ммоль/л, К+ – 5 ммоль/л), так як від цього залежить стан всіх збудливих клітин організма. 5. В’язкість крові – визначає величину її внутрішнього тертя та вимірюється у відносних одиницях (в порівнянні з в’язкістю води). В’язкість плазми крові складає 1,7-2,3 й зумовлена наявністю в ній білків. В’язкість крові складає 4,5-5,0. збільшення в’язкості крові в порівнянні з в’язкістю плазми пов’язана з наявністю в ній форменних елементів, перш за все, червоних кров’яних тілець (еритроцитів). В’язкість крові впливає на рух крові по судинам, особливо мікроциркуляторного русла. 6. Гематокрит – відсотковий вміст форменних елементів в крові. В нормальних умовах складає для чоловіків 40-48%, жінок – 36-42%. Величина змінюється, перш за все, при зміні обміну води. Наприклад, збільшення гематокрита найчастіше є наслідком зневоднення організму. При збільшенні показника зростає в’язкість крові й порушується мікроциркуляція. 7. Щільність крові – визначається наявністю в плазмі крові розчинних речовин (щільність плазми складає 1,025-1,034 г/см3) та форменних елементів (щільність крові – 1,050-1,060 г/см3).
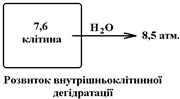
64.Осмотическое давление плазмы крови. Значение и механизмы поддержания изоосмоса. Онкотическое давление плазмы крови и его значение. Вміст йонів в плазмі крові складає близько 310 ммоль/л; на долю катіонів та аніонів припадає по 155 ммоль/л. З катіонів плазми найбільш важливими є йони Na+ (142 ммоль/л) та К+ (5 ммоль/л). З аніонів – йони хлора (Сlˉ – 103 ммоль/л) та бікарбонати (НСО3ˉ - 27 ммоль/л). Хлорид натрію складає 80% від загального вмісту йонів плазми крові; йони натрію, калію, хлора та бікарбоната складають 90% від загального вмісту йонів плазми. Ізойонія необхідна для нормального функціонування всіх клітин, а особливо збудливих, так як від величини градієнта концентрації залежить величина ПС клітинної мембрани Ù здатність до генерації ПД. В забезпеченні ізойонії велику роль відіграють гормони (гормон кіркової речовини наднирників альдостерон, стимулює реабсорбцію йонів Na+ та секрецію йонів К+ канальцями нирок, гормони тиреокальцитонін та паратгормон забезпечують гомеостаз йонів К+). Осмотичний тиск (Росм.) плазми крові складає біля 7,6 атм (біля 5500 мм рт. ст.). Осмотичний тиск – тиск розчинника на напівпроникну мембрану, якщо вона розділяє розчини з різною концентрацією осмотично активних речовин. Загальний осмотичний тиск плазми крові пов’язаний, в основному, з розчиненими в ній йонами (80% Росм. створюється йонами Na+ та Сlˉ, ще 10% – йонами К+ та НСО3ˉ). Певну роль в утворені Росм. крові відіграють й інші осмотично активні речовини – глюкоза, моноцукриди, амінокислоти і т.д. Напівпроникна мембрана пропускає молекули розчинника та не пропускає осмотично осмотично активні речовини. Осмотичний тиск є силою, що змушує розчинник рухатись через напівпроникну мембрану з розчину, де концентрація осмотично активних речовин (Росм.) нижча, в розчин, де концентрація осмотично активних речовин вища. По відношенню до загального осмотичного тиску крові, напівпроникною є зовнішня клітинна мембрана, бо вона вільно пропускає молекули води, але не пропускає йони та інші речовини, що створюють осмотичний тиск. Саме тому, загальний осмотичний тиск впливає на обмін води між внутрішньоклітинним та інтерстиційним (позаклітинним) середовищем. Підвищення Росм. наприклад, до 8,5 атм. може бути наслідком: - втрати води організмом без втрати еквівалентної кількості солей; - введення в організм надлишку солей, наприклад при вживанні дуже солоної їжі. Підвищення Росм. позаклітинної рідини (інтерстиційної рідини та плазми крові) призводить до виходу води з усіх клітин організму Ù їх зморщування (порушення структури) Ù порушення функції клітин. Найбільш чутливими до таких змін є клітини ЦНС, а особливо – клітини головного мозку.
В підтриманні постійності Росм. найбільшу роль відіграють нирки, які при збільшенні Росм. здійснюють: - затримку води в організмі (при цьому посилюється виділення гормона вазопресина, який посилює проникність дистальних канальців нефрона та збиральних трубочок для води Ù її посилена реабсорбція Ù врівноваження Росм. - виводять із організму надлишок солей, а особливо хлорид натрію (при цьому пригнічується секреція гормона альдостерона, який посилює реабсорбцію йонів натрію і секрецію йонів калію Ù посилення виведення йонів натрію, а разом з ним і йонів хлору з організму. При підвищенні Росм. затримка води та виведення солей нирками сприяють нормалізації цього показника. Окрім того, у людини виникає мотивація спраги Ù пошук та вживання води Ù нормалізація Росм. Онкотичний тиск – частина осмотичного тиску, що створюється білками (Ронк.). В утворенні онкотичного тиску найбільшу роль відіграють низькомолекулярні білки альбуміни – саме від їх вмісту в плазмі залежить, перш за все, Ронк.. Його нормальна величина складає 25-30 мм рт.ст. Напівпроникною мембраною для онкотичного тиску є стінка капілярів – вона вільно пропускає розчинник (вода), але не пропускає білки, що створюють онкотичний тиск!!! Білки є осмотично активними речовинами – вони гідрофільні та утримують при собі достатньо велику кількість води. Оскільки, стінка капілярів не пропускає білки в міжклітинну рідину, то це сприятиме затримці води в капілярах. Саме тому, Ронк. Впливає на обмін води між кров’ю та інтерстеціальною рідиною. На обмін води між кров’ю та тканинами за механізмом фільтрації-резорбції впливають: -Ронк. крові (25-30 мм рт.ст.); -Ронк. інтерстеційної рідини (3-5 мм рт.ст.); -Рг.кр.- гідростатичний тиск крові на стінки капілярів (на початку капіляра складає 30 мм рт.ст., а в кінці – біля 15 мм рт.ст.); -Рг.тк.- гідростатичний тиск інтерстеційної рідини на стінки капілярів (складає 3-4 мм рт.ст.). Сумарна сила, що виникає внаслідок додавання чотирьох названих сил, визначає рух води з капілярів в тканини (фільтраційна сила) та із тканин в капіляри (резорбційна сила). Ронк. крові перешкоджає виходу води з капілярів (білки не фільтруються самі та утримують при собі воду). Його величина однакова в артеріальній та венозній частині капіляра. Ронк. інтерстеційної рідини сприяє виходу води з капілярів у тканини (білки інтерстеціальної рідини “тягнуть” на себе воду внаслідок своєї гідрофільності). Рг.тк. перешкоджає виходу води з капілярів в тканини та діє однаково на артеріальний та венозний відділи капіляра. Рг.кр. сприяє виходу води з капілярів в тканини. Величина цього тиску змінюється під час руху крові по капіляру (зменшується від 30 до 15 мм рт.ст.). Тому, сумарна сила спрямована з капіляра в тканини в артеріальному відділі капіляра – це фільтраційна сила, вона зумовлює вихід (фільтрацію) води та розчинених в ній речовин з капіляра в тканини. У венозному відділі капіляра сумарна сила має протилежний напрямок – з тканин в капіляр – резорбційна сила. Вона зумовлює повернення (резорбцію) води та розчинних в ній речовин із тканин в капіляр. Якщо Ронк. крові знижується (довготривале голодування, хвороби печінки та нирок) збільшується фільтраційна сила та зменшується резорбційна збільшується фільтрація та зменшується резорбція рідини надлишок рідини накопичується в інтерстеційному просторі розвивається міжкілітинний набряк. Якщо Ронк. крові підвищується, відбуваються протележні зміни обміну води: збільшується резорбційна сила та зменшується фільтраційна відбуваєтся мобілізація рідини з інтерстеційного простору, перехід її в кров розвивається міжклітинна дегідратація.
65.Белки плазмы крови, их характеристика, функциональное значение. Вміст білків в плазмі крові складає близько 70г/л. Більша частина білків плазми крові представлена низькомолекулярними альбумінами (близько 40г/л), менша – високомолекулярними глобулінами (близько 30г/л). Окрім того, в плазмі знаходиться близько 3г/л фібриногена. Альбуміно-глобуліновий коефіцієнт складає 1,2 – 2,0. Джерелом білків плазми крові є перш за все печінка. Білки плазми крові виконують в організмі наступні функції: 1. Транспортна – зв’язуючись з білками, кров’ю транспортуються багато речовин (йони, ліпіди, жиророзчинні гормони, багато лікарських препаратів). 2. Створюють онкотичний тиск, який впливає на обмін води між кров’ю та інтерстиційною рідиною. 3. Приймають участь в підтриманні постійності рН крові (складають білкову буферну систему). 4. Фібриноген та інші білкові плазменні фактори згортання приймають участь в процесах згортання крові, чим забезпечують захист організму від крововтрати. 5. Багато білків плазми крові виконують функцію захисту організму від чужорідних речовин та мікроорганізмів. Частина з них забезпечують неспецифічний захист (система комплементу, інтерферони, інтерлейкіни і т.д.). Різні класи антитіл (білки-глобуліни) забезпечують специфічний захист. 6. Трофічну функцію білки плазми виконують при різкому або тривалому обмеженні надходження білків в організм. Білки плазми крові в таких умовах розпадаються з утворенням амінокислот, які використовуються клітинами для проходження пластичних процесів (побудова структур).
66.Кислотно-основное равновесие крови, механизмы, которые обеспечивают его постоянство. Роль буферных систем крови в поддержании его постоянства. Кислотно-основний стан (КОС) крові залежить від співвідношення концентрацій іонів Н+ та ОНˉ у плазмі крові. Характеризує КОС рН від’ємний десятковий логарифм концентрації іонів водню. Його нормальна величина – 7,4 в артеріальній крові та 7,36 у венозній. Величина рН крові відображає величину рН інтерстиційної рідини та рідини в клітинах. Внутрішньоклітинний рН визначає активність внутрішньоклітинних ферментів, а, відповідно, і стан обміну речовин в клітинах організму. Буферні системи крові: Сольові. Представлені солями слабких кислот і сильних основ і слабкими кислотами. Рівняння Голдерсона – Гассельбаха дозволяє розрахувати необхідне співвідношення концентрацій солі слабкої кислоти і цієї кислоти для підтримки компонентами сольових буферних систем необхідного рівня рН. рН = рК + lg Рівняння дозволяє, знаючи значення рК, розрахувати, яким має бути співвідношення в розчині слабкої кислоти та її солі для підтримання необхідного рівня рН (7,4). 1. Гемоглобінова буферна система рахуться найбільшою – до 75 % від усієї буферної ємності крові. Ця система складється з відновленого гемоглобіна (ННb) та його калієвої солі (КНb). Буферні властивості ННb зумовлені тим, що він будучи більш слабкою кислотою, ніж Н2СО3, віддає їй йони К+, а сам приєднуючи Н+, стає слабко дисоційованою кислотою. В тканинах система гемоглобіну виконує функцію основи, попереджуючи закислення крові внаслідок надходження до неї СО2 та Н+-йонів. В легенях гемоглобін крові поводить себе як кислота, попереджуючи залужнення крові після видалення з неї СО2. 2. Карбонатна буферна система за силою займає друге місце, а за швидкістю реагування – перше. Складається з вугільної кислоти та бікарбонату натрію (плазма крові) або бікарбонату калію (цитоплазма клітин). Формула карбонатної буферної системи - При утворенні в організмі надлишку кислоти, більш сильної, ніж вугільна, ця кислота реагує з сіллю вугільної кислоти (з бікарбонатом калію чи натрію). В результаті утворюється сіль цієї кислоти і слабка вугільна кислота, котра погано дисоціюєю. Таким чином, сильна кислота заміщується більш слабкою – запобігає зміні рН. При утворенні в організмі надлишку лужних сполук, вони взаємодіють з вугільною кислотою з утворенням бікарбонатів – запобігання зміні рН крові рК вугільної кислоти складає 6,1. Тому карбонатна буферна система забезпечує підтримання рН на рівні 7,4 при умові, що концентрація карбонатів у 20 разів перевищує концентрацію вугільної кислоти. Підтримку нормального співвідношення бікарбонатів та кислоти (20:1) забезпечують: - легені – виводять надлишок СО2 (а відповідно й вугільної кислоти). - нирки – забезпечують надходження в кров бікарбонатних іонів, що утворюються в клітинах ниркового епітелію в ході карбоангідразної реакації. Характеристика бікарбонатної буферної системи: 1.Вона забезпечує швидку нейтралізацію кислот та лугів, що утворюються в ході метаболізму. 2.Має досить велику ємність – від 15 до 40% від загальної буферної ємності крові. 3.Швидко відновлюється за рахунок діяльності легень і нирок. 3. Фосфатна буферна система утворена дигідрофосфатом (NaH2PO4) та гідрофосфатом (Na2HPO4) натрію. Відповідно, формула формула фосфатної буферної системи така:
Перша сполука слабко дисоціює та поводить себе як слабка кислота. Друга сполука має основні властивості. Ця буферна система забезпечує підтримку рН на рівні 7,4 при співвідношенні основної та кислої солей, що рівне 4:1. При введені в кров більш сильної кислоти, вона прореагує з Na2HPO4, утворюючи нейтральну сіль та збільшуючи кількість дигідрофосфату натрію. При введенні в кров сильної основи, вона прореагує з NaH2PO4, утворивши гідрофосфат натрію. Надлишок в крові дигідрофосфату та гідрофосфату натрію буде виводитись із сечею. Внесок у створення загальної буферної ємності відносно невеликий (5-10%). Відновлюється ця система значно повільніше, ніж карбонатна. В цьому процесі важливу роль відіграє вихід фосфорних солей з кісток. 4. Білкова буферна система. Білки плазми крові завдяки своїм амфотерним властивостям відіграють певну роль в кислотно-основній рівновазі. В кислому середовищі білки реагують як основи, а в основному як кислоти. Дата добавления: 2015-12-15 | Просмотры: 1538 | Нарушение авторских прав |
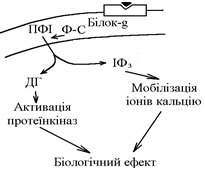 2. Механізм дії гормонів за участю похідних поліфосфатидилінозитольної системи (ПФІ-системи).
2. Механізм дії гормонів за участю похідних поліфосфатидилінозитольної системи (ПФІ-системи). 3. Механізм дії гормонів за участю іонів Са2+ та системи кальцій-кальмодулін як внутрішньоклітинних посередників.
3. Механізм дії гормонів за участю іонів Са2+ та системи кальцій-кальмодулін як внутрішньоклітинних посередників.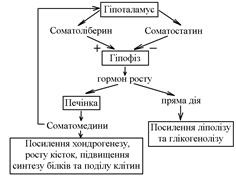 Секреція соматотропного гормону має епізодичний характер (більше у дітей під час сну). Стимулюючий вплив соматотропіну є опосередкованою – під його дією в печінці утворюються соматомедини,які і є безпосередніми факторами росту. Найактивніший серед соматомединів – соматомедин С, котрий у всіх клітинах тіла підвищує синтез білка, стимулюючи таким чином поділ клітин. Соматотропін може впливати на різні клітини і безпосередньо. Так він викликає мобілізацію жиру з депо, посилює глікогеноліз (антиінсуліновий ефект). Таким чином, вплив соматотропіну на організм заключається у посиленні хондрогенезу, росту кісток, поділу клітин, біосинтезу білка, стимулюючи таким чином процеси росту і розвитку.
Секреція соматотропного гормону має епізодичний характер (більше у дітей під час сну). Стимулюючий вплив соматотропіну є опосередкованою – під його дією в печінці утворюються соматомедини,які і є безпосередніми факторами росту. Найактивніший серед соматомединів – соматомедин С, котрий у всіх клітинах тіла підвищує синтез білка, стимулюючи таким чином поділ клітин. Соматотропін може впливати на різні клітини і безпосередньо. Так він викликає мобілізацію жиру з депо, посилює глікогеноліз (антиінсуліновий ефект). Таким чином, вплив соматотропіну на організм заключається у посиленні хондрогенезу, росту кісток, поділу клітин, біосинтезу білка, стимулюючи таким чином процеси росту і розвитку.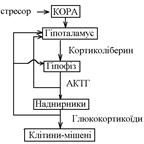 Вітамін D3 є третім важливим фактором, який приймає участь в підтриманні постійного рівня Са2+ в крові. Для його утворення в організм повинні надійти попередники провітаміну – D-ергостерол (препровітамін D3), або дигідроксихолестерол (препровітамін D2), які мають відповідно рослинне та тваринне походження. При дії на шкіру сонячних променів з цих препровітамінів утворюються провітаміни D3 та D2 їх гідроксилювання в печінці в 25-му положенні з утворенням 25-гідроксикальциферолу подальше гідроксилювання цієї сполуки в нирках вже в 1-му положенні з утворенням 1,25-дигідроксикальциферолу, який і являє собою вітамін D3, що має високу біологічну активність і бере участь в підтриманні гомеостазу Са2+ в крові, а саме сприяє всмоктуванню Са2+ в епітелії кишківника. За механізмом негативного зворотнього зв’язку вітамін D3 пригнічує секрецію ПТГ. Таким чином ці два гормони утворюють замкнуту регуляторну систему.
Вітамін D3 є третім важливим фактором, який приймає участь в підтриманні постійного рівня Са2+ в крові. Для його утворення в організм повинні надійти попередники провітаміну – D-ергостерол (препровітамін D3), або дигідроксихолестерол (препровітамін D2), які мають відповідно рослинне та тваринне походження. При дії на шкіру сонячних променів з цих препровітамінів утворюються провітаміни D3 та D2 їх гідроксилювання в печінці в 25-му положенні з утворенням 25-гідроксикальциферолу подальше гідроксилювання цієї сполуки в нирках вже в 1-му положенні з утворенням 1,25-дигідроксикальциферолу, який і являє собою вітамін D3, що має високу біологічну активність і бере участь в підтриманні гомеостазу Са2+ в крові, а саме сприяє всмоктуванню Са2+ в епітелії кишківника. За механізмом негативного зворотнього зв’язку вітамін D3 пригнічує секрецію ПТГ. Таким чином ці два гормони утворюють замкнуту регуляторну систему.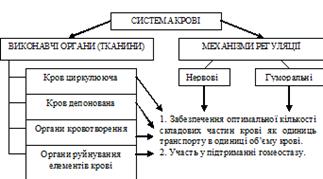
 Гомеостаз – відносна сталість параметрів внутрішнього середовища організму. Внутрішнє середовище – кров, лімфа, міжклітинна рідина. Вони знаходяться в стані динамічної рівноваги. Підтримання сталості параметрів гомеостазу є необхідною умовою нормального функціонування всіх клітин організму (міжклітинна рідина, в якій існують клітини є частиною внутрішнього середовища)! В клініці стан внутрішнього середовища оцінюють за показниками крові, так як її найлегше отримати для дослідження.
Гомеостаз – відносна сталість параметрів внутрішнього середовища організму. Внутрішнє середовище – кров, лімфа, міжклітинна рідина. Вони знаходяться в стані динамічної рівноваги. Підтримання сталості параметрів гомеостазу є необхідною умовою нормального функціонування всіх клітин організму (міжклітинна рідина, в якій існують клітини є частиною внутрішнього середовища)! В клініці стан внутрішнього середовища оцінюють за показниками крові, так як її найлегше отримати для дослідження.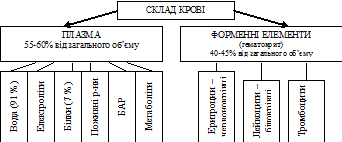
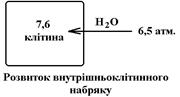 При пониженні Росм., що може спричинити надходженням надлишку води, або втрата солей організмом, проходять протилежні зміни: за градієнтом осмотичного тиску вода рухається в клітини Ù клітини набухають Ù порушується їх структура та функції. Але і в даному випадку найбільше страждають клітини КГМ.
При пониженні Росм., що може спричинити надходженням надлишку води, або втрата солей організмом, проходять протилежні зміни: за градієнтом осмотичного тиску вода рухається в клітини Ù клітини набухають Ù порушується їх структура та функції. Але і в даному випадку найбільше страждають клітини КГМ.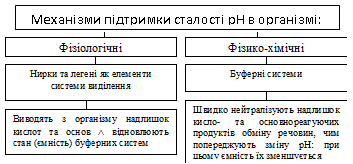
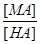 , де рК – від’ємний десятковий логарифм константи дисоціації кислоти, [МА] – концентрація солі в буферній системі, [НА] – концентрація слабкої кислоти в буферній системі.
, де рК – від’ємний десятковий логарифм константи дисоціації кислоти, [МА] – концентрація солі в буферній системі, [НА] – концентрація слабкої кислоти в буферній системі.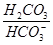 або
або 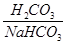 .
.