|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
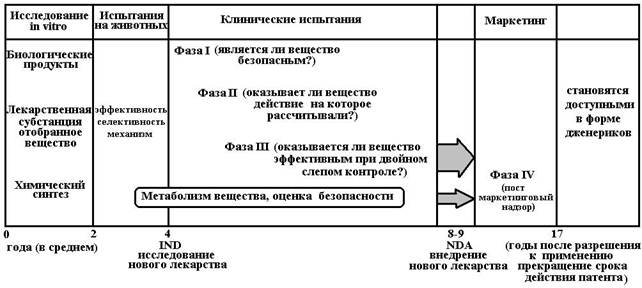
Основные этапы их внедрения в медицинскую практикуИсточниками получения лекарств могут быть: 1. Продукты химического синтеза. В настоящее время большинство лекарств получают именно этим путем. Различают несколько путей изыскания лекарств среди продуктов химического синтеза: [ Фармакологический скрининг (англ. to screen – просеивать). Метод поиска веществ с определенным типом фармакологической активности среди множества химических соединений синтезированных химиками по специальному заказу. Впервые фармакологический скрининг применил немецкий ученый Домагк, который работал в химическом концерне IG-FI и проводил поиск антимикробных средств среди соединений, синтезированных для крашения тканей. У одного из этих красителей – красного стрептоцида и было обнаружено противомикробное действие. Так были открыты сульфаниламидные средства. Проведение скрининга – чрезвычайно трудоемкий и затратный процесс: для обнаружения одного лекарственного средства исследователю приходится тестировать несколько сотен или тысяч соединений. Так, Пауль Эрлих, при поиске противосифилитических средств изучил около 1000 органических соединений мышьяка и висмута и только 606-й препарат – сальварсан, оказался достаточно эффективным. В настоящее время, для проведения скрининга необходимо синтезировать не менее 10.000 исходных соединений, чтобы с большей долей уверенности полагать, что среди них имеется одно (!) потенциально эффективное лекарственное средство. [ Молекулярное конструирование лекарств. Создание сканнирующей томографии и рентгенструктурного анализа, развитие компьтерных технологий позволили получать трехмерные изображения активных центров рецепторов и ферментов и подбирать к ним молекулы, конфигурация которых точно соответствует их форме. Молеуклярное конструирование не требует синтеза тысяч соединений и их тестирования. Исследователь сразу создает несколько молекул идеально подходящих к биологическому субстрату. Однако, по своей экономической стоимости данный метод не уступает скринингу. Методом молекулярного конструирования были получены ингибиторы нейраминидазы – новая группа противовирусных препаратов. [ Воспроизведение биогенных веществ. Таким образом были получены медиаторные средства – адреналин, норадреналин, простагландины; средства с активностью гормонов гипофиза (окситоцин, вазопрессин), щитовидной железы, надпочечников. [ Целенаправленная модификация молекул с уже известной активностью. Так, например, было установлено, что введение атомов фтора в молекулы лекарств, как правило повышает их активность. Путем фторирования кортизола были созданы мощные глюкокортикоидные препараты, при фторировании хинолонов были получены наиболее активные противомикробные средства – фторхинолоны. [ Синтез фармакологически активных метаболитов. При изучении метаболизма транквилизатора диазепама было установлено, что в печени из него образуется вещество с транквилизирующей активностью – оксазепам. В настоящее время оксазепам синтезируется и выпускается как отдельное лекарственное средство. [ Случайные находки («серендипитный» метод). Метод получил свое название по сказке Горация Уолпола «Три принцессы Серендипи». Эти сестры часто совершали удачные открытия и находили решения проблем сами специально не желая того. Примером «серендипитного» получения лекарства является создание пенициллина, которое произошло во многом благодаря тому, что A. Fleming случайно обратил внимание на то, что в заплесневелой чашке, забытой в термостате на Рождество, погибли микроорганизмы. Иногда случайные открытия совершаются в результате ошибки. Так например, ошибочно полагая, что противосудорожное действие фенитоина связано с тем, что он является антагонистом фолиевой кислоты, сотрудники концерна Glaxo Wellcome синтезировали ламотриджин – новое противосудорожное средство. Однако, оказалось что, во-первых, действие фенитоина не связано с фолиевой кислотой, а во-вторых, сам ламотриджин не вмешивается в обмен фолатов. 2. Компоненты растительного сырья. Многие растения содержат вещества, обладающие полезными фармакологическими свойствами, причем до настоящего времени продолжается открытие все новых и новых соединений. Широко известными примерами лекарственных средств, полученных из лекарственного растительного сырья являются морфин, выделенный из опийного мака (Papaver somniferum), атропин, полученный из красавки (Atropa belladonna). 3. Ткани животных. Из тканей животных получают некоторые гормональные препараты – инсулин из тканей поджелудочной железы свиней, эстрогены из мочи жеребцов, ФСГ из мочи женщин. 4. Продукты жизнедеятельности микроорганизмов. Ряд антибиотиков, средства для лечения атеросклероза из группы статинов получают из культуральной жидкости различных грибков и бактерий. 5. Минеральное сырье. Из попутных продуктов нефтеперегонки получают вазелин, используемый в качестве мазевой основы. Каждое лекарственное средство до того, как начнет применяться в практической медицине должно пройти определенную процедуру изучения и регистрации, которая гарантировала бы, с одной стороны эффективность лекарства при лечении данной патологии, а с другой стороны – его безопасность. Внедрение лекарственных средств делят на ряд этапов (см. таблицу 1). На схеме 2 показаны основные этапы движения лекарства в процессе его разработки и изучения. После завершения III фазы клинических испытаний документация вновь поступает в Фармакологический комитет (объем полного досье может составлять до 1 млн. страниц) и в течение 1-2 лет регистрируется в Государственном реестре лекарственных средств и изделий медицинского назначения. Только после этого фармакологический концерн имеет право начать промышленный выпуск лекарственного средства и его распространение через аптечную сеть. Таблица 1. Краткая характеристика основных этапов при разработке новых лекарств.
Дата добавления: 2015-01-12 | Просмотры: 923 | Нарушение авторских прав |