|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
ПАТОГЕНЕЗ РАНЕВОГО ПРОЦЕССА
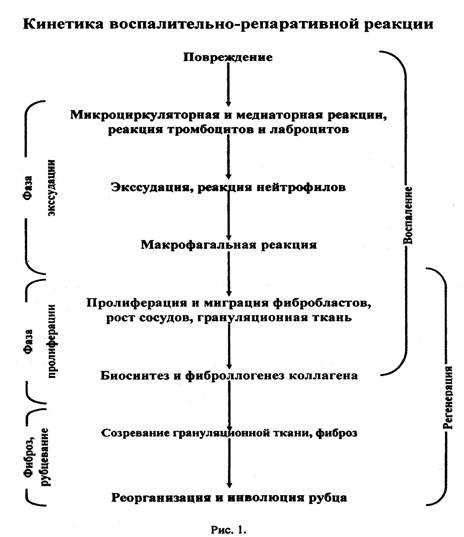
Раневым процессом принято называть совокупность биологических явлений, последовательно развивающихся в тканях раны. А.М. Чернух (1979) предложил различать в динамике воспалительного процесса пять следующих друг за другом стадий: Первая стадия -первичная сосудистая реакция, протекающая двухфазно в виде кратковременной вазоконстрикции с последующим длительным периодом вазодилятации на уровне микроциркуляторного русла и развития повышенной проницаемости сосудов. Вторая стадия -дальнейшее повышение проницаемости сосудов, особенно на уровне посткапиллярных венул, резкое замедление кровотока с адгезией лейкоцитов. Третья стадия -еще большее замедление кровотока вплоть до полной его остановки, экссудация жидкости и миграция лейкоцитов через стенки капилляров и венул. Четвертая стадия -развитие процессов очищения раны с активацией хемотаксиса и фагоцитоза микробных тел и некротических тканей. Пятая стадия -преобладание репаративных процессов. Как следует из представленной классификации, сосудистая реакция, вовлекающая артериолы, капилляры и венулы в зоне повреждения тканей, представлена тремя основными взаимосвязанными процессами. В первую очередь происходят изменения самих сосудов. Развивающаяся сразу после повреждения фаза вазоконстрикции уже через 5-10 минут сменяется фазой вазодилятации, изменяется проницаемость сосудистой стенки. Вторая группа процессов обусловлена внутрисосудистыми изменениями, заключающимися в развитии стаза, нарушении процессов свертывания крови, изменении реологических свойств крови и параметров форменных элементов. И, наконец, третья группа процессов представлена внесосудистыми изменениями, к которым можно отнести развитие, периваскулярного вещества, повреждение нервных окончаний и т.д. Раны различных областей и органов заживают по единым биологическим законам. Морфологически процесс заживления раны может протекать различно в зависимости от анатомического субстрата поражения, степени инфицированности, общего состояния организма, характера лечебных мероприятий. Однако в любом случае течение раневого процесса отражает один из классических типов заживления: заживление первичным натяжением, заживление вторичным натяжением, заживление под струпом. По определению В.И. Стручкова и соавт. (1975), раны, образовавшиеся после операции по поводу острых гнойных процессов (вскрытие абсцессов, флегмон) относятся к первичным гнойным ранам и заживление их протекает по законам вторичного натяжения. Установлено, что в области воспаления отмечается значительная активация окислительных процессов, нарушение электролитного баланса, обусловленное перемещением внутриклеточного калия во внеклеточное пространство, а натрия и воды - внутрь клеток. Вследствие преобладания в условиях кислородной недостаточности анаэробного тканевого обмена и накопления молочной кислоты развивается выраженный тканевой ацидоз. Прогрессирующий ацидоз значительно усиливает явления местного отека тканей, что сопровождается дополнительной ишемией тканей и усилением болевого синдрома. По механизмам развития ацидоз может быть первичным и вторичным. Первичный ацидоз развивается в результате действия повреждающего фактора и нарастает очень быстро. Однако спустя некоторое время развившийся ацидоз будет купирован буферными системами тканей. Вторичный ацидоз возникает в результате метаболических нарушений, включающих нарушения углеводного и белкового обмена, повреждения клеточных структур, снижения дыхательного коэффициента и др. Вторичный ацидоз носит стойкий характер и при значительном снижении рН может приводить к необратимым изменениям в биологических структурах. Для I фазы раневого процесса характерны выраженные воспалительные изменения краев и стенок раны: отечность, гиперемия кожи, прогрессирующая инфильтрация тканей, болезненность при пальпации. При нарастающем поражении подкожной жировой клетчатки зона отечности и инфильтрации нередко очень обширна, что является неблагоприятным признаком. Наличие плотного болезненного инфильтрата без четких границ характерно для развития затеков и распространения гнойного процесса. Нередко гнойный процесс быстро распространяется в подкожной жировой клетчатке. При этом может наблюдаться небольшое гноетечение на фоне высокой лихорадки. Это характерно для некло-стридиальной анаэробной инфекции. Поверхность и стенки раны приобретают серый оттенок, покрываясь сплошным фиброзно-гнойным налетом. В ней определяются участки очевидного некроза. Вид возбудителя воспалительного процесса во многом определяет его течение, характер грануляций и отделяемого. Так, стафилококковому поражению присуще, в основном, бурное течение местного процесса и образование густого гноя желтоватого цвета. Стрептококковая инфекция имеет тенденцию к диффузному распространению. При этом обычно наблюдается массивное пропитывание клетчатки жидким гноем желто-зеленого цвета. Анаэробная инфекция обуславливает альтеративный характер течения воспалительного процесса и жидкое зловонное отделяемое, напоминающее сукровичную жидкость. Для палочки сине-зеленого гноя и протея характерно вялое, затяжное течение с отчетливыми явлениями общей интоксикации. Возникновение явлений, характерных для воспаления, обусловливается накоплением в поврежденных тканях специфических биологически активных веществ. Общим признаком всех этих веществ служит появление или резкая их активация в поврежденных тканях. Другой особенностью химических регуляторов воспаления является то, что большинство из них проявляет высокую активность в ничтожно малых концентрациях. Известные медиаторы раневого процесса имеются, как правило, в любой ране, а их соотношение определяет характер течения патологического процесса и скорость заживления раны. В основном их можно разделить на плазменные (циркулирующие) медиаторы (кинины, факторы свертывания крови и фибри-нолиза, система комплемента) и медиаторы местного происхождения (биогенные амины, простогландины, лейкотрины, лизосомальные компоненты, лимфо-кины, тканевые тромбопластины), связанные со многими клетками крови: ней-трофилами, макрофагами, лимфоцитами, базофилами, тромбоцитами и др. Выделенные из различных клеток биологически активные полипептиды при раневом процессе принимают непосредственное участие в заживлении ран. В общем же виде, независимо от источника клеток - продуцентов, эти биологически активные вещества имеют название цитокинов. Они препятствуют распространению патогена, привлекают гранулоциты, макрофаги и лимфоциты в очаг патогена, осуществляют уничтожение возбудителя и выведение его из организма. Воспалительные реакции регулируются цитокинами, продуцируемыми макрофагами. При тканевой деструкции происходит взаимная регуляция выработки иммунопептидов макрофагами и другими клетками. Интерлейкины (ИЛ-1) и фактор некроза опухоли (ФНОα), секретируемые активированными макрофагами, индуцируют выработку ИЛ-1 и колониестимулирующих факторов (КСФ) клетками эндотелия, фибробластами. КСФ по типу обратной связи активирует фагоцитоз, микробицидность макрофагов и нейтрофилов в очаге воспаления, а также стимулируют миелогенез в костном мозге. Таким образом определенный комплекс цитокинов, включающих ИЛ-1, ФНОα, ИЛ-6, интерфероны (ИФγ), различные КСФ и др., определяют течение воспаления в очаге тканевой деструкции. В результате активации фагоцитов и действия их продуктов - медиаторов воспаления и ферментов - происходит очищение раневой поверхности от гнойно-некротических масс и переход во вторую фазу раневого процесса. Под влиянием медиаторов воспаления формируется грануляционная ткань (рис. 1). Образование и созревание грануляционной ткани - результат действия на ее клеточные элементы ростковых факторов различной гистогенетической направленности, продуцируемых макрофагами, лимфоцитами и фибробластами. Среди цитокинов, регулирующих рост и дифференцировку фибробластов, на ранних сроках заживления выступает ростковый фактор из тромбоцитов. Трансформирующий фактор роста (ТФР) участвует в образовании грануляционной ткани, стимулирует пролиферацию фибробластов и ангиогенез сосудов. Под влиянием цитокинов, в частности ИЛ-1, регулируется рост не только фибробластов, но и клеток эндотелия, стимулируется миграция эпидермальных клеток в ране, новообразование эпидермиса, регенерация нервных окончаний с индукцией выработки ростковых факторов в нервной ткани. Одни цитокины (ИЛ-1, ФНОα и ТФРβ) индуцируют синтез коллагена фибробластами, тогда как другие (ИФγ, ИЛ-1 в высоких дозах, ФНОα) подавляют коллагеносинтетическую функцию. Таким образом, цитокины могут позитивно и негативно регулировать заживление раны. Следовательно, исход раневого процесса определяется совокупностью межклеточных взаимодействий лимфоцитов, макрофагов, фибробластов, эндо-телиапьных и других клеток через прямые рецепторные и медиаторные контакты по принципу саморегуляции. Дисбаланс в выработке цитокинов может нарушить существующие в локальной системе взаимосвязи, что приведет к длительному заживлению раны, образованию келоидов и др.
Дата добавления: 2014-11-24 | Просмотры: 1652 | Нарушение авторских прав |