 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Аеробне окиснення вуглеводівМіж аеробним і анаеробним перетворенням існує тісний зв'язок. Обидва ці процеси на початкових етапах (до утворення пірувату) відбуваються за участю однакових ферментів і з утворенням однакових проміжних продуктів. Як і анаеробне, аеробне окиснення може перебігати тільки при наявності фосфорильованих гексоз. В аеробних умовах вуглеводи повністю окиснюються з утворенням СО2 та Н2О. У цьому окисненні гліколіз становить першу стадію, яка закінчується утворенням піровиноградної кислоти. У наступній стадії, яка носить назву окиснювальне декарбоксилування, піруват перетворюється на ацетил-КоА та СО2. Третім етапом є окиснення двовуглецевих ацетильних груп до СО2 та Н2О в циклі лимонної кислоти і реакціях тканинного дихання. 4.3.1. Окиснювальне декарбоксилування пірувату. Процес окислювального декарбоксилування пірувату включає реакції дегідрування та декарбоксилування, у ході яких карбоксильна група вивільняється у вигляді СО2, а ацетильний залишок переноситься на коензим А: Піруват + НАД+ + НS-КоА ® Ацетил-КоА + СО2 + НАДН + Н+
Піруватдегідрогеназний комплекс являє собою мультиферментну систему з М.м. 4·106 Да і складається з трьох ферментів: піруватдегідрогенази, дигідроліпоїлдегідрогенази та дигідроліпоїлацетилтрансферази (рис. 4.7).Ці ферменти двокомпонентні та містять 5 коферментів: НАД+, ФАД, тіаміндифосфат (ТДФ) або тіамінпірофосфат (ТПФ), ліпоєву кислоту і кофермент ацилювання (КоА-SН).
Перший етап – це взаємодія пірувату та ТДФ з утворенням проміжної сполуки – активного пірувату, який, декарбоксилуючись, під дією ферменту піруватдекарбоксилази перетворюється на оксіетилтіаміндифосфат:
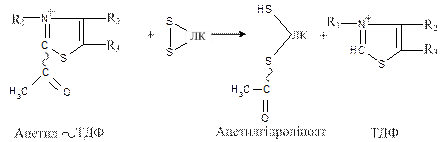
Оксіетил-ТДФ реагує з окисненою формою ліпоєвої кислоти, яка входить до складу ліпоаттрансацетилази, при цьому утворюється ацетил-ТДФ:
На другому етапі за участю ферменту дигідроліпоїлацетилтрансферази залишок ацетату переноситься з ацетил–ТДФ на другу молекулу ліпоєвої кислоти з утворенням ацетил–гідроліпоату:
дигідроліпоїлацетилтрансфераза каталізує і третю стадію – перенесення ацетильної групи на КоА-SH з утворенням кінцевого продукту ацетил-КоА, який є високоенергетичною (макроергічною) сполукою.
На четвертому етапі відбувається зворотне окиснення (реоксидація) аміду дигідроліпоєвої кислоти відбувається за участю ферменту дигідроліпоїлдегідрогенази, яка коферментом містить ФАД. Амід дигідроліпоєвої кислоти окиснюється до аміду ліпоєвої кислоти. Атоми водню передаються на ФАД через третю молекулу ліпоєвої кислоти, ФАД при цьому відновлюється.
Від ФАДН2 за участі дигідроліпоїлдегідрогенази атоми водню відразу ж переходять на окиснену форму НАД+, тому в сумарному рівнянні реакції окиснення пірувату в якості акцептора водню виступає НАД+:
НАДН окиснюється киснем за схемою:
Ацетил-КоА, конденсуючись із оксалоацетатом, перетворюється на лимонну кислоту, яка є одним з компонентів циклу ди- і трикарбонових кислот (циклу лимонної кислоти). За допомогою цього циклу та цитохромної системи ацетил-КоА в результаті низки перетворень окиснюється до кінцевих продуктів СО2 і Н2О.
Вивільнений при цьому КоА-SH може вступати в реакцію з наступними молекулами аміду ацетилліпоєвої кислоти. 4.3.1.1. Біологічна роль і регуляція окиснювального декарбоксилування пірувату. Значення цього процесу для організму людини полягає в наступному:
2) утворюється макроергічна сполука – ацетил-КоА, яка підлягає подальшому окисненню в циклі трикарбонових кислот або використовується в реакціях анаболізму (синтезі жирних кислот, наприклад); 3) синтезується відновлений еквівалент – НАДН, який окиснюється в дихальному ланцюзі мітохондрій. Енергетичний ефект окиснення 1 моля пірувату становить 3 молекули АТФ. Реакції окиснювального декарбоксилування пірувату регулюються на рівні піруватдегідрогенази двома шляхами: 1) алостерично: продуктами реакції - ацетил-КоА та НАДН, фруктозо-1,6-дифосфатом, НАД+; 2) шляхом хімічної модифікації – фофорилуванням (фосфорильована форма - неактивна, а дефосфорильована–активна) (рис. 4.8). 4.3.2. Енергетичний баланс аеробного окиснення глюкози. Енергетична ефективність повного окиснення глюкози до СО2 та Н2О представлена в таблиці 4.3.
Таблиця 4.3. Енергетична ефективність повного окиснення 1 моля глюкози
Отже, сумарний вихід АТФ у результаті повного окиснення глюкози (1 моль) в аеробних умовах становить 38 молекул за умови функціонування малат-аспартатної човникової системи. У випадку використання гліцеролфосфатного човникового механізму енергетична ефективність процесу буде становити 36 молекул АТФ. Дата добавления: 2015-11-25 | Просмотры: 1676 | Нарушение авторских прав |
 Сукупність цих реакцій каталізує піруватдегідрогеназний комплекс. він міститься в мітохондріях, тому піруват, який утворюється в процесі гліколізу в цитоплазмі, мусить переміститися туди.
Сукупність цих реакцій каталізує піруватдегідрогеназний комплекс. він міститься в мітохондріях, тому піруват, який утворюється в процесі гліколізу в цитоплазмі, мусить переміститися туди. При окисненні пірувату утворюється не вільна ацетатна кислота, а так звана “активна” або “активована” ацетатна кислота у вигляді ацетил-КоА. Остання за рахунок наявності макроергічного зв'язку може бути використана в різних синтетичних процесах. Докладне дослідження окиснення пірувату за участю дегідрогенази показало, що реакція відбувається в декілька етапів (для спрощення органічні залишки в молекулі ТДФ позначимо радикалами R1, R2, R3):
При окисненні пірувату утворюється не вільна ацетатна кислота, а так звана “активна” або “активована” ацетатна кислота у вигляді ацетил-КоА. Остання за рахунок наявності макроергічного зв'язку може бути використана в різних синтетичних процесах. Докладне дослідження окиснення пірувату за участю дегідрогенази показало, що реакція відбувається в декілька етапів (для спрощення органічні залишки в молекулі ТДФ позначимо радикалами R1, R2, R3):

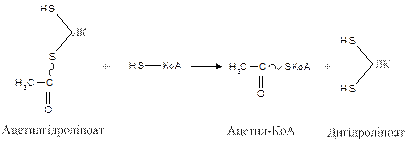

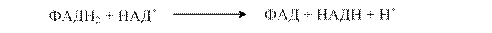


 1) піруват розпадається до одного з кінцевих продуктів – СО2, який виводиться з організму або використовується для синтезу;
1) піруват розпадається до одного з кінцевих продуктів – СО2, який виводиться з організму або використовується для синтезу;