|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Неспецифическая иммунотерапия
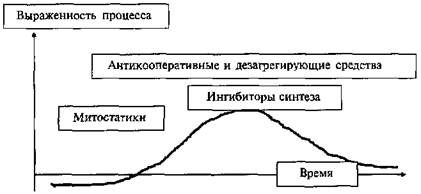
Неспецифическая активная стимулирующая иммунотерапия активирует иммунный ответ. Используются воздействия 3-х видов: биологические, химические, физические. 1. Биологические воздействия: Адьюванты —неспецифические усилителии ммунологических реакций. Они усиливают иммунный ответ на соответствующий антиген, создают депо антигена, способствуют его медленному поступлению в кровь и формированию наиболее эффективной стимуляции иммунного ответа. Это липополисахариды некоторых бактерий. Они стимулируют В-лимфоциты, фагоцитоз, образование интерлейкина-1 и лимфокинов. К ним относятся — адьювант Фрейнда, вакцина БЦЖ для стимуляции антителообразования у человека, бактериальные продукты — продигиозан, пирогенал. Применение их показано при недостатке иммуноглобулинов и функциональной активности В-лимфоцитов. Целесообразно их назначение совместно с макролидами при воспалительных процессах. Противопоказано совместное применение их с цефалоспоринами и бета-лактамами, с которыми они являются антагонистами. Нуклеиновые кислоты или их соли, полинуклеотиды — активируют различные звенья иммунного ответа. Лучше их вводить совместно с антигеном в ранние стадии иммуногенеза. В низких дозах— стимулируя его, в высоких— подавляя. Нуклеинат натрия — натриевая соль дрожжевой РНК. Стимулирует миграцию стволовых клеток, кооперациюТ-, В-лимфоцитов, функциональную активность их популяций, антителогенез. Эффективен при вторичных иммунодефицитах. Витамины — регуляторы биохимических процессов в клетках и тканях, в том числе иммунной системы. Витамин «С» обладает антиоксидантной активностью, стимулирует фагоцитоз, миграцию и дифференцировку Т- и В-лимфоцитов. Обладает противоаллергическим и противовоспалительным действием в больших дозах (1—3 г в сутки). Витамин «Е» усиливает активность Т-хелперов и синтез антител. Витамин «А» обладает адьювантными свойствами, стимулирует активность комплемента, пропердина, усиливает антителогенез и противоопухолевый иммунитет, уменьшает иммунодепрессивное действие глюкокортикостероидов и антибиотиков. 2. Химические воздействия — искусственные полиэлектролиты пентоксил, метилурацил, дибазол, тафцин, диуцифон. Активируют В-лимфоциты и антителогенез на присутствующий в организме антиген. 3. Физические воздействия — в зависимости от вида энергии и её дозы могут стимулировать иммунологические реакции или подавлять иммунореактивность. Ультразвук — стимулирует фагоцитоз, хемотаксис, увеличивает концентрацию и аффинность рецепторов на активированных лимфоцитах. На этом свойстве основано его применение в медицине. Озвучивание селезёнки через кожу приводит к снижению аллергических проявлений при бронхиальной астме, увеличивает количество Т-супрессоров. Озвучивание тимуса у детей при низком уровне Т-лимфоцитов (до 25%) дает хороший результат. Увеличивает их количество, восстанавливает соотношение популяций Th/Ts. Неспецифическая активная подавляющая иммунотерапия. Основана на индукции неспецифического активного подавления иммунореактивности. Это использование гистамина, гистаглобулина по схеме при в/к введении начиная с минимальных доз для выработки блокирующих антител класса IgG. Чаще применяется препарат гистаглобулин— комплекс гистамина на гаммаглобулине. Он стимулирует образование антигистаминных антител, которые связывают гистамин при патохимической фазе анафилаксии. Противопоказания — беременность, острые аллергические реакции. Адаптивная стимулирующая иммунотерапия. Основана на применении и восприятии иммунокомпетентными клетками неспецифических стимулов от гормонов тимуса и других факторов иммунитета, введенных из вне. Эти эффекты свойственны гормонам тимуса, костного мозга, селезёнки, лимфоузлов. Тимозин, тималин, тактивин — используют для лечения первичных и вторичных иммунодефицитов, опухолей. Они восстанавливают нарушенные звенья иммунитета, количество Т-лимфоцитов, стимулируют клеточный иммунитет, фагоцитоз, процессы регенерации тканей и кроветворения, улучшают метаболизм. Неспецифическая пассивная заместительная иммунотерапия характеризуется тем, что больному вводят готовые неспецифические факторы иммунитета и иммунокомпетентных клеток при их недостаточности: пересадка костного мозга, лимфоидной ткани при тяжёлых иммунодефицитах; переливание крови и её препаратов (эффективны, если они не отличаются от донора по антигенам гистосовместимости, иначе эффекта не будет, так как происходит быстрая элиминация клеток); введение иммуноглобулинов для пассивной терапии; введение очищенных гамма-глобулинов различных классов для возмещения из недостаточности; введение комплемента, лизоцима для повышения противоин-фекционной защиты. Неспецифическая пассивная подавляющая иммунотерапия. Направлена на различные звенья иммунитета. Требует особых показаний и контроля за иммунологическим статусом больного и клинико-лабораторными данными. Абсолютным показанием к её назначению является аллотрансплантация органов итканей. Глюкокортикостероиды (преднизолон, метилпреднизолон, дексаметазон, гидрокортизон, кенакорт, триамцинолон) вызывают угнетение реакций при аллергических заболеваниях, отторжении трансплантата, системных заболеваниях соединительной ткани. Они угнетают воспалительные реакции, стабилизируют мембраны лейкоцитов и выброс нейтрофилов из костного мозга, удлиняют время их циркуляции в крови, блокируют миграцию, прилипание и накопление в очагах воспаления. Тормозят все фазы иммунного ответа, вызывают лимфоцитолиз, угнетают фагоцитоз, пролиферацию лимфоцитов и их взаимодействие с другими клетками, тормозят эффекторную функцию лимфоцитов. Цитостатические препараты: • антиметаболиты - антагонисты пурина (меркаптопурин, азатиоприн, имуран) — тормозят синтез ДНК и РНК, блокируют размножение клеток; - антагонисты фолиевой кислоты — (метотрексат) — тормозит синтез и удвоение ДНК. - алкилирующие соединения (циклофосфан, циклофосфамид, мелфалан, милеран) разрушают молекулу ДНК, тормозят синтез белка, лейкеран — избирательно действует на лимфоидную ткань; • антибиотики (актиномицин D и С, пуромицин) — тормозят синтез РНК и белков; • алкалоиды (винкристин) — блокирует митоз в метафазе, тормозит синтез белка; • метаболиты (циклоспорин А) — избирательноугнетаетТ-хелперы, подавляет T-клеточную чувствительность замедленного типа и образование антител. Эффективен при трансплантации органов. Побочно выражено сильное нефротоксическое действие. Ингибирующий эффект на иммунную систему обратим. • Нестероидные противовоспалительные средства (аспирин, диклофенак) подавляют синтез простагландинов, действуют антигистаминно, угнетают миграцию лейкоцитов, снижают хемотаксис, фагоцитоз, отменяют кооперацию Т- и В-лимфоцитов. • Хинолиновые препараты (делагил, плаквенил) — ингибируют активность ферментов, медиаторов воспаления и аллергии, угнетают обмен ДНК. Применяют чаще всего при системных заболеваниях соединительной ткани (СКВ, ревматоидный артрит и др.). • Антилимфоцитарная сыворотка — разрушает лимфоциты и вызывает лимфопению. • • моноклональные антитела (ритуксимаб) к CD19+ T-лимфоцитам. • Ингибиторы аллергических реакций (интал, кромолин, задидет) — действуют на патохимическую фазу аллергии. Антимедиаторные средства: антигистаминные (димедрол, супрастин, тавегил, диазолин, фенкарол, цетиризин, левоцетиризин, лоратадин, дислоратадин, фексофенадин), антисеротониновые препараты (циннаризин, стугерон, перитол) действуют на патохимическую фазу, поэтому не устраняют причины аллергии, при длительном их применении их эффективность снижается. • Физические факторы (рентгеновское, ультрафиолетовое излучения) — действуют как супрессоры; • Плазмафорез, гемосорбция - удаление из крови иммунологических факторов (лимфоциты, ЦИК, антигены, антитела, медиаторы) — вызывают временный супрессивный эффект и нормализуют иммунный статус, особенно при аллергии. Если изобразить периоды обострения и ремиссии аутоиммунных заболеваний в виде схематической кривой, то препараты угнетающие размножение клеток (имуран, меркаптопурин) следует назначать при первых признаках-предвестниках ухудшения состояния и в течении развития патологического процесса, прекращая их применение на пике рецидива. После этого при первых признаках ремиссии необходимо назначать препараты тормозящие синтез белка (актиномицин D и С, ритуксимаб). Вещества, нарушающие кооперативные межклеточные процессы (глюкокортикостероиды, гепарин, аспирин, гормоны), можно назначать всегда, поскольку взаимодействие клеток при иммунном ответе происходит во всех фазах, прежде всего при обострении (рецидиве заболевания) (схема 1.). Любая иммунодепрессивная терапия должна назначаться под прикрытием антибиотиков широкого спектра действия, введением препаратов гамма-глобулинов и содержанием больного в асептических условиях.
Трансфузиологические методы иммунотерапии при интоксикации. В токсическом периоде заболеваний возможность иммунокоррекции ограничена иммунодепрессивным действием интоксикации, которой принадлежит определённая роль в иммуносупрессии организма, подавлении функциональных показателей Т-лимфоцитов и фагоцитоза. Компенсация токсигенной иммуносупрессии возможна путем инфузии препаратов низкомолекулярного поливинилпирролидона: полиглюкин, реосорбилакт, полиоксидоний и др. Механизм дезинтоксикационного действия полиглюкина, реосорбилакта основан на способности связывать в кровяном русле токсины и выводить их из организма. Они предохраняют иммунокомпетентные клетки от иммуносупрессивного действия интоксикации. Их следует применять в сочетании с лекарственными препаратами, используемыми в токсическом периоде: антибактериальными, сердечно-сосудистыми. При этом полиглюкин, реосорбилакт усиливает эффективность антибактериальной терапии. Одним из компонентов крови является плазма, обладающая антитоксическим действием. Действие нативной концентрированной плазмы на иммунную систему проявляется в восполнении недостаточности иммуноглобулинов, медиаторов, цитокинов и компонентов комплемента. Использование её позволило установить эффект в восстановлении функциональной активности Т-лимфоцитов, особенно при высокой активности воспалительного процесса. Положительное иммунное влияние плазмы оказывается только в токсическом периоде. Сущность иммунокорригирующего действия плазмы заключается в контрдействии иммуносупрессивным факторам, свойственным острой фазе воспаления. Это микроорганизмы, вторичные продукты воспаления, лекарственные препараты. Иммунокорригирующее влияние плазмы непродолжительно. Лабораторными критериями показания к трансфузии нативной концентрированной плазмы являются недостаточность клеточного иммунитета и иммуноглобулинов. Дата добавления: 2015-11-25 | Просмотры: 763 | Нарушение авторских прав |