|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Качественные реакции на витамины. Количественное определение витамина С.
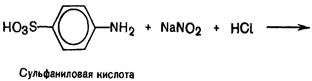
1. Витамин В1 (тиамин) а) с диазореактивом
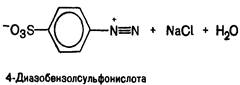
Принцип метода. Сначала образуется диазобензолсульфат (диазобензолсульфокислота):
Раствор тиамина при добавлении диазобензолсульфата и щелочи дает окрашенное соединение. Ход работы. В пробирку последовательно добавляют:
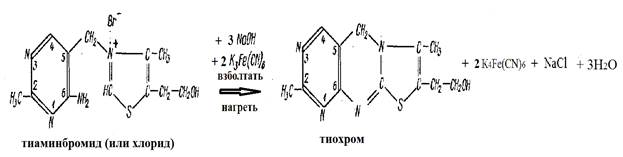
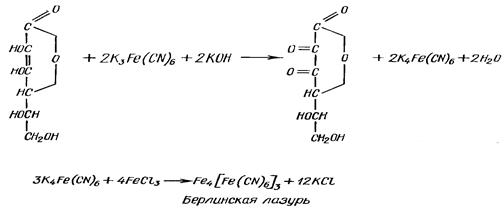
б) окисления в тиохром Принцип метода. При действии K3Fe(CN)6 в щелочной среде тиамин окисляется в желтый тиохром, обладающий голубой флуоресценцией в УФ-свете.
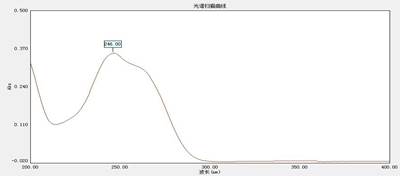
в) снять спектр поглощения (модуль “спектральный”, диапазон от 350 до 220нм) и наблюдать максимум при λ=250-260 нм. График сохранить, перевести в Paint, затем вставить в файл “Графики” (документ Word), подписать и вклеить в отчет. ВНИМАНИЕ! Спектры всех витаминов снимать одновременно, чтобы включать и прогревать спектрофотометр только один раз. УФ-спектр тиамина гидрохлорида (8 мкг/мл) в растворе HCl 0,9%. Максимум при 246 нм.
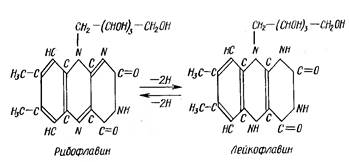
2. Витамин В2 (рибофлавин) а) с металлическим цинком Принцип метода. Рибофлавин восстанавливается выделяющимся водородом в бесцветный лейкофлавин. Наблюдается изменение окраски из желтой в зеленоватую, позже в малиновую, розовую, а затем – цвет исчезает.
Ход работы. В пробирку наливают 1мл взвеси рибофлавина в воде (0,015 - 0,025% раствор), добавляют 10 капель концентрированной HCl и опускают кусочек металическо-го цинка. Начинается бурное выделение пузырьков водорода, и жидкость постепенно окрашивается в розовый или красный цвет, затем окраска жидкости начинает бледнеть и обесцвечиваться (обратное окисление лейкофлавина в рибофлавин).
б) с азотнокислым серебром Принцип метода. Нейтральные или слабокислые растворы рибофлавина (рН 6,5-7,2), реагируя с AgNO3, дают соединение розово-красных тонов. Интенсивность окраски зависит от концентрации витамина. Ход работы. К 1 мл р-ра рибофлавина (0,015 - 0,025%) добавляют 0,5 мл р-ра AgNO3 (0,1%). Появляется розовое окрашивание.
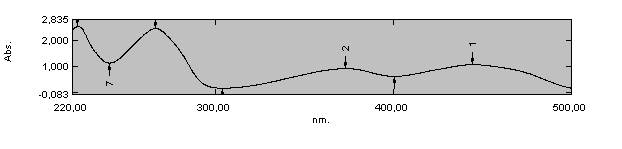
УФ-спектр рибофлавина (35 мкг/мл) в растворе ацетата натрия CH3COONa 0,01%. Максимум при 266,5 нм.
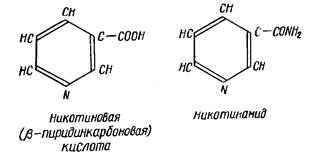
3. Витамин В5 (РР, никотиновая кислота)
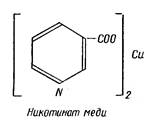
а) с ацетатом меди Принцип метода. При нагревании никотиновой кислоты с уксуснокислой медью образуется осадок медной соли никотиновой кислоты. Ход работы. 5-10 мг никотиновой кислоты растворяют при нагревании в 10-20 каплях 10%-го раствора уксусной кислоты (или готовят 0,75% р-р никотиновой кислоты в горячей воде, а затем к 2 мл этого р-ра добавляют 1 мл 15%-ного р-ра уксусной к-ты). К нагретому до начала кипения раствору добавить равный объем 5%-го раствора уксуснокислой меди. Жидкость становится голубоватой мутной, а при стоянии и охлаждении выпадает осадок никотината меди синего цвета.
б) на запах пиридина Принцип метода. При нагревании никотиновой кислоты с безводным Na2CO3 ощущается неприятный запах пиридина. Ход работы. В небольшом сухом фарфоровом тигле смешивают 0,05 г никотиновой к-ты с 0,1-0,15 г безводного углекислого натрия и подогревают. Появляется резкий запах пиридина.
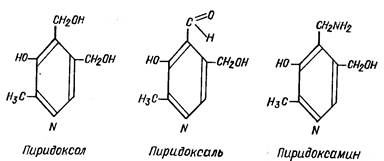
4. Витамин В6 (пиридоксин)
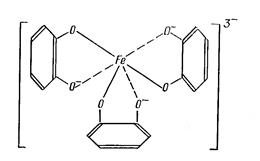
а) с хлорным железом Принцип метода. Витамин В6 образует с хлорным железом комплекс кроваво-красного цвета. Ход работы. 4 мл 0,5-1% р-ра пиридоксина + 0,5мл 1%-ного FeCl3 → встряхнуть и наблюдать красный цвет.
б) ДОПОЛНИТЕЛЬНО –
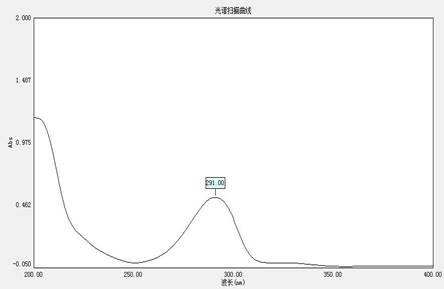
в) снять спектр в 0,1М NaOH (наблюдать максимумы при λ=245 и 308 нм) или воде (см.рис).
УФ-спектр пиридоксина гидрохлорида (15мкг/мл) в воде (рН≈6,0). Максимум при 291 нм.
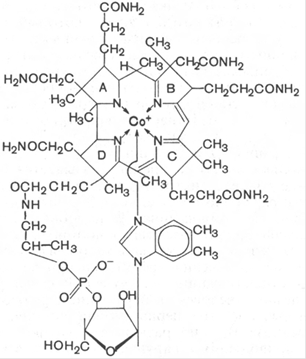
5. Витамин В12 – оформить в отчете, на практике не делаем в связи с высокой токсичностью действующего реактива.
Витамин В12 реагирует с цианидом при рН=10 с образованием пурпурного дицианкобаламина, так как Со окисляется до 3х-валентного и 5’-дезоксиаденозин замещается на анион CN.
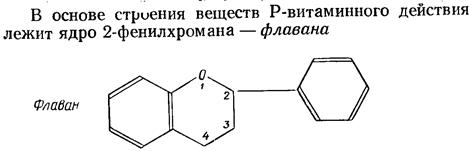
6. Витамин Р (на примере рутина) К веществам Р-витаминного действия относится ряд соединений фенольной природы, основное физиологическое действие которых – уменьшение проницаемости и повышение прочности капилляров. Они способствуют усвояемости вит.С в организме человека и животных, активно участвуют в окислительно-восстановительных процессах, обладают антиокислительными свойствами, залерживая, среди прочего, и окисление адреналина. Они также инактивируют фермент гиалуронидазу, тем самым тормозя распад гиалуроновой кислоты – гетерополисахарида в основном веществе соединительных тканей. Вит. Р угнетают активность холинэстеразы, сукцинатдегидрогеназы и ряда других ферментов.
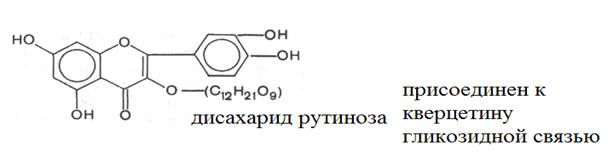
Витаминными свойствами обладает ряд флавонолов (рутин, кверцетин), флаванонов, катехинов, кумаринов, галловая кислота и ее производные, антоцианы (красящие вещества из плодов, ягод, цветков). Многие вещества Р-витаминного действия – это гликозиды флавонолов и флаванонов или агликоны (неуглеводные компоненты гликозидов). Например, рутин – это гликозид, в котором к дисахариду рутинозе присоединен агликон фенольного строения флавонол кверцетин.
а) с хлорным железом
б) с серной кислотой Принцип: Конц серная к-та образует с флавонами (рутином) оксониевые соли, обладающие в растворе желтой окраской. Флаваноны (например, гесперидин) дают с серной к-той малиновое окрашивание.
7. Витамин С а) качественно - с K3Fe(CN)6 Принцип метода: восстановление феррицианида калия витамином С с изменением окраски до синей из-за образования берлинской лазури.
Ход работы. В двух пробирках смешивают 5 капель 5%-го раствора К3Fe(CN)6 c 5 каплями 1%-го раствора FeCl3. В одну из пробирок к зеленовато-бурой жидкости прибавляют 20 капель 1%-го раствора аскорбиновой кислоты или сока капусты, а в другую - столько же дистиллированной воды. Жидкость в первой пробирке приобретает зеленовато-синюю окраску, выпадает синий осадок берлинской лазури; во второй пробирке (контроль) зеленовато-бурая окраска жидкости остается без изменения.
Дата добавления: 2015-11-25 | Просмотры: 2231 | Нарушение авторских прав 12 |