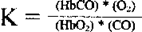|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Механизм токсического действия. Окись углерода, поступающая в легкие с атмосферным воздухом, легко диффундирует в кровь, где вступает в соединение с гемоглобином
Окись углерода, поступающая в легкие с атмосферным воздухом, легко диффундирует в кровь, где вступает в соединение с гемоглобином, образуя прочный комплекс карбоксигемоглобина. Lilienthal с соавторами (1946) приводит простейшую формулу интенсивности поглощения кровью окиси углерода, согласно которой
% СОН = (рСО * т * МОД) * 0,05, где:
рСО — парциальное давление СО в мм рт. ст.,
т — время экспозиции в минутах
МОД — минутный объем дыхания (в литрах) в условиях окружающей температуры, влажности воздуха и постоянном давлении 760 мм рт. ст.
При выведении зависимости авторы использовали различные газовые смеси при условии вдыхания окиси углерода в сроки от 20 до 66 минут. Парциальное давление окиси углерода изучалось в диапазоне от 0,37 до 2,30 мм рт. ст. При исследованиях на уровне моря зависимость носила линейный характер.
Исследования, выполненные Lilienthal с сотрудниками (1946) в условиях различного парциального давления кислорода в воздухе и при различном барометрической давлении, позволили авторам придти к заключению, что скорость поглощения окиси углерода обратно пропорциональна парциальному давлению кислорода. Общая величина барометрического давления не играет в изученных условиях какой-либо существенной роли.
Как известно, 1 г гемоглобина может связать 1,33-1,34 мл кислорода или окиси углерода, при этом сродство гемоглобина к окиси углерода в 250-300 раз больше, чем к кислороду. Если для полного насыщения гемоглобина кислородом необходимо парциальное давление порядка 90-100 мм рт. ст. то для окиси углерода всего 0,45 мм рт. ст. Все это приводит к тому, что в конкуренции за гемоглобин окись углерода имеет преимущества перед кислородом. Скорость образования карбоксигемоглобина прямо зависит от парциального давления окиси углерода во вдыхаемом воздухе. Однако ввиду большого сродства гемоглобина к окиси углерода даже при сравнительно небольшом ее содержании в воздухе образование карбоксигемоглобина отличается высокой интенсивностью. Быстрому накоплению карбоксигемоглобина в крови способствует также то, что его диссоциация происходит в 3600 раз медленнее, чем диссоциация оксигемоглобина.
Присоединение к железу гемоглобина окиси углерода не сопровождает ся изменением его валентности, но при этом происходит перестройка молекулы гемоглобина, причем изменяется характер связи железа с глобином и порфирином. Предполагается, что связь из ионной переходит в ковалентную, т.е. становится более прочной. В результате, несмотря на то, что железо карбоксигемоглобина, как и гемоглобина, является двухвалентным, карбоксигемогло бин полностью выключается из процесса транспорта кислорода. Возникает кислородное голодание, текущее по типу гемической гипоксии, которое осложняется тем, что в присутствии карбоксигемоглобина диссоциация оксигемоглобина затрудняется. Таким образом, при отравлении окисью углерода не только выключается определенная часть гемоглобина из его нормальной физиологической функции, но и одновременно тормозится отдача кислорода еще достаточно полноценным гемоглобином или его отдельными гемами.
Эта сторона токсического действия окиси углерода (эффект Холдена) была подвергнута широкому экспериментальному изучению. Ряд авторов (Драбрин и др. 1943) высказывают предположение, что в процессе интоксикации в крови образуется комплекс гемоглобина, в котором 3 из 4 атомов железа соединены с окисью углерода и только один — с кислородом. В таком соединении Нb4(СО)3(O) 2 кислород прочно удерживается, что усугубляет состояние кислородного голодания. Л.А. Тиунов и В.В. Кустов (1969) считают более правильной оценку эффекта Холдена с позиций «гем-гем» - взаимодействия. Согласно этому представлению, сродство каждого из 4 гемов гемоглобина к кислороду одинаково, но уже после присоединения первой молекулы кислорода сродство остальных гемов возрастает. Этот процесс находит отражение в образной кривой диссоциации оксигемоглобина. В условиях интоксикации присоединение СО вызывает конформационные изменения молекулы гемоглоби на, что приводит к нарушению этого важного физиологического механизма. Эффект Холдена имеет большое клиническое значение и не может не учитываться при оказании помощи лицам, отравленным окисью углерода.
Стабильность комплекса карбоксигемоглобина определяется целым рядом факторов, из которых наибольшее значение имеет концентрация окиси углерода и кислорода во вдыхаемом воздухе, а также величина парциального давления кислорода и углекислоты крови. Соответственно этому содержание карбоксигемоглобина в крови может быть рассчитано по следующей формуле (цит. по Ф.Н. Мельниковой, 1964):
где Х — содержание карбоксигемоглобина в крови; О2 — содержание кислорода во вдыхаемом воздухе, в %; СО — содержание в последнем окиси углерода в %.
Исходя из конкурентных отношений между окисью углерода и кислородом, некоторые авторы (Douglas et а1. 1912) предложили следующую константу равновесия, которая поучила также название коэффициента отравления:
Из указанного равновесия следует, что количество образующегося в крови карбоксигемоглобина прямо пропорционально парциальному давлению окиси углерода и обратно пропорционально парциальному давлению кислорода.
Из приведенных выше данных становится очевидно, что высокое парциальное давление кислорода во вдыхаемом воздухе и соответственно в крови препятствует образованию и ускоряет диссоциацию комплекса карбоксигемог лобина. Н.Н. Савицкий (1940), ссылаясь на Гендерсона и Хаггарда, отмечает, что при вдыхании кислорода скорость выведения окиси углерода увеличивает ся в 1 1/2 раза. Последнее служит основанием для рекомендации широкого применения кислородной терапии при лечении отравлении окисью углерода. Еще лучшие результаты дает методе оксибаротерапии.
Помимо парциального давления кислорода, судьба карбоксигемоглоби на зависит также от величины парциального давления в крови углекислоты. Как известно, увеличение парциального давления углекислого газа ускоряет процесс диссоциации карбоксигемоглобина, ослабляет прочность связи кислорода с гемоглобином и возбуждает деятельность дыхательного центра, что ведет к более интенсивному выделению из организма окиси углерода. Способность углекислоты повышать диссоциацию карбоксигемоглобина была претворена в виде практических рекомендаций применять карбоген при лечении отравлении окисью углерода. Исходя из этого Декрет (цит. по Л.А. Тиунову и В.В. Кустову, 1969) предложил рассчитывать коэффициент токсичности окиси углерода по следующей формуле:
К = (% СО2 * % СО * 500) / (% О2)
Считается, что если К равно единице или меньше ее, то опасность отравления практически исключена. Таким образом, при отравлении окисью углерода ведущим механизмом является образование карбоксигемоглобина, что приводит к возникнове нию гемической формы гипоксии.
Однако, помимо образования карбоксигемоглобина, окись углерода может вступать во взаимодействие с некоторыми другими ферментными системами, особенно ферментами, содержащими двухвалентное железо (цитохромоксидазная система). На основании результатов обширных эксперименталь ных исследований можно считать, что окись углерода способна нарушать функцию цитохромоксидазной системы парализуя течение обменных реакций в терминальной цепи биологического окисления. Следовательно, для отравления окисью углерода характерно развитие не только гемической, но и гистотоксической формы гипоксии.
Вполне понятно, что развитие тяжелого гипоксического состояния приводит к глубоким нарушениям окислительных процессов, а это в свою очередь находит отражение в ограничении образования макроэргических фосфорных соединений, несущих необходимую для жизнедеятельности организма энергию. Однако нарушения в энергетическом обмене не ограничиваются уменьшением запасов энергетических ресурсов. а распространяются также на процесс использования аккумулированной в макроэргических соединениях энергии. Имеются данные о способности окиси углерода подавлять активность фермента аденозинтрифосфатазы. Это заставляет рассматривать окись углерода в качестве токсического агента, в механизме действия которого нарушение процессов образования и использования энергии в тканях животного организма играет едва ли не ведущую роль. Действительно, при воздействии окиси углерода нарушается доставка кислорода к тканям, угнетается активность цитохромоксидазной системы, имеющей непосредственное отношение к процессам сопряженного окислительного фосфорилирования (второй и третий пункты накопления энергии), и наконец, имеет место ингибирование аденозинт рифосфатазы, обеспечивающей освобождение накопленной энергии. В настоящее время имеется значительный экспериментальный материал о влиянии окиси углерода на самые различные ферменты, что, несомненно, находит отражение в динамике развития отравления. Но какими бы ни были нарушения в сфере других ферментных систем, основная угроза жизнедеятельности организма возникает в результате неполноценности энергетического обмена, обеспечивающего организм необходимой для сохранения жизни энергией.
Дата добавления: 2015-02-05 | Просмотры: 712 | Нарушение авторских прав |