|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Механизм возникновения и развития токсического отека легких
Патогенез токсических поражений органов дыхания представляет собой прежде всего проблему молекулярно-мембранной патологии. Согласно биофизике легкие представляют собой мембранную поверхность толщиной от 0,3 до 2 мкм с общей площадью более 100 м2. Из этой мембранной пленки образованы более 7 млн. альвеол, опутанных густой капиллярной сетью. Стенки легочных артериол, капилляров и венул представляет собой идеальную мембрану, полупроницаемую в норме для газов и непроницаемую для воды. Хотя гидростатическое давление крови НуD способствует движению жидкости в просвет легочных альвеол, в нормальных условиях этого не происходит, так как в ткани межальвеолярных перегородок существует осмотическое давление OsD, которое уравновешивает гидростатическое давление крови.
Согласно термодинамике (A. Kolyk, K. Janacer, 1980) объемный поток жидкости VQ через полупроницаемую мембрану Rппм прямо, пропорциона лен разности гидростатического и осмотического давления в тканях:
VQ=RППМ (НуD - OsD).
В нормальных условиях (жидкость не проходят через мембрану, так как гидростатическое давление крови равно осмотическому давлению легочной ткани: НуD = OsD, поэтому VQ=0. При токсическом отеке легких под влиянием нервно-рефлекторных механизмов происходит возрастание гидростатического давления крови. В легочной ткани происходят биохимические изменения, которые полупроницае мую сосудистую мембрану превращают в проницаемую RПМ. Нейроэндокрин ные факторы существенное влияние оказывают на коллоидно-осмотические свойства легочной ткани. В результате осмотическое давление в межальвео лярных перегородках становится союзником гидростатического давления крови, обеспечивающего поток жидкости в направлении: кровеносное русло ® легочная ткань. Согласно процессам термодинамики токсический отек легких можно описать уравнением: VQ=RППМ (НуD + OsD).
Рассмотрим сущность токсико-рефлекторных, биохимических и эндокринных механизмов, участвующих в возникновении и развитии токсического отека легких.
Выдвинуто множество теорий, развития токсического отека легких. Их можно разбить на три группы: 1) — биохимическую, 2) — нервно-рефлектор ную, 3) — гормональную.
Сторонники биохимической теории объясняли развитие токсического отека наличием соляной кислоты, образующуюся при гидролизе фосгена, связывая развитие отека лёгких, с её прижигающим действием на легочную ткань. Например, работами Чистович, Меркулова и др. /цит. по Лазарис Я. А. и др./ было показано гистологическое повреждение действие фосгена и дифосгена на проницаемость легочной мембраны.
Некоторые авторы придавали решающее значение при отравлении дифосгеном образованию дисфосгенового эфира — холестерина. Но отек развивается также при отравлении ядами удушающего и раздражающего действия, когда этот эфир образоваться не может.
Представители этой теории объясняли развитие токсического отека накоплением в организме мочевины, ацетона, аммиака, увеличением гистамина в крови, при нарушениях клеточного метаболизма.
Многие авторы: Х.М. Баймакова, И.Л. Серебровская /1973, 1974/ и др. находили изменение поверхностно-активных свойств липидной выстилки альвеол (сурфактантных систем), способствующей повышению проницаемости легочной воздушно-кровяной мембраны. Они также определили снижение содержания SH-групп при отеке легких, которые необходимы, по-видимому, для поддержания структуры целостности эндотелиальной и соединительной ткани.
В настоящее время биохимическая теория в свете молекулярной биологии рассматриваются следующим образом. Пары фосгена, пропитывая легочную ткань, образуют комплекс с поверхностно-активным липопротеидным веществом сурфактантом, выстилающим внутреннюю полость легочных альвеол. Этот своеобразный гаптен раздражает рецепторы тучных клеток Эрлиха в легочной ткани, что приводит к активизации фосфадиэстеразы и уменьшению запасов циклического аденозинмонофосфата (цАМФ) в тучных клетках. Клетки Эрлиха начинают испытывать энергетический голод. Они перестают удерживать в себе запасы гистамина, серотонина и других активных веществ. Их освобождение активирует гиалуронидазу легочной ткани, под влиянием которой возникает диссоциация кальциевой соли гиалуроновой кислоты — основного вещества соединительнотканной стенки легочного сосуда. Сосудистая мембрана из полупроницаемой становится проницаемой. В легочную ткань устремляются из крови вещества, богатые энергией. В тучных клетках Эрлиха восстанавливается содержание цАМФ. Энергетический голод устраняется ценой повреждения сосудистой мембраны и развития отека легких.
Авторы нервно-рефлекторной теории /А. Луизада, Г.С. Кан и др./ важное значение придавали сосудистой проницаемости. Они полагали, что в основе токсического отека легких лежит нервно-рефлекторный механизм, афферентный путь которого — чувствительные волокна блуждающего нерва, с центром, находящимся в стволовой части головного мозга: эфферентный путь — симпатический отдел нервной системы. При этом отек легких рассматривался как защитная физиологическая реакция, направленная на смывание раздражающего агента. Токсикологическая лаборатория Казанского медицинского института, внесла существенный вклад в её развитие. В 1942-1944 гг. здесь совместно с В.Д. Белогорским работала известный физиолог А.В. Тонких, написавшая специальную монографию по этому вопросу. Труды В.Д. Белогорского (1932, 1936), посвященные изучению гипоксии при поражении дифосгеном, были первыми в мировой литературе и получили широкую известность.
При воздействии фосгена нервно-рефлекторный механизм патогенеза представляется в следующем виде. Афферентным звеном нейровегетативной дуги являются тройничный нерв и вагус, рецепторные окончания которых проявляют высокую чувствительность к парам фосгена и других веществ данной группы. Это приводит к нарушению рефлекса Геринга: дыхание становится частым и поверхностным. В центре блуждающего нерва и других частях мозгового ствола, возникает застойный очаг возбуждения. Как показала А.В. Тонких (1949), это возбуждение иррадиирует на гипоталамус и вовлекает в процесс высшие центры симпатической регуляции, а также заднюю долю гипофиза. Возбуждение эфферентным путем распространяется на симпатические ветви легких, в результате нарушения трофической функции симпатической нервной системы и местного повреждающего действия фосгена возникает набухание и воспаление легочной мембраны и патологическое повышение проницаемости в сосудистой мембране легких. Таким образом, возникают два основных звена в патогенезе отека легких: 1) повышение проницаемости легочных капилляров и 2) набухание, воспаление межальвеолярных перегородок. Эти два фактора и обуславливают скопление отечной жидкости в легочных альвеолах, т.е. приводят к отеку легких.
Следствием повышенной проницаемости сосудов является сгущение крови, замещение тока крови особенно в малом кругу. Из-за набухания и воспаления межальвеолярных перегородок наступает затруднение диффузии газов, что приводит к гипоксемии и ацидозу. В свою очередь отек легких, который сопровождается увеличением их объема, вызывает смещение органов средостения, затрудняет, деятельность сердца, замедляет ток крови в малом кругу, способствуя застою крови в нем.
Совокупность всех перечисленных факторов приводит к развитию тяжелой гипоксии, глубокому парабиозу и истощению жизненно важных центров, что проявляется в периодической одышке, тяжелом коллапсе и в виде других признаков, из которых складывается картина серой гипоксии.
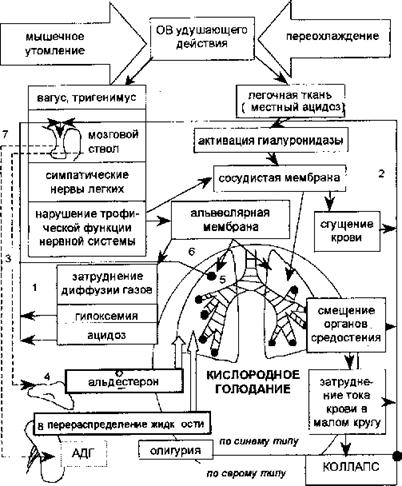
Кроме нервно-рефлекторного механизма важное значение имеют нейроэндокринные рефлексы, среди которых антинатрийурический и антидиуре тический рефлексы занимают особое место. Под влиянием ацидоза и гипоксемии раздражаются хеморецепторы (1), замедление тока крови в малом кругу способствует расширению просвета, вен и раздражению волюменрецепторов (2), реагирующих на изменение объема сосудистого русла. Импульсы с хеморецепторов и волюменрецепторов достигают среднего мозга, ответной реакцией которого является выделение в кровь альдостеронтропного фактора — нейросекрет (3), химическая природа которого еще не расшифрована. В ответ на его появление в крови возбуждается секреция альдостсрона в коре надпочечных желез (4). Минералкортикоид альдостсрон, как известно, способству ет задержанию в организме ионов натрия и усиливает воспалительные реакции. Эти свойства альдостерону легче всего проявить в «месте наименьшего сопротивления», а именно в легких, поврежденных токсическим веществом (5). В результате ионы натрия, задерживаясь в легочной ткани, вызывают нарушение осмотического равновесия. Эта первая фаза нейроэндокринных реакций, которая называется антинатрийурическим рефлексом (1-5).
Вторая фаза нейроэндокринных реакций начинается с возбуждения осморецепторов легких (6). Импульсы, посылаемые ими, достигают гипоталамуса. В ответ на это задняя доля гипофиза начинает продуцировать антидиуретический гормон (7), «противопожарная функция» которого заключается в экстренном перераспределении водных ресурсов организма в целях восстановления осмотического равновесия. Это достигается за счет олигурии и даже анурии (8). В результате приток жидкости к легким еще более усиливается. Такова вторая фаза нейроэндокринных реакций при отеке легких, которая носит название антидиуретического рефлекса (6-8).
Таким образом, можно выделить следующие основные звенья патогенетической цепи при отеке легких 1) нарушение основных нервных процессов в нейровегетативной дуге: легочные ветви вагуса, мозговой ствол, симпатические ветки легких;
2) набухание и воспаление межальвеолярных перегородок вследствие нарушения обмена веществ;
3) повышение сосудистой проницаемости в легких и застой крови малом кругу кровообращения;
4) кислородное голодание по синему и серому типу.
Обилие причин легочного отека, создает определенные трудности в понимании механизмов его развития. Существуют противоречия между стремлениями создать единую теорию патогенеза, объяснениями различных этиологических форм отека, разными патогенетическими факторами или их сочетанием. Поэтому перечисленные выше теории каждая в отдельности, не могут дать объяснения развитию токсического отека легких. Очевидно, что на разных стадиях формирования отека будут принимать участие различные механизмы.
Схема патогенеза токсического отека легких
Дата добавления: 2015-02-05 | Просмотры: 802 | Нарушение авторских прав |