|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Гемодинамическая поддержкаИнфузионная терапия принадлежит к первоначальным мероприятиям поддержания гемодинамики и прежде всего сердечного выброса (категория доказательности В и С). Основными задачами инфузионной терапии у больных с сепсисом являются: восстановление адекватной тканевой перфузии, нормализация клеточного метаболизма, коррекции расстройств гомеостаза, снижение концентрации медиаторов септического каскада и токсических метаболитов. При сепсисе с ПОН и СШ необходимо стремиться к быстрому достижению (первые 6 ч после поступления) целевых значений следующих параметров: ЦВД 8–12 мм рт. ст., АДср>65 мм рт. ст., диурез 0,5 мл/кг/ч, гематокрит более 30%, сатурация крови в верхней полой вене или правом предсердии не менее 70%. Использование данного алгоритма повышает выживаемость при СШ и тяжелом сепсисе. Мониторинг гемодинамики с помощью катетера Swan-Ganz расширяет возможности контроля и оценки эффективности гемодинамической терапии, однако доказательств снижения летальности при его использовании не получено. В силу значительной вариабельности степени повреждения эндотелия и состояния лимфодренажа в легких, диастолической функции желудочков, а также влияния изменений внутригрудного давления однозначно определить величину оптимальной преднагрузки затруднительно, она должна подбираться индивидуально. Объем инфузионной терапии следует поддерживать так, чтобы давление заклинивания в легочных капиллярах не превышало коллоидно-онкотического (КОД) давления плазмы во избежание отека легких и сопровождалось повышением сердечного выброса (категория доказательности С). Следует принимать во внимание параметры, характеризующие газообменную функцию легких, – РаО2 и РаО2/FiO2, динамику рентгенологической картины. Для инфузионной терапии в рамках целенаправленной ИТ сепсиса и СШ практически с одинаковым результатом применяют кристаллоидные и коллоидные инфузионные растворы. Все инфузионные среды имеют как свои достоинства, так и недостатки. Принимая во внимание имеющиеся результаты экспериментальных и клинических исследований, на сегодняшний день нет оснований отдавать предпочтение какой-то из инфузионных сред. Однако следует иметь в виду, что для адекватной коррекции венозного возврата и уровня преднагрузки требуется значительно большие объемы (в 2–4 раза) инфузии кристаллоидов, чем коллоидов, что связано с особенностями распределения растворов между различными секторами. Кроме того, инфузия кристаллоидов более сопряжена с риском отека тканей, а их гемодинамический эффект менее продолжителен, чем коллоидов. В то же время кристаллоиды более дешевы, не влияют на коагуляционный потенциал и не провоцируют анафилактоидных реакций. В этой связи качественный состав инфузионной программы должен определяться особенностями пациента: степенью гиповолемии, фазой синдрома ДВС, наличием периферических отеков и уровнем альбумина крови, тяжестью острого легочного повреждения. Плазмозаменители (декстраны, желатиноль, гидроксиэтилкрахмалы) показаны при выраженном дефиците ОЦК. Гидроксиэтилкрахмалы (ГЭК) с молекулярной массой 200/0,5 и 130/0,4 имеют потенциальное преимущество перед декстранами в силу меньшего риска утечки через мембрану и отсутствия клинически значимого воздействия на гемостаз. Применение альбумина при критических состояниях может способствовать повышению летальности (категория доказательности В). Увеличение КОД при инфузии альбумина носит транзиторный характер, а затем в условиях синдрома "капиллярной протечки" происходит дальнейшая экстравазация альбумина (rebound syndrome). Переливание альбумина, возможно, будет полезным только при снижении уровня альбумина менее 20 г/л и отсутствии признаков его "утечки" в интерстиций. Применение криоплазмы показано при коагулопатии потребления и снижении коагуляционного потенциала крови. По мнению большинства экспертов, минимальная концентрация гемоглобина для больных с тяжелым сепсисом должна быть в пределах 90–100 г/л. Более широкое использование донорской эритроцитной массы необходимо ограничивать ввиду высокого риска развития различных осложнений (острые повреждения легких – ОПЛ, анафилактические реакции и пр.). Низкое перфузионное давление требует немедленного включения препаратов, повышающих сосудистый тонус, и/или инотропную функцию сердца (табл.7). Допамин и/или норадреналин являются препаратами первоочередного выбора коррекции гипотензии у больных с СШ. Допамин повышает АД прежде всего за счет увеличения сердечного выброса с минимальным действием на системное сосудистое сопротивление (в дозах до 10 мкг/кг/мин). В дозе выше 10 мкг/кг/мин преобладает a-адренергический эффект допамина, что приводит к артериальной вазоконстрикции, а в дозе менее 5 мкг/кг/мин допамин стимулирует дофаминергические рецепторы в почечном, мезентериальном иг/мин допамин стимулирует дофаминергические рецепторы в почечном, мезентериальном и коронарном сосудистом русле, что приводит к вазодилатации, увеличению гломерулярной фильтрации и экскреции натрия. Норадреналин повышает АДср и увеличивает гломерулярную фильтрацию. Оптимизация системной гемодинамики под действием норадреналина ведет к улучшению функции почек без применения низких доз допамина. Работы последних лет показали, что применение норадреналина в сравнении с комбинацией допамина в высоких дозировках ± норадреналин ведет к статистически значимому снижению летальности. Адреналин – адренергический препарат с наиболее выраженными побочными гемодинамическими эффектами. Адреналин обладает дозозависимым действием на ЧСС, АДср, сердечный выброс, работу левого желудочка, доставку и потребление кислорода. Однако это действие адреналина сопровождается тахиаритмиями, ухудшением спланхнического кровотока, гиперлактатемией. Поэтому применение адреналина должно быть ограничено случаями полной рефрактерности к другим катехоламинам. Добутамин должен рассматривается как препарат выбора для увеличения сердечного выброса и доставки и потребления кислорода при нормальном или повышенном уровне преднагрузки. Благодаря преимущественному действию на b1-рецепторы добутамин в большей степени, чем допамин, способствует повышению данных показателей.
Рис. 3. Алгоритм выбора адренергических средств. В экспериментальных исследованиях доказано, что катехоламины помимо поддержки кровообращения могут вмешиваться в течение системного воспаления, влияя на синтез ключевых медиаторов, обладающих дистантным эффектом. Под действием адреналина, допамина, норадреналина и добутамина снижались синтез и секреция TNF-a активированными макрофагами (рис. 3).
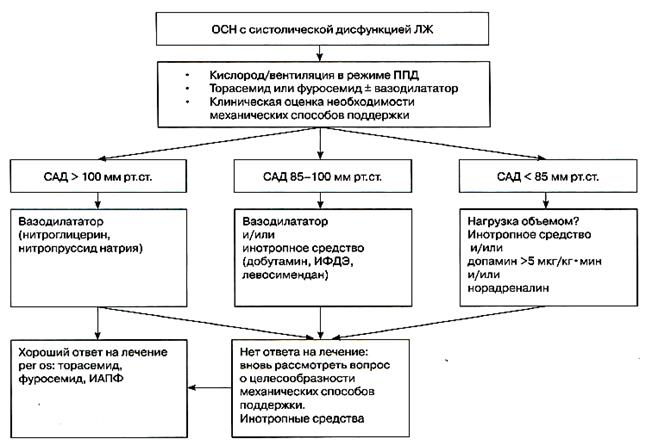
Рис. 4. Алгоритм инотропной и вазопрессорной поддержки. В журнале «Critical care medicine» (2008. Vol. 36, No 1. P. 296-327) опубликованы международные клинические рекомендациипо ведению тяжёлого сепсиса и септического шока «Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock: 2008» (Dellinger R.P., Lev M.M., Carlet J.M. et al.), которые дополняют и уточняют рекомендации 2001 и 2004 г. на основании анализа результатов многочисленных завершённых ипроводимых многоцентровых исследований. Вазопрессоры · Поддерживать САД > 65 мм рт. ст. · Норадреналин и допамин. вводимые в центральную вену, являются исходными вазопрессорами выбора. · При септическом шоке не следует вводить в качестве начальных вазопрессоров адреналин, фенилэфрин (мезатон) или вазопрессин. · Вазопрессин 0,03 ед/мин можно впоследствии добавить к норадреналину в ожидании действия, эквивалентного эффекту одного норадреналина · При септическом шоке как первое средство выбора использовать адреналин, когда артериальное давление слабо отвечает на введение норадреналина или допамина. · Не использовать низкие дозы допамина для почечной протекции. · Если больной нуждается в вазопрессорах, как можно скорее установите для мониторирования артериальный катетер. Таблица 7
Дата добавления: 2015-11-26 | Просмотры: 837 | Нарушение авторских прав |