|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Нейрогормоны гипоталамо-гипофизарной системыГипоталамус Гипофиз
Либерины
ламусе образуются нейропептиды (энкефалины и эндорфины), обладающие болеутоляющим, морфиноподобным действием и играющие важную роль в регуляции вегетативных функций и поведения животных. Таким образом, гипоталамо-гипофизарная система включает в себя три механизма связи: гипоталамус — аденогипофиз;
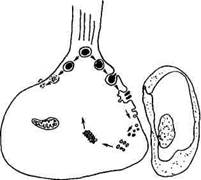
гипоталамус — нейрогипофиз; нейрорегуляторные пептиды. Важно подчеркнуть, что и гипоталамус, и вся гипоталамо-гипофизарная система являются отделами ЦНС и находятся в тесной функциональной взаимосвязи с другими образованиями головного мозга, прежде всего с различными отделами коры больших полушарий (сомато-сенсорной, ассоциативной, слуховой и зрительной корой). ГИПОФИЗ Гипофиз, или нижний мозговой придаток, представляет собой железу внутренней секреции, продуцирующую ряд гормонов, которые, в свою очередь, оказывают регулирующее действие на периферические эндокринные железы и некоторые процессы обмена веществ. Гипофиз лежит в ямке турецкого седла задней клиновидной кости черепа и связан с подбугровой областью (гипоталамусом) с помощью гипофизарной ножки. Анатомически состоит из трех долей: передней, наиболее крупной (аденогипофиз); узкой средней (промежуточная); задней (нейрогипофиз) (рис. 12.6). В эмбриогенезе аденогипофиз возникает путем дорсального выпячивания слизистой оболочки ротовой полости (называемой карманом Ратке) и по мере развития утрачивает с ней связь, приближаясь к задней доле. Нейрогипофиз развивается как выпячивание дна III желудочка мозга, т. е. из одного источника с гипоталамусом. Гипоталамус связан с нейрогипофизом гипоталамогипофи-зарным трактом, который в основном включает отростки клеток нейросекреторных ядер переднего гипоталамуса — супраоптичес-кого и паравентрикулярного. Так называемая воротная или портальная сосудистая система состоит из берущего начало от верхней гипофизарной артерии первичного капиллярного сплетения, дренирующего срединное возвышение и переходящего в воротные вены, поступающие в переднюю долю, где они распадаются на мощную сеть вторичного капиллярного сплетения. Благодаря многочисленным контактам терминалей нейросекреторных волокон различных гипоталамических ядер с сосудами первичной капиллярной сети становится возможным осуществление нейрогумо-ральных влияний на трофные функции аденогипофиза. В гипота-ламо-гипофизарной системе кровь всегда течет по направлению
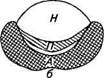
Рис. 12.6. Схема строения гипофиза: а — сагиттальный и б— фронтальный срезы; А — аденогипофиз; П— промежуточная доля; Н— нейрогипофиз от гипоталамуса к гипофизу. Из синусоидов передней доли кровь вытекает через боковые гипофизарные вены в кавернозные синусы. Промежуточная доля гипофиза сравнительно бедна кровеносными сосудами, а кровоснабжение задней доли гипофиза не связано с кровоснабжением передней доли, она получает кровь от нижних гипофизарных артерий и отдает ее через многочисленные вены в кавернозные синусы. Симпатические нервные волокна к гипофизу подходят из верхнего шейного ганглия, сопровождая кровеносные сосуды. Остальные нервные волокна в гипофиз идут из гипоталамуса в составе гипоталамо-гипофизарного тракта, причем большинство его волокон оканчивается в задней доле, но часть проникает в промежуточную и переднюю доли. Для каждой доли гипофиза характерна своя структурная организация, обеспечивающая выполнение специфической функции в системе координации эндокринных регуляторных влияний. Аденогипофиз. По своей цитоархитектонике представляет собой сложную железу, образованную тяжами эпителиальных клеток (аденоцитов), разделенных развитой сетью синусоидных капилляров. По данным светомикроскопического, цитохимического и электронно-микроскопического исследований определены структурные и функциональные особенности различных аденоцитов. Выявлено шесть разновидностей клеток, ответственных за синтез определенного тропного гормона (рис. 12.7).
Соматотропоциты — ацидофильные клетки, продуци
Функциональная активность соматотропоцитов проявляется в числе секреторных гранул. При многократном введении гормона роста и происходящем по принципу отрицательной обратной связи подавлении деятельности железы число секреторных гранул, их размеры и размеры самой клетки заметно уменьшаются, а шероховатый эндоплазматический ретикулум и комплекс Гольджи (структурные компоненты клетки, ответственные за синтез и оформление секреторного продукта) редуцируются, т. е. подавляется синтез и выведение СТГ в кровеносное русло. Напротив, при введении гипоталамических экстрактов, содержащих фактор, стимулирующий отдачу СТГ из гипофиза, в соматотропоцитах наблюдается усиленное выведение секреторных гранул в перикапил-лярное пространство, а также гипертрофия шероховатого эндоп-лазматического ретикулума и комплекса Гольджи. Несмотря на интенсивное выведение секреторных гранул, их число в клетке не отличается от нормы, что говорит о стимуляции не только выведения, но и синтеза СТГ. Деятельность соматотропоцитов находится под контролем гипоталамических структур. При развитии ожирения, вызванного электролитическим разрушением вентромедиальных ядер гипоталамуса, обнаруживается заметное накопление секреторных гранул и появление лизосом, способных разрушать неиспользованные секреторные гранулы. При разрушении дорсомедиальных ядер в соматотропоцитах наблюдается уменьшение числа секреторных гранул. Таким образом, торможение выведения секреторных гранул обусловлено подавлением секреции соматолиберина (GRF) после разрушения вентромедиальных ядер, а усиление выведения секреторного продукта из соматотропоцитов при разрушении дорсомедиальных ядер связано со снижением активности фактора, тормозящего выведение гормона роста (соматостатина, GIF). Лактотропоциты — второй тип ацидофильных клеток, продуцирующих лактотропный гормон (ЛТГ), или пролактин, которые отличаются от соматотропоцитов более крупными размерами и неправильной формой. В цитоплазме лактотропоцитов содержатся немногочисленные секреторные гранулы диаметром 600...800 нм, отличающиеся высокой электронной плотностью и удлиненной формой. Лактотропоциты редко встречаются у половозрелых самцов и самок до достижения ими половой зрелости. Число этих клеток значительно возрастает в аденогипофизе к концу беременности и в период лактации. В лактационный период лактотропоциты содержат высокоразвитый шероховатый эндоплазматический ретикулум, множество связанных рибосом и расширенный комплекс Гольджи с многочисленными незрелыми секреторными гранулами. Зрелые гранулы лежат по периферии клеток вблизи плазматической мембраны. После прекращения лактации число активных лактотропоцитов снижаете?, а число структурных компонентов клетки, ответственных за осуществление секреции, существенно уменьшается. Резкое прерывание лактационного процесса — отъем сосунков через 12...18 ч —приводит к накоплению в цитоплазме зрелых секреторных гранул, а через 24 ч в цитоплазме появляются лизо-сомы, которые поглощают и переваривают «ненужные» продукты секреции. Если в этот период самкам возвратить потомство, то уже через 5... 15 мин выведение секреторных гранул усиливается и их число в цитоплазме значительно уменьшается. В соответствии с этими ультраструктурными перестройками изменяется и уровень пролактина в плазме крови: прекращение кормления снижает уровень пролактина, а его возобновление повышает. Тиреотропоциты— ацидофильные клетки, продуцирующие тиреотропный гормон (ТТГ) — тиреотропин, который стимулирует функции щитовидной железы, способствует накоплению в ней йода и образованию гормонов (трийодтиронина и тироксина). ТТГ усиливает распад тиреоглобулина и способствует переходу активной формы гормона в кровь. Тиреотропоциты — это полигональные или отростчатые базофильные клетки, располагающиеся преимущественно в центральной зоне аденогипофиза, их число сравнительно невелико и составляет 1,8...2,9% общего числа секреторных клеток этой доли. Цитоплазма тиреотропоцитов содержит мелкие секреторные гранулы диаметром 80...150нм; наиболее крупные секреторные гранулы ТТГ обнаружены в аденогипофизе крупного рогатого скота (300...400 нм). Структурные компоненты, участвующие в секреторном процессе в тиреотропоцитах, развиты сравнительно мало. Шероховатый эндоплазматический ретикулум представлен небольшими пузырьками и короткими канальцами, распределенными равномерно по всему пространству цитоплазмы. Комплекс Гольджи занимает околоядерное положение и представлен небольшими вакуолями и микропузырьками. Наиболее значительные ультраструктурные изменения наблюдаются в тиреотропоцитах при выключении функции щитовидной железы (оперативным путем или введением тиреостатических препаратов), т. е. при дефиците ти-реоидных гормонов. В первые дни после удаления щитовидной железы число тиреотропоцитов в аденогипофизе быстро увеличивается, а при углублении гипотиреоидного состояния эти клетки трансформируются в клетки тиреоидэктомии. В расширенных вакуолях этих клеток отмечается накопление крупных электронноплотных гранул, особого развития достигает комплекс Гольджи, и по мере увеличения срока после операции он прогрессивно расширяется. В последующем в цитоплазме появляются лизосомы, контактирующие со структурами комплекса Гольджи и элиминирующие излишние секреторные гранулы. Тиреоидные гормоны, введенные нормальным или тиреоидэктомированным животным, тормозят выделение ри-лизинг-факторов тиреотропного гормона (TRF), в результате чего в
32 — 3389
Кортикотропоциты ответственны за синтез корти-котропина, или адренокортикотропного гормона (АКТГ), который вызывает рост пучковой и сетчатой зон коры надпочечников и стимулирует глюкокортикоидную функцию. По данным иммуноцито-химии с продукцией АКТГ связывают хромофобные (не воспринимающие красители) аденоциты, имеющие неправильную или звездчатую форму. В цитоплазме кортикотропоцитов располагаются немногочисленные секреторные гранулы диаметром 200...260 нм, локализованные вдоль плазматических мембран. Усиление адрено-кортикотропной функции аденогипофиза морфологически выражается в глубокой дегрануляции кортикотропоцитов и гипертрофии шероховатого эндоплазматического ретикулума и комплекса Гольджи, что наблюдается при адреналэктомии или введении препаратов, ингибирующих синтез кортикостероидов. Гонадотропоциты. В гипофизе животных вырабатывается два гонадотропных гормона — фолликулостимулирующий (ФСГ) и лютеинизирующий (ЛГ), которые дополняют друг друга в своем физиологическом действии на половые железы. ФСГ, или фоллитропин, у самок регулирует развитие и созревание фолликулов в яичниках, у самцов — сперматогенез. ЛГ, или лютропин, у самок при совместном действии с ФСГ обеспечивает овуляцию и образование желтого тела в яичниках, у самцов стимулирует развитие интерстициальной ткани в семенниках и выработку мужского полового гормона тестостерона. ФСГ-гонадотропоциты — это крупные округлые базофильные клетки, расположенные вблизи капилляров по периферии аденогипофиза. Отличительной чертой ФСГ-гонадотропоцитов служит наличие в их цитоплазме многочисленных секреторных гранул диаметром 200...300нм, которые обычно расположены равномерно во всей цитоплазме клеток. Гранулы окружены отчетливо выраженной мембраной, которая либо плотно прилежит к ее содержимому, либо отделена от него узким светлым ободком. Часто на месте распада секреторных гранул непосредственно в цитоплазме клеток остаются мелкогранулярные остатки средней электронной плотности. Эндоплазматический ретикулум в ФСГ-гонадотропоцитах представлен небольшими вакуолями или уплощенными канальцами, расположенными обычно по периферии клеток. Степень развития эндоплазматического ретикулума значительно варьирует в зависимости от функционального состояния клетки. Комплекс Гольджи особенно хорошо развит и имеет кольцевидную форму, причем внутренняя зона кольца образована уплощенными ламеллами, а на- ружная — мелкими и крупными вакуолями. Внутри кольца находятся многочисленные микропузырьки (гладкие и окаймленные) и секреторные гранулы на различных стадиях созревания. Лютеинизирующие гонадотропоциты (ЛГ-гонадотропоциты) относятся к группе базофильных клеток, но при этом способны проявлять некоторую ацидофилию, что позволяет отличать их от ФСГ-гонадотропоцитов, окрашивающихся только основными красителями. ЛГ-гонадотропоциты располагаются вблизи доли гипофиза, а также в центре железы, причем эти клетки отличаются от ФСГ-гонадотропоцитов удлиненной или полигональной формой и секреторными гранулами, диаметр которых достигает 250 нм. В отличие от ФСГ-гонадотропоцитов в цитоплазме ЛГ-гонадотро-поцитов размер секреторных гранул не варьирует и отсутствуют набухающие гранулы низкой электронной плотности. Эндоплазматический ретикулум развит слабо и представлен тонкими канальцами, несущими на своей поверхности рибосомы. Комплекс Гольджи компактный. Если у самцов ФСГ-гонадотропоциты обычно содержат большое количество секреторных гранул, то у самок наличие секреторного продукта в цитоплазме зависит от стадии эстрального цикла. В диэструсе клетки содержат небольшое количество секреторных гранул, в начале проэструса размеры клеток увеличиваются и они заполняются гранулами, при эструсе происходит интенсивная дегрануляция клеток, продолжающаяся в мет-эструсе. В диэструсе вновь уменьшаются размеры клеток и отмечается незначительное содержание секреторных гранул. ЛГ-гонадотропоциты редко обнаруживают в аденогипофизе самцов, а у самок эти клетки представлены более значительно и содержание секреторного продукта соответствует фазам эстрального цикла. В диэструсе содержание гранул секрета незначительно, в проэструсе отмечается возрастание секреторной активности, которая снижается в стадии эструс. В метэструсе гранулы вновь появляются, но в диэструсе их количество снова уменьшается. В условиях постоянного эструса, достигаемого введением эстрогенов, секреция ФСГ остается неизменной, в то время как секреция ЛГ существенно подавляется. Секреция ФСГ подавляется при постоянном диэструсе, ФСГ-гонадотропоциты содержат редкие секреторные гранулы, в то время как ЛГ-гонадотропоциты выглядят активированными. У кастрированных животных в гонадотропных клетках гипофиза происходят наиболее глубокие ультраструктурные изменения: в ФСГ-гонадотропоцитах отмечается расширение вакуолей эндоплазматического ретикулума и исчезновение крупных секреторных гранул, далее следует интенсивная вакуолизация, гипертрофия комплекса Гольджи и прогрессивная дегрануляция клеток. В дальнейшем расширенные полости эндоплазматического ретикулума сливаются, заполняются коллоидоподобным веществом, в узком ободке цитоплазмы обнаруживаются лизосомоподобные тельца — клетки приобретают вид, характерный для клеток кастрации. ЛГ-гонадотропоциты реагируют на кастрацию значительно слабее: число секреторных гранул несколько увеличивается вплоть до 14 сут после операции и лишь затем постепенно уменьшается. Липотропоциты продуцируют недавно обнаруженный гормон гипофиза — липотропин. Известны две формы этого гормона: альфа- и бета-липотропины, обладающие мощным жиро-мобилизующим действием. В гипоталамусе и гипофизе липотро-
32* /
Разработаны тонкие приемы хирургического удаления гипофиза у животных, которые после гипофизэктомии могут жить довольно долго. Не являясь жизненно важным органом, гипофиз все же оказывает существенное влияние на состояние организма, особенно молодых животных. После удаления гипофиза 2-месячные щенки очень отстают в росте, крайне вялы и малоподвижны, основной обмен у них понижен на 20...50 %, а температура тела ниже нормальной на L.,1,5 °C; наблюдается ожирение, половые железы не развиваются, а половые инстинкты не проявляются; размеры щитовидной железы и коры надпочечников остаются значительно меньше обычных, а тимус не подвергается инволюции. У взрослых животных удаление гипофиза приводит к понижению уровня энергетического обмена, изменению обмена белков, жиров и углеводов; размеры щитовидной железы, коры надпочечников и половых желез уменьшаются, а в яичниках прекращается созревание фолликулов, овуляция и образование желтых тел. Трансплантация ткани гипофиза или введение ее экстрактов предотвращают развитие дегенеративных процессов, обычно наступающих у животных при гипофизэктомии. Длительное введение экстрактов вещества гипофиза интактным молодым животным вызывает у них чрезмерный рост, у животных более старшего возраста проявляется акромегалия (усиленный рост трубчатых костей) и появление определенных опухолей. Средняя (промежуточная) доля — узкая пластинка многослойного эпителия, отделенная от передней доли гипофизарной щелью, а от нейрогипофиза прослойкой соединительной ткани, содержащей кровеносные сосуды и базальную мембрану. Промежуточная доля гипофиза образует меланоцитстимулирующий гормон (МСГ), называемый также интермедином или меланотропином. Известны две формы: альфа- и бета-МСГ, представляющие собой полипептиды, которые в организме обеспечивают пигментный обмен кожи, волос, радужной и сетчатой оболочек глаза. Мелано-трофный гормон участвует также в процессах адаптации зрительного анализатора. Со стороны гипофизарной щели промежуточная доля гипофиза покрыта слоем уплощенных маргинальных клеток. Лю-менальная (обращенная в просвет гипофизарной щели) плазматическая мембрана содержит короткие микроворсинки и реснички, а соседние маргинальные клетки скреплены соединительными комплексами. За слоем маргинальных клеток находится паренхима промежуточной доли, образованная несколькими рядами железистых клеток; преобладают клетки, вырабатывающие МСГ. Меланотропоциты имеют полигональную форму и соединяются между собой десмосомами. Отличительной характеристикой меланотропоцитов служит наличие в их цитоплазме большого числа секреторных гранул диаметром 200...500 нм. Второй разновидностью железистых клеток промежуточной доли гипофиза являются звездчатые клетки — это редко встречающиеся небольшие клетки, локализованные между крупными мелано-тропоцитами и простирающие между ними длинные цито-плазматические отростки. Отростки этих клеток соединяются между собой посредством десмосом. Несколько объединившихся звездчатых клеток способны формировать псевдофолликул, полость которого заполняется коллоидным содержимым. Объединенные между собой клетки образуют мощные соединительные комплексы, а на поверхности клеток, обращенной в просвет фолликула, сформированы микроворсинки и реснички. В паренхиме промежуточной доли гипофиза присутствуют также клетки, сходные по ультраструктурной организации с кортикотропоцитами аденогипофиза, но они содержат меньшие по размерам гранулы (менее 200 нм). Эти клетки вблизи от нейрогипофиза образуют значительные скопления в ростральной части, где промежуточная доля переходит в аденогипофиз. При электронно-микроскопическом исследовании в промежуточной доле выявлены нервные волокна и их терминали, образующие синаптоидные контакты с железистыми клетками. Описано три вида окончаний: холинерги-ческие, адренергические и пептидергические. Наиболее часто такие контакты присутствуют на поверхности меланотропоцитов и кортикотропоцитоподобных клеток. Функциональная активность клеток промежуточной доли гипофиза в значительной степени зависит от уровня в крови гормонов коры надпочечника. После адреналэктомии ширина этой доли заметно увеличивается за счет гипертрофии железистых клеток. В ме-ланоцитах происходит глубокая дегрануляция, гипертрофия комплекса Гольджи и эндоплазматического ретикулума. При введении животным кортикостероидных гормонов ширина промежуточной доли, напротив, уменьшается и клетки становятся более компактными. Существует достаточно много оснований к тому, чтобы считать возможным выделение АКТГ и МСГ железистыми клетками промежуточной доли и что это связано с последовательностью синтеза гормонов: вначале синтезируется АКТГ, являющийся прогор-
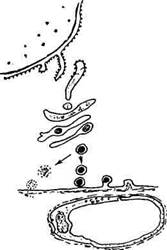
моном для альфа- МСГ. Функции МСГ у млекопитающих не ограничиваются только процессами меланогенеза. Наряду с другими гормонами физиологически активные вещества промежуточной доли способны принимать участие в реакциях адаптации организма к нейрогенному и осмотическому стрессу. Нейрогипофиз — задняя доля гипофиза. Самостоятельная железа внутренней секреции. Нейрогемальный орган, в котором накапливаются и из которого выводятся в кровеносное русло нейрогор-моны — вазопрессин и окситоцж, продуцируемые в крупноклеточных ядрах гипоталамуса. Нейросекреторные клетки супраоптичес-кого и паравентрикулярного ядер гипоталамуса наряду с общими чертами строения типичных нейронов обладают и некоторыми характерными особенностями. Диаметр аксона у места отхождения от тела клетки очень велик, что, очевидно, связано с интенсивным аксональным транспортом нейросекрета. Основными структурными компонентами нейрогипофиза служат нейросекреторные аксоны, их терминали, заканчивающиеся на капиллярах, и особые глиальные клетки — питуициты. Нейросекреторные волокна диаметром от 400 до 600 нм идут обычно параллельно друг другу и собраны в небольшие группы. Расширения и терминали волокон содержат нейросекреторные гранулы (150...200 нм), микротрубочки и нейропротофиламенты. Окончания нейросекретор-ных волокон граничат с перикапиллярным пространством, образуя аксоновазальные контакты. Паренхима нейрогипофиза пронизана многочисленными капиллярами, эндотелиальные клетки которых сильно уплощены и содержат большое количество фе-нестр диаметром около 500 нм, перекрытых тонкими диафрагмами. По размерам и ультраструктуре питуицитов эти клетки разделяются на несколько типов по аналогии с глиальными клетками центральной нервной системы: различают астро-, олиго- и микропитуициты. Астропитуициты — наиболее крупные клетки, имеющие длинные цитоплазматические отростки, многие из которых заканчиваются вблизи перикапиллярного пространства и подстилают на некотором протяжении базальную мембрану капилляров. Олигопитуициты — наиболее часто встречающиеся клетки, в отличие от астропитуицитов имеют меньшее количество отростков, в них более развит шероховатый эндоплазматический ре-тикулум. Характерная их особенность — наличие в цитоплазме многочисленных липидных капель. Микропитуициты встречаются относительно редко, имеют небольшие размеры и очень плотное ядро неправильной формы, но отростков у них немного или они вовсе отсутствуют. Цитоплазматические отростки нескольких питуицитов могут соединяться друг с другом с помощью десмосом, формируя своеобразную сеть, в петлях которой находятся группы нейросекреторных волокон и их варикозные расширения (тельца Геринга). Нейрогормоны задней доли гипофиза непосредственно участвуют в регуляции водно-солевого обмена, и любые сдвиги водно-солевого равновесия отражаются в той или иной степени на ультраструктуре органа. В условиях солевой нагрузки быстро уменьшается число нейросекреторных гранул, появляются остаточные гранулы и множество микропузырьков. Аналогичные признаки активации выведения нейросекрета обнаруживаются у животных с наследственным и экспериментальным (аллоксановым) диабетом и после адреналэктомии. В этих случаях в большинстве нейросекреторных волокон отсутствуют нейросекреторные гранулы, и они заполнены большим количеством микропузырьков. Угнетение функциональной активности гипоталамо-нейрогипофизар-ной системы и блокирование выведения нейрогормонов в кровь наступают при гипергидратации или введении альдостерона. При этом в нейрогипофизе отмечается массивное накопление нейросекреторных гранул в волокнах, их расширениях и крупных тельцах Геринга, а также уменьшение числа нейротрубочек и микропузырьков. Излишек накопленных нейросекреторных гранул может удаляться с помощью лизосомального аппарата. Существуют убедительные доказательства выведения содержимого нейросекреторных гранул из терминален нейросекреторных аксонов путем экзоцитоза. Мембрана нейросекреторной гранулы сливается с мембраной нейросекреторного окончания, на месте слияния образуется отверстие, через которое содержимое гранулы переходит в перикапиллярное пространство. В результате интенсивного включения мембраны гранул в состав плазматической мембраны нейросекреторного окончания может накопиться излишек мембранного материала, который удаляется за счет специального механизма образования микропузырьков в результате эндоцитоза плазматической мембраны нейросекреторных окончаний. Микропузырьки отходят от аксолеммы и формируют скопления правильной гексагональной формы (рис. 12.8). В условиях, когда выделение нейросекреторных гранул не интенсифицируется, ней-росекрет выделяется в виде молекулярных комплексов через неповрежденную мембрану нейросекреторной гранулы и плазматическую мембрану нервного окончания. При резком увеличении выведения нейрогормонов преобладающим становится механизм экзоцитоза. В этом случае активируется деятельность нейротрубочек и нейропротофиламентов, которые обеспечивают перемещение нейросекрета и облегчают контакт гранул с аксолеммой.
Продукты секреторной деятельности паравентрикулярного и супраоптического ядер гипоталамуса, выделяющиеся в кровь из задней доли гипофиза, представляют собой октапептиды циклической природы: окситоцин и вазопрессин, или антидиуретический гормон (АДГ). Окситоцин вы-
зывает сокращения гладкой мускулатуры матки и миоэпителия молочной железы. У самок во время родов окситоцин вызывает и стимулирует родовые схватки и изгнание плода. Степень чувствительности матки к окситоцину зависит от вида животного и его физиологического состояния. Эстрогены (женские половые гормоны) повышают ответную реакцию матки, особенно высока она в середине полового цикла в период овуляции, соответствующий фазе течки. Выделение окситоцина в кровь во время спаривания увеличивает частоту и амплитуду сокращений матки, что обеспечивает перемещение спермы по половым путям в яйцеводы. После овуляции начинает функционировать желтое тело, продуцируется прогестерон и чувствительность матки к окситоцину существенно снижается. Крайне низка ответная реакция матки на окситоцин в начальный период беременности, но в дальнейшем чувствительность повышается, достигая максимума непосредственно перед родами. Вызванное окситоцином сокращение миоэпителия способствует удалению молока из полости альвеол молочной железы, повышает цистернальное и внутрипротоковое давление, активируя молокоотдачу. У самцов окситоцин, очевидно, увеличивает сокращение спермопроводящих путей, обеспечивая процесс эякуляции. В крови окситоцин быстро разрушается специфическим ферментом окситоциназой. Активность этого фермента достаточно высока у беременных самок и во время родов, но резко снижается в первые дни после родов. АДГ ответствен за стимуляцию реабсорбции воды из первичной мочи в дистальном отделе почечных канальцев, а также влияет на минеральный обмен, тормозя реабсорбцию калия, натрия и хлоридов. Вместе с этим АДГ вызывает сокращение артериол и капилляров, действуя непосредственно на гладкомышечные клетки, что ведет к общему повышению артериального давления. Следует, однако, заметить, что для повышения кровяного давления необходимы очень большие дозы гормона, значительно превышающие дозы, оказывающие антидиуретический эффект. Действие вазопрессина на чувствительные ткани достаточно кратковременно: через 1...3 мин активность введенного гормона снижается вдвое за счет разрушения в печени и почках, а 8... 10 % его выделяется с мочой. Интенсивно развивающийся раздел физиологии, изучающий взаимодействие гормонов и других биологически активных веществ с рецепторами, располагающимися в ЦНС, представляет гипоталамо-гипофизарную систему в совершенно новом аспекте. Пептидные гормоны образуют качественно новый класс эндогенных регуляторов функций нервной системы и организма в целом. Некоторые из них (например, вазопрессин, окситоцин, кортико-тропин, тиролиберин) были известны и ранее, но в качестве гормонально-активных субстанций с определенными, узкоспецифичными функциями. Новизна этого класса веществ обусловлена происхождением ряда соединений из одного предшественника — пропиомеланокортина, из которого образуются пептиды, действующие подобно морфину и способные воздействовать на многие функции органов и систем организма. Внимание, восприятие боли, пищевое и половое поведение, обеспечение гомеостаза при стрессовых воздействиях, адаптации организма к экстремальным условиям — это все проявления негормональных функций за счет осуществления связи между нейронами, передача межнейронной информации, модуляция функционального состояния нейронов. Клетки, продуцирующие пептиды, и клетки, чувствительные к ним, образуют мощную гипоталамическую пептидергическую сеть, охватывающую головной и спинной мозг. Влияние эндогенных пептидов на эндокринную систему позволяет им интегрировать множество поведенческих реакций, что говорит о тесной функциональной взаимосвязи между медиаторными и эндокринными системами. Так, вазопрессин и его синтетические аналоги влияют на закрепление условных рефлексов, окситоцин участвует в оптимизации полового поведения, а меланостатин и тиролиберин обладают антидепрессивными свойствами. Общность определенных участков молекулы АКТГ с эндорфи-нами и бета-липотропином, обусловленная происхождением из одного предшественника, объясняет воздействие кортикотропина на многие функции организма: подавление агрессивности, благотворное влияние в стрессовых ситуациях, оказание транквилизирующего эффекта. Эндорфины обладают выраженной опиоидной (мор-финоподобной) активностью, и их применение весьма перспективно при необходимости достижения анальгетического эффекта. Использование таких веществ для фармакологической коррекции патологических состояний организма возможно, так как выявлены терапевтические свойства пептидов как естественных регуляторов физиологических и биохимических процессов. Весьма перспективно и то, что эти вещества эффективны в очень низких концентрациях, не накапливаются в организме и нетоксичны. Дата добавления: 2015-12-15 | Просмотры: 960 | Нарушение авторских прав |
 лы имеют сферическую форму и равномерную высокую электронную плотность.
лы имеют сферическую форму и равномерную высокую электронную плотность. аденогипофизе повышается содержание ТТГ. Дополнительное введение таким животным TRF стимулирует усиление интенсивности выведения секреторных гранул из клеток. При многократном введении TRF количество тиреотропоцитов в аденогипофизе увеличивается, а в клетках наличествуют морфологические признаки интенсификации секреторного процесса.
аденогипофизе повышается содержание ТТГ. Дополнительное введение таким животным TRF стимулирует усиление интенсивности выведения секреторных гранул из клеток. При многократном введении TRF количество тиреотропоцитов в аденогипофизе увеличивается, а в клетках наличествуют морфологические признаки интенсификации секреторного процесса. пины служат предшественниками энкефалинов и эндорфинов, обладающих морфиноподобным действием. Иммуноцитохимичес-кими методами выявлено распределение липотропоцитов: либо групповое, либо в стенке фолликулоподобных структур адено-гипофиза. Ультраструктурная организация этих клеток отличается высокой степенью развития структурных компонентов клеток, осуществляющих секреторный процесс: плотный цитоплазмати-ческий матрикс, обилие органелл и секреторных гранул диаметром 250...500 нм. Методами иммуноцитохимии выявляются и другие более мелкие и менее дифференцированные клетки, которые считают структурами, находящимися на более ранних этапах дифференцировки.
пины служат предшественниками энкефалинов и эндорфинов, обладающих морфиноподобным действием. Иммуноцитохимичес-кими методами выявлено распределение липотропоцитов: либо групповое, либо в стенке фолликулоподобных структур адено-гипофиза. Ультраструктурная организация этих клеток отличается высокой степенью развития структурных компонентов клеток, осуществляющих секреторный процесс: плотный цитоплазмати-ческий матрикс, обилие органелл и секреторных гранул диаметром 250...500 нм. Методами иммуноцитохимии выявляются и другие более мелкие и менее дифференцированные клетки, которые считают структурами, находящимися на более ранних этапах дифференцировки.