 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
ЩИТОВИДНАЯ ЖЕЛЕЗАЩитовидная железа —одна из самых крупных эндокринных желез, располагается в нижней части гортани и верхней части трахеи в виде двух лопастей, соединенных между собой перешейком, лежащим на вентральной поверхности трахеи. Снаружи покрыта соединительнотканной капсулой, в толще которой располагаются мелкие сосуды, капилляры, а также миелинизированные и немие-линизированные нервные волокна. От капсулы внутрь железы отходят соединительнотканные тяжи (септы), по которым проходят кровеносные и лимфатические сосуды, нервные волокна. Паренхима органа включает в себя несколько типов клеток: тиреоидные
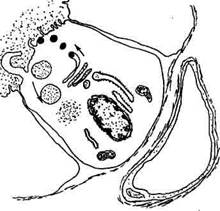
(формирующие стенку фолликула), парафолликулярные и интерфолликулярные. Фолликулярный эпителий состоит в основном из паренхимных клеток и образует основную структурно-функциональную единицу щитовидной железы — фолликул (округлой или овальной формы пузырек). Между фолликулами находятся прослойки соединительной ткани, пронизанные кровеносными капиллярами. Просвет фолликула заполнен коллоидом, который непосредственно прилежит к апикальной поверхности тиреоцита с многочисленными микроворсинками, образованными выступами плазматической мембраны. Противоположная сторона тиреоцита тесно контактирует с перикапиллярным пространством, причем в базальном отделе клетки плазматическая мембрана образует глубокие складки, что значительно увеличивает ее поверхность, контактирующую с кровеносной системой. Боковые поверхности тиреоцитов соединяются за счет замыкательных комплексов, что надежно изолирует внутреннее пространство фолликула от окружающей соединительной ткани. В цитоплазме тиреоцитов особенно сильно развит шероховатый эндоплазматический ретику-лум из многочисленных канальцев и более крупных полостей, заполненных гомогенным мелкозернистым материалом. Комплекс Гольджи очень хорошо выражен и представлен тремя основными компонентами: крупными вакуолями, уплощенными цистернами (ламеллами) и микропузырьками. В зоне комплекса Гольджи обнаруживаются секреторные гранулы различной величины, электронной плотности и формы, окруженные мембраной. Кроме характерных гранул в апикальной части цитоплазмы выявляются коллоидные капли, окруженные мембраной. Исходными продуктами для биосинтеза йодированных гормонов служат аминокислота тиронин и йодид. Поставляемый с кровью йодид в тиреоцитах, подвергаясь окислению, превращается в молекулярный йод, который вступает в соединение с тиронином, и через ряд промежуточных соединений (монойодтиронин, дийод-тиронин) образуются тироксин (тетрайодтиронин) и трийодтиро-нин. Считается, что эти гормоны синтезируются в свободном состоянии в цитоплазме фолликулярных клеток и необходимое для организма количество гормона сразу после образования поступает в кровь, а его избыток включается в молекулы тиреоглобулина и накапливается в коллоиде. Тиреоглобулин — крупная гликопротеи-новая молекула, синтезированная по общей схеме синтеза белка. Освобождение тиреоглобулина из секреторных гранул в полость фолликула происходит либо путем диффузии через ограничивающую мембрану, либо путем экзоцитоза. Иодирование тиреоглобулина происходит в основном в просвете фолликула и на границе между коллоидом и апикальной плазматической мембраной. При снижении потребности организма в тиреоидных гормонах внутриклеточный гидролиз тиреоглобулина прекращается и белок выво- дится в полость фолликула, где накапливается в виде гормонального резерва. Накопленный в полости фолликула тиреоглобулин поступает в цитоплазму тиреоцита за счет микропиноцитоза коллоида: при повышенной потребности возможно захватывание крупных порций с помощью псевдоподий. Образовавшиеся в результате эндоцитоза коллоидные капли постепенно перемещаются к базальной части клетки; при встрече с лизосомами происходят их тесный контакт и слияние, причем гидролитические ферменты лизосом поступают внутрь коллоидных капель. Коллоидные капли уменьшаются, а поступившие в цитоплазму тиреоидные гормоны диффундируют в перикапиллярное пространство и затем проникают в кровеносное русло. При истощении запасов коллоида в полости фолликула синтез, йодирование и протеолити-ческое расщепление тиреоглобулина полностью осуществляются в цитоплазме тиреоцитов (рис. 12.9).
Трийодтиронин непрочно связан с белками крови и быстро проникает в клетки, а у тироксина эта связь прочнее, поэтому он способен длительно циркулировать в кровеносном русле. Физиологическим действием в основном обладает трийодтиронин, так как он в 5...6 раз активнее тироксина и, проникая в клетки тканей-мишеней, воздействует на ферментные системы, локализованные в митохондриях (ферменты трикарбонового цикла, фосфорилиро-вания, железосодержащие дыхательные и др.). Гормоны щитовидной железы регулируют процессы роста и развития, величину энергетического обмена, белковый, углеводный, жировой, водный и минеральный обмен, тем самым влияя на деятельность сердца, нервную систему и половые железы.
Демонстративным примером участия тиреоидных гормонов в регуляции роста и развития служит влияние щитовидной железы на метаморфоз амфибий. При удалении щитовидной железы головастики никогда не превратятся во взрослую форму, вырастая, остаются на стадии личинки, а скармливание щитовидной железы или введение на ее основе препаратов ускоряют метаморфоз амблистомы (личиночной формы аксолотлей) и других земноводных. У птиц и млекопитающих гормоны щитовидной железы играют важную роль во время эмбрионального развития. При выключении функции железы у птиц тормозится рост тела, задерживаются процессы окостенения в конечностях, нарушается процесс эмбрионального оперения и т. д. С активностью щитовидной железы связаны и видовые особенности развития птиц. Так, у выводковых видов птенцы сразу после вылупления из яйца способны бегать и самостоятельно питаться, так как щитовидная железа активно функционирует уже на ранних стадиях зародышевого развития. У птенцовых видов, птенцы которых вылупляются слепыми и беспомощными, щитовидная железа в эмбриональный период развита слабо и ее активность возрастает только после вылупления из яйца. Аналогичная закономерность обнаруживается и у млекопитающих — зрелорожденные детеныши (способные самостоятельно передвигаться) имеют щитовидную железу, активно функционирующую на ранних стадиях эмбрионального развития. У млекопитающих, детеныши которых появляются на свет слепыми и голыми, деятельность щитовидной железы проявляется незадолго до рождения. Следует, однако, учитывать, что некоторое количество тиреоидных гормонов потомство получает из организма матери через плаценту и с молоком. Гормоны щитовидной железы существенно влияют на развитие костной ткани. При удалении щитовидной железы за счет действия соматотропного гормона усиливается рост трубчатых костей, стимулируется пролиферация эпифи-зарных хрящей, но задерживается дифференциация костной ткани. Введение тироксина гипофизэктомированным животным вызывает окостенение эпифизов при незначительном росте костей. Рост и прорезывание зубов у млекопитающих зависят от содержания в крови тиреоидных гормонов. Тиреоидные гормоны стимулируют регенерацию тканей и способствуют заживлению ран: грануляционная ткань быстрее заполняет дно раны, и эпителизация идет более интенсивно. Влияние щитовидной железы ярко проявляется при оценке основного обмена: тиреоидэктомия снижает его на 45...59 %. Повышение содержания гормонов за счет введения тироксина увеличивает уровень основного обмена до 50 % по сравнению с нормой и выход энергии при выполнении механической работы. Гормоны щитовидной железы резко усиливают окислительные процессы и теплопродукцию, причем этот эффект обнаруживается и на изолированных органах. Инкубируемые фрагменты мышц, печени и почек от животных, которым предварительно вводили тироксин, потребляют значительно больше кислорода, чем аналогичные ткани, взятые у тиреоидэктомированных животных. In vivo при гипофункции щитовидной железы у животных нарушается терморегуляция, понижается температура тела и они плохо переносят охлаждение. Гормоны щитовидной железы способны значительно повысить потребность организма в метаболитах: усиливается расходование белка и жира, азотистый баланс становится резко отрицательным, азот в составе мочевины выводится с мочой. При гиперфункции щитовидной железы возрастает интенсивность основного обмена: обнаруживается резкое похудание, расходуется до 70 % запасов жировых депо, содержание холестерина в крови снижается. Углеводный обмен также интенсифицируется: уровень глюкозы в крови несколько повышается, а печень быстро теряет запасы гликогена. В основе физиологического действия тиреоидных гормонов лежит регуляция интенсивности дыхания клеток, их непосредственное влияние на поглощение кислорода митохондриями и другими структурными компонентами клеток, усиление окислительных реакций и последующее изменение активности ряда ферментов и влияние на ядерный аппарат клеток. Тироксин способствует переносу аминокислот к рибосомам, причем максимальное использование резорбированных аминокислот происходит в том случае, когда все они присутствуют в клетке в соответствии с требованиями определенного количественного соотношения и последовательности информационной РНК. Развитие и функциональное состояние нервной системы находятся под постоянным влиянием щитовидной железы. Ее удаление приводит к нарушению развития мозга: нейроны имеют меньшие размеры, задерживается миелинизация нервных волокон. Полноценная дифференцировка развивающегося мозга происходит при достаточном уровне тиреоидных гормонов в организме. В ходе дифференцировки и созревания нервной клетки существует критический период, во время которого гормоны оказывают свое влияние на морфогенез, поэтому нарушение функций щитовидной железы в раннем возрасте приводит к кретинизму. В дальнейшем они необходимы для поддержания метаболизма и функциональной активности нейрона. Тиреоидэктомия резко снижает возбудимость животных и ослабляет у них активные и пассивные оборонительные реакции, подавляет деятельность высших нервных центров. При гипотериозе условные рефлексы вырабатываются с большим трудом и требуют постоянного подкрепления: введение тиреоидина восстанавливает рефлекторную деятельность мозга. Гормоны щитовидной железы существенно влияют на деятельность сердца, изменяя ритм его сокращений. При удалении щито-
видной железы сокращения сердца урежаются, а при введении тироксина интактным животным частота сердечных сокращений повышается в 1,5 раза. Передозировка гормона может привести к трепетанию предсердий. При функциональных гипотиреоидных состояниях, характерных для зимнеспящих животных (медведей, ежей, сурков, летучих мышей), наблюдается снижение температуры тела, уменьшение уровня основного обмена и существенное замедление ритма сердечных сокращений. Периоду пробуждения у этих животных предшествует активизация деятельности щитовидной железы; введением тироксина можно прекратить зимнюю спячку и обеспечить пробуждение у ежей. Физиологический ги-пертиреоз отмечается при функциональных состояниях животных, которые требуют интенсификации обмена веществ: беременность, лактация (особенно у высокопродуктивных животных). Тиреоидные гормоны ускоряют всасывание глюкозы в желудочно-кишечном тракте, участвуют в регуляции уровня гликогена в печени, усиливают секрецию молока и увеличивают содержание в нем жира. Под действием тиреоидных гормонов резко ускоряются процессы окисления жирных кислот в митохондриях. Регуляция секреции тиреоидных гормонов осуществляется прежде всего за счет выделения специфического стимулирующего вещества — тиреотропного гормона передней доли гипофиза. У гипофизэктомированных животных уменьшаются размер и масса щитовидной железы, развивается атрофия ткани и в первую очередь редуцируются новообразованные фолликулы на фоне симптомов тиреоидной недостаточности. Повышение секреции тиреотропного гормона увеличивает продукцию и поступление в кровь гормонов щитовидной железы. Но увеличение концентрации тиреоидных гормонов сказывается на продукции тиролиберина в гипоталамусе: избыток гормона тормозит тиреотропную функцию гипофиза, что ведет к снижению секреции тироксина в щитовидной железе и реализации обратной отрицательной связи, обеспечивающей в норме постоянство гормонального уровня. Наряду с системой гуморальной регуляции, в которой тирео-тропная функция гипофиза коррелируется с выделением АКТГ и соматотропного гормона, активность щитовидной железы существенно зависит от функционального состояния и энергетических потребностей организма. При охлаждении, вызывающем раздражение Холодовых рецепторов, рефлекторно усиливается секреция тиреотропных гормонов, обусловленная воздействием гипоталамического тиролиберина. Вместе с влиянием гипоталамуса регулирующее воздействие на состояние щитовидной железы оказывает вегетативная нервная система: симпатический отдел усиливает активность органа, а парасимпатический угнетает. Влиянием симпатического отдела вегетативной нервной системы объясняется ускоренное выделение тиреоидных гормонов в усло- виях стрессовых ситуаций, что обеспечивает приспособление организма к неблагоприятным факторам среды: охлаждению, отрицательным эмоциям и т. д. Наиболее часто нарушение деятельности щитовидной железы вызвано недостаточным поступлением йода в организм. Снижение уровня тиреоидных гормонов сказывается на деятельности гипоталамуса и гипофиза, который отвечает усиленной секрецией тиреотропина, вызывающего разрастание ткани щитовидной железы (зоб). Увеличение железы может быть за счет разрастания соединительной ткани (простой зоб) или увеличения объема фолликулярной ткани (коллоидный зоб). В местностях, где почва и вода бедны йодом (горные районы, зоны подзолистых, серых лесных и солонцовых почв), возможно развитие зобных эндемий. Недостаточное поступление йода в организм приводит к снижению образования тиреоглобулина, обладающего свойствами каротиназы (фермента, ответственного за превращение каротина в витамин А). Таким образом, избыток тиреоидных гормонов в тканях организма нейтрализуется витамином А и в случаях гипертиреоза возможен А-авитаминоз. Поступление витамина А или каротина с кормом нормализует основной обмен и поднимает уровень гликогена в печени. На активность щитовидной железы оказывают влияние полноценность белков, жиров, углеводов и наличие антитиреоидных веществ гойтро-генов (содержатся в соевых бобах, горохе, белом клевере, капусте и турнепсе), которые избирательно нарушают процессы связывания йода в щитовидной железе. Недостаток тирозина и фенилаланина, избыток растительных жиров и длительное, однообразное углеводное питание приводят к развитию дистрофических изменений в железе и нарушению продукции тиреоидных гормонов. Парафолликулярные клетки (К-клетки) располагаются в интерфолликулярных островках и стенке фолликулов щитовидной железы. Они существенно отличаются по своей структуре от тиреоцитов: имеют низкую электронную плотность (светлые клетки) и содержат в цитоплазме большое количество секреторных гранул и везикул. К-клетки не контактируют с коллоидом и максимально приближены к капиллярам в интерфолликулярных островках; располагаются на периферии и на наружной поверхности фолликулов. Гранулы, локализованные в цитоплазме К-клеток, имеют диаметр 200...280 нм, содержат тонко-гранулированный материал и окружены одиночной мембраной. Вблизи плазматической мембраны обнаруживаются признаки экзоцитоза — слияния мембраны секреторной гранулы с плазма-леммой и освобождения ее содержимого в перикапиллярное пространство. Установлено, что К-клетки продуцируют тиреокаль-цитонин — полипептид, состоящий из 32 аминокислот, вызыва-
Околощитовидные (паращитовидные) железы. У млекопитающих представляют собой парные образования и расположены около щитовидной или вилочковой железы либо погружены в их ткань. Эти небольшие округлые железы окружены собственной соединительнотканной капсулой. От капсулы в толщу органа отходят тонкие септы, между которыми находятся тяжи и группы железистых клеток — паратиреоцитов. Паратиреоциты располагаются радиально вокруг многочисленных капилляров, пронизывающих тело органа. Структурная организация клеток паренхимы околощитовидной железы носит характерные признаки интенсивного секреторного процесса: развитой эндоплазматический ретикулум представлен многочисленными уплощенными канальцами и сво-боднолежащими рибосомами, обусловливающими мелкозернистую структуру цитоплазмы; комплекс Гольджи хорошо развит и представлен большим количеством микропузырьков, имеющих мелкозернистое содержимое. Кроме микропузырьков в цитоплазме паратиреоцитов обнаруживаются более крупные (диаметр 150...200нм) гранулы, формирующиеся в комплексе Гольджи и выделяющиеся из клеток в области латеральных клеточных контактов. Наряду с секреторными структурами паратиреоциты могут содержать липидные капли, липопигментные тельца и лизосомальные образования. Кроме этих клеток, описываемых при световой микроскопии как «главные», паренхима околощитовидных желез содержит электроно-плотные, или «оксифильные», клетки, функциональное значение которых еще не установлено. Не исключена возможность того, что околощитовидные железы образованы клетками одного типа (главными клетками), цитоплазма которых может меняться в широких пределах в зависимости от функционального состояния. Паратиреоциты контактируют с одним или несколькими капиллярами, причем периэндотелиальное пространство расширено и содержит кроме двух базальных мембран и специальные клетки сосудистого окружения — перициты. Эндотелий капилляров уплощен и имеет многочисленные фенестры. Если у животного удалить околощитовидные железы (парати-реоидэктомия), то на 2...3-е сутки нарушается возбудимость нервной системы: походка становится более напряженной, появляется фибриллярное подергивание отдельных мышц головы и туловища. Единичные сокращения усиливаются и переходят в бурные приступы общих судорог (титания), которые повторяются все чаще. Животное вскоре погибает за счет понижения содержания кальция в крови, поскольку определенный уровень кальция необходим для течения важнейших жизненных процессов. Внутривенное введение хлористого кальция оперированным животным способно временно прекратить судороги и снизить возбудимость ЦНС. Околощитовидные железы секретируют гормон — паратгор-мон, полипептид с молекулярной массой около 8500, состоящий из 83 аминокислотных остатков. Паратгормон регулирует концентрацию кальция и фосфора. В результате его действия повышается уровень кальция в крови и тканях организма, а содержание фосфатов снижается. Исходя из того, что кальций попадает в организм с пищей и поступает в кровь в тонком кишечнике, действие гормона проявляется уже на уровне кальцийтранспортирующих систем — энтероцитов. Основным депо кальция в организме служит костная ткань, содержащая до 99 % всего кальция в составе гидрооксиапатита. Действие паратгормона проявляется в мобилизации запасенного в кости кальция. Усиливается деятельность разрушающих кость остеокластов и подавляется функция фиксирующих кальций остеобластов, происходит деполимеризация мукополисаха-ридов основного вещества кости, ее декальцинация и поступление ионов кальция и фосфорной кислоты в кровь. Одновременно с этим уменьшается реабсорбция фосфатов из мочи: они быстро выводятся, и их уровень в крови быстро снижается. Продукция паратгормона регулируется в основном уровнем кальция в крови по принципу обратной отрицательной связи. В случаях высокой потребности организма в кальции, наступающей при беременности и лактации, когда для развивающегося плода или образования казеина необходимо поступление дополнительных значительных количеств кальция, обнаруживается физиологическая гиперфункция околощитовидной железы. Если не увеличить содержание кальция в корме, то возможна декальцинация (остеомаляция и остеопороз) костной ткани материнского организма. НАДПОЧЕЧНИКИ Надпочечник — парный эндокринный орган, состоящий фактически из двух самостоятельных желез: коры и мозгового вещества, т. е. разнородных эндокринных компонентов, имеющих различное происхождение и продуцирующих различные гормоны. Адренокортикоциты — железистые клетки коры надпочечника секретируют стероидные гормоны, а хромафинные клетки —
33 — 3389 клетки мозгового вещества синтезируют катехоламины адреналин и норадреналин. Кора надпочечников. Кора надпочечника состоит из трех ясно выраженных зон: клубочковой, пучковой и сетчатой. Клубочковая зона. Располагается непосредственно под соединительнотканной капсулой надпочечника и представлена изогнутыми тяжами адренокортикоцитов, составляющими 4...6 рядов. Адренокортикоциты клубочковой зоны имеют удлиненную форму и эксцентрически расположенное округлое ядро, а также ли-пидные включения, сосредоточенные в одном из полюсов клетки. Липидные включения (липосомы) тесно контактируют с митохондриями и каналами эндоплазматического ретикулума. Каналы эн-доплазматического ретикулума обычно не несут на своей поверхности рибосом. Свободные рибосомы, собранные в розетки, располагаются в цитоплазме между пузырьками ретикулума и липосомами. Комплекс Гольджи хорошо развит и представлен параллельно ориентированными ламеллами, небольшими вакуолями и микропузырьками. Вблизи комплекса Гольджи располагаются плотные тельца, по своей организации соответствующие лизосомам. Эндокринные клетки клубочковой зоны являются местом образования стероидных гормонов, называемых минералокортико-идами за их влияние на минеральный и водный обмен. Действие этих гормонов реализуется в почках, где они стимулируют реабсорбцию ионов натрия и хлора, тормозят реабсорбцию ионов калия, магния, водорода и аммония в канальцах. К минералокорти-коидам относятся альдостерон и l-дезоксикортикостерон, которые обеспечивают задержку в организме натрия и выведение калия, а также поддерживают ионный и осмотический гомеостаз. Альдостерон в основном повышает проницаемость для натрия клеточной мембраны эпителия, обращенной в просвет канальца, тем самым облегчая проникновение этого иона в клеточное пространство и делая его более доступным для транспортной системы натрий-калиевой помпы, локализованной в базолатеральной мембране клетки. Таким образом, альдостерон регулирует солевой и водный обмен: обеспечивает усиленный переход натрия из клеток в тканевую жидкость, а затем воды по осмотическому градиенту, в результате этого увеличивается объем тканевой жидкости и плазмы крови, возрастает клубочковая фильтрация и из организма выделяется значительное количество воды. Альдостерон выступает как антагонист вазопрессина. Секреция альдостерона стимулируется за счет усиления образования ренина юкстагломерулярным аппаратом почки. Напротив, увеличение содержания в крови натрия тормозит выделение из надпочечников альдостерона. Пучковая зона. Морфологический переход клубочковой зоны в пучковую происходит постепенно и проявляется в уменьшении числа внутриклеточных липидных включений. Адренокортикоциты этой зоны располагаются радиальными тяжами, отграниченными кровеносными капиллярами и соединительнотканными септами. Клетки пучковой зоны несколько крупнее клеток клубочковой зоны и имеют угловатую форму. На поверхности клеток, обращенной к перикапиллярному пространству, находится значительное количество микроворсинок. Клетки этой зоны содержат многочисленные митохондрии, во внутреннем пространстве которых от внутренней митохондриальной мембраны могут отпочковываться везикулы, заполняющие митохондриальное пространство. Кроме этого в митохондриях присутствуют кристаллоиды, состоящие из скоплений плотно упакованных трубочек, предположительно принимающих участие в стероидогенезе. Эндоплазматический ретикулум клеток пучковой зоны представлен короткими уплощенными канальцами или округлыми пузырьками, не несущими на своей поверхности рибосом и тесно связанными с митохондриями и липосомами. В пучковой зоне надпочечников образуются стероидные гормоны, называемые глюкокортикоидами, так как они преимущественно регулируют углеводный и белковый обмен. К глюкокор-тикоидам относятся гидрокортизон (кортизол), кортизон, корти-костерон, причем существуют видовые различия в продукции кортикостероидов. У обезьян, овец и морских свинок образуется в основном гидрокортизон; у мышей, крыс, кроликов и птиц — кортикостерон, а у крупного рогатого скота, свиней, собак и кошек — оба эти гормона. Из кортизола у млекопитающих может образовываться вне надпочечников некоторое количество кортизона. В крови гидрокортизон быстро связывается с альфа-глюко-протеином (транскортином) и сывороточным альбумином. Связанный с транскортином гидрокортизон физиологически не активен, и лишь достигая ткани мишени и освободившись от белка-носителя, реализует свое действие. Глюкокортикоиды обеспечивают превращение белков в углеводы, активируя процессы глюконеогенеза. Усиливается распад белков, стимулируется окислительное дезаминирование аминокислот с образованием пировиноградной кислоты и превращением ее в глюкозо-6-фосфат или глюкозо-1-фосфат. Это вызывает повышение содержания глюкозы в крови и увеличение запасов гликогена в печени. Введение больших доз глюкокортикоидов значительно уменьшает количество белка в мышечной и соединительной ткани, а также в плазме крови. При этом усиливается выведение азота с мочой и азотистый баланс становится отрицательным. Глюкокортикоиды тормозят превращение углеводов в жиры, а при недостатке глюкозы обеспечивают мобилизацию жира из депо и его быстрое использование для обеспечения энергетических процессов. В почках глюкокортикоиды уменьшают реабсорбцию глюкозы, что ведет к снижению почечного порога для глюкозы и ее выведению с мочой — развивается глюкозурия (своеобразная форма стероидного сахарного диабета).
33* Особого внимания заслуживает способность глюкокорти-коидов проявлять противовоспалительное действие — практически угнетать все проявления воспалительной реакции: уменьшается экссудация, снижается проницаемость капилляров, тормозится миграция лейкоцитов и ослабляется их фагоцитарная активность. Торможение активности лимфоидной системы проявляется в том, что при введении глюкокортикоидов уменьшаются в размерах лимфоузлы и наступает быстрая инволюция тимуса, понижается количество лимфоцитов и эозинофилов в крови, подавляется выделение гистамина и кининов. Вместе с этим рецепторы кортикостероидов обнаружены и непосредственно в иммункомпетентных клетках — лимфоцитах, моноцитах, макрофагах и фибробластах, что обусловливает их противовоспалительное и антиаллергическое действие. В соединительной ткани глюкокортикоиды уменьшают количество основного вещества, число фибробластов и содержание коллагена за счет активации гиалуронидазы и усиленного распада мукополисахаридов, составляющих основу соединительной ткани. Глюкокортикоиды понижают адренокортикотропную активность гипофиза, изменяют строение островковой ткани эндокринного отдела поджелудочной железы, повышают чувствительность яичников к гонадотропным гормонам. Благодаря наличию рецепторов к кортикостероидам в ЦНС (лимбической системе, коре головного мозга, гипоталамусе, гипофизе, в нейронах варолиевого моста, в моторных ядрах среднего и продолговатого мозга) изменяются возбудимость и условно-рефлекторная деятельность. Сетчатая зона. Тяжи клеток пучковой зоны постепенно переходят в сетчатую, где анастомозируют друг с другом, формируя сеть. Адренокортикоциты сетчатой зоны весьма различаются по своей форме: наряду с округлыми или бокаловидными клетками встречаются клетки полигональной формы. Ядра клеток этой зоны в основном округлые и содержат значительно конденсированный хроматин, расположенный по периферии. Митохондрии занимают большую часть цитоплазмы адренокортикоцитов, причем клетки, расположенные на границе с пучковой зоной, содержат везикулярные митохондрии, а по мере погружения в сетчатую зону эти органеллы приобретают тубулярные кристы. Эндоплаз-матический ретикулум и комплекс Гольджи по своей структуре весьма близки к организации этих структурных компонентов клетки в клубочковой и пучковой зонах. В сетчатой зоне продуцируются половые гормоны — аналоги стероидных гормонов, вырабатываемых в половых железах. К анд-рогенам (мужским половым гормонам) относятся андростендион, 1 -оксиандростендион и дегидроэпиандростендион, причем наибольшая гормональная активность присуща андростендиону, однако она в пять раз ниже, чем у тестостерона, образованного в семен- никах. Наличие андрогенов в надпочечниках не зависит от пола животного и имеет особое значение в период до полового созревания, обеспечивая анаболическое действие, усиливая рост тела и развитие скелетной мускулатуры. Эстрогены, в основном эстрон и эстрадиол, вырабатываются в надпочечниках также в очень малых количествах, и их влияние проявляется в случаях развития опухоли коры надпочечника. Прогестерон образуется в коре надпочечников из холестерина в процессе образования других стероидных гормонов, а в ходе дальнейших превращений может служить предшественником 11-дезоксикортикостерона и альдостеро-на. Его действие на матку и другие прогестерончувствительные ткани аналогично гормону желтого тела; у самок некоторых видов млекопитающих он способствует сохранению беременности при недостаточности функций желтого тела. Регуляция секреции половых стероидов, вырабатываемых в сетчатой зоне надпочечников, осуществляется посредством троп-ных гормонов передней доли гипофиза: ФСГ для эстрогенов и ЛГ для андрогенов и прогестерона. Вместе с этим рост пучковой и сетчатых зон, а также образование и секреция глюкокортикоидов стимулируются адренокортикотропным гормоном (АКТГ). Даже однократное введение АКТГ приводит к снижению содержания в коре надпочечника холестерина, аскорбиновой кислоты и гликогена, используемых для синтеза глюкокортикоидов. АКТГ стимулирует и образование дегидроэпиандростерона и андростендиола у зародышей млекопитающих, тогда как у взрослых животных основным регулятором секреции надпочечнико-вых андрогенов становится Л Г. Гормоны надпочечника в реакциях адаптации организма. В 1936 г. Г. Селье установил, что при действии самых различных патогенных и чрезмерных по силе и длительности раздражителей в организме возникают определенные неспецифические изменения, названные им общим адаптационным синдромом. Это состояние может развиваться, когда организм попадает в неадекватные условия существования: многочисленные травмы, чрезмерная мышечная нагрузка, охлаждение, отравления, инфекции, сильное эмоциональное возбуждение. Общим для всех этих воздействий является ответная реакция организма, выражающаяся в гипертрофии коры надпочечника, уменьшении тимуса, селезенки и лимфатических узлов. На фоне этих изменений развиваются дегенеративные процессы в печени, отечность, снижается тонус мышц и температура тела, появляются кровоизлияния и язвы желудочно-кишечного тракта. Факторы, вызывающие эту неспецифическую реакцию, принято называть стрессорами, поскольку общий адаптационный синдром возникает при таком состоянии организма, которое Г. Селье назвал состоянием «напряжения» (stress). В ходе адаптации организма к неблагоприятным условиям происходит мобилизация механизмов, снижающих патологическое
воздействие. Если предотвратить развитие адаптационных реакций, существенно понижается сопротивляемость организма и может наступить смерть. В развитии общего адаптационного синдрома выделяют три стадии. Первая стадия — «реакция тревоги», характеризуется усиленной секрецией адренокортикотропного гормона, который, в свою очередь, стимулирует секрецию глюкокортикоидов и выделение их в кровоток. В крови уменьшается число нейтрофилов, понижается уровень глюкозы, повышается проницаемость стенок кровеносных сосудов, появляются точечные кровоизлияния. Вторая стадия — «стадия резистентности». При продолжающемся воздействии повреждающего фактора происходит гиперплазия коры надпочечников, наряду с усиленным синтезом глюкокортикоидов в надпочечнике накапливаются холестерин и аскорбиновая кислота. Процессы обмена веществ приходят в норму, выравниваются сдвиги метаболизма, обнаруживаемые в начале неблагоприятного воздействия. Наряду с этим уменьшаются тимус и лимфатические узлы. Третья стадия — «стадияистощения», наступает, если напряжение слишком велико или неадекватно длительно и организм не может к нему приспособиться. Кора надпочечника, несмотря на гиперплазию, не способна вырабатывать нужное количество гормонов; клетки содержат мало липоидных гранул и аскорбиновой кислоты. В крови нарастает количество эозинофилов и лимфоцитов, отмечается гипертрофия лимфатических узлов. В условиях нарушения адаптации и истощении защитных механизмов наступает смерть как следствие нарушения резистентности организма и развития инфекционных процессов. Вполне очевидно, что в развитии общего адаптационного синдрома главную роль играют гипофиз и кора надпочечников. Гипофиз секретирует АКТГ, стимулирующий синтез и выделение глюкокортикоидов, представляющих собой, по мнению Г. Селье, адаптационные гормоны. Адаптационные гормоны (кортикостерон, гидрокортизон), обладая противоспалительным действием, подавляют реакции соединительной ткани на патогенный раздражитель, усиливая катаболические процессы в организме. Их природными антагонистами являются соматотропный гормон и минералкортикоиды коры надпочечника (альдостерон, дезоксикортикостерон), стимулирующие анаболические процессы и усиливающие воспалительную реакцию. Следует учитывать, что «стрессоры» прежде всего действуют на рецепторы и состояние «напряжения» развивается рефлекторно с непосредственным участием ЦНС: кора больших полушарий и подкорковые образования воздействуют на гипоталамические структуры, ответственные за выделение кортиколиберина. Усиленная продукция кортиколиберина, АКТГ и глюкокортикоидов — три необходимые составные части формирования об- щего адаптационного синдрома. В этой связи весьма интересной для понимания проблемы адаптации является индивидуальная чувствительность организма к стрессорным воздействиям. При различном исходном уровне возбудимости животные различных типов нервной деятельности неадекватно реагируют на однозначные по величине факторы среды. В этой связи промышленное животноводство, неизбежно сталкивающееся со стрессорны-ми воздействиями, требует соответствующей селекционной работы, направленной на отбор «стрессоустойчивых» животных, у которых неблагоприятные факторы среды меньше влияют на уровень продуктивности и состояние их здоровья. Мозговое вещество надпочечника. Образовано скоплениями крупных клеток округлой и полигональной формы, содержащими значительное число секреторных гранул. Согласно данным гистохимических и ультраструктурных исследований, в мозговом веществе различают клетки, продуцирующие адреналин — адрено-циты и норадреналин — норадреноциты. Адреналиновые клетки составляют большинство клеток мозгового вещества, содержат секреторные гранулы диаметром 300 нм, лежащие в центре пространства, ограниченного мембраной, и окруженные электроно-прозрачным ободком. Норадреноциты отличаются более плотными секреторными гранулами, располагающимися эксцентрично в ограниченном мембраной пространстве везикулы. Мозговое вещество надпочечников вырабатывает два гормона из группы катехоламинов — адреналин и норадреналин, которые являются производными аминокислот фенилаланина и тирозина. Поскольку тирозин отличается от фенилаланина только наличием одной гидроксильной группы у фенольного кольца, то из тирозина ферментативным путем (фермент тирозиназа) образуется ди-оксифенилаланин (ДОФА), который при декарбоксилировании переходит в дофамин. Окисляясь, дофамин превращается в норадреналин, при метилировании которого образуется основной гормон мозгового вещества — адреналин. Физиологическое действие катехоламинов (адреналина и нор-адреналина) заключается в обеспечении экстренной перестройки функций, направленной на повышение работоспособности организма в чрезвычайных ситуациях, когда требуется мобилизация всех резервов. Ответная реакция различных органов на воздействие катехоламинов проявляется в виде ослабления кровоснабжения кожи и внутренних органов и значительного усиления кровоснабжения головного мозга, сердца и скелетной мускулатуры. Наряду с перераспределением крови между органами «быстрого реагирования» ее объем увеличивается за счет выхода в общий кровоток депонированной крови, а насыщение крови кислородом усиливается за счет расширения бронхов и усиления вентиляции альвеол легкого. Катехол амины вызывают учащение ритма и увеличение силы сокращений сердечной мышцы за счет повышения ее возбудимости
и проводимости. Вместе с этим расширяются коронарные сосуды, обеспечивающие усиление сердечного кровотока. Особенность реакций сосудов различных органов на действие адреналина и норадреналина определяется функциональной гетерогенностью рецепторов, которые подразделяются на альфа-и бета-адренорецепторы: при взаимодействии катехоламинов с альфа-адренорецепторами развиваются эффекты возбуждения — сужаются сосуды, сокращается гладкая мускулатура матки и т. д., а с бета-адренорецепторами — реакция торможения: расширяются сосуды, расслабляются бронхи, тормозится сократительная реакция миоэпителия альвеол молочных желез и т. д. Конечная реакция органа на действие катехоламинов определяется соотношением рецепторов различного типа и их структурной локализацией. Важно заметить, что адреналин влияет на оба типа рецепторов, а норадреналин взаимодействует только с альфа-адренорецепторами. Адреналин значительно повышает возбудимость ЦНС, причем существенно усиливается реактивность анализаторов (слуха, зрения). При активации деятельности нервной системы значительно повышается поглощение глюкозы тканями мозга и кислорода нейронами. Активное состояние ЦНС определяется влиянием адреналина на ретикулярную формацию, которая, в свою очередь, активирует нейроны коры больших полушарий. На адреналин реагируют некоторые ядра гипоталамуса, стимулирующие выработку в гипофизе АКТГ и подавляющие продукцию вазопресси-на и окситоцина. Системные эффекты адреналина и норадреналина тесно связаны с непосредственным их влиянием на регуляцию углеводного обмена. В печени и мышцах интенсифицируется распад гликогена, в результате в крови повышается содержание свободной глюкозы и молочной кислоты. Адреналин повышает потребление кислорода мышцами и другими тканями, в результате основной обмен значительно возрастает (до 50 %), а также усиливает теплопродукцию, что в совокупности со снижением теплоотдачи в результате сужения периферических сосудов приводит к повышению температуры тела. Регуляция секреторного процесса в клетках мозгового вещества надпочечника происходит двумя путями — рефлекторным и гуморальным. Нервная регуляция обеспечивается за счет нервных импульсов, идущих по симпатическим волокнам чревного нерва, причем адреноциты и норадреноциты иннервируются самостоятельными нервными волокнами и за счет этого достигается возможность независимых изменений в продукции каждого из катехоламинов. Интенсивная нервная стимуляция приводит к выделению из клеток готового гормона и усиленному его новообразованию. Нервная регуляция выброса катехоламинов в кровь определяется деятельностью коры больших полушарий. При воздействии внешних и внутренних раздражителей, эмоциях (страх, гнев, ярость) отмечается выброс в кровоток больших количеств адреналина. Например, при виде кошки содержание адреналина в крови и у собаки и у кошки резко повышается. Гуморальная регуляция секреторного процесса в мозговом веществе надпочечника тесно связана с гипергликемическим действием катехоламинов: при снижении уровня сахара в крови усиливается секреторная функция адрено- и норадреноцитов. Гормоны мозгового вещества надпочечника не накапливаются в организме и обладают кратковременным действием. Катехоламины, оказав свое физиологическое действие, быстро разрушаются за счет окислительного дезаминирования при участии моноаминооксидаз, а также метилирования. Часть адреналина, норадреналина и продуктов их превращения связывается в печени с глюкуроновой и серной кислотами и выводится из организма с мочой. Таким образом, гормоны надпочечников как коркового слоя — кортикостероиды, так и мозгового вещества — катехоламины, участвуют в адаптации, усиливая устойчивость организма к неблагоприятным воздействиям. Выживание особи в экстремальных, неблагоприятных условиях обеспечивается совместной деятельностью симпатоадреналовой и гипоталамо-гипофизарно-надпо-чечниковой систем. Дата добавления: 2015-12-15 | Просмотры: 941 | Нарушение авторских прав |
 ющий падение уровня кальция и фосфора в крови. Это снижение концентрации кальция в циркулирующей крови обусловлено торможением его мобилизации из костей, причем существенно меняется деятельность клеток костной ткани: угнетаются остеокласты и активируются остеобласты, что приводит к фиксации кальция и фосфора. Наряду с этим существенно увеличивается удаление фосфора с мочой. Тиреокальцитонин усиленно секрети-руется и поступает в кровь при повышении концентрации кальция, что является важным звеном в поддержании постоянства его уровня во внутренней среде организма.
ющий падение уровня кальция и фосфора в крови. Это снижение концентрации кальция в циркулирующей крови обусловлено торможением его мобилизации из костей, причем существенно меняется деятельность клеток костной ткани: угнетаются остеокласты и активируются остеобласты, что приводит к фиксации кальция и фосфора. Наряду с этим существенно увеличивается удаление фосфора с мочой. Тиреокальцитонин усиленно секрети-руется и поступает в кровь при повышении концентрации кальция, что является важным звеном в поддержании постоянства его уровня во внутренней среде организма.