 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Количественная характеристика травленияПрирода процессов травления Согласно химической теории травление рассматривается как обычная гетерогенная реакция, и потому весь процесс травления расчленяют на пять этапов: -диффузия реагента к поверхности; -адсорбция реагента; -поверхностная химическая реакция; -десорбция продуктов взаимодействия; -диффузия продуктов реакции от поверхности. Так как каждый из реагентов травителя должен пройти эту последовательность, то кинетика всего процесса может быть очень сложной. По электрохимической теории, как и в химической теории, травление рассматривается так же, как гетерогенная реакция, которая по этой теории имеет электрохимическую природу. Воздействие растворов травителей на полупроводник может осуществляться или под действием электрического тока, или самопроизвольно. Эти процессы соответственно называются электрохимическим и химическим травлением.
Количественная характеристика травления
Суммарный процесс травления контролируется или химической реакцией, или процессами диффузии. Адсорбция и десорбция характеризуется малыми энергиями активации, протекают сравнительно быстро по сравнению с другими процессами и поэтому лишь в редких случаях лимитируют процесс. Рассмотрим отдельные стадии травления и закономерности, характерные для стационарного состояния. 1.2.1.Диффузия. Основная диффузионная модель была разработана Фиком, в её основе лежит предположение о том, что процессы диффузии и теплопроводности описываются одним и тем же типом уравнений. Согласно закону Фика скорость диффузии определяется выражением
vдифф
где D – коэффициент диффузии; S – поверхность фронта диффузии; δ – толщина фронта диффузионного слоя; с и с' – концентрации вещества в объеме и поверхностном слое; kдифф – единичная скорость процесса диффузии. В начальный момент травления с = с', и диффузия не происходит. Потребление травителя снижает с', а скорость диффузии возрастает. Через некоторое время, если устанавливается стационарный процесс, скорость диффузии достигает определенной величины и больше не изменяется.
Различают три основных типа твердофазного травления:
1) химический процесс на поверхности идет медленно, и наблюдаемая скорость является скоростью поверхностного процесса; 2) химический процесс на поверхности настолько быстр, что конвекция и диффузия не могут обеспечивать достаточной концентрации реагента у поверхности. Наблюдаемая скорость является скоростью переноса (диффузии) к поверхности; 3) скорость диффузии и химической реакции одного порядка (потребление реагента в реакции соизмеримо с его переносом в результате диффузии), однако концентрация реагента на поверхности не снижается на столько, чтобы сдерживать реакцию.
Характерными признаками реакции, контролируемой диффузией, являются:
1) Энергия активации зависит от вязкости. 2) Скорость реакции увеличивается при перемешивании реагента. Исключение составляет эффект автокатолиза NO при травлении кремния в HNO3. Продукты этой реакции (NO) способствуют ее же развитию. Интенсивное перемешивание приводит к уменьшению скорости реакции. 3) Все материалы независимо от ориентации кристаллических плоскостей травятся с одинаковой скоростью. 4) Энергия активации при перемешивании растет. Исключением является травление кремния в HNO3 (DH =100 ккал/моль), в ходе которого значительное количество тепла, выделяемое в результате экзотермической реакции, приводит к увеличению скорости диффузии и скорости травления. Перемешивание в этом случае привело бы к уменьшению скорости травления из-за диссипации тепла.
Характерными признаками процессов, контролируемых скоростью химической реакции, являются:
1) зависимость скорости реакции от концентрации травителя; 2) отсутствие зависимости скорости от перемешивания; 3) энергия активации.
1.2.2.Химическая реакция. Скорость взаимодействия между атомами кристалла и частицами травителя должна быть пропорциональна концентрации атомов кристалла и частиц травителя. Концентрация атомов зависит от природы материала и является величиной постоянной для данного полупроводника.
1.2.3.Скорость суммарного процесса. Скорость суммарного процесса определяется наиболее медленной стадией. Диффузионный контроль наблюдается при применении растворов травителей с низкими концентрациями реагентов, при низких температурах или при процессах, сопровождающихся образованием плохо растворимых продуктов, затрудняющих диффузию. При этом отмечается резко выраженная зависимость скорости процесса от интенсивности перемешивания, вязкости раствора и малая зависимость от нагревания и структуры поверхности. Незначительное влияние температуры на скорость диффузии связано с небольшой энергией активации диффузии, составляющей всего ккал/моль, в то время как энергия активации химических реакций имеет порядок десятков или сотен ккал/моль. Травители с диффузионным контролем называются полирующими. Их особенность заключается в сглаживании шероховатостей, нечувствительности к физическим и химическим неоднородностям поверхности. Травители, в которых самой медленной (контролирующей) стадией служит химическая реакция, называются селективными. При этом скорость травления зависит от температуры, от структуры поверхности, от ее ориентации, но не зависит от перемешивания и вязкости. В селективных травителях выявляется неоднородность поверхности, отдельные участки ее с разными энергиями активации травятся с различной скоростью. В первый момент травления скорость диффузии равна нулю, концентрация травителя вблизи поверхности такая же, как в объеме, условия для протекания химической реакции наиболее благоприятны. Травление – селективное. Через некоторое время концентрация травителя вблизи поверхности снизится до значения с', скорость диффузии возрастет, а скорость химической реакции, наоборот, уменьшится. При достижении стационарного состояния обе скорости станут равными по величине. С этого момента с' больше изменяться не будет и скорость травления постоянна. Дата добавления: 2015-12-15 | Просмотры: 770 | Нарушение авторских прав |
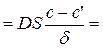 kдифф (с-с’) (1),
kдифф (с-с’) (1),