 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
ДИФФУЗНЫЙ ТОКСИЧЕСКИЙ ЗОБ(Базедова болезнь, болезнь Грейвса) Диффузный токсический зоб (ДТЗ) - это генетическое аутоиммунное заболевание. Он встречается повсеместно. Наиболее часто заболевание возникает в возрасте от 20 до 50 лет, чаще у женщин, чем у мужчин (соотношение составляет 10:1). Следует помнить, что на фоне токсического зоба рак щитовидной железы выявляется определяется в 0,4-2,5% клинических наблюдений. Этиология. Предрасполагающим фактором в развитии заболевания является наследственность. Установлено, что диффузный токсический зоб нередко возникает в ряде поколений у нескольких членов одной семьи. Этот факт связывают с наследованием особого рецессивного гена: причем у женщин он проявляется чаще, чем у мужчин. Заболевание провоцирует психическая травма, острые и хронические инфекции, заболевания гипоталамо-гипофизарной системы, черепно-мозговая травма, перегревание организма, беременность и др. Патогенез диффузно-токсического зоба недостаточно ясен. Предполагается, что диффузный токсический зоб развивается вследствие первичного дефекта иммунного надзора, по-видимому, дефекта или дефицита супрессоров, допускающего выживание и пролиферацию так называемого запрещенного клона хелперов Т-лимфоцитов. При непосредственном участии последнего В-лимфоциты и их производные плазматические клетки синтезируют тиреостимулирующие иммуноглобулины. Взаимодействие их с комплиментарным антигеном мембран тиреоидного эпителия оказывает ТТГ-подобное действие и ведет к усилению синтеза и секреции тиреоидных гормонов. Эти иммуноглобулины объединены под общим названием TSI. Наиболее изучен длительно действующий стимулятор щитовидной железы LATS-фактор. Он обнаруживается у больных с тиреотоксикозом в 14-76% наблюдений. TSI встречаются не только при базедовой болезни, их определяютт также при подостром тиреоидите и тиреоидите Хашимото. Наряду с TSI-антителами к рецептору цитоплазматических мембран тиреоцитов (возможно, к рецептору ТТГ), у больных часто обнаруживают антитела к тиреоглобулину, микросомальной фракции и нуклеарному компоненту. В развитии клинической картины тиреотоксикоза придают определенное значение увеличению чувствительности адренорецепторов к катехоламинам. Установлено также, что симпатические нервные импульсы вызывают в щитовидной железе усиление выделения и образования гормонов. Определенное значение в патогенезе заболевания имеет и нарушение метаболизма тиреоидных гормонов в периферических тканях - печени, почках, мышцах. Клинические проявления токсического зоба обусловлены биологическим эффектом тиреоидных гормонов и катехоламинов. Клиника. Основными жалобами больного с диффузным токсическим зобом являются похудание, тахикардия, дрожание рук, ног, потливость, раздражительность, экзофтальм, нарушение сна (бессонница, прерывистый неглубокий сон), снижение работоспособности. Женщины нередко предъявляют жалобы на нарушение менструального цикла. Похудание является одним из часто встречаемых симптомов диффузного токсического зоба. Чрезмерная секреция тиреоидных гормонов приводит к усилению процесса расхода энергетических ресурсов в организме, что проявляется усиленным катаболизмом белков, распадом гликогена печени и липолизом. Сердечно-сосудистые нарушения. Они обусловлены, с одной стороны, повышенной чувствительностью сердечнососудистой системы к катехоламинам, с другой — прямым воздействием избытка тироксина на сердечную мышцу, что приводит к нарушению внутри клеточных процессов. В результате возникает дистрофическое поражение сердечной мышцы, симптомами которого являются нарушение ритма (от тахикардии до аритмии), ишемия миокарда и сердечная недостаточность. Нервно-мышечная система и психика. В клинической картине заболевания расстройства центральной и периферической нервной системы занимают одно из первых мест. Характерно дрожание тела (симптом телеграфного столба) и отдельных его частей: языка, опущенных век и т.д. При расслабленной кисти наблюдается мелкий тремор раздвинутых пальцев вытянутых рук (симптом Мари). Нередко возникает мышечная слабость. Изменения психики выражаются в моторной возбудимости, частой смене настроения, бессоннице. В редких случаях бывают тиреотоксические психозы. В связи с воздействием тиреоидных гормонов на центр терморегуляции у больных с токсическим зобом иногда наблюдаются нарушения терморегуляции с колебаниями температуры в течение дня от 37,3 до 37,6 гр. С. У некоторых больных отмечены трофические нарушения: выпадения волос, истончение и ломкость ногтей. Эндокринная система. Помимо нарушений функции щитовидной железы у больных нередко происходят изменения функции других желез внутренней секреции. Часто страдают половые железы - у женщин нарушается менструальный цикл, снижается либидо; у мужчин развивается импотенция и снижается либидо. Изменения в функциональном состоянии коры надпочечников проявляются усилением функции при легких формах заболевания и постепенным снижением, вплоть до истощения, при тяжелых формах. Диффузный токсический зоб часто сопровождается эндокринной офтальмопатией. Одним из наиболее характерных глазных симптомов является экзофтальм. Считают, что экзофтальм обусловлен аутоиммунными процессами. При нем возникает отек и увеличивается объем ретробульбарной клетчатки, отмечаются также явления миозита и разрастание соединительной ткани экстраокулярных мышц. Кроме экзофтальма при эндокринной офтальмопатии могут наблюдаться и ряд других глазных симптомов, в основном связанных с повышенной активностью симпатико-адреналовой системы. Наиболее часто встречаются симптомы Краусса, Грефе, Кохера, Мебиуса, Штельвага, Дельримпля, Еллинека. Симптом Краусса выражается в сильном блеске глаз. Этот симптом может встречаться при туберкулезе, функциональных расстройствах нервной системы, ревматизме, у здоровых людей. Симптом Грефе заключается в отставании верхнего века от радужной оболочки при фиксации зрением медленно перемещающегося вниз предмета, в связи с чем между верхним веком и радужной оболочкой остается белая полоска склеры. Симптом связан с повышением тонуса мышцы, поднимающей верхнее веко. Симптом Кохера объясняют увеличенным сокращением (ретракцией) верхнего века, вследствие чего белая полоска склеры между верхним веком и радужной оболочкой появляется при фиксации зрением предмета, перемещаемого вверх. Симптом Мебиуса заключается в слабости конвергенции, т.е. потери способности фиксировать предметы на близком расстоянии. Симптом Штельвага - редкое (при норме 6-8 раз в минуту) и неполное мигание. Его расценивают как проявление понижения чувствительности роговицы. Широкое раскрытие глазных щелей (стимптом Дельримпля) с появлением белой полоски между радужной оболочкой и верхним веком обусловлено парезом круговой мышцы век. Симптом Еллинека характеризуется пигментацией вокруг глаз. В ряде случаев наблюдают мелкий тремор закрытых век (симптом Розенбаха), отсутствие наморщивания лба при взгляде кверху, (симптом Жоффруа). Щитовидная железа обычно при диффузном токсическом зебе увеличена диффузно, одна доля может быть увеличена больше другой. Консистенция ее мягкая или умеренно уплотненная. Тяжесть диффузного зоба не зависит от степени увеличения железы, а обусловлена ее гиперфункцией и реакцией организма на избыточно продуцируемые тиреоидные гормоны. Лабораторные данные. Из специфических тестов при ДТЗ наблюдается увеличение ТЗ и Т4, понижение способности ТСГ связывать меченый трийодтиронин, ТТГ не изменен или снижен, повышен основной обмен. В крови определяются тиреостимулирующие антитела; нередко повышен титр антител к тиреоглобулину; увеличено количество СБЙ, и активируется поглощение железой йод-131. Классификация. Общепринятой является классификация, рекомендованная в 1961 году Международным эндокринологическим конгрессом. ДТЗ разделяют по тяжести - легкая, средняя и тяжелая и по степени увеличения щитовидной железы (0,1,2,3,4,5). При легкой форме повышается нервная возбудимость, несколько снижается работоспособность, отмечается похудание (обычно 10-15% от исходной массы тела), постоянная тахикардия, но не более 100 ударов в 1 минуту. Основной обмен не превышает +30 %. При заболевании средней тяжести значительно повышена нервная возбудимость, снижена работоспособность, отмечается похудание на 20 % от должной массы, тахикардия от 100 до 120 ударов в минуту, основной обмен повышен от +30 до +60%. К группе с тяжелой формой заболевания относят больных с резко выраженной нервной возбудимостью, полной утратой работоспособности, потерей массы тела до 50% от должной, тахикардией больше 120 в одну минуту. Основной обмен превышает +60%. В эту группу входят больные, течение болезни которых осложнилось мерцательной аритмией, сердечной недостаточностью и психозами. Различают 5 степеней увеличения щитовидной железы: I степень - прощупывается увеличенный перешеек железы. При осмотре щитовидная железа не визуализируется. II степень - железа легко прощупывается и заметна на глаз при глотательных движениях. III степень - «толстая шея» (щитовидная железа хорошо видна при осмотре). IV степень — выраженный зоб, резко меняющий конфигурацию шеи. V степень - зоб достигает очень больших размеров. При 0 степени щитовидная железа не прощупывается или немного прощупывается, но не увеличена. Стадии развития базедовой болезни (по Milcu): Невротическая - эта стадия трудно отличается от вегетативного невроза. Характеризуется повышенной возбудимостью нервной системы, сердцебиением и тремором рук. Нейро-гуморальная стадия - наблюдается увеличение щитовидной железы с ясно выраженными симптомами тиреотоксикоза. Дистрофическая или кахектическая стадия - больные в очень тяжелом состоянии, с выраженной общей дистрофией или кахексией. Существует склонность к мерцанию предсердий, коматозным состояниям и тиреотоксическим комам, которые часто становятся причиной смерти. Диагноз ДТЗ ставят на основании клинических симптомов и данных дополнительных методов исследования, включающих, в первую очередь, определение БСЙ крови, основного обмена, радиойоддиагностику, УЗИ и определение уровня гормонов в крови. У больных юношеского возраста и пожилых имеются некоторые особенности клиники. Например, у пожилых он чаще развивается медленно, тогда как у детей и юношей - нередко бурно. Иногда тиреотоксикоз у пожилых длительное время остается нераспознанным. Это бывает в тех случаях, когда сердечно-сосудистые расстройства, обусловленные в действительности тиреотоксикозом, рассматриваются как следствие заболеваний сердца. Тиреотоксический криз - это лавинообразное нарастание симптомов тиреотоксикоза, возникающее вследствие резкого увеличения содержания в плазме крови трииодтиронина в сочетании с повышенной чувствительностью Б-адреноблокаторов. Признаками криза являются тахикардия, рвота, понос, психомоторное возбуждение, размашистый тремор, сердечная недостаточность, гипердинамический синдром. При изучении уровней Т3 и Т4 выявляется их существенное увеличение. Дифференциальная диагностика. Диффузный токсический зоб дифференцируют от ТТГ - продуцирующей аденомы гипофиза, токсической аденомы щитовидной железы, нейроцир-куляторной дистонии, ревмокардита, туберкулеза, атеросклеротического кардиосклероза, тахиаритмической формы мерцательной аритмии. Лечение. В настоящее время существуют три основных метода лечения ДТЗ: медикаментозная терапия, хирургическое вмешательство (субтотальная резекция щитовидной железы) и лечение радиоактивным йодом. Все имеющиеся методы терапии приводят к снижению повышенного уровня циркулирующих тиреоидных гормонов до нормальных цифр. Каждый из этих методов имеет свои показания и противопоказания и должен определяться для больных индивидуально. Выбор метода зависит от тяжести болезни, размеров щитовидной железы, возраста больных и сопутствующих заболеваний. Для медикаментозного лечения диффузного токсического зоба используют мерказолил и метилтиоурацил, блокирующие синтез тиреоидных гормонов на уровне перехода монойодтирозина в дийодтирозин. К антитиреоидным препаратам, применяемым для лечения ДТЗ, относится также перхлорат калия, блокирующий проникновение йода в щитовидную железу. Лечебное применение препаратов йода в настоящее время строго ограничено, т.к. у больных ДТЗ в результате длительной терапии этими лекарственными веществами увеличивается и уплотняется щитовидная железа при отсутствии достаточной компенсации тиреотоксикоза. Эффект испльзования препарата носит преходящий характер, нередко наблюдается постепенный возврат симптомов тиреотоксикоза с развитием рефрактерное™ к йоду и другим антитиреоидным средствам. Препараты йода лишь в редких случаях могут быть использованы как самостоятельный метод лечения. Из этих лекарственных веществ чаще применяют диийодтирозин по 0,05 г три раза в день (курсами), и раствор Люголя. В качестве самостоятельного лечения при легкой и средней тяжести тиреотоксикоза в отдельных случаях используется карбонат лития. Он непосредственно ингибирует синтез гормонов в железе и влияет на периферический обмен тиронинов. Условием для успешного медикаментозного лечения является увеличение железы до 3 степени. Лечение тиреостатическими препаратами, по данным разных авторов, даёт стойкий терапевтический эффект лишь в 40-50% клинических наблюдений, у лиц юношеского возраста ещё ниже - от 19 до 27%. Учитывая патогенетические механизмы формирования кардио-васкулярных нарушений при ДТЗ, наряду с вышеперечисленными препаратами, применяют бета-адреноблокаторы (индерал, обзидан, анаприлин). В лечении ДТЗ широко используют кортикостероиды. Положительный эффект их применения обусловлен компенсацией относительной надпочечниковой недостаточности при ДТЗ, влиянием на ме таболизм тиреоидных гормонов, а также иммунодепрессивным действием. Для воздействия на иммунные нарушения, лежащие в основе патологического процесса, помимо кортикостероидов, применяют иммунокорригирующую терапию - левамизол (декарис), курсами в течение 4-6 месяцев под контролем анализов крови. Комплексное лечение ДТЗ проводится на фоне седативной терапии (седуксен, тазепам, элениум). Лечебное применение йод -131. Показания к терапии радиоактивным иодом являются: лечение должно проводиться в возрасте старше 40 лет; наличие тяжелой сердечной недостаточности у больных, при которой хирургическое лечение рискованно; сочетание ДТЗ с туберкулезом, тяжелой гипертонической болезнью, перенесенным инфарктом миокарда, нейропсихическими расстройствами, геморрагическим синдромом; рецидив тиреотоксикоза после субтотальной резекциии щитовидной железы; категорический отказ больного от оперативного вмешательства на железе. Противопоказанием к лечению йод-131 считают беременность, период лактации, детский, юношеский и молодой возраст; большая степень увеличения щитовидной железы или загрудинное расположение зоба; заболевания крови, почек и язвенная болезнь желудка и 12-перстной кишки. При расчете терапевтической дозы на 1 гмассы щитовидной железы у больных со среднетяжелым течением тиреотоксикоза необходимо вводить от 60-70 мкКи, а при тяжелом и лицам более молодого возраста до 100 мкКи. Причем расчет первоначальной дозы при всех формах заболевания не должен превышать 4-8 мКи. Критерием оценки лечебного эффекта йода-131 является функциональное состояние щитовидной железы, определяемое по содержанию тироксина, трийодтиронина, ТТГ, тесту с тиролиберином или включение в щитовидную железу Тс-99. Лечение тиреотоксического криза проводится в условиях реанимационных отделений и заключается в использовании охлаждающих процедур (холодные ванны, обертывания влажными полотенцами или простынями). Из препаратов применяют Б-адреноблокаторы, раствор йодида калия (по 5 капель внутрь каждые 8 часов), дексаметазон (2-4 мг каждые 6 часов). Проводят инфузионную и посиндромную терапию. В тяжелых случаях осуществляют перфузионную детоксикацию. Оперативное лечение. Хирургическое лечение тиреотоксикоза начали применять с того момента, когда было установлено, что щитовидная железа играет ведущую роль в возникновении и развитии гипертиреоидизма. Всеобщее признание, как радикальный метод лечения гипертиреоидизма, тиреоидэктомия получила в 1884 году, когда Miculicz предложил свой хирургический метод, состоящий в двусторонней клиновидной резекции щитовидной железы после перевязки верхних щитовидных артерий. Kocher в 1902 году разработал более радикальный оперативный метод, считающийся классическим, состоящий в субтотальной резекции щитовидной железы после перевязки 4 щитовидных артерий. У оперированных таким способом больных рецидивы тиреотоксикоза резко уменьшились. На сегодняшний день оперативное лечение тиреотоксикоза, несмотря на конкурентность тиреостатической и радиоизотопной терапии, воспринимается как самый надежный, самый быстрый и практически самый безопасный лечебный метод, приводящий к окончательному выздоровлению 95-97% больных с восстановлением трудоспособности. Рецидивы после хирургического лечения значительно более редки (1-3%), чем при лечении радиоактивным йодом (17%). Послеоперационные осложнения при хорошей оперативной технике и предоперационной подготовке можно свести к минимуму. Показания к оперативному лечению: • При всех средних и тяжелых формах тиреотоксикоза у больных моложе 40 лет, у которых консервативное лечение тиреостатиками в продолжение 4-6 месяцев оказалось безрезультатным. • При тиреотоксикозе в детском возрасте, так как этот вид лечения не приводит к нарушениям роста и умственного развития детей. • При средних и тяжелых формах тиреотоксикоза диффузным высокостепенным зобом (3 и 4 ст.), у которых консервативное лечение не дало удовлетворительных результатов. • При ретростернальных или интраторакально расположенных зобах, зобах больших размеров, вызывающих сдавление органов шеи (пищевода, кровеносных сосудов и т. д.). • При тиреотоксикозе, осложнившемся сердечно-сосудистыми поражениями, которые после операции часто проходят. • При отсутствии стойкой компенсации на фоне проводимой консервативной терапии. • При непереносимости тиреотоксических препаратов. Обязательным условием проведения хирургического вмешательства является тщательная предоперационная подготовка, целью которой является достижение эутиреоидного или близкого к нему состояния: уменьшение тахикардии, нормализация артериального давления, увеличение массы тела, нормализация психоэмоционального состояния. Подготовка проводится тиреотоксическими препаратами в комбинации с кортикостероидами и бета-блокаторами.
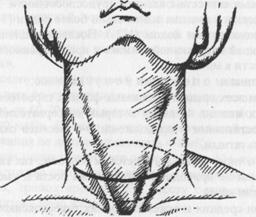
Оперативные вмешательства на щитовидной железе при ДТЗ предпочтительнее проводить под эндотрахельным наркозом. Оперативный доступ представлен на рис.3.
ß Рис. 3. Оперативный доступ при струмэктомии. Операции при диффузном токсическом зобе относятся к тяжелым вмешательствам, так как при нем в железе заметно увеличивается количество сосудов и понижается свертываемость крови. В прошлом эти операции относились к самым кровавым. Основоположником тиреоидной хирургии по праву считается Кохер. В 1902 году он предложил свой радикальный метод лечения тиреотоксикоза путем перевязки 4 щитовидных артерий и субтотальной экстрафасциальной резекции обеих долей щитовидной железы. При тяжелых формах базедовой болезни Кохер проводил перевязку щитовидных артерий в 2-3 этапа, а резекцию щитовидной железы - через некоторое время, после стихания тиреотоксического синдрома. Ткань, остающаяся в культях резецированной этим способом железы, обычно весит 4-6 г. С тех пор оперативный метод Кохера постоянно усовершенствовался. Метод Кохера обусловил значительное число послеоперационных рецидивов тиреотоксикоза (24% по данным Кохера). Во избежание последних было создано множество оперативных способов и модификаций для радикального лечения гипертиреоидизма. Наиболее важные из них: метод Зудека (состоит в тотальном удалении щитовидной железы; метод Зауэрбруха (состоит в субтотальной струмэктомии по способу Кохера с одновременным удалением вилочковой железы); способ Йонеску (субтотальная резекция щитовидной железы по Кохеру и удалением звездчатого узла симпатического ствола) и др. В настоящее время при оперативном лечении базедовой болезни используют только методы Кохера и О.В.Николаева в некоторых модификациях. Метод Кохера применяется большинством хирургов Западной Европы и Америки.
Рис. 4. Субфасциальная струмэктомия по Николаеву а) мобилизация правой доли щитовидной железы
Для доступа к щитовидной железе большинство хирургов используют воротниковой разрез, предложенный Кохером. Его проводят на 1-2 см выше края рукоятки грудины по ходу нижней кожной складки шеи. Длина кожного разреза варьирует в зависимости от размеров зоба (в среднем 8-10 см). Во время струмэктомии и после нее могут быть следующие осложнения: кровотечение, ранения трахеи и пищевода, трахеомаляция, повреждение возвратного нерва (0,1-4-6 %) и околощитовидных желез с развитием гипопаратиреоза (0,57-0,8 %), тиреотоксический криз (0,48-1,4 %), гипотиреоз. Гипотиреоз после операции по поводу ДТЗ развивается по данным эндокринологического научного центра РАМН до 68 % клинических наблюдений, в основном в течении первого года после операции, чаще у мужчин и пожилых женщин. Диагносцируется гипотиреоз клинически и по уровню гормонов щитовидной железы в крови; корригируется введением гормонов. Дата добавления: 2015-01-18 | Просмотры: 2637 | Нарушение авторских прав |
 По мнению многих хирургов, занимающихся данной проблемой, сейчас практически не существует противопоказаний к оперативному вмешательству при тиреотоксикозе. Наличие сердечнососудистой, печеночной, почечной и дыхательной недостаточности у больных базедовой болезнью на современном этапе развития эндокринологии и хирургии являются временными и преодолимыми.
По мнению многих хирургов, занимающихся данной проблемой, сейчас практически не существует противопоказаний к оперативному вмешательству при тиреотоксикозе. Наличие сердечнососудистой, печеночной, почечной и дыхательной недостаточности у больных базедовой болезнью на современном этапе развития эндокринологии и хирургии являются временными и преодолимыми.
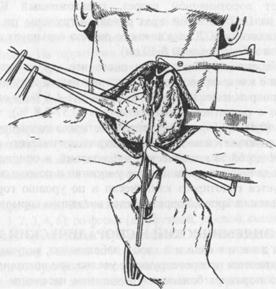
 В нашей стране чаще всего применяется метод О.В.Николаева (субтотальная субфасциальная резекция щитовидной железы) (рис. 4) из-за своей радикальности и безопасности повреждения околощитовидных желез и возвратных нервов. Операция производится в поле, находящемся кнутри от расположения этих образований. Метод Николаева основывается на анатомических исследованиях фасциального строения шеи и щитовидной железы. Автор исходил из того, что 4-ая фасция шеи (по Шевкуненко) своим висцеральным листком плотно охватывает щитовидную железу, покрывая ее подобно настоящей капсуле, не давая перегородок, проникающих в ее паренхиму. Париетальный листок этой фасции делает дупликатуру висцерального листка, покрывая еще раз щитовидную железу. Выделение щитовидной железы по О.В.Николаеву производят под самим висцеральным листком 4 фасции. С железы осторожно снимают висцеральную оболочку. При этом щитовидная железо, кровоточит умеренно, т.к. там располагаются только тонкие веточки щитовидных артерий, проникающие в паренхиму железы. Преимущество метода Николаева состоит в том, что выделение щитовидной железы производится кнутри от расположения околощитовидных желез и возвратных нервов. Таким оперативным способом избегают тяжелых осложнений резекции щитовидной железы - тетании и афонии. От каждой доли сохраняют маленькие участки тиреоидной ткани, размером приблизительно 2-2,5 х 1,5 х 0,3 см, весом от 1-3 г до 4-6 г с каждой стороны. Величина оставляемой паренхимы строго индивидуализируется в зависимости от тяжести тиреотоксического синдрома. Большинство авторов считает, что оптимальный суммарный остаток ткани щитовидной железы должен составлять 4-8 г. Наиболее объективным методом определения объёма оставляемой ткани является интраоперационное УЗИ.
В нашей стране чаще всего применяется метод О.В.Николаева (субтотальная субфасциальная резекция щитовидной железы) (рис. 4) из-за своей радикальности и безопасности повреждения околощитовидных желез и возвратных нервов. Операция производится в поле, находящемся кнутри от расположения этих образований. Метод Николаева основывается на анатомических исследованиях фасциального строения шеи и щитовидной железы. Автор исходил из того, что 4-ая фасция шеи (по Шевкуненко) своим висцеральным листком плотно охватывает щитовидную железу, покрывая ее подобно настоящей капсуле, не давая перегородок, проникающих в ее паренхиму. Париетальный листок этой фасции делает дупликатуру висцерального листка, покрывая еще раз щитовидную железу. Выделение щитовидной железы по О.В.Николаеву производят под самим висцеральным листком 4 фасции. С железы осторожно снимают висцеральную оболочку. При этом щитовидная железо, кровоточит умеренно, т.к. там располагаются только тонкие веточки щитовидных артерий, проникающие в паренхиму железы. Преимущество метода Николаева состоит в том, что выделение щитовидной железы производится кнутри от расположения околощитовидных желез и возвратных нервов. Таким оперативным способом избегают тяжелых осложнений резекции щитовидной железы - тетании и афонии. От каждой доли сохраняют маленькие участки тиреоидной ткани, размером приблизительно 2-2,5 х 1,5 х 0,3 см, весом от 1-3 г до 4-6 г с каждой стороны. Величина оставляемой паренхимы строго индивидуализируется в зависимости от тяжести тиреотоксического синдрома. Большинство авторов считает, что оптимальный суммарный остаток ткани щитовидной железы должен составлять 4-8 г. Наиболее объективным методом определения объёма оставляемой ткани является интраоперационное УЗИ. Рис. 4. б) рассечение перешейка
Рис. 4. б) рассечение перешейка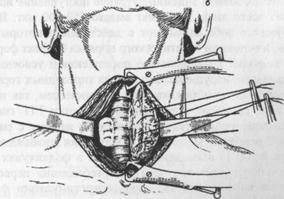
 Рис. 4. в) формирование культи резецированной доли железы
Рис. 4. в) формирование культи резецированной доли железы