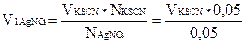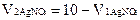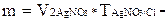|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Визначення хлоридів по методу ФольгардаДо виданого в мірній колбі розчину хлориду натрію додаємо до мітки дистильованої води, виливаємо в іншу колбу. Добре перемішуємо. Відбираємо піпеткою Мора 5 мл розчину і поміщаємо в конічну колбу, додаємо 2,5 мл 6н HNO3. Потім додаємо з бюретки 10мл 0,05н розчину AgNO3. Потім додаємо 1мл чистого нітробензолу, 0,5мл індикатора і сильно взбовтуємо, щоб викликати коагуляцію осаду. Надлишок нітрату аргентуму відтитровують 0,05н тіоціанатом калію до появи червоно-коричневого забарвлення. Вміст хлоридів у наважці розраховують наступним чином. 1. Шукаємо, скільки мілілітрів розчину AgNO3 пішло на зворотнє титрування KSCN.
2. Шукаємо кількість мілілітрів AgNO3 витрачених на осадження Cl-, врахувавши, що додавали в колбу 10мл титрованого розчину нітрату аргентуму
3. Обчислюємо вміст Cl- за формулою
1. Для розрахунку вмісту хлоридів у всій наважці, домножуємо значення m на 10, бо для титрування брали 1/10 загального об’єму розчину.
Завдання для контролю кінцевого рівня знань В методах осадження використовують реакції: а) комплексоутворення; б) осадження; в) всі можливі реакції. В способі Мора індикатором є: а) дихромат калію; б) залізо-амонійні квасці; в) хромат калію. Робочим розчином меркуриметрії є: а) Нg(NO3)2; б) Нg2(NO3)2; в)НgSO4. Способом Фольгарда визначення ведуть у: а) нейтральному середовищі; б) лужному середовищі; в) кислому середовищі. В методах осадження головною вимогою до осадів є: а) осад повинен бути практично нерозчинним; б) осад повинен бути дрібнокристалічним; в) осад повинен мати якомога більшу еквівалентну масу. Точність методів осадження визначається: а) кількість робочого розчину; б) повнотою осадження визначуваного тону; в) кислотністю середовища. Індикатором способу Фольгарда є: а) хромат калію; б) залізо-амонійні квасці; в) без індикатора. Робочим розчином меркурометрії є: а) Нg(NO3)2; б) Нg2(NO3)2; в)НgSO4. Способом Мора титрування в: а) нейтральному чи слабо лужному середовищі; б) нейтральному чи слабокислому середовищі: в) не залежить від середовища; Закінчіть рівняння реакції: Аg2СrО4 + 2Сl- = а) Аg + СгO42- + 2С1-; б) АgС1 + СrO42-; в) 2АgС1 + СrO42-. Дата добавления: 2015-02-05 | Просмотры: 1176 | Нарушение авторских прав |