|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Синдром хронической абдоминальной ишемииХроническое нарушение висцерального кровообращения — это заболевание, для которого характерны ише-мические расстройства кровообращения органов брюшной полости вследствие различных нарушений проходимости висцеральных артерий. В литературе эта нозологическая форма больше известна под термином angina abdominalis, впервые предложенным Васеlli (1903). Механизм происхождения болей идентичен стенокардии напряжения и связан с недостатком притока крови к активно функционирующим органам брюшной полости вследствие нарушения кровотока по измененным висцеральным артериям. История изучения патологии висцеральных ветвей брюшной аорты началась в 1843 г., когда немецкий патологоанатом Tiedemann на вскрытии выявил бессимптомную окклюзию верхней брыжеечной артерии. В 1869 г. Chiene на вскрытии обнаружил окклюзию всех трех висцеральных артерий у больной, умершей от разрыва аневризмы брюшной аорты. На развитие абдоминальных болей в результате недостаточности кровоснабжения кишечника указывали Schnitzler (1901), Pal (1905), Warburg (1905) и др. Perutz (1908) утверждал, что появление болей в животе при диффузном атеросклерозе свидетельствует об окклюзионных поражениях мезентериальных артерий, и их следует расценивать, как angina abdominalis. Goyet (1912) настаивал на том, что боли в животе возникают вследствие ишемии кишечника, вызванной сосудистыми атеромами. Schnitzler (1901) впервые систематизировал симптоматику, наблюдающуюся у больных с синдромом хронической абдоминальной ишемии и выделил триаду симптомов: боли в животе, дисфункция кишечника, прогрессирующее похудание. ВасеШ (1903) подтвердил возмож- ность развития абдоминальных болей при атеросклеротических окклю-зирующих поражениях висцеральных ветвей аорты. При этом автор высказал предположение о возможности их единого генеза с болями, наблюдаемыми при angina pectoris, в результате ишемии миокарда. Учитывая, что клинически эти патологические процессы сопровождаются болями, автор предложил называть симптоматику, проявляющуюся при недостаточности висцерального кровообращения, по аналогии термином angina abdominalis. Поворотным этапом в изучении хронических окклюзирующих поражений висцеральных ветвей брюшной аорты стали разработка и внедрение в практику рентгеноконтраст-ных методов исследования сосудов. В 1959 г. Mikkelsen и Zaro с помощью ангиографии выявили стеноз верхней брыжеечной артерии, а несколько раньше, в 1958 г., Shaw и Maynard сообщили об успешной трансаортальной эндартерэктомии из верхней брыжеечной артерии. В России первая успешная операция на висцеральных артериях (протезирование чревного ствола) была произведена А.В. Покровским (1962). Вопрос о терминологии в литературе до сих пор полностью не разрешен. Известно более 20 терминов, определяющих указанный симпто-мокомплекс. Наиболее известными из них являются "брюшная ангина", "интестинальная ангина", "мезенте-риальная интестинальная недостаточность", "хроническая ишемия кишечника", "абдоминальный ишемический синдром", "хроническая ишемия органов пищеварения" и др. Термин "синдром хронической абдоминальной ишемии", предложенный А.В. Покровским и П.О. Казанчяном (1979), наиболее точно отражает патогенез заболевания.
9 - 4886
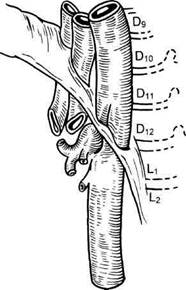
Частота заболевания точно не известна. По данным вскрытий, частота поражения висцеральных артерий колеблется от 18,7 до 76 % общего числа патологоанатомических наблюдений [Курбангалиев СМ. и др., 1974; Menon, Gratt, 1983; Bangash, 1990], в то время как при ангиогра-фическом исследовании частота обнаружения поражения висцеральных артерий достигает 10—77 % [Покровский А.В., 1979; Hansen et al, 1983; Ernst etal, 1993]. Конечно, частота выявленных поражений зависит и от контингента изучаемых больных, поэтому многие авторы отмечают, что общая частота клинического проявления поражений висцеральных артерий значительно меньше и колеблется от 2 до 36,5 % [Покровский А.В. и др., 1989; Olbbert et al., 1990]. Операции при этой патологии в среднем составляют 2 % всех операций на брюшной аорте и ее ветвях. Патофизиология кровообращения. Физиология висцерального кровообращения характеризуется тем, что Рис. 6.38. Чревно-брыжеечный анастомоз (малая дуга Риолана) при окклюзии чревного ствола. Путь коллатерального кровотока из верхней брыжеечной артерии указан стрелками. фактически все три висцеральные артерии еще в период внутриутробного развития составляют как бы единый сосуд. Три непарные ветви (чревный ствол, верхняя брыжеечная и нижняя брыжеечная артерии) соединяются между собой, образуя потенциально существующий единый сосудистый путь кровотока, по которому кровь может двигаться в любом направлении (каудальном и краниальном), подчиняясь законам гидродинамики (от большего в сторону меньшего артериального давления). Такое единство сосудистой системы органов брюшной полости обусловлено наличием врожденных коллатеральных анастомозов (внутрисистемные анастомозы). Чревно-брыжеечный анастомоз (малая дуга Риолана), обеспечивающий коллатеральные связи бассейна чревного ствола и верхней брыжеечной артерии и осуществляющий компенсацию дефицита кровотока в этих артериях соответственно в краниальном или каудальном направлениях, формируется за счет ветвей поджелудочно-двенадцатиперстного комплекса: верхняя панкреатодуоде-нальная артерия, являющаяся ветвью чревного ствола, огибая головку поджелудочной железы по ее периметру, анастомозирует с нижней панкреато-дуоденальной артерией, второй ветвью верхней брыжеечной артерии (рис. 6.38). Путь кровотока следующий: a.coeliaca — a. gepatica communis — a.gastro-duodenalis — a.pancrea-ticoduodenalis superior (из бассейна чревного ствола) — a.pancreatico-duodenalis inferior — a.mesenterica superior (в бассейн верхней брыжеечной артерии). Межбрыжеечный анастомоз, осуществляющий коллатеральные связи верхней и нижней брыжеечной артерий, формируется за счет анастомозов верхней брыжеечной артерии с нижней брыжеечной артерией (рис. 6.39). Прямой межбрыжеечный анастомоз известен в литературе как дуга Риолана. Последняя хорошо развита в
85 % случаев. Важным связующим звеном верхней и нижней брыжеечных артерий является краевая маргинальная артерия Дрюмонда. В области селезеночного угла толстой кишки левая ободочная ветвь средней ободочной артерии из системы верхней брыжеечной артерии анастомо-зирует с левой ободочной артерией из системы нижней брыжеечной артерии: a.mesenterica superior — a.colica media (из системы верхней брыжеечной артерии) — a.colica sinistra — a.mesenterica inferior (в систему нижней брыжеечной артерии). Это так называемая точка Гриффита — критический сегмент в области селезеночного угла толстой кишки. У 15 % людей анатомически межартериальные анастомозы врожденно не развиты и бассейны кровотока верхней и нижней брыжеечной артерий разомкнуты, что создает реальные предпосылки для ишемии именно селезеночного угла толстой кишки при любом снижении перфузионного давления в системе брыжеечных артерий. Таким образом, за счет чревно-брыжеечного и межбрыжеечного анастомозов кровообращение во всех трех висцеральных артериях тесно взаимосвязано и представляет собой как бы единый сосудистый бассейн. В норме органы брюшной полости содержат 25—35 % крови всего организма, при этом в печени и портальной системе — 65 % этого количества и еще 10 % в селезенке. Только 25 % находится в сосудах желудка, кишечника и поджелудочной железы. В целом висцеральный кровоток составляет приблизительно 1,3—1,5 л/мин (чревный ствол — 700—750 мл/мин, верхняя брыжеечная артерия — 450— 500 мл/мин, нижняя брыжеечная артерия — 150—200 мл/мин). В процессе пищеварения направление кровотока варьирует. Сначала основная масса крови направляется в бассейн чревного ствола, затем поочередно в бассейн верхней и нижней брыжеечной артерий.
Рис. 6.39. Межбрыжеечный анастомоз (дуга Риолана) при окклюзии нижней брыжеечной артерии. Путь коллатерального кровотока из верхней брыжеечной артерии указан стрелками. При ишемии в первую очередь страдает слизистый и подслизистые слои желудочно-кишечного тракта, развивается дистрофия железистого аппарата, что приводит к снижению продукции активных пищеварительных ферментов. Однако степень выраженности ишемии зависит от изменения объемной скорости кровотока в висцеральных артериях и степени ее компенсации. При стенозе или окклюзии одной или нескольких висцеральных артерий меняется направление кровотока по коллатералям. Так, при окклюзии верхней брыжеечной артерии в первую очередь изменяется направление кровотока по панкреато-дуоденальным анастомозам, и кровь из чревной артерии поступает в систему верхней брыжеечной артерии
9*
Рис. 6.40. Стеноз чревного ствола и окклюзия верхней брыжеечной артерии (левая боковая проекция). Заполнение бассейна верхней брыжеечной артерии осуществляется из чревного ствола за счет чревно-брыжеечного анастомоза. (рис. 6.40). При окклюзии чревного ствола компенсация кровотока осуществляется из системы верхней брыжеечной артерии через те же панкре-атодуоденальные анастомозы, по которым кровоток осуществляется уже в краниальном направлении. При этом компенсация кровотока в системе чревной артерии меняется в зависимости от того, в каком участке желудочно-кишечного тракта идет пищеварение. Так, при переваривании пищи в желудке компенсаторный кровоток из системы верхней брыжеечной артерии по объему большой. Затем, когда пища поступает в тонкую кишку (бассейн кровоснабжения верхней брыжеечной артерии), вся кровь направляется к ней. В это время верхняя брыжеечная артерия уже не может отдать часть крови в бассейн стенозированной чревной артерии, поэтому в бассейне чревно- го ствола, несмотря на наличие кол-латералей, наступает дефицит кровотока из-за недостаточного сброса крови из системы верхней брыжеечной артерии. При стенозе или окклюзии нижней брыжеечной артерии коллатеральный кровоток осуществляется за счет верхней брыжеечной артерии по дуге Риолана. При одновременной окклюзии верхней и нижней брыжеечных артерий вся компенсация осуществляется за счет чревной артерии и ка-удального направления кровотока по коллатералям. В случаях же одновременной окклюзии чревной и верхней брыжеечной артерий компенсация нарушенного висцерального кровотока осуществляется из нижней брыжеечной артерии в краниальном направлении через дугу Риолана, а затем панкреатодуоденальные анастомозы (рис. 6.41). Существует еще один вариант висцерального кровообращения при окклюзии брюшной аорты. В этих случаях нижняя брыжеечная артерия благодаря ее анастомозам с внутренними подвздошными артериями осуществляет кровоснабжение органов таза и нижних конечностей. Наблюдается специфический steal syndrome (синдром обкрадывания) висцерального кровообращения (рис. 6.42). Если проксимальные висцеральные артерии (чревный ствол, верхняя брыжеечная артерия) не поражены, то этот дефицит кровотока обычно хорошо компенсируется. Однако при окклюзии нижней брыжеечной артерии происходит двойное "обкрадывание" бассейна проксимальных висцеральных ветвей. В момент физической нагрузки на нижние конечности резко обедняется висцеральный кровоток (за счет aorto-iliac steal-синдрома и внутри-висцерального обкрадывания). При экстравазальном сдавлении чревной артерии кровообращение в ее системе нарушается не только за счет снижения объемной скорости кровотока, но и вследствие рефлек- /
Рис. 6.41. Серийные ангио-граммы больного неспецифическим аортоартерии-том с окклюзией чревного ствола и верхней брыжеечной артерии (прямая проекция). Кровоснабжение кишечника осуществляется из нижней брыжеечной артерии ретроградно в краниальном направлении. Первоначально заполняется бассейн верхней брыжеечной артерии (через дугу Риолана), затем — чревного ствола (чревно-брыжеечный анастомоз). торного спазма дистального сосудистого русла. При наличии атеросклеротичес-кой бляшки в устье висцеральной артерии нельзя исключить еще один механизм нарушения кровообращения в ее бассейне — микроэмболии кусочками тромба или бляшки. Этиология. Синдром хронической абдоминальной ишемии обусловлен функциональными, органическими и комбинированными причинами поражения сосудов. К функциональным изменениям следует отнести артериоспазм, гипо-тензии центрального происхождения, гипогликемии, лекарственные заболевания, полицитемии. Органические изменения могут быть обусловлены большой группой врожденных и приобретенных причин поражения (по классификации А.В. Покровского, 1979), каждая из которых включает экстравазальные и интравазальные факторы. Врожденные экстравазальные причины, как правило, обусловливают патологию чревной артерии. К ним следует отнести аномальное отхож-дение чревного ствола своего обыч- ного анатомического варианта, синдром "вожжей" (нижние диафрагмаль-ные артерии отходят), сдавление
Рис. 6.42. Ангиограмма больного с высокой окклюзией брюшной аорты (атеросклероз). Возникает внутривисцеральное обкрадывание бассейнов чревной и верхней брыжеечной артерии за счет кровоснабжения органов таза и артерий нижних конечностей. чревной артерии элементами диафрагмы (медиальная ножка и серповидная связка) и некоторые другие. Приобретенные экстравазальные причины могут быть обусловлены сдавлением артерии опухолями пан-креатодуоденальной зоны, рубцами (периартериальный фиброз), аневризмой брюшной и торакоабдоми-нальной аорты. Врожденные интравазальные причины нарушения кровообращения по висцеральным артериям встречаются редко (аплазия, гипоплазия висцеральных артерий, фибромышечная дисплазия). Основную роль в генезе развития синдрома хронической абдоминальной ишемии отводят приобретенным интравазальным причинам, к которым в первую очередь относят атеросклероз. Второе место среди этиологических факторов принадлежит неспецифическому аортоартерииту. Из других заболеваний, обусловливающих интравазальные приобретенные поражения висцеральных артерий, следует отметить облитери-рующий тромбангиит, узелковый пе-риартериит, системную красную волчанку и др. С учетом существенного повышения частоты травматических (колото-резаных и огнестрельных) повреждений, особенно в последние годы, резко возрастает значение травматических артериовенозных свищей висцеральных артерий в патогенезе развития синдрома хронической абдоминальной ишемии. B.C. Савельев и соавт. (1999) отдельно выделяют ишемическую дисфункцию органов пищеварения, наблюдающуюся при полной интакт-ности магистральных висцеральных артерий, но возникающую на фоне изолированных нарушений микро-циркуляции при дислипопротеиде-мии, которую, по мнению автора, можно рассматривать как отдельную форму ишемической болезни органов пищеварения со своими особен- ностями диагностики и клинического течения. Течение заболевания. Окклюзиру-ющие поражения висцеральных ветвей аорты вызывают различную степень циркуляторных расстройств в органах пищеварения. И это вполне закономерно, поскольку они различны по своему генезу, локализации и объему поражения, развиваются у лиц с неодинаковыми компенсаторными возможностями коллатерального кровообращения. Эти факторы обусловливают наличие определенных стадий в течении поражений висцеральных ветвей и циркуляторных расстройств, развившихся в органах пищеварения. В течении хронических нарушений висцерального кровообращения выделяют три стадии: 1) компенсированную, или доклиническую; 2) стадию субкомпенсации; 3) стадию декомпенсации. Компенсированная стадия свидетельствует о функционально незначимой степени стенозирования артерий либо о наличии хорошего коллатерального кровообращения, обеспечивающего переток достаточного количества крови в бассейн пораженной магистрали. В этой стадии ишемия как таковая в органах пищеварения отсутствует. Адекватность кровоснабжения органов всех трех артериальных бассейнов сохранена. Поражения висцеральных ветвей в этой стадии выявляются случайно, при обследовании больных по поводу патологии аорты и других ее ветвей. По мере прогрессирования окклю-зирующего процесса и снижения компенсаторных возможностей коллатерального кровообращения имеющееся равновесие нарушается. Появляются начальные признаки ишемии органов пищеварения. Первоначально они обнаруживаются на высоте их функциональной активности — при переваривании пищи, когда органы брюшной полости находятся в состоянии активной функциональной деятельности. В нормальных условиях благодаря перераспределению кровотока между различными артериальными бассейнами и направлению кровотока к органам, находящимся в функционально активном состоянии, приток крови к органам брюшной полости на высоте пищеварения увеличивается (в среднем на 32 %). Весь этот процесс регулируется сложными нервно-рефлекторными и гуморальными механизмами. При наличии окклюзии одной или двух висцеральных ветвей дефицит кровотока компенсируется благодаря возрастающей функциональной активности коллатерального висцерального кровообращения. Появление абдоминального симп-томокомплекса свидетельствует о срыве компенсаторных возможностей коллатерального кровообращения и наступлении следующей стадии в течении заболевания — стадии субкомпенсации висцерального кровообращения. Первоначально возникшие клинические симптомы, появлявшиеся лишь при функциональной нагрузке на органы пищеварения, постепенно нарастают и возникают в дальнейшем даже при минимальной физиологической нагрузке на пищеварительный тракт, а порой и сохраняются вне акта пищеварения — в состоянии функционального покоя органов брюшной полости, что свидетельствует о наличии постоянного дефицита в кровоснабжении органов пищеварения и о наступлении стадии декомпенсации. В этой стадии обычно отчетливо проявляются, как правило, все симптомы хронической абдоминальной ишемии: боль в животе после приема пищи, нарушение абсорбционной и моторной функций кишечника и прогрессирующее похудание. Поражение висцеральных артерий при атеросклерозе характеризуется тем, что атеросклеротическая бляшка чаще всего располагается в проксимальном сегменте артерии, как правило, на протяжении не более 1,5—2 см от устья и обычно переходит со стенки аорты. При этом заболевании значительно чаще в процесс вовлекается нижняя брыжеечная артерия, нежели чревный ствол и верхняя брыжеечная артерия. Напротив, для неспецифического аортоартери-ита более характерно одновременное поражение чревного ствола и верхней брыжеечной артерии. Характер подобных вовлечений идентичен атеросклеротическому — поражаются проксимальные сегменты указанных артерий. Как при атеросклерозе, так и при неспецифическом аортоартериите поражение только висцеральных артерий наблюдается очень редко. Как правило, они сочетаются с одновременным вовлечением в патологический процесс и брюшной аорты. Практическое значение имеет следующая закономерность: причиной изолированного поражения чревной артерии чаще всего является экстра-вазальная компрессия; верхняя брыжеечная артерия несколько чаще поражается неспецифическим аор-тоартериитом, чем атеросклерозом. Нижняя брыжеечная артерия преимущественно страдает при атеросклерозе. Экстравазальная компрессия и неспецифический аортоартериит чаще наблюдаются у женщин: атеросклероз, как известно, — болезнь мужчин. Течение синдрома хронической абдоминальной ишемии — неуклонно прогрессирующее. В связи с тем что приобретенные заболевания не могут оставаться стабильными всю жизнь больного и прогрессируют, то имеющаяся степень стеноза со временем постепенно увеличивается. При экстравазальной компрессии постоянная травма артерии приводит к ее рубцовому стенозу. Острое нарушение висцерального кровообращения — одно из закономерных последствий синдрома хронической абдоминальной ишемии. Клиническая картина. Понятием "синдром хронической абдоминальной ишемии" объединены клинические симптомы ишемии трех различных бассейнов: чревного ствола, верхней и нижней брыжеечных артерий. При гипотетически полной изоляции этих бассейнов, по-видимому, клиническая картина ишемии каждого из них была бы более очерченной и яркой. Однако наличие единой системы висцерального кровообращения в значительной степени смешивает клинику ишемии этих бассейнов, создает затруднения при проведении дифференциального диагноза за счет синдромов обкрадывания. Тем не менее можно выделить по преимущественным клиническим проявлениям четыре формы заболевания: • чревную (болевую); • проксимальную брыжеечную — проксимальная энтеропатия (дисфункция тонкой кишки); • дистальную брыжеечную — терминальная колопатия (дисфункция преимущественно левой половины толстой кишки); • смешанную. М.Р. Кузнецов и соавт. (1999) считают целесообразным выделение шести клинических вариантов течения синдрома хронической абдоминальной ишемии: эрозивно-язвен-ного, псевдопанкреатического, дис-кинетического, холецистоподобно-го, гастралгического и псевдотумо-розного. Основной жалобой больных при синдроме хронической абдоминальной ишемии является боль как результат ишемии органов пищеварения, которая ведет к гипоксии и метаболическим нарушениям. Последние передают раздражение в солнечное или верхнебрыжеечное нервное сплетение. При поражении чревной артерии болевой синдром связан и с гипоксией печени. Боль обычно появляется через 20—25 мин после приема пищи и продолжается 2—2,5 ч, т.е. в течение всего периода пассажа пи- щи через кишечник. Обычно боль стихает самостоятельно и возникает вновь при приеме пищи. В большинстве случаев боль локализуется в эпигастральной области и иррадиирует в правое подреберье (зона ишемии бассейна чревного ствола). Кроме того, она может локализоваться также в мезогастральной (бассейн верхней брыжеечной артерии) и в левой подвздошной (дефицит кровотока по нижней брыжеечной артерии) областях. Болевой синдром уменьшается при резком ограничении приема пищи — синдром малой пищи. Некоторые больные отмечают чувство постоянной тяжести в животе, особенно в эпигастральной области. Редко наблюдается рвота. Вторым основным симптомом хронической абдоминальной ишемии является дисфункция кишечника, выражающаяся нарушениями моторной, секреторной и абсорбционной функций. Выделяют две формы дисфункции кишечника при его хронической ишемии — проксимальную и терминальную энтеропатии. При поражении верхней брыжеечной артерии в основном страдают секреторная и абсорбционная функции кишечника, при окклюзии нижней брыжеечной артерии нарушается эвакуаторная функция толстой кишки. Эти изменения вначале проявляются в виде неустойчивого неоформленного, жидкого, зловонного стула, мучительного поноса плохо переваренной пищей, позывов на дефекацию вскоре после еды, чувства переедания, ощущения дискомфорта в кишечнике, метеоризма. Изнуряющий понос сменяется мучительным и стойким запором. В дальнейшем появляется вздутие живота. Проксимальная энтеропатия имеет три стадии: • ишемическая функциональная энтеропатия, при которой наблюдаются повышенная моторика, нарушения абсорбции и метеоризм на фоне усиленной перистальтики; • ишемическии энтерит с различной болью в животе, паралитической непроходимостью, рвотой, меленой, повышением СОЭ, лейкоцитозом, нейтрофилезом (изъязвления слизистой оболочки, отек подслизисто-го слоя, кровотечения); • преходящая ишемия тонкой кишки — формирование стриктур или инфаркта тонкой кишки. Терминальная колопатия также имеет три стадии развития: ▲функциональная ишемическая колопатия (вздутие живота, упорный запор, "овечий" стул); ▲ишемический колит (изъязвления слизистой оболочки кишки, отек под слизистого слоя, кровотечения); ▲преходящая ишемия толстой кишки, образование ишемических стриктур, а в терминальной стадии — развитие гангрены толстой кишки. Трем клиническим стадиям поражения кишки соответствует и глубина поражения ее стенки. Ишемия только слизистой оболочки приводит к обратимым изменениям — энтериту и колиту; ишемия слизистой оболочки и мышечного слоя — к фиброзу, Рубцовым изменениям и стриктурам; трансмуральная ишемия — к необратимому изменению стенки кишки с гангреной и перфорацией. Страдает и моторная функция, причем чаще наблюдается не усиление, а ее угнетение. При стенозе или окклюзии чревного ствола в клинической картине доминирует болевой синдром. Для поражения верхней брыжеечной артерии наиболее характерны вздутие живота и неустойчивый стул, для поражения нижней брыжеечной артерии — запоры. Третий основной симптом хронической абдоминальной ишемии — прогрессирующее похудание. Оно обусловлено несколькими факторами: во-первых, болевой симптом заставляет сократить объем, а затем и уменьшить частоту приемов пищи; во-вторых, резкие нарушения секреторной и абсорбционной функций кишечника также ведут к потере массы тела. В связи с этим похудание фактически обусловлено тремя факторами: алиментарным (отказ от еды, фобия перед едой и последствия нарушений секреторно-абсорбционной и моторной функций кишечника); обезвоживанием организма вследствие поноса, искусственно вызываемой рвоты, приема слабительных средств; вследствие болевого фактора. Некоторые больные жалуются на усиленную пульсацию в животе, другие — на боль в левой подвздошной области, возникающую при интенсивной ходьбе, что связано с обкрадыванием кровотока по нижней брыжеечной артерии. Выраженность клинической картины абдоминальной ишемии зависит от локализации и этиологии поражения, а также от сопутствующей артериальной гипертензии. Экстра-вазальная компрессия и атеросклероз почти всегда сопровождаются клиническими проявлениями. При неспецифическом аортоартериите клинические признаки обычно отсутствуют. Чем больше степень стеноза и объем поражения висцеральных артерий, тем выраженнее клиническая картина; чем старше больной, тем декомпенсация чаще. Клиника и стадия декомпенсации независимо от этиологии чаще наблюдаются у нормото-ников, нежели у гипертоников. Диагностика. Перечисленные не всегда характерные жалобы больных, анамнестические данные, убедительные признаки нарушения кровообращения в других артериальных бассейнах, неоднократные и безрезультатные обследования больных в различных по профилю лечебных учреждениях, а также безрезультатность проводимого нередко длительного лечения позволяют предположить диагноз синдрома хронической абдоминальной ишемии. Физикаль-ные методы исследования могут давать некоторые опорные пункты диагностики, но, как правило, они ма- лоинформативны у этих пациентов. Осмотр больных хронической абдоминальной ишемией не выявляет никаких специфических признаков заболевания, кроме похудания. Лишь у 50 % больных при аускультации выслушивается систолический шум, который при стенозе чревного ствола локализуется на 2—4 см ниже мечевидного отростка, при стенозе верхней брыжеечной артерии — на границе средней и нижней трети линии, соединяющей пупок с мечевидным отростком. Шум свидетельствует о возможном поражении артерии (стеноз от 70 до 90 %), но его отсутствие не является поводом для исключения поражения висцеральных ветвей. Целесообразно аускультировать больных в положении стоя и даже на корточках, так как при экстравазаль-ной компрессии в этих позициях может появиться шум в проекции чревного ствола. При аускультации больного со стороны спины, слева от позвоночника, усиление интенсивности систолического шума свидетельствует о том, что шум скорее всего исходит из аорты, а не из пораженных висцеральных артерий. Ослабление систолического шума сзади, очевидно, свидетельствует, что он является следствием поражения висцеральных артерий. Алиментарные провокационные пробы основаны на тесной взаимосвязи болевого синдрома или дисфункции кишечника с приемом пищи: • проба Миккельсена — в течение 1 ч больной должен выпить 1 л молока. Появление болей в животе свидетельствует об ишемическом генезе заболевания. Пробу используют как дифференциально-диагностический тест синдрома хронической абдоминальной ишемии и язвенной болезни желудка и двенадцатиперстной кишки; • проба "насильственного кормления" основана на ежедневном приеме высококалорийной пищи (5000 ккал), провоцирующей типичную клинику ишемии; • проба регулярного приема пищи обычной калорийности с исключением острых блюд (четырехразовое питание). Л.В. Поташев и соавт. (1985) предлагают проводить физические пробы — поднятие тяжестей, длительный физический труд в наклонном положении, быстрая ходьба, бег, велоэргометрическая проба — для выявления экстравазальной компрессии чревного ствола. Существуют также лекарственные пробы, провоцирующие синдром (вазоспастичес-кие средства) и ликвидирующие его (вазодилататоры). Из лабораторных методов исследования в первую очередь необходимо использовать такие, которые могли быть дать оценку абсорбционной и секреторной функциям кишечника, а также сведения о функции печени и поджелудочной железы. Стандартные биохимические методы исследования функционального состояния печени выявляют нарушение соотношения белковых фракций, снижение количества альбуминов и повышение концентрации глобулинов. Повышена также плотность де-фениламиновой реакции (ДФА), увеличены показатели АлАТ, активности ЛДГ и 5-оксииндолуксусной кислоты в моче. Проба с а-ксилозой определяет состояние абсорбции в проксимальном отделе тонкой кишки. В дис-тальных отделах тощей кишки состояние абсорбции определяется методом выведения витамина В12, меченного 58Со. Проба с а-ксилозой оказывается положительной приблизительно у Уз пациентов, с витамином В12 — у 40 % больных. Изучение желудочной секреции методом внутрижелудочной рН-мет-рии в состоянии покоя и на фоне максимальной стимуляции гистами-ном выявляет угнетение функции пилорических желез у больных с поражением чревного ствола и верхней брыжеечной артерии. При радиоизотопной гепатогра-фии выявляется нарушение функции полигональных клеток более чем у 50 % больных. Рентгенологическое исследование желудочно-кишечного тракта может выявить некоторые неспецифические изменения, в частности медленный пассаж бария по желудку и кишечнику, повышенное газообразование, дефекты наполнения кишечной стенки. В толстой кишке исчезают гаустры, замедляется опорожнение. Частым спутником поражения висцеральных ветвей являются язвы желудка и двенадцатиперстной кишки. Ирригоскопия выявляет неравномерное распределение и фрагментацию взвеси сульфата бария, длительную задержку его в кишке, исчезновение гаустраций в стенозированных отделах кишки. Выделяют такие рентгенологические признаки ишемии стенки толстой кишки, как дефекты наполнения, вызванные отечностью слизистой оболочки и кровоизлияниями в под слизистом слое и напоминающие "отпечатки пальцев" или "дымящую трубу". Между стенкой кишки и взвесью бария могут прослеживаться щелевидные участки просветления, обусловленные сегментарными спазмами и ригидностью кишки, находящейся в состоянии ишемии. Возможны сегментарные стенозы, которые выявляются в основном в селезеночном углу (точке Гриффита). При гастроскопии обычно диагностируют атрофический гастрит либо язвенную болезнь желудка. При колоноскопии обнаруживают диффузный или сегментарный колит с избыточной продукцией слизи, атрофию слизистой оболочки и нередко полипы. Реже видны эрозии в месте перехода нисходящей кишки в сигмовидную, сегментарные стенозы кишки с исчезновением гаустраций. Перифокальные изменения при эрозиях отсутствуют. При гистологическом исследовании биоптатов выявляют отек собственной пластинки слизистой обо- лочки, уменьшение количества крипт, развитие участков фиброза, дилата-цию и эктазию сосудов под слизистого слоя. Свидетельством диффузного хронического колита являются очаговые лимфоидно-клеточные инфильтраты в поверхностных слоях слизистой оболочки и подслизисто-го слоя. Копрологическое исследование свидетельствует о наличии в кале больных большого количества слизи, нейтрального жира, непереваренных мышечных волокон, соединительной ткани. При исследовании висцеральных артерий методом дуплексного сканирования можно работать в системе серой шкалы и получать изображение просвета и стенки сосудов в реальном масштабе времени, затем переходить в режим цветного доппле-ровского картирования потока на основании анализа скоростей кровотока либо энергии отраженного допплеровского сигнала в зависимости от клинической ситуации, а также регистрировать в импульсном режиме спектрограммы кровотока исследуемых сосудов. В клинике, руководимой А.В. Покровским, впервые проведено углубленное изучение возможностей ультразвуковой диагностики поражений висцеральных ветвей брюшной аорты (1982). Многолетние исследования свидетельствуют о том, что чувствительность дуплексного сканирования в определении поражений чревной и верхней брыжеечной артерий при сравнении с ангиографией составляет 71 %, а специфичность метода — 96 %. Исследование проводят в сагиттальном, продольном и поперечном направлениях. Качественный анализ спектрограмм чревного ствола свидетельствует о высоком уровне конечной диастолической скорости, непрерывном характере кровотока и звукового сигнала, что указывает на низкое периферическое сопротивление в бассейне этой артерии (рис. 6.43).
Рис. 6.43. Спектрограмма кровотока по чревному стволу в норме. Продольное сканирование в эпи-гастральной области позволяет получить изображение и верхней брыжеечной артерии, которая расположена
Рис. 6.44. Ультразвуковая эхограмма (продольное В-сканирование) брюшной аорты при атеросклерозе. Отчетливо прослеживается ствол верхней брыжеечной артерии. ниже чревного ствола, направляется каудально и визуализируется на протяжении 5—7 см от устья (рис. 6.44), однако в связи с тем, что устья чревной и верхней брыжеечной артерий располагаются не в одной проекции, не всегда можно визуализировать их на одном сагиттальном скане. В этом случае, получив хорошее изображение устья чревной артерии, датчик следует несколько ротировать против часовой стрелки для хорошей локации устья верхней брыжеечной артерии. Регистрацию же спектрограммы кровотока верхней брыжеечной артерии целесообразно проводить в устье, где угол между анатомическим ходом сосуда и ультразвуковым лучом не превышает 60°. Качественные характеристики спектра кровотока по верхней брыжеечной артерии отличаются снижением уровня конечной диастоличес-кой скорости, прерывистым звуковым сигналом, свидетельствующим о высоком периферическом сопротивлении в бассейне этой артерии (рис. 6.45). Независимо от причины, приводящей к сужению просвета артерии более чем на 60 %, у пациентов имеет место увеличение ЛСК с локальными изменениями кровотока, приобретающего турбулентный характер, что нашло подтверждение при анализе спектрограмм и цветно-
Рис. 6.45. Спектрограмма кровотока по верхней брыжеечной артерии в норме. го допплеровского картирования (рис. 6.46). В случаях окклюзии исследуемых артерий метод импульсной доппле-рографии не дает возможности зарегистрировать спектр кровотока, а цветное допплеровское картирование не окрашивает поток в сосуде. При ге-модинамически незначимом сужении сосуда информативность импульсной допплерографии существенно снижается, а оценку степени стеноза проводят, используя режим ЦДК, с расчетом процента стеноза по площади поперечного сечения или по диаметру. Существенными преимуществами ультразвукового исследования в сравнении с ангиографией являются, безусловно, неинвазивность метода и возможность проведения исследования в динамике, однако ультразвуковое исследование не дает информацию о состоянии нижней брыжеечной артерии в связи с малым ее диаметром и о характере коллате- рального кровотока (по ветвям, формирующим чревно-брыжеечный и межбрыжеечный анастомозы), в связи с чем отсутствует возможность оценки процессов компенсации между тремя непарными ветвями брюшной аорты. Заключительным и наиболее информативным методом диагностики является ангиография висцеральных артерий. Проведение аортографии обязательно в двух проекциях — передне-задней и левой боковой. Данные, полученные в боковой проекции, особенно важны, так как позволяют увидеть и оценить состояние устьев чревной и верхней брыжеечной артерий. Снимки только в одной перед-незадней проекции не могут быть признаны достаточно объективными. Предпочтительнее использовать методику Сельдингера, однако если у больных имеется поражение брюшной аорты и подвздошных артерий, то следует производить высокую
Рис. 6.46. Спектрограмма кровотока, зарегистрированная на участке стеноза ствола верхней брыжеечной артерии (турбулентный кровоток). транслюмбальную пункцию аорты на уровне ТhXII. Селективная мезентерикография информативна при поражении дис-тального отдела верхней брыжеечной артерии, при наличии второго блока, для оценки перетоков в систему чревного ствола и нижней брыжеечной артерии (чревно-брыжеечного и межбрыжеечного анастомозов). Выделяют прямые и косвенные ангиографические признаки поражения висцеральных артерий, фиксирующие перестройку висцерального кровообращения, развитие коллатеральных путей кровотока. К прямым признакам относят лишь те, которые выявляются в боковой проекции и неопровержимо свидетельствуют о вовлечении в процесс висцеральных артерий: • стеноз; • деформацию;
• окклюзию; • аневризму. При экстравазальной компрессии чревного ствола аорта и ее ветви обычно интактны. В боковой проекции ствол искривлен и образует угол, открытый кверху и кпереди. По верхнему контуру чревного ствола "фиксируется" стеноз в виде выемки. Нижний контур артерии обычно ровный. Дистальнее стеноза нередко выявляется постстенотическое расширение и возможен перегиб ствола. Чревный ствол приобретает форму песочных часов. Указанная ангиографическая картина характерна для компрессии чревного ствола срединной связкой диафрагмы (рис. 6.47—6.51). При сужении сосуда на протяжении можно предположить его компрессию медиальной ножкой диафрагмы или ганглиями солнечного сплетения. Часть чревного ствола, распола-
Рис. 6.47. Неспецифический аортоарте-риит (левая боковая проекция). Стеноз устья верхней брыжеечной артерии. Рис. 6.48. Экстравазальная компрессия чревного. ствола (левая боковая проекция).
Рис. 6.49. Неспецифический аортоартери-ит (прямая проекция). Определяется стеноз интер- и инфраренального сегментов аорты, обеих почечных артерий, стеноз чревного ствола и окклюзия верхней брыжеечной артерии. Резко расширена и извита нижняя брыжеечная артерия, функционирующая в краниальном направлении. Рис. 6.50. Неспецифический аортоартери-ит (прямая проекция). Окклюзия чревного ствола и верхней брыжеечной артерии. Видна резко расширенная нижняя брыжеечная артерия, участвующая в формировании межбрыжеечного анастомоза.
гающаяся проксимальнее сужения, как бы прижата к аорте, исчезает присущее ему расположение параллельно верхней брыжеечной артерии. Признаки атеросклеротических стенозов, а также поражений, обусловленных неспецифическим аортоар-териитом, не отличаются от таковых в других бассейнах. При неспецифическом аортоартериите выявляются резкое расширение и удлинение дуги Риолана. О поражении магистральных висцеральных артерий (в переднезадней проекции) косвенно свидетельствуют следующие ангиографические признаки: • расширение ветвей чревно-брыжеечного и межбрыжеечного анастомозов; • ретроградное заполнение ветвей и ствола окклюзированной магистрали; • превышение диаметра печеночной артерии над селезеночной, ха-
Рис. 6.51. Сдавление чревного ствола элементами диафрагмы. рактерное для стенозов чревного ствола; • более интенсивное контрастирование пораженной магистрали и ее ветвей; • отсутствие обратного сброса контрастного вещества в аорту. Два последних косвенных ангио-графических признака характерны только для селективной целиако- и мезентерикографии. Следует подчеркнуть, что лишь на основании объективных и лабораторных методов исследования, ультразвукового и ангиографического исследования не всегда представляется возможным составить окончательное представление о характере окклюзирующего процесса, о тяжести циркуляторных нарушений, иногда и о природе заболевания. Ответы на эти вопросы можно получить после интраоперационной ревизии висцеральных ветвей брюшной аорты, которая включает ревизию ветвей аорты; интраоперационную ультразвуковую допплерографию с определением функционального состояния дуги Риолана и флоуметрию; определение градиента артериального давления между аортой и висцеральными ветвями; ревизию органов брюшной полости. Диагноз синдрома хронической абдоминальной ишемии устанавливают на основании наличия характерной клинической симптоматики (боль в животе, дисфункция кишечника, прогрессирующее похудание), объективных симптомов, выявленных нарушений проходимости висцеральных артерий на основании комплексного ультразвукового и ангиографического исследования. Если больному не были произведены полноценное ультразвуковое исследование и ангиография, то диагноз нельзя ни поставить, ни отвергнуть. Большую помощь в правильной диагностике могут оказать следующие две особенности, присущие больным с синдромом хронической абдоминальной ишемии. Во-первых, это длительные, многократные и, главное, безрезультатные обследования больных в различных по профилю лечебных учреждениях и неэффективность проводимого лечения. Во-вторых, одновременное с висцеральными ветвями поражение других артериальных бассейнов (брахиоцефаль-ных артерий, артерий нижних конечностей, почечных артерий и др.), наблюдаемое обычно при атеросклерозе и неспецифическом аортоарте-риите [Казанчян П.О., 1979]. При проведении дифференциальной диагностики в первую очередь следует думать о возможности воспалительных заболеваний или злокачественного новообразования органов панкреатодуоденальной зоны. Для их исключения обязательно проведение ультразвукового исследования органов брюшной полости и за-брюшинного пространства, рентгенологических и эндоскопических исследований желудочно-кишечного тракта, радиоизотопных исследований печени и поджелудочной железы, а также компьютерной томографии, МРТ и др. Если у больного отмечаются сопутствующие поражения аорты и ее ветвей, то вероятность заинтересованности висцеральных артерий возрастает. Схожая клиническая симптоматика может наблюдаться при многих заболеваниях (язвенная болезнь, гастрит, холецистит, панкреатит, неспецифический язвенный колит, болезнь Крона, опухоли и пр.), однако ни при одном из них нет подобной ультразвуковой и ангиографической картины поражения висцеральных артерий. Лечение. Прогноз и показания к хирургическому лечению определяют на основании того, что органическое нарушение проходимости висцеральных артерий будет постепенно прогрессировать и имеющаяся ишемия органов пищеварения приведет сначала к функциональным, а затем и к структурным изменениям органов. Консервативное лечение хронической абдоминальной ишемии является симптоматическим и состоит из диетотерапии, лечения спазмолитиками, сочетающимися с применением широкого спектра препаратов, используемых в гастроэнтерологии. Больным рекомендуют соблюдать диету, принимать пищу часто и малыми порциями. Применение антикоагулянтов нецелесообразно. Очень важна правильно подобранная терапия, направленная на улучшение реологических свойств крови. При проведении терапии антиаг-регантными препаратами (ацетилсалициловая кислота, трентал, куран-тил, тиклид и др.) приходится решать вопрос о длительности лечения каждым препаратом антиагрегантного ряда и с чем следует сочетать данный препарат для повышения клинического эффекта. Считается, что при эффективности антиагрегантной терапии она должна быть длительной, нередко пожизненной и непрерывной. Продолжительность же лечения каждым препаратом определяется сохранением его эффективности при длительном приеме при отсутствии побочных реакций. Кроме того, существует большое количество препаратов, применение которых оправдано поливалентностью патогенеза синдрома хронической абдоминальной ишемии: нормализация липидного обмена (статины), антиоксидантной защиты (антиок-сиданты), метаболизма и прочих нарушений. Больные неспецифическим аор-тоартериитом и облитерирующим тромбангиитом в обязательном порядке должны пройти комплексное противовоспалительное лечение (терапия нестероидными противовоспалительными средствами, плазмафе-рез, гемосорбция, "пульс-терапия" ударными дозами цитостатиков и кортикостероидных препаратов). Терапия длительными курсами стероидных препаратов в малых дозах (30— 60 мг) противопоказана. Принципиально важны регулярность и сезонность комплексного противовоспалительного лечения (осенне-весенние периоды). Хирургическое лечение. Возможности консервативной терапии оцениваются реально. Это лечение может уменьшить симптоматику, но не ликвидировать сужение сосуда, поэтому радикальное лечение синдрома хронической абдоминальной ишемии возможно только хирургическим путем. Хирургическое вмешательство направлено на предотвращение острых и усугубления хронических расстройств мезентериального кровообращения. Показанием к операции считают наличие у больных отчетливой клинической картины синдрома хронической абдоминальной ишемии, т.е. стадий субкомпенсации и декомпенсации. При асимптомном течении поражений висцеральных ветвей брюшной аорты (в стадии компенсации) придерживаются выжидательной тактики. К хирургическому лечению необходимо прибегать в двух случаях бессимптомного течения, когда при операции по поводу патологии аорты висцеральные ветви находятся в зоне оперативного вмешательства и когда встает вопрос о реконструкции почечных артерий при вазоренальной гипертензии, так как возникшая послеоперационная нормотензия может ухудшить висцеральное кровообращение и вызвать его декомпенсацию [Казанчян П.О., 1979]. Некоторые авторы [Спиридонов А.А., Клионер Л.И., 1989; Kieny et al., 1976] считают наличие окклю-зирующего поражения висцеральных артерий прямым показанием к операции и отстаивают необходимость превентивных вмешательств. По мнению В.П. Поташева и соавт. (1985), декомпрессию чревного ствола надо считать профилактикой ишемичес-ких гастритов, дуоденитов, хронических панкреатитов и гепатитов. В связи с этим декомпрессия чревного ствола сегодня рассматривается как патоге-
10-4886 нетическое лечение особой популяции язв желудка ишемического генеза, что следует расценивать как появление нового направления в хирургии хронических окклюзирующих поражений висцеральных артерий. Такой подход оправдан и вполне логичен. Современная гастроэнтерологическая практика показывает, что определенный процент больных язвенной болезнью желудка и двенадцатиперстной кишки не поддается консервативному лечению в течение длительного времени. Если у данного контингента больных при ультразвуковом и ангиографическом исследовании выявляется поражение висцеральных артерий, то становится понятной бесперспективность консервативного лечения. А.А. Спиридонов и Л.И. Клионер (1989) совершенно справедливо считают, что первоначально целесообразно устранить ишемический фактор, а затем на фоне восстановленного кровообращения пытаться провести консервативное или хирургическое лечение язвенной болезни. Противопоказания к операции на висцеральных ветвях брюшной аорты такие же, как и при других сосудистых операциях: это острый инфаркт миокарда, острый инсульт (в сроки до 3 мес), тяжелая сердечно-легочная и печеночно-почечная недостаточность и другие тяжелые сопутствующие заболевания, облитерация дистального сосудистого русла. Выделяют 3 основные группы операций на висцеральных артериях: • реконструктивные; • условно-реконструктивные (де-компрессивные); • создание обходных шунтирующих путей оттока (операции "переключения"). Операции "переключения", направленные на создание обходных анастомозов (аортоселезеночный, почеч-но-селезеночный, подвздошно-верх-небрыжеечный анастомозы и др.) практически повсеместно оставлены ввиду их гемодинамической малой эффективности и выполняются редко—в случаях трудного выделения пораженных артерий и прилегающего сегмента аорты при кальцинозе или при повторных оперативных вмешательствах. Условно-реконструктивные (де-компрессивные) вмешательства производят в основном при экстрава-зальной компрессии чревного ствола с целью освобождения его от сдавливающих факторов. В комплекс де-компрессивных оперативных вмешательств входят: • рассечение серповидной связки диафрагмы; • пересечение медиальной ножки диафрагмы (круротомия); • удаление ганглиев и пересечение нервных волокон солнечного сплетения (спланхникганглионэктомия); • освобождение артерии от окутывающих ее фиброзных тканей и ликвидация различных приобретенных компрессионных факторов (удаление опухоли, аневризмы, фиброзных тяжей, резекция поджелудочной железы). Для декомпрессии чревного ствола используют два оперативных доступа: верхнюю срединную лапаро-томию и левостороннюю торакофре-нолюмботомию. А. В. Покровский и соавт. (1962, 1999) считают применение лапаротомного доступа нецелесообразным, поскольку подход к чревному стволу из лапаротомии затруднен, что не позволяет выполнить основное условие вмешательства — выделение чревной артерии по всей окружности от устья до трифур-кации. Доступом выбора для подхода к висцеральным ветвям, по мнению А.В. Покровского и др., является левосторонняя торакофренолюмбото-мия, позволяющая не только создать хорошую экспозицию для реконструкции чревного ствола, но и мобилизовать торакоабдоминальный сегмент аорты, другие ее ветви (верхнюю брыжеечную и почечные артерии), а при необходимости и расширить объем намеченного оперативного вмешательства. Техника декомпрессии чревного ствола из лапаротомного доступа следующая: желудок отводят влево. В бессосудистой зоне продольно рассекают печеночно-желудочковую связку и вскрывают полость малого сальника. При ретроградном выделении чревного ствола обнаруживают одну из его ветвей — печеночную или левую желудочную артерию, которая служит ориентиром. Чревный ствол выделяют до устья по всей своей окружности, при этом происходит освобождение ствола от сдавливающих факторов (периартериального фиброза, ганглиев гипертрофированного солнечного сплетения). Рассечение серповидной связки — основной этап декомпрессии чревного ствола. Связку отводят от ствола, пережимают и рассекают на зажимах. При компрессии медиальной ножкой диафрагмы последнюю пересекают. Важно убедиться не только в том, что чревный ствол после декомпрессии полностью расправился, но и что кровоток по артерии приобрел магистральный характер. С этой целью измеряют градиент артериального давления в аорте и чревном стволе, выполняют интраоперационную фло-уметрию и допплерографию. При выявлении градиента артериального давления и коллатерального кровотока по чревному стволу ставят вопрос о чрезаортальной дилатации или протезировании чревной артерии. При выполнении чрезаортальной дилатации артерии необходимо убедиться в том, что артерия также полностью расправилась, ликвидирован градиент артериального давления в аорте и чревном стволе и кровоток, по данным интраоперационной УЗДГ, носит по чревной артерии магистральный характер. Предпочтение все-таки отдают левостороннему торакофренолюмбо-томическому доступу, который позволяет не только мобилизовать тора-коабдоминальный сегмент аорты, но и при необходимости расширить объем оперативного вмешательства, а также создать хорошую экспозицию для пластики чревной артерии. Кожный разрез проводят по девятому межреберью от задней подмышечной до параректальной линии на уровне пупка. Рассекают диафрагму вплоть до аортального кольца. Брюшинный мешок, левую почку с паранефраль-ной клетчаткой отводят кпереди и вправо. Рассекают и резецируют левую медиальную ножку диафрагмы. Чревный ствол выделяют антеградно вплоть до трифуркации. Затем резецируют серповидную связку диафрагмы. Реконструктивные вмешательства направлены на восстановление нормального кровотока по пораженной магистрали. Среди оперативных вмешательств выделяют эндартерэкто-мию, резекцию с протезированием, реплантацию. Реконструкцию висцеральных ветвей методом эндартерэктомии следует выполнять при локализации ок-клюзирующего процесса в проксимальном сегменте (не дистальнее 1,5—2 см). Дезоблитерацию можно производить как при атеросклерозе, так и в склеротической стадии неспецифического аортоартериита. Известны две методики эндартерэктомии: трансартериальная и трансаортальная. На наш взгляд, выполнение трансартериальной эндартерэктомии при окклюзирующих поражениях висцеральных артерий нецелесообразно, так как не всегда обеспечивается достаточный визуальный контроль за полнотой эндартерэктомии из дистальной порции реконструируемой артерии и прилегающего сегмента аорты, что создает угрозу тромбоза или эмболии дистального сосудистого русла фрагментами атеро-склеротической бляшки. К тому же при выполнении чрезартериальной эндартерэктомии необходимо накладывать шов на узкую по диаметру артерию или заплату. Поэтому дезоблитерацию висцеральных ветвей сле-
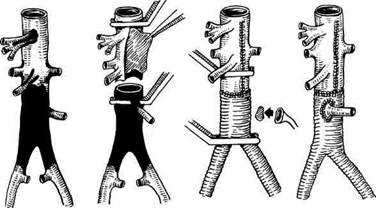
ю* дует выполнять по методике транс-аортальной эндартерэктомии. При поражении чревного ствола и верхней брыжеечной артерии операцию выполняют из левостороннего торакофренолюмботомического доступа. Выделяют и мобилизуют аорту и пораженную артерию — чревный ствол или верхнюю брыжеечную артерию. Аорту пристеночно отжимают и просвет ее вскрывают дугообразным разрезом, окаймляющим устье артерии. Осторожно надсекают интиму и отслаивают ее по всей окружности. Затем под визуальным контролем, частично инвагинируя артерию в просвет аорты, выполняют эн-дартерэктомию из пораженной артерии. Контролируют адекватность эндартерэктомии, после чего аортото-мическое отверстие ушивают. Выполнение данной методики целесообразно при наличии изолированного поражения чревной или верхней брыжеечной артерии. Учитывая, что при атеросклерозе и неспецифическом аортоартерии-те, как правило, наблюдается одномоментное поражение нескольких висцеральных артерий, часто с вовлечением и почечных артерий, при- менение методики трансаортальнои эндартерэктомии, требующей повторных отжатий аорты, вскрытий ее просвета в нескольких местах, нецелесообразно. А.В. Покровским и соавт. (1971) была разработана и с успехом применяется новая методика операции — одномоментная трансаортальная эн-дартерэктомия из брюшной аорты, висцеральных и почечных артерий, сущность которой заключается во вскрытии просвета аорты продольным разрезом по левой заднебоковой поверхности и удалении единым блоком пораженной интимы и бляшек из аорты, висцеральных и почечных артерий (рис. 6.52). При распространении окклюзиру-ющего процесса более чем на 2 см от устья реконструкцию артерий выполняют методом резекции с протезированием, для чего используют протезы диаметром 8 мм, а также имплантацию артерии в протез или в новое устье (рис. 6.53). К группе комбинированных реконструктивных операций относят вмешательства, направленные на одномоментное восстановление кровотока в нескольких висцеральных ветвях и аорте.
Рис. 6.52. Одномоментная трансаортальная эндартерэктомии из брюшной аорты, висцеральных, почечных артерий и бифуркационное аортобедренное протезирование с реплантацией в протез нижней брыжеечной артерии на аортальной площадке.
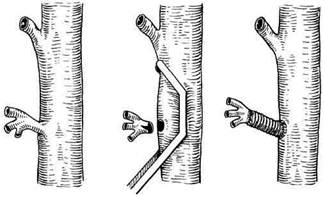
Рис. 6.53. Протезирование чревного ствола. Подобная необходимость возникает обычно в следующих ситуациях: • при необходимости одновременной реконструкции нескольких висцеральных и почечных артерий; • при выполнении операции аор-тобедренного шунтирования; • при реконструкциях торакоабдо-минального сегмента аорты в сочетании с реваскуляризацией висцеральных и почечных артерий. При сочетанных поражениях чревного ствола и верхней брыжеечной артерии следует производить одновременную реваскуляризацию обоих бассейнов. Обычно методом выбора является трансаортальная эндар-терэктомия. В условиях изолированной реконструкции почечных артерий и наступившей вследствие этого нор-мотензии висцеральное кровообращение в целом может оказаться в условиях как бы гипотензии, что повлечет за собой возможный срыв компенсаторных механизмов коллатерального кровообращения и вполне реальное развитие острого нарушения мезен-териального кровообращения. Поэтому нецелесообразно придерживаться тактики максимального радикализма при подобных сочетанных поражениях и выполнять одновременную реваскуляризацию обоих бассейнов. Методом выбора обычно является операция трансаортальной эндартерэктомии. Другой альтернативой, появившейся только в последние годы, является баллонная дилатация чревной или верхней брыжеечной артерии с последующим стентированием. К сожалению, несмотря на большую перспективность и эффективность подобных вмешательств, они еще не нашли широкого распространения в клиниках и выполняются лишь в немногих центрах мира. Появление в литературе большого количества работ, посвященных развитию острых нарушений висцерального кровообращения после аорто-бедренных реконструкций, связано с развитием феномена обкрадывания висцерального кровообращения после пуска большого потока крови в нижние конечности (aorto-iliac steal синдром). С этим вопросом переплетается и другой — о реваскуляризации нижней брыжеечной артерии при реконструкции терминальной аорты, которую, как известно, нередко перевязывают. Между тем анастомозы между средней и левой толстокишечными артериями, формирующими дугу Риолана, как уже указывалось выше, анатомически хорошо бывают развиты лишь у 85 % пациентов. У оставшихся 15 % больных такой межбрыжеечный анастомоз, являющийся связующим звеном в кровообращении двух брыжеечных артерий, просто не существует. В связи с
Рис. 6.54. Трансаортальная эндартерэктомия из нижней брыжеечной артерии при аортобедрен-ном шунтировании. этим и aorto-iliac steal синдром, и перевязка нижней брыжеечной артерии при выполнении аортобедрен-ного шунтирования могут повлечь за собой, во-первых, возникновение синдрома обкрадывания кровотока по верхней брыжеечной артерии и развитие дефицита кровотока в бассейне указанной артерии, а также чревного ствола и, во-вторых, ишемию (возможно, острую) левой половины толстой кишки. С учетом этих обстоятельств оправдано придерживаться тактики максимального радикализма в отношении нижней брыжеечной артерии при аортобед-ренных реконструкциях и выполнять реваскуляризацию ее бассейна там, где это возможно. В большинстве случаев применяют методику трансаортальной эндар-терэктомии из нижней брыжеечной артерии (рис. 6.54; 6.55), а при невозможности ее выполнения производят реплантацию артерии в протез на аортальной площадке (аортальный валик). По мере прогрессирования окклю-зирующего процесса в аорте в краниальном направлении нижняя брыжеечная артерия постепенно вовлекается в основной процесс, и кровоток по ней постепенно редуцируется. Дефицит кровотока в ее бассейне компенсируется за счет верхней брыжеечной артерии через функционирующий межбрыжеечный анастомоз в каудальном направлении. В этих условиях при интактной верхней брыжеечной артерии лигирование нижней брыжеечной артерии при аортобед-ренном шунтировании допустимо и безопасно. При наличии же соче-танного поражения чревного ствола
Рис. 6.55. Реплантация нижней брыжеечной артерии на аортальной площадке при аортобедрен-ном протезировании. и верхней брыжеечной артерии или же при недостаточном развитии межбрыжеечного анастомоза может создаваться угроза ишемических расстройств в левой половине толстой кишки. Свести к минимуму эту угрозу можно, выполнив реконструкцию нижней брыжеечной артерии. Дата добавления: 2015-02-06 | Просмотры: 1754 | Нарушение авторских прав |