|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Повторные операции на аортобедренном сегментеНепосредственный успех хирургического лечения аортобедренных окклюзии с купированием симптомов ишемии конечностей возвращает к трудоспособности значительную часть больных в ближайшие сроки после реконструктивных операций. В то же время возникновение местных поздних осложнений в отдаленные сроки сводит на нет успех реконструктивной операции, обусловливает инвалидизацию успешно оперированных больных или требует выполнения у них повторных оперативных вмешательств. Различный генез отдаленных осложнений реконструктивных операций на сосудах определяет сложность и многообразие проблемы лечения этих больных и диктует дифференцированный подход к показаниям и противопоказаниям, выбору метода хирургической коррекции. Повторные вмешательства выполняют при тромбозах трансплантатов, гемоди-намически значимых стенозах анастомозов, ложных аневризмах проксимального и дистальных анастомозов, инфицировании протезов, прогрес-сировании заболевания в дисталь-ном русле. Самым частым среди поздних осложнений является тромбоз сосудистого трансплантата, проявляющийся клинической картиной ишемии конечности. В структуре поздних осложнений тромбозы составляют, по данным различных авторов, от 60 до 90 % [Говорунов Г.В., 1987; Таше-новД.К., 1989; Затевахин И.И. и др., 1993; Brewster D. et al., 1987; Fairdutti etal., 1991]. Большинство исследователей выделяют три основные причины развития тромбозов: прогрессирование основного заболевания, интималь-ную гиперплазию и технические и тактические ошибки [Волколаков Я.В., Тхор С.Н., 1981; Клионер Л.И., Беляев Н.И., 1986].
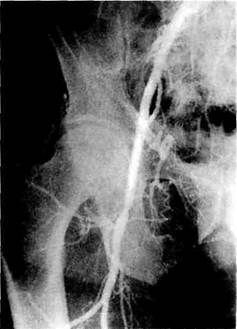
Причины поздних реокклюзий. Наиболее частой причиной тромботи-ческих осложнений является прогрессирование атеросклероза, которое чаще развивается в зонах дистальных анастомозов и в поверхностных бедренных артериях [Brewster D. et al., 1987]. Реже атеросклероз прогрессирует в проксимальном направлении, что ведет к снижению объемного кровотока по аорте и браншам протеза. Более 50 % случаев тромбозов в отдаленные сроки обусловлены про-грессированием атеросклеротического процесса. Вторым фактором, способствующим возникновению тромбоза и рецидива ишемии конечностей, является стеноз анастомозов, получивший в литературе название "рес-теноз анастомозов" (рис. 6.57; 6.58). Третий фактор включает ошибки
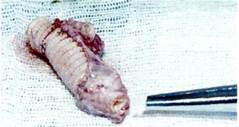
Рис. 6.58. Резецированный стенозиро-ванный дистальный анастомоз. тактического и технического плана, ведущие к возникновению тромбо-тических осложнений. К ошибкам тактического плана следует отнести: некорригированный стеноз проксимального или дистального сегмента, наложение низкого проксимального анастомоза в зоне, наиболее подвер-
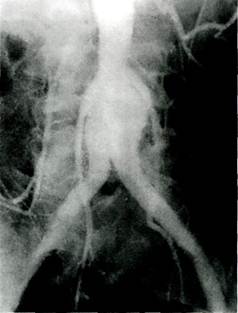
Рис. 6.59. Тромбоз правой бранши протеза. Проксимальный анастомоз наложен на уровне бифуркации. Имеется избыток основной бранши аортобедренно-го протеза. женнои атеросклерозу, оставление перегибов и избытков сосудистых протезов (рис. 6.59), выполнение операций при неадекватном состоянии дистального артериального русла. По данным И.И.Затевахина и соавт. (1993), около 1/3 осложнений в отдаленные сроки обусловлены ошибками как технического, так и тактического плана. Ложные аневризмы дистальных анастомозов являются причиной почти 6 % всех поздних тромботичес-ких осложнений [Brewster D. et al., 1987]. Другие причины тромботичес-ких осложнений, такие как экстрава-зальная компрессия, сдавление бранши протеза сигмовидной кишкой или паховой связкой, фиброзным околопротезным кольцом, безусловно, имеют место, но у весьма ограниченной части больных (менее 1 %) и в клинической практике представляют скорее теоретический интерес [Rabe et al., 1982]. Обезвоживание организма, возникающее при приеме большого количества алкоголя, может вызывать развитие тромбоза и при отсутствии упомянутых трех основных причин [Тхор С.Н., 1978]. Тромбозы могут возникать также на фоне повышенного свертывания крови или дефицита антитромбина [Reininger et al., 1992]. Эти нарушения возможны при гематологических или онкологических заболеваниях, а также как проявление инфекционного процесса. В структуре тромбозов они составляют около 4 % [Brewster D. et al., 1987]. Причины поздних реокклюзий выявить не всегда удается. Согласно имеющимся наблюдениям определенное значение имеют сроки их развития [Затевахин И.И. и др., 1993]. Атеросклеротические рестено-зы и реокклюзий возникают, как правило, не менее чем через 3—5 лет после первичных оперативных вмешательств [Robbs, 1981]. Между тем ошибки тактического и технического плана проявляются значительно раньше и сопровождаются возникнове- нием реокклюзий в ближайшие 1—2 года [Tyson et al., 1978; Brewster D. et al., 1987], однако четкую зависимость между сроками и причиной реокклюзий удается провести далеко не всегда. По данным большинства авторов, реокклюзий в 50—80 % случаев возникают в ближайшие 2 года после оперативных вмешательств. При изучении сроков возникновения тромбозов нами было выявлено, что из 132 больных с тромбозами трансплантатов в первые 2 года после реконструктивных вмешательств тромбоз возник у 55 пациентов (42 %), в сроки от 2 до 6 лет — у 58 (44 %), в сроки более 6 лет — у 19 пациентов (14 %) после первичного оперативного вмешательства. Ретроспективный анализ позволил установить, что у 36 из 55 (65 %) больных, у которых тромботические осложнения развились в первые 2 года после операции, причинами их возникновения явились хирургические погрешности: у 15 больных — наложение низкого проксимального анастомоза на уровне бифуркации аорты, у 10 — не была произведена коррекция стеноза глубокой бедренной артерии ниже наложения дистального анастомоза, у 4 — имелся избыток бранши или перекрут протеза, у 2 пациентов превышены показания к выполнению первичного реконструктивного вмешательства. У 5 больных были допущены технические ошибки: сужение дистального анастомоза — в 2 случаях и выполнение закрытой эндартерэктомии из поверхностной бедренной и подвздошной артерий — в 3 наблюдениях. Третья основная причина возможного развития тромбозов связана с появлением, развитием и прогресси-рованием стенозов дистальных анастомозов. Истинная частота возникновения тромбозов на почве стенозов анастомозов, по-видимому, очень значительна. В частности, среди наблюдаемых нами 10 пациентов со стенозами анастомозов более 60 % у 7 человек произошел тромбоз в первый год с момента выявления стеноза, а из 20 стенозов менее 60 % тромбоз возник в 4 случаях. Патогенез интималыюй гиперплазии. Ни один из системных факторов статистически достоверно не повышает риск возникновения рестенозов анастомозов. Предполагается, что развитие стенозов анастомозов в большей степени обусловлено гемодинами-ческими особенностями в области анастомозов и исходной способностью гладкомышечных клеток к про-лиферативной активности. Некоторые авторы считают артериальную гипертензию, курение, повышение уровня холестерина теми системными факторами, которые способствуют возникновению усиленной пролиферации интимы и развитию ин-тимальной гиперплазии при наличии местных условий [Bujan et al., 1992; Kauffman et al., 1992; Munro et al., 1994; Conte et al., 1995]. Экспериментальные модели развития стенозов позволили во многом пролить свет на генез и прогрессиро-вание рестенозов анастомозов. Несмотря на различное трактование причин возникновения интимальной гиперплазии, экспериментальные исследования установили, что развитие интимальной гиперплазии в зоне анастомозов обусловлено ответом гладкомышечных клеток на растяжение сосудистой стенки [Morinaga et al., 1987], вызванное гидродинамическим ударом [Pomposelli et al., 1984; Zwolak et al., 1987; Binns et al., 1989; Sottiurai et al, 1994], и зависит от угла наложения и ригидности трансплантата [Hason et al., 1985; Sottiurai et al., 1994; Fei et al., 1994]. На основании различного растяжения участков артерии в зонах анастомозов некоторые исследователи предприняли попытки прогнозировать развитие интимальной гиперплазии в соответствующих областях анастомоза [Sottiurai et al., 1983]. Для изучения морфологических особенностей и патогенеза развития и прогрессирования стенозов анастомозов нами было проведено имму-номорфологическое исследование. Установлено, что в области дисталь-ного анастомоза происходит интенсивное развитие атеросклероза. По мнению И.И.Затевахина и соавт. (1993), очаговые разрастания "неоинтимы" представляют собой атеро-склеротические бляшки на ранней стадии их развития. В то же время другие исследователи считают, что экспериментальная гиперплазия интимы в ответ на повреждение не может полностью отождествляться с морфогенезом атеросклеротических бляшек. Таким образом, у пациентов, оперированных по поводу облитерирую-щего атеросклероза, процесс атеро-генеза и интимальной гиперплазии может протекать одновременно. Это согласуется с результатами, полученными Г.В.Говоруновым (1987), который выявил в 80 % наблюдений наряду с равномерной интимальной гиперплазией фиброзные утолщения и атеросклеротические бляшки. Причины ложных аневризм анастомозов. Этиологические факторы развития ложных аневризм различны. В первые годы становления реконструктивной сосудистой хирургии эти осложнения наблюдались очень часто и были обусловлены разрушением и фрагментацией шовного материала [Gardner et al., 1972; Van den Akker et al., 1989]. Ложные аневризмы появлялись в первые 4 года после выполненного реконструктивного вмешательства. С внедрением в качестве шовного материала полипропилена частота возникновения ложных аневризм значительно снизилась [Freisch-lang, Moore, 1989]. Данные литературы свидетельствуют, что развитие поздних ложных аневризм (свыше 3,5 года) имеет мультифакторный ге-нез [Зырянов Б.Н. и др., 1980; Кара-зеев Г.Л., 1992]. В развитии ранних ложных аневризм главной причиной являются инфекционные осложнения [Haimo- vici, 1976; Crawford et al., 1977; Vol-mar, 1980; Wandscheider et al., 1988]. Раневая инфекция также играет значительную роль и в генезе поздних ложных аневризм. В то же время Pircher и др. (1980) не отметили статистически достоверной разницы в развитии поздних аневризм у больных с гладким послеоперационным течением и у больных, перенесших глубокое нагноение в зоне анастомозов. Некоторые авторы предполагают, что в генезе поздних ложных аневризм играет роль фактор первичной бактериемии, которая способствует фиксации инфекционного агента на синтетическом материале и развитию в отдаленные сроки ложных аневризм [Freischlang, Moore, 1989]. Существует мнение, что развитие ложных аневризм непосредственно обусловлено применением синтетических материалов [Gardner et al., 1972]. Объяснение этого факта, по-видимому, лежит в разной степени упругости бранши протеза и стенки артерии. Было доказано, что растяжимость артерии в 10—15 раз больше, чем у тефлонового протеза, при этом ригидность последнего возрастает с течением времени [Patel et al., 1961; Gozna et al., 1972]. Этот фактор обусловливает разницу в растяжении протеза и артерии в зоне анастомоза, что ведет к прорезыванию стенки артерии. В литературе имеются сообщения о влиянии артериальной гипер-тензии на развитие ложных аневризм у больных, страдающих артериальной гипертензией [Гамбарин Б.Л., 1982; Szilagyi et al., 1975; Van der Akker et al., 1989]. По-видимому, механизм влияния гипертензии заключается в усилении гидродинамического удара за счет большего объемного кровотока в зоне анастомоза. Как показали наши наблюдения, у больных с артериальной гипертензией имеется более чем 1,5-кратное увеличение частоты ложных аневризм — 11,3 % по сравнению с пациентами без артериальной гипертензии — 6,8 %. Немаловажным фактором в генезе ложных аневризм является гидродинамический удар в зоне анастомоза. Szilagyi и др. (1975) установили, что в конструкциях анастомозов конец в бок давление по линии анастомозов выше, чем при анастомозах конец в конец. По данным большинства исследователей, частота развития ложных аневризм при анастомозах конец в бок статистически выше, чем при анастомозах конец в конец [Трипонис В.И., 1982; Gardner et al., 1972; Brewster et al., 1987]. Нам удалось установить, что у больных, оперированных по поводу ложной аневризмы дистального анастомоза, ге-нез которых не был обусловлен шовным материалом или инфекцией протеза, частота возникновения аневризмы контралатерального дистального анастомоза выше, чем у первичных пациентов, перенесших аор-тобедренные реконструкции, — соответственно 11,8 и 7,5 %. Это подтверждают данные литературы о предрасположенности ряда больных к возникновению ложных аневризм дистального анастомоза, возможно, обусловленной слабостью артериальной стенки. Интересные статистические данные, основанные на 29-летнем опыте Детройтской клиники сосудистой хирургии, приводят Szilagyi и соавт. (1986), которые выявили, что при наложении анастомозов по типу конец в конец во время повторных реконструктивных вмешательств по поводу ложных аневризм дистальных анастомозов частота возникновения ложных аневризм не только не снижается, но и возрастает с 5,6 % после первичных аортобедренных реконструкций до 15,6 % после операций по поводу ложных аневризм и до 17,4 % после повторных вмешательств по поводу ложных аневризм. Эти факты свидетельствуют, что в генезе развития ложных аневризм ведущую роль все же играют не гемодинамические факторы, а слабость артериальной стенки в зоне наложения анастомо- зов или процессы прогрессирования атеросклероза. По-видимому, важную роль в ослаблении артериальной стенки может играть эндартерэктомия. Единичные экспериментальные исследования также указывают на то, что при регрессе атеросклеротических бляшек также может возникать ослабление каркаса артериальной стромы [Zarins et al., 1992]. По мнению Freischlag, Moore (1989), дегенеративные изменения в стенке артерий могут быть обусловлены маловирулентными бактериями. Ложные аневризмы дистальных анастомозов в 76 % случаев возникают в сроки свыше 3 лет, в то время как ложные аневризмы проксимального анастомоза более чем в половине случаев возникали в первый год [Покровский А.В., Зотиков А.Е., 1996]. Диагностика поздних осложнений. Клиническая картина тромботичес-ких осложнений достаточно ярка. Более чем у 80 % больных ишемия, возникающая при реокклюзии, более выражена, чем до первичной реконструкции. В большинстве случаев более чем у 90 % больных тромбоз трансплантата может быть выявлен на основании исчезновения пульсации и отсутствия систолического шума при аускультации. В 7 % случаев на стороне тромбоза сохраняется ослабленная пульсация на бедренной артерии, которая обусловлена сохраненной остаточной проходимостью стенозированного подвздошно-бедренного сегмента. Чрезвычайно важной является ранняя диагностика стенозов анастомозов, которая позволит улучшить отдаленные результаты аортобедренных реконструкций. Наибольшая диагностическая ценность принадлежит дуплексному сканированию и рентгеноконтрастной ангиографии. Эти исследования, как правило, не только вносят ясность в установление состояния трансплантата или стеноза анастомоза, но и позволяют судить о состоянии ниже-
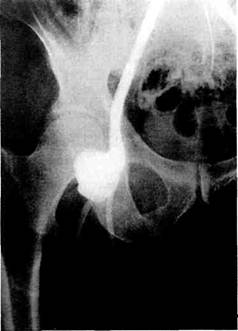
Рис. 6.60. Ангиограмма. Ложная аневризма правого дистального анастомоза. лежащих сегментов глубокой артерии бедра и состоянии аорты выше проксимального анастомоза. В диагностике ложных аневризм ангиологическое исследование имеет чрезвычайно важное значение. Наличие классической триады симптомов: опухолевидное пульсирующее образование, систолический шум и боли в паховой области — позволяет установить диагноз у большинства больных уже на догоспитальном этапе. Вместе с тем литературные данные свидетельствуют, что у половины больных ложные аневризмы небольшого размера асимптомны и выявляются лишь при контрольном ультразвуковом исследовании [Van der Akker et al., 1989] или ангиографии (рис. 6.60). Характерным для ложных аневризм дистального анастомоза является овальное образование в виде темного поля, вокруг которого обнаруживались тромботи-ческие массы, проявлявшиеся на экране светлыми участками — симптом снежной пыли. Значительно труднее обнаружить ложную аневризму проксимального анастомоза, что объясняется скудностью клинических симптомов. Наиболее частый клинический признак — боль в пояснице: этот симптом не является специфичным, однако, по нашим наблюдениям, около 80 % боль-
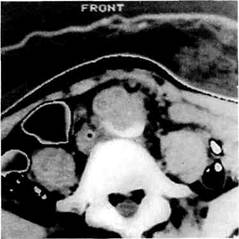
Рис. 6.61. Компьютерная томограмма. Визуализируется основная бранша протеза, наложенная по типу конец в бок с аортой.
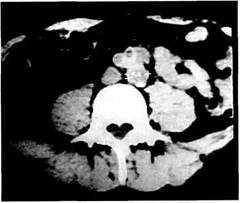
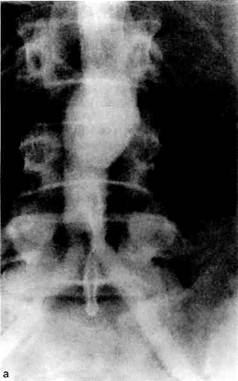
Рис. 6.62. Компьютерная томограмма. Спереди от аорты и справа от протеза имеется дополнительная тень размером до 1 см. ных отмечают его. Наличие пульсирующего образования в животе обнаруживают у 50—60 % пациентов. Решающая роль в диагностике ложных аневризм проксимального анастомоза принадлежит ультразвуковому исследованию и компьютерной томографии (рис. 6.61; 6.62). Характерным томографическим признаком ложной аневризмы проксимального анастомоза является дополнительная тень, лежащая рядом с сосудистым трансплантатом или между сосудистым протезом и аортой. Использование малых доз контрастного вещества позволяет установить осложненные формы ложных аневризм, такие как надрыв или разрыв проксимального анастомоза. Следует помнить о возможности наличия истинной аневризмы в зоне проксимального анастомоза (рис. 6.63). В этих случаях расширенная аорта на сканах плавно переходит в протез без появления дополнительной тени вокруг протеза или аорты. Важную роль компьютерная томография играет в выявлении инфекции сосудистых трансплантатов. Ангиографическое исследование — второй метод, несущий исключительно важную информацию для диагностики ложных аневризм проксимального анастомоза (рис. 6.64). Обязательным правилом при подоз-
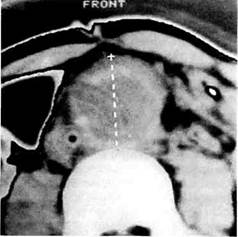
Рис. 6.63. Компьютерная томограмма. Истинная аневризма аорты выше проксимального анастомоза. рении на аневризму проксимального анастомоза является выполнение ангиографического исследования в 2 проекциях (рис. 6.65). Это положение представляется чрезвычайно важным, поскольку исследование только в переднезадней проекции может привести к ложноположительному результату у больных с функционирующими аортобедренными трансплантатами при анастомозах конец в бок. В то же время наличие тромботичес-
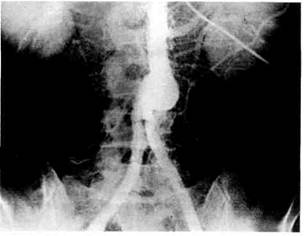
Рис. 6.64. Ангиограмма, прямая проекция. Ложная аневризма проксимального анастомоза. ких масс в полости аневризматичес- Только при значительных размерах прямая проекция обеспечивает надежную информативность. Показания и противопоказания к повторным операциям на аортобед-ренном сегменте: • наличие тромбоза одной или обеих браншей аортобедренного трансплантата при наличии ишемии не ниже ПБ степени по классификации А.В.Покровского; • стеноз дистального анастомоза более 70 %; • наличие ложной аневризмы дистального или проксимального анастомоза независимо от ее размеров.
Больным с плохими путями оттока, окклюзией основного ствола глубокой артерии бедра и подколенной артерии ниже щели коленного сустава повторные оперативные вмешательства показаны при хронической ишемии III—IV степени. В тех случаях, когда у пациентов с функционирующими аортобедренными трансплантатами при окклюзии бедрен-но-подколенного сегмента сохранялась ПБ—IV степень ишемии при наличии проходимой подколенной артерии и артерии голени, показано бедренно-подколенное шунтирование. Общими противопоказаниями к выполнению реконструктивных вмешательств являются инфаркт миокарда, нарушение мозгового кровообращения (менее 3 мес), терминальная стадия почечной недостаточности, сердечно-легочные забо-
Рис. 6.65. Ангиограмма. Ложная аневризма проксимального анастомоза. а — прямая; б — боковая проекция. левания в стадии декомпенсации, неоперабельные онкологические заболевания. Местными противопоказаниями служат гангрена стопы с переходом на проксимальный отдел или нижнюю треть голени; тотальная окклюзия глубокой и поверхностной бедренной артерии на протяжении, создающая техническую неосуществимость наложения разгрузочного анастомоза на уровне бедра при выполнении одномоментных многоэтажных реконструкций; окклюзия подколенной и всех берцовых артерий; острая ишемия свыше ША степени. Таким пациентам показана первичная ампутация конечности. Выбор характера операции у больных с реокклюзиями. В отношении выбора видов повторных оперативных вмешательств на аортобедрен-ном сегменте не существует единого подхода. Большинство авторов предпочитают методику непрямой тромб-эктомии с реконструкцией дисталь-ного анастомоза [Тхор С.Н., 1987; Покровский А. В., Зотиков А.Е., 1996; Brewster D. et al., 1987]. Выполнение непрямой тромбэктомии с реконструкцией дистального анастомоза показано в тех случаях, когда удается восстановить адекватный кровоток из бранши протеза, однако в структуре повторных операций непрямые тромбэктомии с реконструкцией дистального анастомоза составляют лишь 58—62 % [Гамбарин Б.Л., 1982; Brewster D. et al, 1987]. Успех или неудача при выполнении тромбэктомии из бранши протеза обусловлены как состоянием аорты выше проксимального анастомоза, так и временем, прошедшим с момента возникновения тромбоза. Ряд исследователей ограничивают возможность выполнения тромбэктомии сроком 2—3 мес после тромбоза [Bernhard et al., 1977]. Другие авторы сообщают об успешных тромб-эктомиях через 6 и даже 7 мес [Conn et al, 1970; Brewster D. et al., 1987]. Так, если в первый месяц с момента возникновения тромбоза успех тромбэктомии достигает 95 %, то в более поздние сроки адекватную тромбэк-томию удается выполнить лишь в 80 % случаев [Brewster D. et al., 1987]. Большую роль в успехе тромбэктомии играет тип протеза. Выполнение тромбэктомии из протезов из политетрафторэтилена (гортекс, экофлон) наиболее затруднительно и возможно лишь в более ранние сроки. Наиболее легко тромбэктомия осуществима из отечественных тканых протезов "Север". Так, нам удавалось выполнять тромбэктомию из этих протезов в сроки более 2 лет с момента наступления тромбоза. Ряд авторов предпочитают повторное аортобедренное протезирование при тромбозе протеза с заменой тромбированной бранши новой [Grawford et al., 1977; Volmar, 1980; Benhamou et al., 1984]. В качестве аргумента эти исследователи приводят данные о происходящих структурных нарушениях в тромбированной бранше протеза. Вместе с тем нет единого мнения о том, что замена протеза статистически достоверно дает лучшие результаты, чем непрямая тромбэктомия с реконструкцией анастомоза. Большинство хирургов стоят на позиции, что повторное аортобедренное протезирование показано лишь при невозможности выполнения адекватной тромбэктомии или при поражении аорты выше проксимального анастомоза [Говорунов Г.В., 1987; Покровский А.В. и др., 1990; Затевахин И.И. и др., 1993; Bernhard et al., 1987]. Прежде всего это обусловлено более высокой госпитальной летальностью при замене аортального протеза, которая колеблется от 5,7 до 20 % [Crawford et al., 1977; Benhamou et al., 1984; Szilagyi et al., 1986; Ernst et al., 1987], в то время как летальность при тромбэктомиях с резекцией анастомоза составляет от 1 до 1,9 % и не превышает 3 % [Brewster et al., 1987]. При невозможности или неадекватности выполнения
11 - 4886 тромбэктомии у наиболее тяжелых больных возможно выполнение перекрестного шунтирования от функционирующей бранши [Crawford et al., 1977; Benhamou et al., 1984]. Причиной возникновения тромбозов служат гемодинамические нарушения, в первую очередь возникающие из-за стенозов дистальных анастомозов или прогрессирования процесса в дистальном артериальном русле. В связи с этим тромбэктомия в подавляющем большинстве случаев должна завершаться реконструкцией дистального анастомоза. Интраопе-рационными критериями адекватности тромбэктомии служили появление отчетливой пульсации на бранше протеза и наличие пульсирующего струйного кровотока. Показаниями к повторным аорто-бедренным реконструкциям являются: • тромбоз обеих и основной бран-шей протеза; • наличие низко наложенного проксимального анастомоза при тромбозах одной бранши протеза; • поражение аорты, выявляемое ангиографически выше зоны проксимального анастомоза; • невозможность получения адекватного кровотока из браншей после выполнения неоднократных тромбэктомии во время реконструкций дистальных анастомозов; • наличие аневризмы проксимального анастомоза. Чрезвычайно важным является восстановление кровотока по глубокой артерии бедра, поскольку у 85 % пациентов с реокклюзиями шунтов имеется окклюзия поверхностной бедренной артерии [Brewster D. et al., 1987]. Включение в кровоток глубокой артерии бедра при повторных операциях выполняют более чем у 75 % больных. Причиной неадекватности восстановления кровотока по глубокой артерии бедра может быть анатомо-функциональное состояние глубокой артерии бедра (плохие перетоки из системы глубокой артерии бедра в подколенную), недостаточный ее диаметр (менее 4 мм) или короткий ствол. В этих случаях тромб-эктомию с реконструкцией дистального анастомоза необходимо дополнить одномоментным бедренно-подколенным или бедренно-берцо-вым шунтированием. Необходимость выполнения одномоментных комбинированных вмешательств колеблется от 5 до 32 % [Harris, 1985; Szilagyi, 1986; Brewster et al., 1987]. При окклюзии глубокой артерии бедра на протяжении выполняют аортоподко-ленное шунтирование с разгрузкой в огибающую артерию бедра. Выбор тактики лечения у больных с ложными аневризмами анастомозов. Выбор тактики лечения ложных аневризм анастомозов зависит прежде всего от этиологии ложной аневризмы и ее локализации. Хирургическое лечение ложных аневризм, обусловленных парапротезной инфекцией, рассматривается в соответствующем разделе (см. "Парапро-тезная инфекция"). Наличие ложной аневризмы анастомоза независимо от ее размеров является показанием к хирургическому вмешательству, поскольку ложные аневризмы имеют тенденцию к росту, высока вероятность их разрыва и эмболизации мелких тромбов в дистальное артериальное русло [Говорунов Г.В., 1987; Szilagyi et al., 1986; Gawenda et al, 1994]. Это обусловлено тем, что формирование ложных аневризм связано с разрывом или прорезыванием швов по линии анастомоза; кроме того, возникающая в этой области турбуленция потока крови вызывает прогрессивный рост аневризмы, что повышает вероятность тромбоза в области анастомоза и тромбоэмболии в дистальное артериальное русло. При неинфицированных аневризмах дистального анастомоза подавляющее большинство хирургов применяют методику резекции ложной аневризмы. При наличии небольших и средних размеров ложных анев- ризм дистального анастомоза (менее 5 см), которые пальпаторно определяются ниже пупартовой связки, используют бедренный доступ. Забрю-шинный доступ был показан в тех случаях, когда верхний полюс аневризмы уходит под пупартову связку, в случаях ранее выполненных высоких дистальных анастомозов, а также при разрывах ложных аневризм или их инфицировании. Малооправданным является предложение В.И.Три-пониса (1982) проводить повторное протезирование обходным путем, оставляя саму аневризму. Практически все хирурги отказались от предложенного Christensen и соавт. (1977) ушивания дефекта в анастомозе даже при его небольших размерах. При резекции ложных аневризм дистального анастомоза последний необходимо накладывать по типу "конец в конец". Особую группу составляют пациенты с ложными аневризмами проксимального анастомоза. Резекция аневризмы с протезированием аорты аллонадставкой из основной бранши сосудистого протеза является операцией выбора. Исключение составляют больные с инфицированными трансплантатами (см. "Парапротезная инфекция"). Мнение некоторых авторов [Скрипниченко Д.Ф., Иваненко А.А., 1986], что все ложные аневризмы проксимального анастомоза являются инфицированными, малообос-новано. Поэтому операция экстраанатомического шунтирования должна выполняться лишь при доказанном инфекционном генезе аневризмы. Широкое использование подмы-шечно-бедренных шунтов, предлагаемое некоторыми авторами, менее рационально, чем повторные реконструктивные операции, в связи с более высоким риском тромботичес-ких осложнений [Нерр et al., 1988; Mason et al, 1989; Harris et al., 1990; Schroe et al., 1990; Dujardin et al., 1991; Schneider et al, 1992]. Повторное аортобедренное шун- тирование целесообразно выполнять лишь при наличии аневризмы проксимального и дистального анастомозов или при сочетании аневризмы проксимального анастомоза с реок-клюзиями в области дистального анастомоза или тромбозе бранши [Kraus et al., 1994]. Дата добавления: 2015-02-06 | Просмотры: 1462 | Нарушение авторских прав |