|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Эмиграция лейкоцитов в очаг воспаления.Важнейшим признаком венозной гиперемии является эмиграция лейкоцитов из сосудов в воспаленную ткань. Процессу эмиграции предшествует нарушение осевого тока движения крови внутри сосуда. В условиях замедления кровотока эритроциты, объединяясь в «монетные столбики», занимают центральную часть сосуда, а лейкоциты, имеющие более низкую удельную массу, выходят из осевого тока сначала на границу плазматического слоя, а затем начинают прилипать к эндотелиальным клеткам сосуда. Важная роль в адгезии (лат. adhaesio - прилипание) лейкоцитов отводится так называемым эндотелиально-лейкоцитарным адгезивным молекулам (ЭЛАМ), которые экспрессируются на поверхности лейкоцитов, эндотелиальных клеток и макромолекулах межклеточного матрикса в очаге воспаления. Активаторами экспрессии ЭЛАМ на лейкоцитах и эндотелиальных клетках в зоне воспаления являются биологически активные вещества-цитокины, такие как ИЛ-1, ИЛ-8, ЛТ В4, ФАТ, ФНО-α, γ-интерферон, фракции комплемента С5а и Bb, хемотаксиче-ские факторы, липополисахариды бактерий и др. Под влиянием указанных медиаторов в лейкоцитах и клетках эндотелия сосудов происходят конформационные изменения мембраны, освобождаются и экспресссируются молекулы адгезии. В процессе острого воспаления важную роль для течения воспаления и его исходов имеет процесс выхода лейкоцитов из кровеносного русла –эмиграции. Лейкоциты – в очаге воспаления выполняют несколько важнейших функций. 1 – защитную; 2 – регуляторную; 3 – очищение зоны повреждения и подготовку к пролиферации Механизмы эмиграции: · I стадия – обратимая адгезия, скольжение лейкоцитов (30-60 мин.) · II стадия – необратимая адгезия к эндотелию, трансэндотелиальная миграция (несколько минут) · III стадия – хемотаксис (несколько суток) Адгезия лейкоцитов к эндотелию сосуда. Под влиянием медиаторов воспаления происходит активация эндотелия и стимуляция синтеза адгезивных молекул. Быстрее всех молекул адгезии (в течение нескольких мин) на эндотелии начинает функционировать Р-селектин, который исходно содержится в эндотелиальных клетках. Остальные эндотелиальные молекулы адгезии появляются последовательно в течение нескольких часов, поскольку они синтезируются эндотелием. В настоящее время известно несколько классов молекул клеточной адгезии: 1. Селектины - лектиновые молекулы клеточной адгезии, опосредующие самую раннюю стадию взаимодействия лейкоцитов и сосудистой стенки. Селектины экспрессируются рано и не обеспечивают прочного прикрепления лейкоцитов к эндотелию сосудов. Выделяют три вида селектинов: L-селектины синтезируются всеми лейкоцитами, Е-селектины синтезируются эндотелиоцитами. Указанные селектины обеспечивают феномен краевого стояния лейкоцитов. Источником P-селектинов являются тромбоциты и эн-дотелий сосудов, помимо участия в процессах маргинации лейкоцитов, они способствуют адгезии тромбоцитов.
Табл. 14. Селектины и их функции
2. Интегрины – это гетеродимерные белки, экспрессируемые различными лейкоцитами и клетками гемопоэтического ряда. Эндотелий экспрессирует лишь некоторые интегрины. В настоящее время идентифицировано пять видов интегринов. Наиболее важными для миграционного и фагоцитарного процесса являются три гетеродимера. Указанные интегрины ответственны за поздние стадии взаимодействия лейкоцитов, тромбоцитов и эндотелия сосудов. Таблица 15. Интегрины и их роль
3. Адгезивные молекулы суперсемейства иммуноглобулинов (ICAM) - трансмембранные протеины с пятью внеклеточными доменами, экспрессируемые преимущественно эндотелием. Некоторые из этих молекул синтезируются неактивированными клетками и определяют интенсивность физиологической миграции лейкоцитов. В зоне воспаления под влиянием ИЛ-1, ФНО, гамма-интерферона активируются синтез и экспрессия молекул ICAM, что обеспечивает отсроченную фазу адгезии и эмиграции лейкоцитов. В группу белков, подобных иммуноглобулинам, включены лимфоцитарные рцепторы - СD2, СD58 (LFA-3). Они экспрессируются на Т-лимфоцитах и антигенпредставляющих клетках, участвуют в презентации антигена и контакте цитотоксических лимфоцитов с клетками-мишенями. 4. Адрессины - белки эндотелиальных клеток венул лимфоидных органов. Имеют большое значение в миграции лимфоцитов в очаги хронического и аутоиммунного воспаления. При остром воспалении адрессины менее значимы. 5. Хрящевые соединительные белки. Экспрессируются всеми видами лейкоцитов, распознают гиалуроновую кислоту, что обеспечивает перемещение лейкоцитов в основном веществе соединительной ткани. В результате активации эндотелия и экспрессии на мембране Р-селектина и возникает слабое взаимодействие лейкоцитов и эндотелиоцитов, что сопровождается «прокатыванием» (роллинг) лейкоцитов вдоль сосудистой стенки под действием тока крови. Выделение Е-селектина замедляет роллинг лейкоцитов, а после появления на эндотелиоцитах молекул адгезии ICAM-1 и VCAM-1 клетки закрепляются непосредственно на поверхности эндотелия для последующего выхода из сосудов в очаг воспаления. Последовательность выхода лейкоцитов в очаг воспаления получила название закона Мечникова, согласно которому спустя несколько часов (1,5-2 часа) с момента действия флогогена интенсивно эмигрируют нейтрофилы и другие сегментоядерные лейкоциты, а затем моноциты и лимфоциты. Последовательность эмиграции обусловлена последовательностью синтеза и экспрессии молекул адгезии на эндотелии. Так, для эмиграции нейтрофильных лейкоцитов достаточно взаимодействие с Е-селектином, максимальная экспрессия которого происходит через 1-4 ч после начала воспаления. Для эмиграции моноцитов и лимфоцитов, а также для усиления адгезии нейтрофилов необходимо взаимодействие также с молекулами ICAM-1 и VCAM-1. Максимальная экспрессия этих молекул адгезии происходит после 12-24 ч, поэтому выход моноцитов и лимфоцитов из сосудов отсрочен по сравнению с нейтрофилами, которые начинают выходить в очаг воспаления практически сразу после его начала. При развитии аллергического воспаления могут в большом количестве выходить также эозинофильные лейкоциты. Адгезия лейкоцитов обеспечивается взаимодействием молекул адгезии на лейкоцитах с молекулами адгезии на эндотелиальных клетках венозных сосудов, поэтому выход лейкоцитов происходит только на уровне венул. Маргинация начинается на стадии смешанной гиперемии и продолжается, вместе с выселением лейкоцитов, при венозной гиперемии и стазе. Полный стаз приводит к уменьшению эмиграции. 2. Прохождение лейкоцита через сосудистую стенку (диапедез). Все гранулоциты, имеющие сегментированное ядро проходят между эндотелиальными клетками, поскольку их ядро, которое может изменять форму, позволяет проходить через узкие щели (интерэндотелиально). Мононуклеарные клетки, такие как моноциты и лимфоциты также способны проходить между эндотелиальными клетками при значительной активации эндотелия и изменении его формы при воспалении. Кроме того, эти клетки могут идти и через эндотелиальные клетки, т.е. через трансэндотелиальный канал. Продоление базальной мембраны сосудистой стенки осуществляется под действием лизосомных гидролаз ферментов (протеиназ, эластазы, коллагеназы, гиалуронидазы). Лимфоциты, помимо вышеописанного пути эмиграции, обладают способностью проникать прямо через цитоплазму живых клеток сосудистой стенки, не повреждая их. Это явление называется эмпериполез. Эмпериполез участвует в осуществлении миграции лимфоцитов в тимус, в реализации реакции хоуминга лимфоцитов, в частности, при стрессе. Он используется также при эмиграции этих клеток в воспалительные очаги. Не все лейкоциты при воспалении завершают диапедез, некоторые остаются в сосудистой стенке. Пассивному диапедезу вместе с лейкоцитами может подвергаться некоторое количество эритроцитов. Прохождение лейкоцитов через базальную мембрану затруднено связи с плотностью ее структуры. Однако, известно, что лейкоциты имеют рецепторы к элементам базальной мембраны, что обеспечивает их взаимодействие. Кроме того, лейкоциты способны выделять протеолитические ферменты, в частности коллагеназу, которые разрушают элементы базальной мембраны, что облегчает проход лейкоцитов через нее.
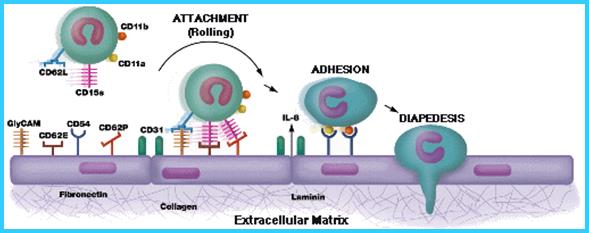
Рис.7. Механизмы адгезии и диапедеза.
3. Движение лейкоцита к очагу воспаления. Процесс движения лейкоцитов (микрофагов, макрофагов) в очаг воспаления называется хемотаксисом, а вещества, вызывающие это направленное движение клеток - хемоаттрактантами. Хемоатрактанты по происхождению подразделяются на экзогенные и эндогенные. К экзогенным хемоаттрактантам относят продукты жизнедеятельности или структурные элементы микроорганизмов, а также другие чужеродные вещества. Хемотаксис опосредуется различными группами веществ: 1. Цитотаксигенами, которые, не являясь хемоаттрактантами, генерируют факторы хемотаксиса. 2. Цитотаксинами, которые оказывают прямое воздействие на лейко-циты. Некоторые цитотаксины специфичны для нейтрофилов (например, экстракт культуры Е.coli), а другие цитотаксины индуцируют миграцию гранулоцитов и моноцитов. Основная же роль в стимуляции хемотаксиса лейкоцитов принадлежит эндогенным хемоаттрактантам. Эндогенные хемоаттрактанты бывают неспецифическими и специфическими. В качестве неспецифических хемоаттрактантов выступают большинство биологически активных веществ, а также продукты повреждения клеток и медиаторы воспаления (гистамин, серотонин, АТФ, ДНК, продукты деградации фибрина (ПДФ), продукты деградации коллагена, фибронектин, тромбин). Некоторые вещества имеют принципиальное значение для хемотаксиса, а нарушение их образования существенно влияет на выход лейкоцитов из сосудов. Эти вещества получили название специфических хемоаттрактантов. К ним относятся: лейкотриен В4 и комплемент (С5а, С3а) (они определяют хемотаксис нейтрофилов, эозинофилов и моноцитов); фактор активации тромбоцитов (влияет на хемотаксис нейтрофилов и эозинофилов) Специфичность лейкотриена В4, комплемента и ФАТ достаточно условна, т.к. эти вещества имеют много других эффектов, из которых стимуляция хемотаксиса – одна из важнейших. При воспалении они образуются в большом количестве и привлекают в очаг воспаления преимущественно нейтрофильные лейкоциты. Важная роль в регуляции хемотаксиса принадлежит – хемокинам (цитокины, образующиеся преимущественно для регуляции хемотаксиса). Наиболее важными химокинами для привлечения лейкоцитов в очаг воспаления являются: интерлейкин-8 (хемотаксис нейтрофилов); эотаксин (хемотаксис эозинофилов); моноцитарный хемотаксический протеин-1 (MCP-1) (хемотаксис моноцитов и Т-лимфоцитов). Хемокины отвечают за более точную регуляцию выхода из сосудов различных лейкоцитов, что способствует правильной последовательности эмиграции лейкоцитов. Табл. 17. Классификация хемоаттрактантов
Точная регуляция последовательности выхода лейкоцитов из сосудов имеет важное биологическое значение. Первой линией защиты при любом воспалении выступают нейтрофильные лейкоциты, которые относятся к неспецифическому иммунитету. При невозможности быстрого уничтожения антигена происходит активное подключение специфического иммунитета, и в очаг воспаления выходят сначала антиген-презентирующие клетки (моноциты крови), а затем лимфоциты.
Дата добавления: 2015-11-28 | Просмотры: 2576 | Нарушение авторских прав |