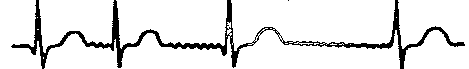|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
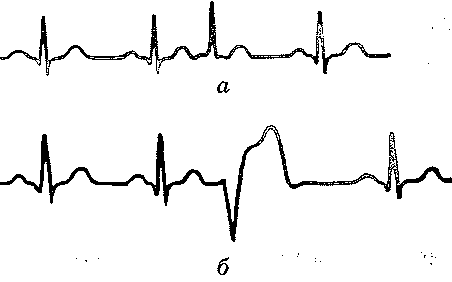
Залізодефіцитні анемії у дітей: причини і механізми розвитку, типові зміни периферичної крові, патогенез основних клінічних проявів. Залізорефрактерні анемії. 6 страницаРис. 122. Спонтанна генерація потенціалів дії в клітинах синусно-передсердного вузла Зміна рівня максимального діастолічного потенціалу, критичного потенціалу або швидкості діастолічної деполяризації в той чи той бік веде до зміни частоти генерації імпульсів або до появи інших джерел імпульсації, якщо ці зміни виникають в інших, здатних до збудження ділянках серця і призводять до появи в них потенціалів дії. При зменшенні рівня максимального діастолічного потенціалу клітин синусно-передсердного вузла, при наближенні до нього критичного потенціалу або збільшенні швидкості повільної діастолічної деполяризації імпульси генеруються частіше, розвивається тахікардія. Це відбувається під впливом підвищеної температури тіла, при розтягненні ділянки синусно-передсердного вузла, при збудженні симпатичних нервів і дії катехоламінів. Навпаки, зменшення швидкості повільної діастолічної деполяризації, гіперпо-ляризація в діастолі й віддалення критичного потенціалу від рівня максимального діастолічного, як це спостерігається при подразненні блукаючого нерва, супроводжуються уповільненням генерації імпульсів, а отже, і скорочень серця — брадикардією. Періодичні зміни тонусу блукаючого нерва під час акту дихання можуть викликати дихальну аритмію (прискорення серцебиття при вдиху, уповільнення — при видиху). Дихальна аритмія в нормі буває у дітей, але зрідка може спостерігатися і у дорослих. 27.20. Які аритмії виникають у результаті порушення збудливості міокарда? Який механізм їх розвитку? В основі аритмій, пов'язаних з порушеннями функції збудливості, лежить поява розташованих поза синусно-передсердним вузлом так званих ектопічних осередків збудження, що генерують позачергові імпульси до скорочення. У патологічних умовах може виявитися власний автоматизм нижчерозташова-них відділів провідникової системи серця (потенційних водіїв ритму). Такі умови можуть виникнути при зниженні автоматизму синусно-передсердного вузла або при підвищенні здатності до генерації імпульсів в інших ділянках міокарда. У цих випадках частота імпульсів, що генеруються нормальним водієм ритму, виявляється недостатньою для пригнічення автоматизму інших відділів, що призводить до появи додаткових імпульсів з ектопічно розташованих осередків збудження. Іншим механізмом, що призводить до появи ектопічних осередків збудження, може бути виникнення різниці потенціалів між розташованими поруч міоцитами внаслідок, наприклад, неодночасного закінчення реполяризації в них, що може викликати збудження у волокнах, які вже вийшли з фази рефрактерності. Це явище спостерігається при локальній ішемії міокарда і при отруєнні серцевими глікозидами. Серед аритмій цієї групи найчастіше бувають екстрасистолія і пароксизмальна тахікардія. 27.21. Що таке екстрасистолія? Назвіть види екстрасистол і їх основні електрокардіографічні характеристики. Екстрасистолія - це вид аритмій, обумовлених порушеннями функції збудливості, що виявляє себе виникненням позачергових скорочень серця або тільки шлуночків. Такі позачергові скорочення отримали назву екстрасистол. Залежно від локалізації осередку, з якого виходить позачерговий імпульс, розрізняють кілька видів екстрасистол: синусну (або номотопну), передсердну, передсерд-но-шлуночкову і шлуночкову (рис. 123). Оскільки хвиля збудження, що виникла в незвичному місці, поширюється в зміненому напрямку, це відображається на структурі електричного поля серця й знаходить відображення на електрокардіограмі. Кожний вид екстрасистоли має свою електрокардіографічну картину, що дає можливість визначити місце ектопічного осередку збудження. Синусна екстрасистола виникає внаслідок передчасного збудження частини клітин синусно-передсердного вузла. Електрокардіографічно вона не відрізняється від нормального скорочення, за винятком укорочення діасто-лічного інтервалу Т-Р. Унаслідок укорочення діастоли й зменшення наповнення шлуночків пульсова хвиля при екстрасистолі зменшена. Передсердна екстрасистола спостерігається при наявності осередку ектопічного збудження в різних ділянках передсердь. Характеризується зміною форми зубця Р (знижений, двофазний, негативний) при збереженому комплексі QRS і деякому подовженні діастолічного інтервалу після екстрасистоли. Це обумовлено тим, що, ідучи ретроградним шляхом, збудження передчасно розряджає нормальний синусний імпульс, який збігається у часі зі збудженням шлуночків. Наступний передсердний імпульс, що виникає через нормальний інтервал, виявляється трохи віддаленим у часі від моменту закінчення збудження шлуночків - неповна компенсаторна пауза. Передсердно-шлуночкова екстрасистола спостерігається при виникненні додаткового імпульсу в передсердно-шлуночковому вузлі. Хвиля збудження, що виходить з верхньої і середньої частин вузла, поширюється у двох напрямках: у шлуночках — у нормальному, у передсердях — у ретроградному. При цьому негативний зубець Р може накладатися на комплекс QRS. Діастолічний інтервал після екстрасистоли трохи подовжений. Екстрасистола може супроводжуватися також одночасним скороченням передсердь і шлуночків. При передсердно-шлуночковій екстрасистолі, що виходить із нижньої частини вузла, виникає компенсаторна пауза, така ж, як і при шлуночковій екстрасистолі. Для шлуночкової екстрасистоли характерна наявність повної компенсаторної паузи після позачергового скорочення. Вона виникає внаслідок того, що збудження, яке охопило шлуночки, не передається через передсердно-шлуночковий вузол назад на передсердя, водночас черговий нормальний імпульс збудження, що йде від синусно-передсердного вузла, не поширюється на шлуночки, бо вони перебувають у фазі рефрактерності. Наступне скорочення шлуночків виникає тільки після приходу до них чергового нормального імпульсу. Тому тривалість компенсаторної паузи, разом з інтервалом, що передує екстрасистолі, дорівнює тривалості двох нормальних діасто-лічних пауз. Однак якщо скорочення серця настільки рідкі, що до моменту приходу чергового нормального імпульсу шлуночки встигають вийти зі стану рефрактерності, то компенсаторної паузи не буває. Позачергове скорочення потрапляє в інтервал між двома нормальними і в цьому випадку воно має назву вставної екстрасистолії. Оскільки хвиля збудження при шлуночковій екстрасистолії поширюється по шлуночках як у прямому, так і в ретроградному напрямках, це супроводжується значними змінами форми комплексу QRS, його деформацією. Рис. 123. Екстрасистоли: а — передсердна, б — шлуночкова 27.22. Що таке пароксизмальна тахікардія? Чим вона характеризується? Пароксизмальна тахікардія - це аритмія, обумовлена порушеннями функції збудливості, яка виявляється виникненням групи екстрасистол, що швидко повторюються і повністю пригнічують фізіологічний ритм. При пароксизмальній тахікардії нормальний ритм серця раптово переривається нападом скорочень частотою від 140 до 250 ударів за хвилину. Тривалість нападу може бути різною - від кількох секунд до кількох хвилин, після чого він так само раптово припиняється і установлюється нормальний ритм. Найчастіше спостерігається передсердна форма пароксизмальної тахікардії. А оскільки тривалість потенціалів дії і тривалість рефрактерних періодів збільшується по ходу провідникової системи, то дистально розташовані ділянки її не завжди здатні відтворити частоту імпульсації, що надходить з проксимальних відділів. Тому більша частина імпульсів при передсердній тахікардії не може проводитися передсердно-шлуночковим вузлом. Оскільки тривалість рефрактерних періодів і потенціалів дії у волокнах правої ніжки пучка Гісса більші, ніж у лівій, при високій частоті імпульсів частіше порушується проведення збудження саме до правого шлуночка. 27.23. Які аритмії виникають у результаті порушень функції провідності міокарда? Виділяють дві групи аритмій, пов'язаних з порушеннями провідності. 1. Блокади серця. Це аритмії, обумовлені уповільненням або повним припиненням проведення імпульсів по провідниковій системі. Причиною блокади може бути ушкодження провідникових шляхів, що веде до подовження рефрактерного періоду і уповільнення або повного припиненням проведення імпульсу. Порушення провідності можуть виникати між синусно-передсердним вузлом і передсердями, усередині передсердь, між передсердями і шлуночками, а також в одній із ніжок пучка Гісса. Тому виділяють такі види блокад: а) внутрішньопередсердну; б) передсердно-шлуночкову; в) внутрішньошлуночкову. 2. Прискорене проведення імпульсів - синдром Вольфа-Паркінсона-Уайта (див. запит. 27.1.25). 27.24. Дайте характеристику передсердно-шлуночкової блокади серця. Передсердно-шлуночкова, або поперечна, блокада серця може бути повною і неповною. У неповній блокаді серця розрізняють три ступені (рис. 124). Передсердно-шлуночкова блокада І ступеня характеризується збільшенням часу проведення імпульсу від передсердь до шлуночків, що супроводжується подовженням інтервалу P-Q (0,2-0,5 с). Блокада II ступеня (періоди Венкебаха) характеризується прогресуючим збільшенням інтервалу P-Q доти, доки одне із збуджень, найчастіше восьме-десяте, не проводиться. Після випадіння скорочення шлуночка інтервал P-Q відновлюється, поступово подовжуючись із кожним наступним скороченням серця. Вважають, що цей феномен пов'язаний з прогресуючим утрудненням проведення імпульсів через вузол. При блокаді III ступеня спостерігають випадання кожного другого-третього скорочення або, навпаки, проводиться тільки кожне друге, третє або четверте збудження передсердь. При повній передсердно-шлуночковій блокаді передсердя і шлуночки скорочуються незалежно одне від одного, кожне у своєму ритмі: передсердя з частотою близько 70, шлуночки — близько 35 скорочень в 1 хв. (ідіовентрикулярний ритм). Особливе значення має момент переходу неповної блокади в повну, коли до шлуночків не надходять імпульси від передсердь. Повільна діастолічна деполяризація в потенційних водіях ритму виникає тільки через якийсь час після припинення надходження імпульсів від синусно-передсердного вузла. Цей період носить назву пре-автоматичної паузи, під час якої спостерігається асистолія шлуночків. При цьому внаслідок припинення надходження крові до головного мозку виникає втрата свідомості, судоми (синдром Морганьї—Едемса—Стокса). Можлива смерть, але найчастіше при поновленні скорочень шлуночків зазначені явища проходять. Синдром може повторюватися багаторазово.
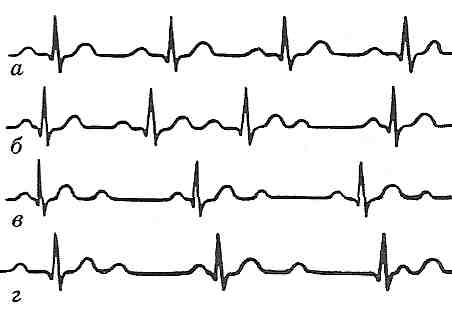
Рис. 124. Передсердно-шлуночкова блокада: а — І ступеня; б—II ступеня; в — III ступеня; г - повна поперечна блокада 27.25. Чим може бути обумовлений розвиток синдрому Вольфа-Паркінсона-Уайта? Синдром Вольфа—Паркінсона—Уайта характеризується прискореним проведенням імпульсів від передсердь до шлуночків, у результаті чого відбувається передчасне збудження останніх, розвивається тахікардія, зменшується інтервал P-Q на електрокардіограмі. Причиною розвитку цього синдрому вважають існування додаткових шляхів проведення імпульсів. До таких шляхів відносять (рис. 125): а) пучок Паладіно—Кента: видозмінена міокардіальна тканина, локалізована в зоні атріовентрикулярного кільця. Може існувати два пучки (лівий і правий), що містяться відповідно у кільцях двостулкового і тристулкового клапанів. Зазначені пучки проводять імпульси від передсердь до шлуночків, минаючи перед-сердно-шлуночковий вузол;
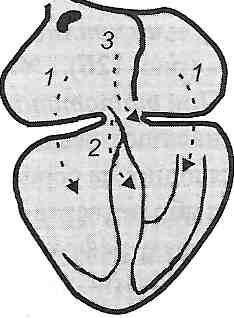
Рис. 125. Додаткові провідникові шляхи серця: 1 — пучок Паладіно— Кента; 2 — пучок Махайма; 3 — пучок Джеймса б) пучок Махайма. З'єднує верхню частину пучка Гісса зі шлуночками; в) пучок Джеймса. Зв'язує передсердя з нижньою частиною передсердно-шлуночкового вузла або з пучком Гісса. По додаткових провідникових шляхах імпульси проводяться швидше і досягають шлуночків раніше імпульсів, які йдуть звичайним чином через передсердно-шлуноч-ковий вузол. Це призводить до передчасної активації частини шлуночків, інша їх частина збуджується пізніше імпульсами, що проходять через передсердно-шлуноч-ковий вузол., 27.26. Які аритмії виникають у результаті одночасного порушення функцій збудливості й провідності? 1. Тріпотіння передсердь (частота скорочень передсердь — 250-400/хв.). 2. Миготіння передсердь (частота імпульсів, що виникають у передсердях, становить 400-600/хв.). Тріпотіння й миготіння передсердь мають однакові причини розвитку і можуть переходити одне в одне. Тому ці два види порушень ритму серця поєднують одним поняттям — миготлива аритмія. 3. Тріпотіння шлуночків (частота скорочень шлуночків — 150—300/хв.). 4. Миготіння (фібриляція) шлуночків (частота імпульсів у шлуночках- 300-500/хв, серце не скорочується). 27.27. Якими ознаками виявляє себе миготлива аритмія? Які механізми її розвитку? При наявності численних ектопічних осередків збудження і такої зміни проведення імпульсу, при якій порушується швидкість його проведення по різних ділянках міокарда або відбувається поширення імпульсу тільки в одному напрямку, створюються умови для тривалої циркуляції хвилі збудження в певному відділі серця, виникають розлади ритму —миготлива аритмія, що може виявлятися тріпотінням [миготінням передсердь (рис. 126).
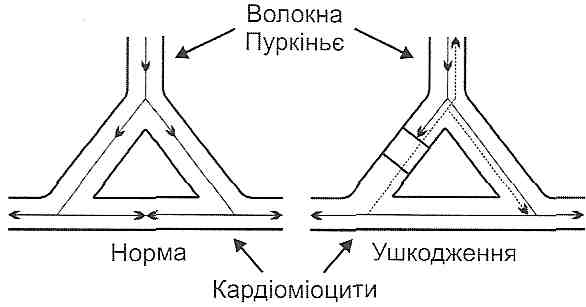
Рис. 126. Миготлива аритмія При тріпотінні передсердь частота їхніх скорочень досягає 250—400/хв. При цьому внаслідок нездатності шлуночків відтворювати високий ритм передсердь розвивається відносна серцева блокада; шлуночки відповідають скороченням на кожне друге, третє або четверте скорочення передсердь, тому що інші хвилі збудження потрапляють у фазу рефрактерності. Скорочення шлуночків можуть виникати раніше, ніж настане достатнє наповнення їх кров'ю - це викликає важкі порушення кровообігу. Якщо кількість імпульсів у передсердях досягає 400-600/хв, говорять про миготіння, або фібриляцію передсердь. При цьому скорочуються лише окремі м'язові волокна, а все передсердя перебуває в стані неповного скорочення, його участь у перекачуванні крові припиняється. Імпульси, що безладно приходять до передсерд-но-шлуночкового вузла по окремих м'язових волокнах передсердя, здебільшого нездатні викликати його збудження, тому що застають вузол у стані рефрактерності або не досягають критичного рівня. Тому передсердно-шлуночковий вузол збуджується нерегулярно, і скорочення шлуночків носять випадковий характер. Як правило, число скорочень шлуночків за хвилину перевищує нормальне. Нерідко скорочення шлуночків відбуваються до їх наповнення кров'ю й не супроводжуються пульсовою хвилею. Тому частота пульсу стає меншою за частоту скорочень серця (дефіцит пульсу). Найчастіше причиною розвитку миготливої аритмії є (правило 03): а) стеноз лівого атріовентрикулярного отвору, б) тиреотоксикоз; в) атеросклеротичний кардіосклероз. Нині найбільш визнаною теорією, що пояснює механізми розвитку миготливої аритмії (і екстрасистолії!), є теорія повторного входження імпульсів (re-entry) (рис. 127). Відповідно до неї, тріпотіння і миготіння виникають як наслідок порушень провідності, при яких поширення імпульсів припиняється тільки в одному (антеградному) напрямку і зберігається у зворотному (ретроградному). При цьому створюються умови для постійного руху імпульсів по колу в міокарді. У нормальних умовах хвиля збудження, виникнувши в одному місці, поширюється в обидва боки серцевої камери. Досягнувши протилежної стінки, вона згасає, зустрівшись з іншою хвилею, що залишила за собою зону рефрактерності. Якщо ж унаслідок виникнення тимчасового блоку або запізнення приходу збудження по деяких волокнах міокарда збудження приходить до місця, що вже вийшло зі стану рефрактерності, то створюються умови для тривалеї циркуляції імпульсу, що виник.
Рис. 127. Механізм повторного входження імпульсів 27.28. Що таке фібриляція шлуночків? Коли вона виникає й чим виявляє себе? При деяких патогенних впливах (проходження електричного струму через серце, наркоз хлороформом або циклопропаном, закупорка вінцевих артерій або інші випадки різкої гіпоксії, травма серця, дія токсичних доз наперстянки і кальцію) виникає фібриляція шлуночків. При цьому внаслідок хаотичного скорочення окремих м'язових волокон пропульсивна сила скорочень практично зникає, кровообіг припиняється, швидко настає втрата свідомості і смерть. Фібриляції сприяють зменшення концентрації внутрішньоклітинного калію, що веде до зниження мембранного потенціалу кардіоміоцитів і легшого виникнення в них деполяризації та збудження, а також зміна вмісту нервових медіаторів, особливо катехоламінів. При лікуванні фібриляції шлуночків найефективнішим є пропускання через серце короткого сильного одиничного електричного розряду (дефібриляція). При цьому відбувається одночасна деполяризація всіх волокон міокарда і припиняються асинхронні збудження м'язових волокон. Як захід, що попереджає розвиток фібриляції, застосовують корекцію електролітного складу крові. 27.29. Чим може бути обумовлений розвиток порушень скорочувальної функції міокарда? У клітинах робочого міокарда відбувається п'ять процесів, які визначають скорочувальну функцію серця. Усі вони можуть порушуватися і становити основу розвитку недостатності серця. Розлади скорочувальної функції міокарда можуть бути обумовлені порушеннями: 1) збудження кардіоміоцитів; 2) електромеханічного спряження; 3) процесів власне скорочення; 4) процесів розслаблення; 5) енергозабезпечення міокарда. 27.30. Які фактори впливають на характер потенціалу дії і збудливість кардіоміоцитів? Якими електрофізіологічними ознаками виявляють себе зміни їхньої збудливості? а) характеру електричної імпульсації, що надходить до кардіоміоцитів по провідниковій системі серця. При аритміях можливе порушення основних параметрів потенціалу дії волокон робочого міокарда і його збудливості; б) стану (властивостей) сарколеми кардіоміоцитів, і насамперед іонних каналів. Нині відомі хімічні агенти, здатні вибірково порушувати провідність цих каналів. Це блокатори Na-каналів, Са-каналів, К-каналів; в) концентрації позаклітинних іонів, що беруть участь у формуванні електричних потенціалів на мембрані кардіоміоцитів. В умовах in vivo найбільше значення має позаклітинна концентрація іонів калію. Зміни збудливості волокон міокарда можуть виявляти себе: 1) змінами тривалості потенціалів дії, а отже, і сили серцевих скорочень. Зменшення тривалості потенціалів дії виникає при збільшенні частоти стимуляції, збільшенні позаклітинної концентрації іонів калію, при дії ацетилхоліну. Збільшення тривалості потенціалу дії характерно для охолодження; 2) змінами тривалості періодів абсолютної і відносної рефрактерності, а отже, здатності сприймати імпульсацію (засвоювати ритм). Тривалість цих періодів залежить від тривалості потенціалів дії. 27.31. Як впливають зміни позаклітинної концентрації іонів калію на збудливість міокарда? Позаклітинна концентрація іонів калію впливає на збудливість міокарда через рівень потенціалу спокою кардіоміоцитів. Збільшення концентрації іонів калію — гіперкаліємія - викликає деполяризацію мембрани м'язових волокон. При цьому характер змін збудливості міокарда залежить від рівня гіперкаліємії. Виділяють такі діапазони концентрацій іонів калію, для яких характерні певні картини порушень: 1) від 4 до 8 ммоль/л. Відбувається незначна деполяризація, мембранний потенціал падає від -90 мВ до -80 мВ. При цьому стан Na-каналів сарколеми істотно не змінюється. Унаслідок того, що величина мембранного потенціалу наближається до критичного рівня деполяризації, збудливість м'язових волокон і швидкість проведення імпульсів зростають; 2) від 8 до 35 ммоль/л. Мембранний потенціал падає від -80 мВ до -40 мВ. При такому рівні деполяризації значно зменшується провідність швидких потенціал-залежних Na-каналів (період відносної рефрактерності). Наслідком є зменшення збудливості і провідності, а також зміни характеру потенціалів дії (зменшення тривалості, амплітуди, крутості); 3) понад 35 ммоль/л. Мембранний потенціал стає менше -40 мВ. При цьому всі швидкі потенціалзалежні Na-канали перебувають у стані інактивації (абсолютна рефрактерність) — відбувається зупинка серця. Зменшення позаклітинної концентрації іонів калію — гіпокаліємія — викликає гі-перполяризацію мембрани. Якщо гіпокаліємія досягає рівня 2—3 ммоль/л, дещо збільшується поріг деполяризації, зменшується збудливість, збільшуються тривалість потенціалів дії і сила скорочень серця. 27.32. Що таке кардіоплегія? Які використовують підходи до її здійснення? Кардіоплегія — це штучна зупинка серця, яку застосовують під час операцій на "сухому" серці. Розроблено такі підходи до здійснення кардіоплегії: а) ішемічна кардіоплегія. Перетискають аорту до відходження вінцевих артерій. Оскільки через 30 хв. починаються необоротні зміни в міокарді, цей підхід можна використати при короткочасних операціях (до 10—15 хв.); б) хімічна кардіоплегія. У вінцеві артерії вводять кардіоплегічні розчини, до складу яких входять високі концентрації іонів калію, ацетилхолін і деякі інші препарати. Цей метод дозволяє проводити операції на "сухому" серці протягом 40-60 хв.; в) холодова кардіоплегія. її досягають зрошенням серця охолодженим до +4 °С... — 5 °С фізіологічним розчином. Тривалість операцій на серці при цьому може становити 60 хв. 27.33. Які фактори впливають на характер електромеханічного спряження в міокарді? 1. Тривалість потенціалу дії. 2. Частота потенціалів дії. 3. Концентрація іонів кальцію в позаклітинній рідині. 4. Стан Са-каналів сарколеми кардіоміоцитів. 5. Стан систем видалення іонів кальцію із цитоплазми м'язових волокон. 27.34. Як зміни тривалості і частоти потенціалів дії впливають на силу серцевих скорочень? Зміни тривалості потенціалів дії в кардіоміоцитах відбуваються за рахунок укорочення або подовження фази "плато ", під час якої іони Са2+ через потенціалзалеж-ні Са-канали сарколеми надходять у саркоплазму. З урахуванням того, що концентрація іонів Са2+ у цитоплазмі м'язових волокон визначає кількість актоміозинових комплексів, що утворюються, а отже, і силу скорочень, можна зробити такий висновок. При зменшенні тривалості потенціалу дії зменшується надходження іонів Са2+ у саркоплазму і, як наслідок, зменшується сила скорочення м'язового волокна. При збільшенні тривалості потенціалу дії — все навпаки. Тривалість потенціалу дії кардіоміоцитів зменшується при гіперкаліємії, при дії на м'язові волокна ацетилхоліну. Збільшення тривалості потенціалу дії характерне для гіпокаліємії, охолодження серця. При збільшенні частоти потенціалів дії, незважаючи на те, що тривалість кожного окремого потенціалу, а отже, і фази "плато" зменшується, сумарна тривалість зазначеної фази за одиницю часу збільшується. Це означає, що в кардіоміоцитах створюються більш високі концентрації Са2+ і, як наслідок, збільшується сила скорочення м'язових волокон. Цим, зокрема, пояснюється хроноінотропний механізм негайної компенсації серця (див. запит. 27.10). При зменшенні частоти потенціалів дії (наприклад, при брадикардії) сумарна тривалість фази "плато" за одиницю часу зменшується, що веде до зменшення концентрації Са2+ у саркоплазмі і зменшення сили скорочень серця. 27.35. Як впливає позаклітинна концентрація іонів кальцію на силу скорочень серця? Що таке "кальцієвий парадокс"? На початку XX ст. Рінгером було показано, що в розчині, позбавленому іонів кальцію, ізольоване серце швидко зупиняється. Нині відомо, що причиною цього є повне роз'єднання збудження і скорочення. В умовах норми іони кальцію, що надходять під час фази "плато" потенціалу дії з позаклітинного середовища в саркоплазму кардіоміоцитів, "запускають" вивільнення Са2+ із саркоплазматичного ретикулуму й поповнюють його запаси в цих структурах м'язових волокон. При зменшенні позаклітинної концентрації Са2+ його запаси в саркоплазматичному ретикулумі швидко виснажуються, концентрація Са2+ у саркоплазмі падає й, отже, зменшується сила серцевих скорочень. "Кальцієвий парадокс" — це експериментальний феномен, що розвивається після того, як у безкальцієвий розчин, яким здійснювали перфузію серця протягом декількох хвилин, вносять іони кальцію. При цьому розвивається необоротне ушкодження міокарда: зменшується вміст АТФ і креатинфосфату, з кардіоміоцитів виходять білки, у тому числі ферменти (міоглобін, креатинкіназа), руйнується саркоплаз-матичний ретикулум. "Кальцієвий парадокс" пояснюють тим, що в безкальцієвому розчині відбувається розшарування глікокалікса кардіоміоцитів (зовнішній шар глікокалікса відокремлюється від внутрішнього), у результаті чого значно зростає проникність сарколеми до іонів кальцію. При наступному внесенні в середовище іонів Са2+ відбувається їх масивне надходження у клітини, різко зростає його концентрація в саркоплазмі, що "запускає" кальцієві механізми ушкодження (див. розд. 11). 27.36. Які фактори впливають на стан кальцієвих каналів сарколеми кардіоміоцитів? Чим можуть бути обумовлені їх активація і блокада? У сарколемі кардіоміоцитів є потенціолзалежні повільні Са-канали. Це білкові молекули, вмонтовані в плазматичну мембрану і здатні пропускати через себе іони кальцію в тому випадку, коли вони відкриті. Відкриття Са-каналів відбувається при деполяризації мембрани. Відкриватися здатні не всі наявні канали, а тільки фосфо-ровані (активовані). Під активацією Са-каиалів розуміють їх фосфорування, у результаті чого збільшується кількість Са-каналів, здатних відкриватися при виникненні потенціалу дії. В основі фосфорування Са-каналів лежить збільшення концентрації цАМФ у саркоплазмі м'язових волокон. Усі фактори, що викликають утворення цАМФ, ведуть до активації Са-каналів. До таких, зокрема, належать: а) катехоламіни і фармакологічні агенти, що активують fi-адренорецептори; б) інгібітори фосфодіестерази (метилкеантини: теофілін, кофеїн та ін.). Зазначені агенти збільшують вміст цАМФ або через активацію аденілатциклази (через 0-адренорецептори), або через пригнічення руйнування цАМФ (інгібітори фосфодіестерази). З активацією Са-каналів пов'язаний позитивний інотропний ефект катехола-мінів/Q основі його така послідовність подій: катехоламіни → активація р-адрено-рецепторів → активація аденілатциклази → утворення цАМФ → активація проте-їнкіназ → фосфорування Са-каналів сарколеми → збільшення надходження Са2+ у саркоплазму під час потенціалів дії →збільшення концентрації Са2+ у саркоплазмі → збільшення сили скорочень серця. В умовах блокади Са-капалів зменшується надходження іонів Са в саркоплазму кардіоміоцитів і, отже, зменшується сила серцевих скорочень. Блокаду Са-каналів викликають: а) ендогенні фактори — дефіцит АТФ, дефіцит цАМФ, іони водню (ацидоз); б) екзогенні фактори — двовалентні іони (Ni2+, Со2+, Мп2+), деякі тривалентні іони (La3+), органічні сполуки, що їх застосовують у практичній медицині (верапаміл, ніфедипін та ін.). 27.37. Які фактори впливають на стан систем видалення іонів кальцію з кардіоміоцитів і, як наслідок, на силу серцевих скорочень? До таких чинників відносять: а) серцеві глікозиди — фармакологічні препарати рослинного походження, що підвищують силу скорочень серця (препарати дигіталісу, строфантин та ін.); б) ендогенні дигіталісоподібні і строфантиноподібні фактори. Вважають, що серцеві глікозиди, яких здавна використовують в медицині, імітують дію цих, відносно недавно відкритих, ендогенних природних факторів. Фізіологічне значення останніх сьогодні ще не встановлено. Механізм дії серцевих глікозидів і подібних до них ендогенних факторів пов'язаний з пригніченням активності Na-K-АТФ-ази кардіоміоцитів. Наслідком цього є порушення роботи Na-K-насосів сарколеми, зменшення градієнта концентрацій іонів Na+ по обидва боки плазматичної мембрани м'язових волокон. Це призводить до порушення Na-Ca-обмінного механізму в кардіоміоцитах, у результаті чого зменшується видалення Са2+ із саркоплазми в позаклітинне середовище і збільшується внутрішньоклітинна концентрація Са2+. Останнє і обумовлює збільшення сили серцевих скорочень. Дата добавления: 2016-03-26 | Просмотры: 561 | Нарушение авторских прав |