|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
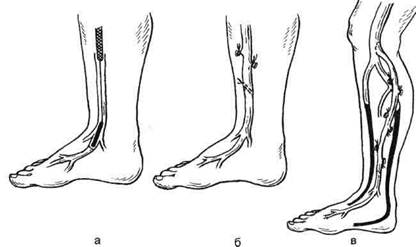
Артериализация венозного кровотока стопыНесмотря на значительные успехи сосудистой хирургии, лечение больных с окклюзирующими поражениями дистального артериального русла нижних конечностей остается актуальной проблемой клинической ангиологии. У 14,9—20 % больных из-за окклюзии артерий голени и стопы реконструктивные операции не выполняют, а производят первичную ампутацию конечности. Неудовлетворенность большим числом тромботических осложнений и ампутаций конечностей при лечении окклюзии дистального артери- ального русла заставляет хирургов искать более эффективные методы реваскуляризации. В последнее время предложены микрососудистая трансплантация сальника на нижнюю конечность, лечение экстравазатами крови по Бытка, продольная ком-пактотомия по Илизарову и реваску-ляризирующая остеотрепанация по Зусмановичу. Эти методы позволяют улучшить кровообращение конечности при окклюзии дистального артериального русла за счет развития коллатерального кровообращения. Однако для получения эффекта пос- ле таких операций необходим срок от 1 до 3 мес, поэтому их применение ограничено у больных с критической ишемией (III и IV степень ишемии конечности). История артериализации. На протяжении столетия интерес хирургов привлекало использование венозного сосудистого русла для доставки артериальной крови к дистальным отделам ишемизированной конечности. В 1896 г. A. Francois-Frank, наложив у собак анастомоз между бедренной артерией и веной, отметил выраженную дилатацию артериали-зованной вены. В 1902 г. было опубликовано 2 сообщения о применении артериовенозного анастомоза на бедре для лечения гангрены нижних конечностей. В обоих наблюдениях не удалось остановить прогрессиро-вание гангрены, однако эта проблема становится предметом экспериментальных и клинических исследований с публикацией большого числа работ, посвященных артериализации венозного кровотока для лечения хронической артериальной недостаточности нижних конечностей. Успех артериализации был достигнут лишь в единичных случаях, как, например, у A.E.Halsted в 1912 г., — у 3 больных из 42 оперированных. Авторы связывали многочисленные тромбозы с наличием в венозной системе клапанов, которые препятствуют ретроградному кровотоку артериальной крови. Был предпринят другой путь артериализации венозного кровотока — через поверхностную венозную систему. A.Sheil в 1977 г. использовал большую подкожную вену in situ для транспорта крови в ретроградном направлении с целью артериализации поверхностных вен стопы. У 3 больных из 6 удалось компенсировать тяжелую ишемию и спасти конечность от ампутации. Позднее, в 1982 г., F.Lenqua и соавт. использовали реверсированную аутовену для артериализации поверхностных вен стопы с наложением дистального анасто- моза в области медиальной лодыжки. У 3 больных из 8 был получен хороший результат, у 2 пациентов — временное улучшение. Разрушение клапанов в истоках большой подкожной вены авторы этой методики не выполняли. Успех операции связывали с тем, что в поверхностных венах стопы часто отсутствуют клапаны и возможно получение реверсии кровотока в дистальных отделах венозного русла. В отделении хирургии сосудов Института хирургии им. А.В.Вишневского с июня 1986 г. А.В.Покровским и соавт. стала применяться методика артериализации, предложенная A.Sheil, но с обязательным разрушением венозных клапанов в истоках большой подкожной вены в ретроградном направлении. В 1987 г. А.В.Покровский и соавт. впервые в мире стали выполнять артериализацию и реверсию венозного кровотока в глубокую венозную систему стопы с формированием дистального анастомоза на уровне голеностопного сустава. Для этой цели были использованы дис-тальная часть задней берцовой вены и плантарная вена. Успех реваскуля-ризации зависит от адекватного разрушения клапанов в венах стопы. В плантарной вене таких клапанов может быть 4—5. Патогенез. Каково же патогенетическое обоснование клинического улучшения кровообращения конечности при артериализации и реверсии венозного кровотока стопы? Существует 4 основных механизма купирования явлений критической ишемии при артериализации и реверсии венозного кровотока стопы: • улучшение оксигенации тканей через венозную систему за счет артериализации и реверсии венозного кровотока; • блокировка артериовенулярного сброса за счет повышения давления в венулах; • увеличение притока артериальной крови к ишемизированной ко- нечности за счет создания дополнительного пути оттока; • формирование артериовенозной фистулы является мощным стимулом для развития коллатерального кровообращения конечности. Три первых механизма проявляется в первые часы после операции, что очень важно для больных с критической ишемией конечности. Отмечаются купирование болевого синдрома, улучшение оксигенации тканей, способствующее уменьшению трофических нарушений на стопе или позволяющее выполнять хирургическую обработку язв стопы. Четвертый механизм направлен на развитие артериальной коллатеральной сети голени и стопы, что в последующем, несмотря на тромбоз артери-овенозного трансплантата, в срок более 6 мес с момента операции не приводило к рецидиву ишемии конечности. Показания к артериализации и реверсии венозного кровотока стопы: ▲неэффективность консервативных мероприятий в купировании явлений критической ишемии; ▲окклюзия артерий голени и стопы; ▲наличие условий местной операбельности (распространение язвенно-некротических дефектов не выше границы дистальной и средней трети стопы; ▲отсутствие острого флебита на стопе; проходимая подколенная артерия или поверхностная бедренная артерия в нижней трети. Для выполнения артериализации венозного кровотока стопы существуют следующие противопоказания: ▲гангрена стопы с переходом на область голеностопного сустава; ▲противопоказания, относящиеся к любому хирургическому вмешательству (инсульт головного мозга и инфаркт миокарда сроком до 3 мес; де-компенсированная стадия сердечно-легочной, печеночно-почечной недостаточности). Техника артериализации истоков большой подкожной вены на стопе реверсированной аутовеной. Забор вены производят на бедре. Операцию начинают с выделения подколенной или бедренной артерии в непораженном сегменте. Если информация о наличии проходимого участка артерии стопы неубедительна, выполняют интраоперационную артерио-графию с предварительным введением в артерию 4 мл папаверина или но-шпы. При подтверждении окклюзии всех артерий голени и стопы выделяют истоки большой подкожной вены. Разрез кожи выполняют дугообразно от переднего края медиальной лодыжки с переходом на тыл стопы до уровня проксимальной головки II плюсневой кости. Основной ствол большой подкожной вены и его ветви мобилизуют. После системной гепаринизации больного (5000 ЕД на 70 кг массы тела) разрушают венозные клапаны на стопе. Для этого через поперечное веното-мическое отверстие или крупную ветвь в области голеностопного сустава в ретроградном направлении по отношению к естественному венозному кровотоку вводят металлический буж диаметром 2—3 мм (рис. 7.24, а). Буж упирается в створку венозного клапана, и достаточно небольшого усилия, чтобы ее разрушить. Затем на противоположной стенке вены разрушают вторую створку, после чего буж свободно проходит к наружной поверхности стопы в поверхностную венозную дугу. Обычно в вене на стопе имеется 1—2 клапана. Если клапан разрушить не удалось, то производят поперечную венотомию в его проекции и иссекают его створки, после чего ушивают отверстие в вене в поперечном направлении узловыми швами нитью пролен 7/0. При малейших сомнениях в надежности разрушения клапанов следует выполнять интраоперационную ретроградную флебографию, потому что неразрушенная створка может служить причиной тромбоза в бли-
Рис. 7.24. Артериализация истоков большой подкожной вены реверсированной ауто-веной (объяснение в тексте). жаишем послеоперационном периоде. Для контроля за разрушением клапанов может использоваться ан-гиоскопия. Аутовену, взятую на бедре, после отмывания от крови и сгустков изотоническим раствором натрия хлорида с добавлением 5000 ЕД гепарина подвергают гидравлической дила-тации, реверсируют и формируют дистальный анастомоз (рис. 7.24, б). Дистальный анастомоз накладывают конец в конец с большой подкожной веной на тыле стопы. Стенки соединяемых сосудов срезают косо, чтобы просвет в зоне анастомоза не был сужен и длина соустья была не менее 1—1,5 см. Анастомоз накладывают обвивным швом нитью пролен 7/0. Желательно использовать при этом микрохирургический инструментарий и операционные лупы с 3,5—5,5-кратным увеличением. После формирования дистального анастомоза аутовенозный трансплантат проводят подкожно и проксимальный анастомоз накладывают с непораженным участком подколенной или бедренной артерии в нижней трети (рис. 7.24, в). Проксимальный анастомоз длиной 1,5—2,0 см формируют конец в бок непрерывным обвивным швом нитью пролен 6/0. При пуске кровотока сначала снимают зажим с артерии, а после заполнения протеза кровью снимают зажим с истоков большой подкожной вены. После восстановления кровотока мы всегда выполняем контрольную ангиографию с контрастированием сосудов стопы и зоны дистального анастомоза. Интраоперационный контроль позволяет выявить неразрушенные створки клапанов, большой сброс крови в глубокую венозную систему и обкрадывание за счет этого поверхностной венозной дуги. Обнаруженные недостатки устраняют перевязкой 1—2 крупных ветвей в зоне голеностопного сустава; неразрушенные створки иссекают. Техника артериализации истоков большой подкожной вены на стопе по методике in situ. При наличии на голени непораженного магистрального ствола большой подкожной вены, проходимого на всем протяжении и без признаков воспаления, предпочтительна артериализация по методике in situ. Оставление на месте ствола большой подкожной вены, исполь- зуемого в качестве артериального протеза, значительно упрощает реконструктивную операцию, не нарушает питания стенки сосуда. Очень важным показанием к использованию аутовены по методике in situ является высокий уровень наложения проксимального анастомоза — общая бедренная артерия и поверхностная бедренная артерия до гунтеро-ва (приводящего) канала. Операцию начинают с выделения истоков большой подкожной вены на стопе. Затем мобилизуют артерию и участок большой подкожной вены в зоне предполагаемого проксимального анастомоза, вену пересекают, проксимальный конец ее перевязывают, а дистальный участок перемещают к артерии и накладывают анастомоз по типу конец в бок (рис. 7.25, а). Анастомоз длиной 1,5—2 см накладывают непрерывным обвивным швом нитью пролен 6/0. После пуска кровотока появляется пульсация вены до уровня первого клапана. Со стопы через крупную ветвь в области голеностопного сустава или через поперечное венотомическое от- верстие в основной ствол большой подкожной вены вводят антеградно разрушитель клапанов. Нами использовались разрушитель венозных клапанов Халла в модификации I.Gruss, а также металлический клапанотом фирмы "Baxter". Разрушитель заводили за первый клапан, на котором прекращался артериальный кровоток, и затем плавно низводили вниз к стопе (рис. 7.25, б), при этом его головка разрывала створки клапанов. Манипуляцию повторяли 2—3 раза с поворотом головки вокруг собственной оси для разрушения всех створок, после чего из проксимального конца вены появлялся хороший пульсирующий кровоток. Затем ретроградным блокированием разрушают клапаны на стопе. Ветвь или отверстие, через которые вводили разрушитель клапанов, перевязывают или ушивают (рис. 7.25, в). После пуска кровотока появляется отчетливая пульсация основного ствола и ветвей большой подкожной вены на стопе. Для того чтобы уменьшить сброс артериальной крови в глубокую ве-
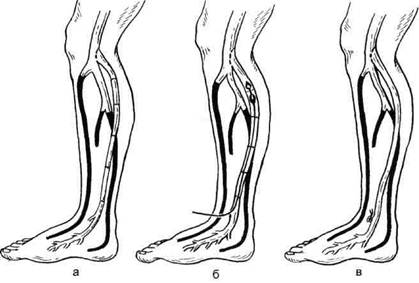
Рис. 7.25. Артериализация истоков большой подкожной вены по методике in situ (объяснение в тексте). 15-4886
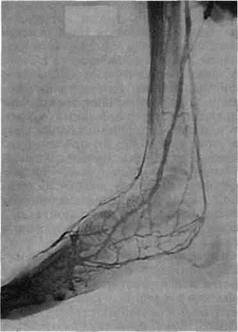
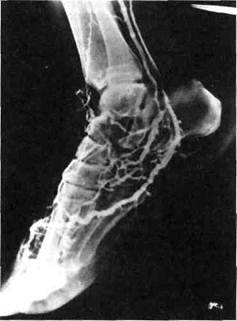
Рис. 7.26. Контрольная ангиограмма после артериализации истоков большой подкожной вены.
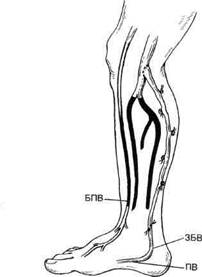
Рис. 7.27. Артериализация глубокой венозной системы стопы. БПВ — большая подкожная вена; ПВ — план-тарная вена; ЗБВ — задняя берцовая вена. нозную систему на голени, перевязывают крупные коммуникантные ветви большой подкожной вены. Места отхождения крупных ветвей определяют пальпаторно по характерному систолодиастолическому дрожанию. Для более точного определения ветвей, по которым осуществлялся артериовенозный сброс, используют рентгеноконтрастную ангиографию, ангиоскопию или же интраопераци-онное дуплексное сканирование. Кожу в этом месте рассекают, ветвь вены лигируют. После пуска кровотока всегда выполняют контрольную ангиографию (рис. 7.26). Техника артериализации глубокой венозной системы стопы (рис. 7.27). Операцию начинают с выделения самого дистального артериального сегмента с неизменным магистральным кровотоком. Этот уровень используют для наложения проксимального анастомоза. В сомнительных случаях выполняют интраоперационную ангиографию дистального артериального русла с фармакопробой (4 мл папаверина). Убедившись в отсутствии магистральных артерий на голени и стопе, выделяют сосудисто-нервный пучок позади медиальной лодыжки. На одну из заднеберцовых вен накладывают держалку. Следующим этапом производят забор большой подкожной вены на бедре через отдельные разрезы, выполняют ее гидравлическую ди-латацию. При отсутствии достаточной длины неизменной аутовены формируют комбинированный трансплантат с протезом из ПТФЭ, причем реверсированную аутовену ставят в дистальную позицию. После системной гепаринизации (5000 ЕД гепарина) пересекают заднюю берцовую вену на уровне голеностопного сустава, проксимальный конец лигируют, а в дистальный конец в ретроградном направлении по отношению к венозному току крови вводят последовательно металлические бужи диаметром 1,5—3 мм и разрушают клапаны. Важным условием успеха операции считается адекват- ное разрушение клапанов в плангарной вене. После разрушения клапанов проверяют дебит по вене шприцем и одновременно плантарную вену подвергают гидравлической ди-латации. При адекватном разрушении клапанов сопротивление жидкости, вводимой шприцем, практически отсутствует, при затруднении выполняют повторное разрушении клапанов. Если после повторных попыток разрушения клапанов сопротивление в вене сохраняется, следует произвести дистальную флебографию. После подготовки берцовой вены формируют дистальный анастомоз по типу конец в конец нитью пролен 7/0, желательно с применением операционных луп с увеличением 3,5—5,5. После наложения дистального анастомоза трансплантат подкожно или подфасциально проводят в подколенную область или на бедро и формируют проксимальный анастомоз по типу конец в бок нитью пролен 6/0 с проходимым артериальным сегментом. После пуска кровотока выполняют контрольную ангиографию или интраоперационную ангиоскопию (рис. 7.28). В выборе пластического материала для данной реконструктивной операции отдают предпочтение аутове-не. Однако отсутствие вены не является противопоказанием к артериа-лизации. В таких случаях в качестве сосудистых протезов используют го-моартериальные трансплантаты и синтетические протезы из ПТФЭ. Необходимо подчеркнуть важность разрушения клапанов в истоках большой подкожной вены и в пл ангарной вене. Общее количество клапанов обычно составляет 3,1 ± 0,31. Количественную характеристику функции артериовенозного трансплантата можно получить при помощи интраопе-рационной флоуметрии. Объемная скорость кровотока по артериове-нозному трансплантату должна превышать 100 мл/мин.
Рис. 7.28. Контрольная ангиограмма плантарной вены после разрушения в ней клапанов. Интраоперационная ангиография является менее информативным методом контроля за эффективностью артериализации венозного кровотока стопы, так как не всегда удается объективно оценить качество разрушения клапанов в аутовене и выявить остатки разрушенных клапанов и обрывки интимы. Для контроля за качеством наложения дистального анастомоза и заполнением венозной системы стопы после артериализации ангиография является адекватным методом. Особенности послеоперационного ведения. У больных с артериализаци-ей венозного кровотока стопы особое значение придается послеоперационной терапии, направленной на профилактику ранних тромбозов. Предпочтение отдают гепаринотера-пии по схеме: в первые 3—5 сут — введение гепарина (суточная доза 20 000—30 000 ЕД) осуществляют че-
15*
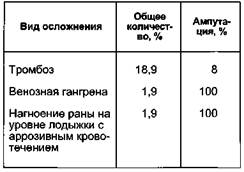
рез перфузор под контролем времени свертывания крови, в последующем этих пациентов переводят на подкожное введение гепарина (суточная доза 20 000 ЕД) в течение 5—10 сут с дальнейшим переходом на дезагре-гантную терапию (ацетилсалициловая кислота — 100 мг). Осложнения раннего послеоперационного периода представлены в табл. 7.2. В ближайшем послеоперационном периоде самым частым осложнением является тромбоз артериовенозного трансплантата. В таких случаях показано срочное повторное оперативное вмешательство, направленное на выявление причин тромбоза и их устранение. Основная причина тромбоза — обычно неразрушенная створка клапана в венах стопы. Повторные оперативные вмешательства не всегда
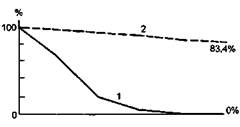
Рис. 7.29. Кумулятивная проходимость артериовенозных трансплантатов (1) и кумулятивный процент сохраненных конечностей (2). дают возможность восстановить магистральный кровоток по артериове-нозному шунту, и при нарастании ишемии выполняют ампутацию конечности. Такие осложнения, как венозная гангрена стопы и нагноение дисталь-ной раны с развитием аррозивного кровотечения, всегда требуют ампутации конечности, несмотря на функционирование артериовенозного шунта. Результаты лечения критической ишемии конечности артериализацией и реверсией венозного кровотока стопы. Анализ результатов артериализа-ции венозного кровотока стопы, выполненной более чем у 150 пациентов, свидетельствует о том, что в ближайшем послеоперационном периоде удается купировать явления критической ишемии у 79,7 % больных с облитерирующим тромбанги-итом и у 93,8 % больных с облитерирующим атеросклерозом. Кумулятивная проходимость артериовенозных трансплантататов и кумулятивный процент сохраненных конечностей представлены на рис. 7.29. Исходя из отдаленных результатов, можно заключить, что самым важным механизмом в сохранении конечности в отдаленные сроки после артери-ализации является быстрое и бурное развитие коллатерального кровообращения в нижней конечности. Тромбоз артериовенозного трансплантата в отдаленные сроки не приводит к ампутации и, как правило, происходит незаметно для больного. Таким образом, артериализация венозного кровотока стопы является альтернативой ампутации конечности у больных с критической ишемией нижних конечностей, когда нет возможности выполнить стандартную реконструктивную операцию, а консервативные мероприятия неэффективны. Артериализация венозной системы стопы позволяет избавить более 80 % больных от ампутации и обеспечить высокий процент сохраненных конечностей в будущем. Литература Бытка П.Ф., Чикалэ Е.Т., Жица В. Т. Морфологические изменения в зоне экстравазатов, созданных в целях борьбы с ишемией тканей у больных с хроническими облите-рирующими поражениями периферических артерий//Здравоохранение (Кишинев). — 1978. - № 6. - С. 3-6. Бытка П. Ф., Чикалэ Е. Т. Феномен искусственно наведенной регенерации микрососудов как лечебный фактор в борьбе с ишемией тканей при хронических облитериру-ющих заболеваниях//Острые хирургические заболевания органов брюшной полости. — Кишинев, 1979. — С. 8—9. Бытка П.Ф., Чикалэ Е.Т. Стимуляция кровотока в конечностях при облитерирующих поражениях артерий//Хирургия. — 1982. — №7.-С. 102-110. Илизаров Г.А., Зусманович Ф.И. Способ лечения хронической ишемии нижних конеч-ностей//Авторс. св-во. № 061803, 1983. Кириллов Б. П. Проблема создания искусственного окольного кровообращения//Хи-рургия. - 1953. - № 2. - С. 3-13. Кириллов Б.П., Кириллов Ю.Б. Постоянное обходное шунтирование при нарушении кровотока в аортобедренном сегменте//Хи-рургия. - 1968. - № 5. - С. 50-56. Путелис Р.А. Причины смерти больных после ампутации конечностей при поражении артерий//Хирургия. — 1982. — № 7. — С. 52-52. Фокин А.А., Кулак А.И., Фокин Ал.А., Вербо-вицкий Л.П. Лечение окклюзионных заболеваний артерий нижних конечностей по методу Г.А.Илизарова//Хирургия. — 1988. — № 8. - С. 82-85. Casten D.F., Alday E.S. Omental transfer for revascularization of the extremities//Surg. Gynec. Obstet. - 1971. - Vol. 132. -P. 301-304. Francois-Frank A. Note a propos de la communication de M.Raymond Potit sur la suture arterio-veineuse//Compt. reud. Soc. biol. - 1896. - Vol. 10. - P. 150-156. Lenqua F., Nuss J.M. Long term result of six arteriovenous anastomosis in patients with early necrosis of the foot due to obliterative arterial disease//Chirurgie. - 1982. - Vol. 108. -P. 121-130. Maurya Sh.D., Singhal S., Gupta H.Ch. et al. Pedicled omental grafts in revascularisation of ischemic limb in Buerger's disease//Int. Surg. — 1985. - Vol. 70. - P. 253-255. San Martin, Satrustegui A. Anastomose arterio-veineuse pour remedier a obturation des arteries des membres//Bull. Med. — 1902. — Vol. 16. - P. 451. Sheil A.G.R. Treatment of critical ischemia of the lower limb by venous arterialization: an ihterium report//Brit. J. Surg. — 1977. — Vol. 64. - P. 197-199. Shumichi H. Long term result of omental transplantation for occlusive arterial disease// Int. Surg. - 1983. - Vol. 68. - P. 47-51. Szilagyi D.E., Jay G.D., Munnel E.D. Femoral arterio-venous anastomosis in the treatment of occlusive arterial disease//Arch. Surg. — 1951. — Vol. 63. - P. 435-451. Wolfe J.KM. Defining the outcome of critical ischaemia: a one year prospective study//Brit. J. Surg. - 1986. - Vol. 73. - P. 321. Дата добавления: 2015-02-06 | Просмотры: 2706 | Нарушение авторских прав |