|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Микотические аневризмы
В 1885 г. W.Osler ввел термин "мико-тическая" применительно к аортальной аневризме, развившейся как следствие бактериального эндокардита. Микотические (вторично-инфекционные) аневризмы образуются как следствие длительно существующего инфекционного процесса. Наиболее часто микотические аневризмы являются осложнением септического бактериального эндокардита. Наши данные свидетельствуют, что примерно у 75 % больных источником осложнения служит аортальный клапан, у 12,5 % больных — митральный клапан и у 12,5 % больных — аортальный и митральный клапаны. В целом микотические аневризмы могут явиться следствием инфекции костей, легких; описано образование микотичес-ких аневризм после коронарной ангиопластики, после катетеризации бедренной артерии. Локализация ми-котических аневризм может быть самой разнообразной: сонные, плечевые, подвздошные, бедренные артерии и артерии подколенно-тибиаль-ной области. Наиболее излюбленная локализация — артерии нижних конечностей (до 75 %), на все остальные сосудистые регионы приходится лишь 25 %. Этиология, классификация, течение. Наличие микотических аневризм всегда ассоциировано с понятием сепсис. Сепсис может быть как первопричиной, так и вторичным проявлением инфекционной эмболии. При классифицировании микотических аневризм принято выделять первичный регион и цель поражения септическим эмболом: бифуркация артерии, vasa vasorum, атеросклероти- ческая бляшка; вторичное инфицирование атеросклеротической аневризмы. Локально — непосредственное инфекционное поражение артериальной стенки в месте проникновения инфекционного агента; инфекционные ложные аневризмы (травматические или как следствие хирургического вмешательства), т.е. первичные и вторичные. Сифилитические и туберкулезные аневризмы характерны для аорты и в настоящий момент большого клинического значения не имеют. Следует выделить несколько механизмов инфицирования сосудистой стенки: ▲ эмболизация сосуда септичес ▲вторичное инфицирование ате-росклеротических аневризм при бактериемии в местах развившихся гематом; ▲инфицирование сосудистой стенки из периартериальных лимфатических коллекторов и сплетений; ▲инфицирование сосудистой стенки как следствие перенесенной травмы или операции (последний путь инфицирования можно рассматривать как ятрогенный). Таким образом, механизм образования аневризм заключается в эмболии инфекционного агента в дистальное сосудистое русло с последующей фрагментацией стенки и изменением ее прочности. Большую роль в развитии аневризм придают фактору разрушения внутренней эластической мембраны. Дальнейшее развитие аневризмы может быть аналогичным развитию атеросклеротических или ложных аневризм. Бактериология. При бактериологическом исследовании микотических аневризм выявляется широкий спектр микроорганизмов: пневмококки, стрептококки, стафилококки, энтеро-бактерии, клебсиелла, протей, эшери-хии, клостридии, бактероиды и т.д. Среди всех микотических аневризм различной локализации у 83 % больных с аневризмами, вызванными грамотрицательной флорой, появляется разрыв. При микотических аневризмах, вызванных грамположи-тельной флорой, он наблюдается значительно реже и не превышает 10 %. По нашим данным, наиболее часто причиной микотических аневризм являются стафилококковая флора (65,5 %) и сальмонеллы (34,5 %). Хирургическая тактика при наличии микотической аневризмы и сопутствующего порока сердца имеет особенности, связанные с тем, что изолированная резекция аневризмы нецелесообразна, а коррекция первым этапом порока сердца без резекции аневризмы имеет в своей основе два порочных момента: • остается источник инфицирования, что особенно опасно при наличии искусственных клапанов сердца; • ограничения движения в конечности, болевой синдром не позволяют проводить активизацию больных после операций на сердце, что является принципиально важным для начала ранней реабилитации больных. Поэтому наиболее целесообразно проведение одномоментной операции — коррекции клапанного порока сердца и резекции периферической микотической аневризмы. Приводим клиническое наблюдение больного с микотической аневризмой и одномоментным протезированием клапанов сердца. Больной К., 34 лет, поступил в плановом порядке с жалобами на повышение температуры, общую слабость, головокружение, одышку, возникавшую при подъеме на 1-й этаж. Боли в правой нижней конечности в покое распирающего характера появились внезапно на фоне относительного благополучия. Считает себя больным в течение 1 года. Заболевание началось остро, с повышения температуры; больной с диагнозом "острое респираторное заболевание" лечился сначала амбулаторно, затем стационарно. При поступлении в клинику состояние больного тяжелое. Кожные покровы бледные. Тоны сердца ясные, ритмичные. На аорте II тон отсутствует. Систолодиастоли-ческий шум на аорте с проведением в левую подмышечную область. Слабый систолический шум на основании сердца. АД 120/10 мм рт.ст. Пульс 90 в 1 мин. Печень увеличена на 5 см. Эхокардиографи-ческое заключение: недостаточность аортального и митрального клапанов. Фракция выброса 70 %. Правая нижняя конечность прохладная, отечная, движения в коленном и голеностопном суставах ограничены, вынужденное согнутое положение в коленном суставе. В подколенной области определяется пульсирующее образование, над которым выслушивается систолический шум. Чувствительность сохранена. При ультразвуковой допплерогра-фии лодыжечно-плечевой индекс 0,43. При дуплексном сканировании выявлена трехкамерная аневризма подколенной артерии (рис. 7.37). Аневризматические мешки располагались в проекции трех
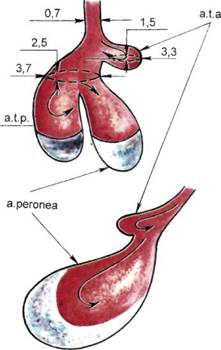
Рис. 7.37. Данные УЗИ при микотической аневризме подколенной артерии. а. реrоnеа — малоберцовая артерия; a.t.a. — передняя большеберцовая артерия; a.t.p. — задняя большеберцовая артерия.
Рис. 7.38. Ангиограмма. Микотическая аневризма подколенной артерии. основных артерий голени. При ангиографии выявлена разорвавшаяся аневризма подколенной артерии (рис. 7.38). Диагноз: активный бактериальный эндокардит аортального и митрального клапанов; вторичная инфекционная аневризма правой подколенной артерии. Боль и вынужденное положение конечности мы объяснили как следствие разорвавшейся аневризмы. Учитывая необходимость последующей реконструктивной операции, мы приняли решение о проведении одномоментной реконструкции клапанного порока сердца и резекции вторичной инфекционной аневризмы с восстановлением кровотока в подколенной области. Больному в плановом порядке выполнена операция протезирования аортального и митрального клапанов с резекцией аневризмы подколенной артерии. Первый этап операции. После раздельной канюляции полых вен и восходящей аорты начато искусственное кровообращение, достигнута гипотермия 27 °С. Пережата и продольно вскрыта аорта; кардиоплегия в коронарные артерии (впоследствии каждые 20 мин). Вскрыто левое предсердие. При ревизии аортального клапана выявлено, что левая коронарная створка разрушена, имеется также краевое разрушение правой коронарной створки с кальцинированными веге-тациями, пролабирующими в полость левого желудочка. Клапан иссечен. При ревизии митрального клапана обнаружен отрыв основной хорды передней створки, на желудочковой поверхности последней — кальцинированные вегетации. Иссечен митральный клапан. Отдельными П-образными швами (N-14) в митральную позицию подшит протез ЭМИКС-31, левое предсердие ушито. В аортальную позицию отдельными П-образными швами (N-16) подшит протез ЭМИКС-25, ушита аорта. После профилактики воздушной эмболии восстановлен сердечный ритм. Дренированы полость перикарда и переднее средостение. Гемостаз. Послойное ушивание ран. Общее время искусственного кровообращения составило 132 мин, пережатия аорты — 94 мин. Второй этап операции. Второй этап начат после окончания первого. В нижней трети бедра рассечены кожа и подкожная жировая клетчатка, выделена подколенная артерия. Рассечены кожа и подкожная жировая клетчатка от подколенной области до средней трети голени в проекции задней большеберцовой артерии. Выше суставной щели пережата подколенная артерия, после чего вскрыты фасция и большая полость, заполненная свежими тромботическими массами. Аневризматическое изменение подколенной артерии начинается на 3 см дистальнее щели коленного сустава, устья артерий голени и начальные сегменты задней и передней большебер-цовых артерий отсутствуют на протяжении 6—8 см. Измененные стенки артерии определяются только по задней стенке аневризмы и представлены белесыми истонченными и изъеденными отдельными тяжами. Собственно полость аневризмы представляет собой трехкамерное образование, распространяющееся в проекции хода трех основных сосудов голени (12— 12—18 см). Отмечается активное кровотечение из многочисленных коллатеральных перетоков и зияющих (неспадающих-ся) основных магистралей в ретроградном направлении. Из просвета аневризмати-ческого мешка прошиты и перевязаны все кровоточащие магистрали и их ветви.
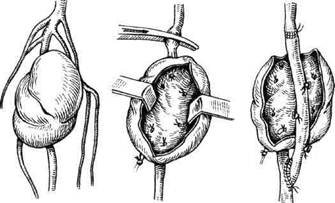
Рис. 7.39. Резекция аневризмы подколенной артерии с аутове-нозным протезированием. В средней трети голени выделена задняя болынеберцовая артерия, стенки артерии мягкие, ретроградный кровоток слабый. После забора и обработки аутовенозно-го трансплантата из большой подкожной вены наложены проксимальный анастомоз с подколенной артерией конец в конец и дистальный анастомоз конец в бок с задней болыиеберцовой артерией под операционным микроскопом нитью пролей 8/0 непрерывным обвивным швом. После снятия зажимов определяется отчетливая пульсация на задней болыиеберцовой артерии дистальнее анастомоза (рис. 7.39). После тщательного гемостаза рана ушита послойно с оставлением активных дренажей. Общая кровопотеря за время операции — резекции аневризмы подколенной артерии составила 2,3 л, из которых 2 л были возвращены больному аппаратом реинфузии ("Cell Saver", Италия). Послеоперационный период протекал относительно гладко. ЛПИ увеличился до 1,2 с восстановлением магистрального кровотока. Швы сняты на 12-е сутки. В послеоперационном периоде больной прошел курс консервативного лечения, включавший инфузионную терапию ан-гиопротекторами и лечебную физкультуру. На момент выписки ограничений функции оперированной конечности не было. Таким образом, своевременная диагностика и адекватная хирургическая тактика позволяют эффективно лечить группу заболеваний, объединенных общим названием "аневризмы периферических артерий". Литература Абалмасов К.Г., Морозов К.М., Тутов Е.Г. и др. Опыт одномоментной коррекции клапанных пороков сердца и хирургии мико-тических аневризм периферических артерий//Анналы хирургии. — 1996. — № 3. — С. 12-27. Петровский Б.В. Прогресс современной ангиохирургии/Хирургия. — 1991. — № 1. — С. 9-16. Покровский А.В., Земское Н.Н., Шор НА. Повреждения магистральных сосудов конечностей. — Киев, 1983. — С. 231—234. Спиридонов А.А., Омиров Ш.Р. Хирургия аневризм брюшной аорты//Грудн. и сер-деч.-сосуд, хир. — 1992. — № 9—10. — С. 33-36. Чазов Е.И. Болезни сердца и сосудов: Руководство для врачей. — М.: Медицина, 1993. - С. 443. Coley B.D., Roberts А.С., Fellmeth B.D. et al. Postangiographic femoral arteria pseudoaneu-rysms //J. Radiol. (California, San Diego). — 1995. - Vol. 194, N 2. - P. 307-311. Kotval P.S., Shah P.M., Babu S.C. et al. Popliteal vein compression due to popliteal artery aneurysm: effects of aneurysm size//J. Ultrasound. Med. — 1995. — Nov. — Vol. 14, N 11. - P. 805-811. Lascaratos J. Surgery on Aneurysms in Byzantine Times (324—1453 a.d.)//Europ. J. Vase. Endovasc Sure. — 1998. — February. — Vol. 15. Mooney M.J., Tollefson D.F., Andersen С A. et al. Duplex-guided compression of iatrogenic femoral pseudoaneurysms//J. Amer. Coll. Surg. (KY, USA). - 1995. - Aug. - Vol. 181, N 2. - P. 155-159. Nahrstedt U., Ruckert K. Isolated, true aneurysm of the tibiofibular trunk-a rarity among peripheral aneurysms. Das isolierte, echte Aneurys-ma des Truncus tibiofibular — eine Raritat unter den peripheren Aneurysmen//Vasa. — 1995. — Vol. 324, N 4. - P. 373-376. Nguyen H.H., Chleboun J. O. False popliteal aneurysm after femoral embolectomy//Aust. N-Z. J. Surg. - 1995. - May. - Vol. 65, N 5. - P. 362-364. Rieck В., Kupsch E., Wittig K. et al. Traumatic aneurysms of the hand. Description of 5 cases: Traumatische Aneurysmata der Hand. Bes-chreibung von funf Fallen (Hannover, Ger-many)//1995. - Dec. - Vol. 27, N 3. — P. 132-136. Saito К., Baskaya M.K., Shibuya M. et al. False traumatic aneurysm of the dorsal wall of the su-praclinoid internal carotid artery — case re-port//Neurol. Med. Chir. - Tokyo. - 1995. -Dec. - Vol. 35, N 12. - P. 886-891. YusufS.W., Baker D.M., Hind R.E. et al. En-doluminal transfemoral abdominal aortic aneurysm repair with aorto-uni-iliac graft and fem-orofemoral bypass//Brit. J. Surg. (Nottingham, UK). - 1995. - Jul. - Vol. 82, N 7. - P. 916. Zell S. С Mycotic false aneurysm of the superficial femoral artery. Delayed complication of Salmonella gastroenteritis in a patient with the acqujred immunodeficiency syndrome//West. J. Med. (Reno, USA). - 1995. - Jul. - Vol. 163, N 1. - P. 72-74. Дата добавления: 2015-02-06 | Просмотры: 1731 | Нарушение авторских прав |