|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
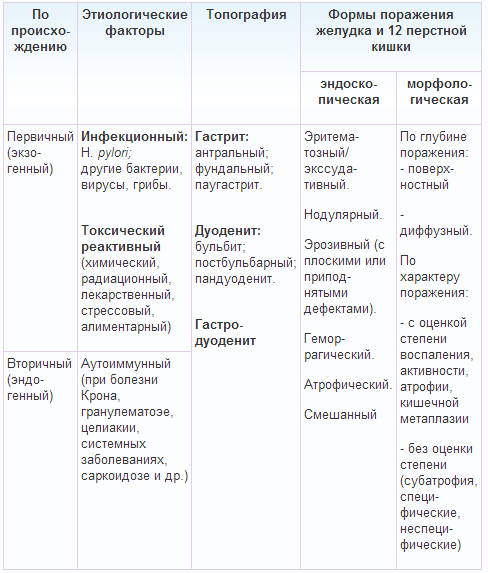
Хронические гастродуодениты у детей. Этиопатогенез, классификацияХронический гастрит - хроническое рецидивирующее очаговое или диффузное воспаление слизистой (подслизистой) оболочки желудка с нарушением физиологической регенерации, склонный к прогрессированию, развитию атрофии и секреторной недостаточности, лежащих в основе нарушения пищеварения и обмена веществ. Хронический гастродуоденит - хроническое воспаление со структурной (очаговой или диффузной) перестройкой слизистой оболочки желудка и двенадцатиперстной кишки, а также формированием секреторных, моторных и эвакуаторных нарушений. Код по МКБ-10 К29. Гастрит и дуоденит. Эпидемиология хронического гастрита и гастродуоденита Хронический гастрит и хронический гастродуоденит - наиболее распространённые гастроэнтерологические заболевания детского возраста, встречающиеся с частотой 300-400 на 1000 детского населения, причём изолированные поражения не превышают 10-15%. В структуре заболеваний верхних отделов ЖКТ хронический гастродуоденит составляет 53,1%, хронический гастрит - 29,7%, хронический дуоденит - 16,2%. Неязвенной гастродуоденальной патологией страдают дети всех возрастных групп, однако наиболее часто заболевание диагностируют в возрасте 10-15 лет. В младшем школьном возрасте половых отличий в частоте хронического гастрита и хронического гастродуоденита нет, а в старшем школьном возрасте чаще страдают мальчики. Частота хронического гастрита, связанного с инфекцией H. pylori, варьирует в зависимости от возраста ребёнка и составляет у детей 4-9 лет 20%, 10-14 лет - 40%, старше 15 лет и у взрослых - 52-70%. Классификация хронического гастрита и гастродуоденита В педиатрической практике за основу была принята классификация хронического гастрита, хронического дуоденита и хронического гастродуоденита, предложенная в 1994 году А.В. Мазуриным и соавт. В 1990 году на IX Международном конгрессе по гастроэнтерологии была разработана современная классификация гастритов, называемая Сиднейской системой, дополненная в 1994 году. На её основе была несколько пересмотрена и дополнена классификация, принятая в России на IV Съезде Союза педиатров России в 2002 году. Причины и патогенез хронического гастрита и гастродуоденита Хронический гастрит и хронический гастродуоденит - мультифакториальные заболевания. Имеют значение: наследственно-конституциональная предрасположенность к заболеваниям органов пищеварения - показатель семейной отягощенности составляет 35-40%; инфицированность Helicobacter pylori; погрешности питания (нерегулярное, неполноценное по составу, плохое пережевывание, злоупотребление острой пищей); химические, в том числе медикаментозные, воздействия; физические и психоэмоциональные перегрузки; пищевая аллергия; очаги инфекции, паразитозы и болезни других органов пищеварения. На фоне сохранения актуальности алиментарного, кислотно-пептического, аллергического, аутоиммунного, наследственного факторов в развитии хронического гастрита и хронического гастродуоденита инфекционный фактор считают решающим и определяющим. Н. pylori - основной этиологический фактор развития хронических воспалительных заболеваний органов гастродуоденальной зоны, который существенно повышает риск развития язвенной болезни и рака желудка. Длительное пребывание Н. pylori в слизистой оболочке желудка приводит к нейтрофильной и лимфоцитарной инфильтрации со стимуляцией провоспалительных и иммунорегуляторных цитокинов, что формирует специфический Т- и В-клеточный ответ и провоцирует атрофический процесс, интерстициальную метаплазию и неоплазию. У детей ассоциация гастродуоденальной патологии с инфекцией Н. pylori при эрозивных поражениях слизистой оболочки желудка и двенадцатиперстной кишки колеблется от 58 до 85%, а при гастритах или гастродуоденитах без деструктивных изменений - от 43 до 74%. Основные пути передачи Н. pylori - орально-оральный через предметы личной гигиены, а также фекально-оральный. Агрессивная среда желудка критически непригодна для обитания микроорганизмов. Благодаря способности продуцировать уреазу Н. pylori может превращать мочевину, проникающую в просвет желудка путём пропотевания через стенки капилляров, в аммиак и СО2. Последние нейтрализуют соляную кислоту желудочного сока и создают локальное защелачивание вокруг каждой клетки Н. pylori. В этих условиях бактерии активно мигрируют сквозь слой защитной слизи, прикрепляются к эпителиальным клеткам, проникают в крипты и железы слизистой оболочки. Антигены микроорганизмов стимулируют миграцию нейтрофилов и способствуют развитию острого воспаления. В основе данных состояний лежат регуляторные расстройства, затрагивающие корковые и подкорковые центры, вегетативную нервную систему, рецепторный аппарат желудка, систему нейротрансмиттеров и биологически активных веществ. В этом процессе сложную роль играют нейромедиаторы (катехоламины, серотонин, гистамин, брадикинин и др.), о чём свидетельствует открытие всё большего количества этих веществ, общих для ткани мозга и желудка. Циркулируя в крови. они оказывают не только прямое воздействие на рецепторы органов и тканей, но и регулируют деятельность гипофиза, структур ретикулярной формации, формируют долговременное стрессовое состояние. Помимо хронического гастрита, ассоциированного с Н. pylori, 5% детей страдают аутоиммунным гастритом, вызванным образованием антител к слизистой оболочке желудка (атрофический гастрит в Сиднейской системе классификации).Истинная частота аутоиммунного гастрита у детей неизвестна. Обнаружена взаимосвязь аутоиммунного хронического гастрита с другими аутоиммунными заболеваниями (пернициозной анемией, аутоиммунным тиреоидитом, полиэндокринным аутоиммунным синдромом, сахарным диабетом I типа, хроническим аутоиммунным гепатитом, первичным билиарным циррозом, неспецифическим язвенным колитом, идиопатическим фиброзирующим альвеолитом, гипогаммаглобулинемией, болезнью Аддисона, витилиго). Частота аутоиммунного хронического гастрита при этих заболеваниях значительно превышает аналогичный показатель в популяции (12-20%)
Основным антигеном для аутоантител на слизистой оболочке желудка ранее считали секреторные канальцы и микросомы париетальных клеток. Современные биохимические и молекулярные исследования идентифицировали в качестве основного антигена париетальных клеток а- и бета-субъединицы Н+, К+-АТФазы, а также внутренний фактор и гастринсвязывающие белки. Важную роль в патогенезе аутоиммунных органоспецифических заболеваний, в том числе аутоиммунного хронического гастрита, играет система HLA, необходимая для процессинга и презентации антигенов. Такая презентация инициирует сложное взаимодействие между антигенами клеток-мишеней, антигенпрезентирующими клетками. CD4-хелперными Т-лимфоцитами, эффекторными Т-клетками и СD8+-супрессорными Т-лимфоцитами. В результате активации Т-лимфоцитов запускается продукция у-интерферона, некоторых цитокинов и добавочных молекул (молекулы межклеточной агрессии ICAM-1, белки теплового шока, CD4+ и другие, необходимые для координации иммунных реакций). Одновременно происходит индукция синтеза определённых антител В-лимфоцитами. Все эти вещества приводят к экспрессии клетками-мишенями антигенов HLA класса II, ICAM-1, различных цитокинов и аутоантигенов, ещё более модифицирующих иммунные реакции. Предполагают, что инфекция H. pylori может не только вызывать классический антральный гастрит В, но и играть роль триггерного механизма в запуске аутоиммунных реакций в слизистой оболочки желудка. В экспериментах на мышах показано, что продукция антипариетальных аутоантител зависит от антигенного статуса. Эти феномены связаны с молекулярной мимикрией и высокой гомологией между антигенами H. pylori и Н+\ К+-АТФазой париетальных клеток. В настоящее время триггерную роль в иммунопатологических поражениях верхних отделов ЖКТ отводят вирусу герпеса IV типа, вирусу Эпстайна-Барр, цитомегаловирусу, а также сочетанию вышеперечисленных вирусов с H. pylori. Особые формы гастрита, отнесённые к химическим, радиационным, лекарственным и другим поражениям, диагностируют у 5% детей; остальные типы гастритов встречаются ещё реже. Нередки случаи, когда у одного и того же больного сочетается нескольких этиологических факторов. Дата добавления: 2014-12-11 | Просмотры: 1663 | Нарушение авторских прав |