|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Особенности обследования больного с подозрением на аневризму грудного отдела аортыКлиническая картина при аневризмах грудного отдела аорты весьма вариабельна и зависит от локализации и размеров аневризмы. 2.1. При опросе больного: 1). Жалобы по основному заболеванию: приблизительно в 75 % наблюдений заболевание протекает совершенно бессимптомно. Наиболее характерным субъективным симптомом при аневризмах восходящего отдела аорты являются загрудинные боли вследствие или самого поражения стенки аорты, или сдавления окружающих органов, или стенокардитического характера при поражении коронарных артерий. Компрессия верхней полой вены сопровождается отеканием верхних конечностей, головы и шеи. Также отмечаются симптомы сердечной недостаточности: сердцебиение, одышка, головокружение, снижение физической нагрузки при сопутствующем поражении аортального клапана. При аневризмах дуги и нисходящего отдела грудной аорты болевой синдром может возникать как за грудиной, так и в межлопаточной области. При этом местоположении аневризм более характерна симптоматика, связанная с компрессией окружающих органов и тканей. Так, сдавление пищевода проявляется дисфагией, при компрессии возвратного нерва развивается дисфония, а при сдавлении блуждающего нерва отмечается брадикардия и слюнотечение. Компрессия трахеи и левого главного бронха может сопровождаться одышкой, стридором, развитием застойных явлений в легких. Поражение аневризматическим процессом ветвей дуги аорты сопроваждается клиникой хронической сосудисто – мозговой недостаточности, симптомами преходящих или острых нарушений мозгового кровообращения по полушарному или веерному типу. Аневризмы торакоабдоминального отдела аорты часто сопровождаются болью в животе, особенно в эпигастральной области; для них характерна симптоматика, связанная с вовлечением в процесс ветвей брюшного отдела аорты и развитием ишемии соответствующих органов. Это признаки хронической абдоминальной ишемии при поражении чревного ствола, верхней брыжеечной артерии, тяжелая вазоренальная гипертензия при сужении почечных артерий, в некоторых случаях ишемия нижних конечностей. Очень редко при окклюзии межреберных артерий развиваются ишемические поражения спинного мозга вплоть до парапарезов и параплегий. 2). Анамнез заболевания: в большинстве случаев развитие аневриз аорты происходит медленно, симптоматика нарастает постепенно. Течение болезни прогрессирующее, однако, встречаются случаи острого развития заболевания. 3). Анамнез жизни: Сбор анамнеза может указать на наличие врожденных заболеваний у родственников (синдром Марфана), перенесенная травма грудной клетки. Важно выяснить факт заболевания в анамнезе сифилисом, перенесенный эпизод острого системного воспаления (неспецифический аортоартериит). Наличие оперативных вмешательств на аорте (аневризмы могут развиться в области сосудистого шва). 2.2. Клиническое физикальное обследование (характерные особенности при данном заболевании): 1). Оценка общего состояния больного Сознание как правило ясное. Конституциональные особенности – астеники. 2). Сбор информация о внешнем виде больного: Аневризма грудного отдела аорты: Внешний осмотр пациента с аневризмой грудного отдела аорты обычно малоинформативен, за исключением больных с синдромом Марфана, в основе которого лежит аномалия развития соединительной ткани, имеет характерный внешний вид: высокий рост, узкое лицо, непропорционально длинные конечности и паукообразные пальцы. 3). «Locus morbi»: Следует обратить внимание на видимую невооруженным взглядом пульсацию в надключичных областях и яремной вырезке, что в ряде случаев является признаком аневризмы грудной аорты. Редко при гигантских аневризмах (в основном сифилитических) происходит узурация и деструкция ребер, грудины, так, что пульсация аневризмы видна прямо под кожей. У худых пациентов с торакоабдоминальными аневризмами больших размеров можно увидеть пульсацию передней брюшной стенки. Сдавление шейного симпатического ствола проявляется синдромом Бернара – Горнера. Пальпация эффективна при определении асимметрии пульсации периферических артерий, что может указывать на вовлечение в аневризматический процесс ветвей дуги аорты и подвздошных артерий. Асимметрию пульсации следует так же определять в надключичных областях и яремной вырезке. При аневризмах торакоабдоминального отдела аорты пульсация в эпигастральной и мезогастральных областях помогает определить размеры аневризмы, её соотношение с органами брюшной полости, и провести дифференциальную диагностику между торакоабдоминальной аневризмой и аневризмой инфраренального отдела брюшной аорты. Если поперечно расположенной к ходу аорты ладонью удается отграничить аневризму от реберной дуги, т. е. аккуратно и медленно завести её между пульсирующим образованием и реберной дугой, то, как правило, аневризма не распространяется выше уровня отхождения почечных артерий от брюшной аорты. Наиболее важным среди физикальных методов является аускультация. Наличие систолического шума над аортой определяется в 70 % случаев при аневризмах грудной аорты. При аускультации аортального клапана можно сделать вывод о наличии аортальной недостаточности (при выслушивании диастолического или систолодиастолического шума). Ослабленное дыхание над поверхностью легких. 4). Обследование состояния костно–мышечного аппарата: у больных с аневризмой грудного отдела аорты кифосколиоз, воронкообразная грудная клетка, патологическая подвижность и деформация суставов. 5). Ведущий клинический симптом: при аневризме грудного отдела аорты: боль в грудной клетке. 6). На основании полученных данных опроса и клинического физикального обследования больного, возможно, выставить следующий клинический диагноз: АНЕВРИЗМА ГРУДНОГО ОТДЕЛА АОРТЫ. 2.3 Дополнительные методы исследования: 1. Клинический анализ крови. 2. Коагулограмма 3. Измерение АД на всех четырех конечностях 4. Рентгенологическое исследование. 5. Компьютерная томография. 6. Ангиографическое исследование. 7. Трансторакальная эхокардиография. 8. Чрезпищеводная эхокардиография. 1). Клинический анализ крови: изменения неспецифичны: возможны анемия, незначительное повышение СОЭ. 2). Коагулограмма - явления гиперкоагуляции. 3). Измерение АД на всех четырех конечностях выполняется манжеточным методом или с помощью допплерографии. В норме АД на ногах должно равняться АД на руках или превышать его не более чем на 10 – 20 мм рт. ст. Градиент АД более 10 мм рт. ст. между руками может свидетельствовать о поражении ветвей дуги аорты или стенозе аорты при аневризмах дуги и нисходящего отдела. Градиент АД между руками и ногами (со снижением АД на ногах) может говорить о стенозировании аорты при аневризмах нисходящего или торакоабдоминального отдела. 4). Рентгенологическое исследование: рентгенологическим признаком аневризмы грудного отдела аорты является наличие гомогенного образования с четкими контурами, не отделяемого от тени аорты и пульсирующего синхронно с ней. Можно также обнаружить смещение аневризмой трахеи, бронхов, пищевода. Обызвествление по контуру аорты в большинстве случаев свидетельствует об аневризматическом поражении аорты. 5). Компьютерная томография (КТ) позволяет определить размеры, локализацию аневризмы аорты. Очень важной при КТ является информация об экстравазации крови и состоянии окружающих аорту тканей. При КТ уточняются размеры стенок аорты и их изменения, содержимое просвета аорты (тромб, отслоенная интима), проходимость и вовлечение ветвей аорты, вовлечение костных структур (грудина, позвоночник), расположение, степень вовлечения и размер прилежащих магистральных сосудов, наличие аортовенозных фистул, наличие жидкости в полости перикарда. При расслаивающейся аневризме аорты определяется два просвета и два контура стенки аорты. 6). Ангиографическое исследование. Для полноценной оценки состояния грудной аорты исследование проводится в 3 проекциях - прямой, левой и косой боковых проекциях. Определяется локализация, протяженность аневризмы, наличие тромботических масс. Основным ангиографическим признаком расслаивающейся аневризмы является двойной контур аорты 7) Трансторакальная эхокардиография. У большинства пациентов позволяет визуализировать корень аорты и проксимальную часть восходящей аорты, выявить расширение этого сегмента, утолщение стенки, наличие отслоенной интимы, сдавление левого предсердия. Эхокардиография также позволяет получить информацию о выраженной артериальной недостаточности, выпота в полости перикарда, систолической и диастолической дисфункции левого желудочка сердца. Визуализация дуги аорты и нисходящего отдела грудной аорты является обычно более проблематичной и может требовать исследования из дополнительных доступов (супрастернального, левых и правых высоких парастернальных, над – и подключичных). 8). Чрезпищеводная эхокардиография. Позволяет установить точную локализацию и размеры аневризмы в восходящем и нисходящем отделах грудной аорты, наличие тромбов в просвете, оценить функцию аортальных клапанов и выраженность аортальной регургитации, достоверно дифференцировать аневризму аорты от расслоения и инрамуральной гематомы. 2.4. Дифференциальная диагностика: аневризма грудного отдела аорты – опухоли средостения, легких. 2.5. Обоснование и формулирование клинического диагноза (с учетом классификации заболевания, наличия осложнений и сопутствующей патологии): 1) основной – аневризма грудного отдела аорты 2) осложнения (основного заболевания если они есть) 3) сопутствующая патология (если она есть) 2.6. Лечение больного с аневризмой грудного отдела аорты 2.6.1. Выбор лечебной тактики: лечение больных с аневризмами аорты только хирургическое. 2.6.2. Виды оперативных вмешательств Аневризма восходящего отдела грудной аорты - оперативное лечение показано при нарастающих гемодинамических нарушениях, обусловленных недостаточностью аортального клапана и/или прогрессирующим расширением восходящей аорты. Операция заключается в протезировании восходящей аорты и аортальных клапанов. Аневризма дуги аорты- аллопротезирование дуги аорты и ее ветвей. Аневризма нисходящего отдела грудной аорты- иссечение аневризмы с аллопротезированием. 2.6.3. Возможные послеоперационные осложнения: - внутриполостное кровотечение; - динамическая кишечная непроходимость; - тромбоэмболические осложнения; - острая сердечно – легочная недостаточность 2.6.4. Неотложные состояния Расслоением аорты называется расхождение (разделение) медии аорты на два слоя за счет попадания внутри просветной крови через разрыв интимы и возникновения патологического сообщения между истинным просветом аорты и образовавшимся каналом в среднем слое аорты, называемым ложным просветом. При расслоении аорты отмечают периоды: · острый (до 48 часов с момента расслоения); · подострый (до 2 – 4недель); · хронический (до 2 месяцев с момента расслоения).
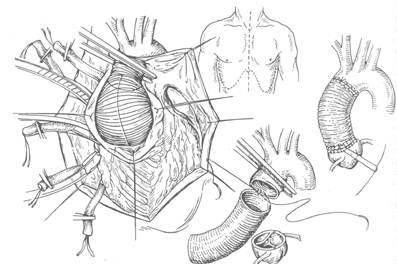
Типы расслоения аорты по локализации и протяженности представлены двумя классификациями: De Bakey (1965 г.) разделил расслоения аорты следующим образом: I тип – расслоение начинается в восходящем отделе, переходит через дугу в нисходящий отдел, а далее может распространяться на любом протяжении; II тип – расслоение захватывает только восходящую аорту; IIIа тип – расслоение начинается ниже устья левой подключичной артерии и распространяется в пределах нисходящего отдела аорты; IIIb тип – расслоение такое же, как и при IIIa, но распространяется через аортальное отверстие диафрагмы на брюшную аорту. Второй оригинальной классификацией явилась классификация Стэнфордского университета, предложенная Daily P.O. и соавт. в 1970 г.: · тип А – любое расслоение, вовлекающее восходящую аорту; · тип В – любое расслоение, располагающееся ниже уровня отхождения левой подключичной артерии. Клиническая картина расслоения аорты характеризуется острым, практически мгновенным началом на фоне повышения артериального давления с развитием интенсивного болевого синдрома, выраженного настолько, что внешне, несмотря на гипертензию, больной выглядит как находящийся в колаптоидном состоянии (заторможенность, фиксация взора, холодный липкий пот, слабая периферическая пульсация). Снижение артериального давления приводит к приостановке расслоения аорты и уменьшению выраженности болевого синдрома со стабилизацией общего состояния, но затем возможно нарастание этого процесса вновь и вновь. Локализация боли зависит от места начала расслоения: за грудиной – при I и II типах, в межлопаточной области – при III типе. Отмечается проявление ишемии прочих органов и систем: коронарная недостаточность, инсульт или преходящее нарушение мозгового кровообращения, парапарез или параплегия, клиника мезентериального тромбоза, острой почечной недостаточности, острой артериальной непроходимости нижних конечностей. Диагностика. При физикальной диагностике необходимо обращать внимание на различие пульсации между артериями верхних или верхних и нижних конечностей, наличие признаков тампонады сердца (парадоксальная пульсация, ослабление тонов сердца) и аортальной недостаточности (диастолический шум). Тактика ведения больного заключается в ургентной госпитализации в стационары сосудистого профиля в палаты интенсивной терапии и выполнении следующих мероприятий: · медикаментозная терапия; · выполнение диагностических исследований; · подготовка к возможной операции. Больному с подозрением на расслоение аорты устанавливают центральный венозный катетер большого диаметра и максимально быстро начинают введение b – блокаторов и вазодилятаторов для замедления ритма и снижения АД. Частота сердечных сокращений должна колебаться в пределах 60 – 70 ударов в 1 минуту, а систолическое давление необходимо поддерживать в пределах 90 – 100 мм рт. ст. Одновременно с введением артериального катетера в лучевую артерию, катетера Свана – Ганца - в легочную налаживают ЭКГ – мониторирование, проводят катетеризацию мочевого пузыря с определением почасового диуреза, выполняют рентгенологическое исследование органов грудной клетки. Проводят сбор анамнеза и проводят физикальный осмотр с учетом неврологического статуса и проходимости конечностей. Последнее обстоятельство важно для выбора схемы подключения АИК. Болевой синдром контролируют на основании частоты сердечных сокращений и АД, но если они снижены до указанных пределов, а боли сохраняются, то вводят наркотические анальгетики. В обязательном порядке обеспечивают ингаляцию кислорода, устанавливают группу крови, определяют и мониторируют уровень гемоглобина, гематокрита, электролитов, газового состава и основных биохимических показателей крови. Следует избегать переливания большого объёма жидкостей из – за опасности повышения АД вследствие гиперволемии. Прежде чем начинать диагностические мероприятия, необходимо провести дифференциальную диагностику между острым расслоением аорты и острой ишемией миокарда. Окончательное и быстрое решение данного вопроса жизненно важно для таких больных, поскольку необходимое при коронарной недостаточности немедленное введение тромболитиков приведет к фатальному исходу расслоения. Цель диагностической стратегии при остром расслоении – прежде всего выявление расслоенной мембраны и её дифференциация с интрамуральной гематомой, т.е. подтверждение или исключения диагноза собственно расслоения. Вторым принципиальным моментом в диагностике острых расслоений является определение локализации процесса. В случае выявления мембраны при остром проксимальном расслоении операция является абсолютно показанной без дополнительной диагностики в отсутствие осложняющих факторов, так как состояние дуги аорты и устьев коронарных артерий может быть адекватно оценено интраоперационно. Больных с нестабильной гемодинамикой и отсутствием эффекта от первичных немедленных медикаментозных воздействий при подозрении на проксимальное расслоение переводят в операционную, где после начала общей анестезии одновременно с подготовкой к хирургическому вмешательству (подключение линий мониторирования) выполняют чреспищеводную ЭхоКГ. При подтверждении диагноза производят операцию. В случае исключения диагноза расслоения или затруднительности визуализации аорты больной после стабилизации или начала относительной контролируемости состояния может быть переведен в блок интенсивной терапии для дальнейшего лечения или перемещен в другие диагностические кабинеты (КТ, ангиография). При относительно стабильном состоянии пациентов с острым расслоением аорты методом выбора в диагностике является та же чреспищеводная ЭхоКГ. Следующее место по доступности, быстроте, аккуратности и распространенности занимает КТ с контрастированием, причем использование спирального КТ с трехмерной реконструкцией, возможно, повысит точность метода. Применение МРТ при остром расслоении аорты ограничено, хотя по точности этот метод диагностики даже несколько опережает чреспищеводную ЭхоКГ. Использование МРТ возможно в редких случаях острого расслоения только у полностью стабильных пациентов, способных обойтись значительное время без медикаментозной поддержки и мониторинга. Кроме того, данная методика иногда абсолютно необходима при остром расслоении для выявления состояния дуги аорты (невозможность визуализации при чреспищеводной ЭхоКГ) в случае подозрения на ретроградное расслоение при III и В-типах расслоения. Частота использования ангиографии при острых расслоениях постепенно снижается прежде всего из-за травматичности метода для крайне тяжелых пациентов. Тем не менее, если учитывать состояние (проходимость) ветвей аорты при расслоении, ангиография остается методом выбора. О необходимости выполнения коронарографии при остром расслоении единого мнения у хирургов нет. С одной стороны, ряд авторов считают, что у 10—30 % пациентов с поражением коронарных артерий и проксимальным расслоением аорты интраоперационная оценка вполне достаточна для решения вопроса об одномоментной реваскуляризации миокарда. С другой стороны, было доказано, что выполнение одномоментного аортокоронарного шунтирования у больных с проксимальным расслоением аорты не влияло на госпитальную выживаемость, хотя отдаленная выживаемость у больных с сопутствующей ИБС без реваскуляризации миокарда была достоверно ниже. Показания к оперативному лечению: ▲ при остром проксимальном расслоении аорты показана экстренная операция из-за крайне высокого риска разрыва аорты или тампонады сердца. При выраженной тампонаде сердца и гипотензии во время подготовки к операции для восстановления жизненно важных функций организма показана пункция перикарда с постепенным дренированием для профилактики возможного разрыва аорты вследствие резкого возрастания АД. Неврологический дефицит не является противопоказанием к операции, так как у большинства пациентов происходит его полный регресс после вмешательства; ▲ при хроническом проксимальном расслоении аорты показано плановое оперативное вмешательство вне зависимости от размера аорты, симптоматики, обусловленной расширением аорты, осложнений вследствие произошедшего острого расслоения или выполненных ранее хирургических вмешательств; ▲ при остром дистальном расслоении аорты оперативное лечение считается показанным в случае рефрактерности артериальной гипертензии или болевого синдрома к медикаментозной терапии, рецидиве болей, увеличении диаметра аорты свыше 5 см, возникновении осложнений, связанных с нарушением проходимости ветвей аорты (почечная недостаточность, парапарез/параплегия, ишемия конечностей и/или кишечника), разрыве аорты; ▲ при хроническом дистальном расслоении аорты оперативное лечение показано больным с симптомным течением заболевания, при размерах аорты более 5см и при росте диаметра аорты более 1 см в год. Операции на проксимальной грудной аорте при дегенеративных заболеваниях. Кпринципиальным вопросам, возникающим при планировании оперативной тактики во время указанных вмешательств, относятся два: насколько сохранена синотубулярная борозда и насколько выражены аневризматические изменения дуги аорты. При сохранении синотубулярной борозды достаточно линейного протезирования восходящей аорты в зависимости от состояния аортального клапана, дополненного раздельным протезированием. В обратной ситуации, при расширении корня аорты, показано протезирование аортального клапана и восходящей порции аорты клапансодержащим кондуитом. Если дистальная порция восходящей аорты имеет нормальный размер или умеренно расширена на уровне безымянной артерии, то может быть наложен прямой дистальный анастомоз с проксимальной порцией дуги или косой под зажимом, расположенным от точки тотчас проксимальнее устья брахиоцефального ствола и косо захватывающим проксимальную часть нижней полуокружности дуги аорты. При аневризматическом расширении большей части дуги необходимо использование глубокой гипотермии с остановкой кровообращения и ретроградной перфузией головного мозга. При расширении проксимального отдела нисходящей грудной аорты или необходимости применения техники «хобот слона» необходима имплантация ветвей дуги аорты в протез дуги на площадке, а если расширение оканчивается проксимальнее левой подключичной артерии, то возможно формирование дистального анастомоза с косо срезанным линейным протезом или с таковым, выкроенным в виде языка, анастомозированным кпереди и сзади ветвей дуги, когда сам анастомоз завершается на уровне отхождения безымянной артерии. Линейное протезирование восходящей аорты. Операцию начинают со срединной стернотомии, вскрывают полость перикарда на всем протяжении по его передней поверхности, на его рассеченные края накладывают держалки и разводят (рис. 3). Подключают АИК по схеме правое предсердие (или полые вены) — проксимальная часть дуги аорты (реже бедренная артерия). Аорту пережимают тотчас проксимальнее уровня отхождения брахиоцефального ствола, вскрывают полость аневризмы и аорту полностью пересекают сразу над верхними точками прикрепления коммисур аортального клапана и проксимальнее аортального зажима. Полное пересечение аорты облегчает контроль за герметичностью анастомоза и снижает риск развития ложных аневризм в отдаленном периоде. Производят ревизию аортального клапана и подтверждают его состоятельность. Первым накладывают дистальный анастомоз с линейным протезом нитью пролен 3—0 непрерывным обвивным швом, вначале сшивают заднюю стенку, затем переднюю. Проксимальный анастомоз выполняют таким же образом. Больного переводят в положение Тренделенбурга, эвакуируют воздух, начинают параллельное икуственное кровообращение (ИК), во время которого контролируют герметичность анастомозов. После восстановления сердечных сокращений и постепенной стабилизации гемодинамики параллельно снижают объем перфузии, а затем аорту деканюлируют. Далее деканюлируют правые отделы сердца, осуществляют гемостаз и остатками аневризматического мешка укрывают протез. Перикардотомическое отверстие закрывают заплатой. Дренируют полость перикарда и переднее средостение через контрапертуры ниже мечевидного отростка. Стальной проволокой сводят края грудины. Разрез грудины полностью укрывают мышечно-фасциальными швами и зашивают кожу.
Рис. 3.Линейное протезирование восходящей аорты.
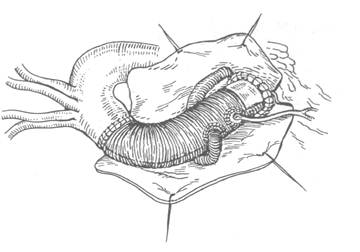
Раздельное протезирование аортального клапана и восходящей аорты показано больным при сочетании аортального порока и аневризмы восходящей аорты без расширения аортального кольца. После вскрытия полости аневризмы и пересечения аорты, как описано выше, иссекают створки аортального клапана и имплантируют его протез с использованием стандартной техники. Далее ход операции полностью повторяет линейное протезирование восходящей аорты. При более выраженном аннулярном расширении, особенно у пожилых пациентов, допустимо использовать технику, разработанную M.N. Wheat (1964), когда аорту пересекают проксимально тотчас над фиброзным кольцом с оставлением стенок, выкроенных над устьями коронарных артерий. В этой ситуации первоначально накладывают проксимальный анастомоз с обрезанным соответственно ходу линии резекции аорты линейным протезом, так что устья коронарных артерий как бы инкорпорируются в анастомоз и укрываются им. Для усиления проксимального анастомоза в швы захватывают протез аортального клапана. Протезирование аортального клапана и восходящей аорты клапансо-держащим кондуитом Показано пациентам с расширением кольца аортального клапана, синотубулярной борозды или синусов Вальсальвы. После начала ИК, пережатия аорты и остановки сердца восходящую аорту пересекают в дистальном отделе, иссекают створки аортального клапана с оставлением 1—2 мм ободка на фиброзном кольце, накладывают швы на комиссуры и измеряют диаметр клапанного кольца для подбора кондуита. Далее ход вмешательства зависит от выбора способа оперативной коррекции. Существуют три классические методики протезирования восходящей аорты клапансодержащим кондуитом, различающиеся по технике включения в кровоток коронарных артерий. При методике Бенталла—Де Боно устья коронарных артерий непосредственно, в своей естественной позиции в стенке аневризматического мешка, анастомозируют с отверстиями в стенке кондуита. Было также предложено выкраивать устья коронарных артерий на площадках и производить мобилизацию начальных отделов венечных артерий на протяжении, что позволяет увеличить длину сосудов и свободно реплантировать их в стенку аортального протеза. Третьей классической методикой является техника Каброля, когда устья коронарных артерий анастомозируют с 8- или 10-миллиметровым линейным протезом, который подшивают по типу бок в бок к кондуиту. Первоначально последний анастомоз размещали на передней поверхности аортального протеза, затем методика была усовершенствована и анастомоз стали накладывать с задней поверхностью кондуита. Методика Каброля значительно облегчает доступ к коронарным анастомозам и линии шва на клапанном кольце при необходимости дополнительного гемостаза, но в дальнейшем за счет анастомоза бок в бок между линейным протезом к коронарным артериям и кондуитом остается высокой вероятность перегиба первого протеза вплоть до развития окклюзии какой-либо из браншей к коронарным артериям. Для устранения приведенных недостатков L.G. Svensson (1997 г.) предложил включать в кровоток левую венечную артерию протезом от кондуита, а правую — реплантировать на площадке (рис.4). Последняя методика позволяет легко визуализировать все анастомозы, исключает риск перегиба коронарной бранши, делает возможным полное поперечное пересечение аорты (не требуется окутывания кондуита из-за надежности гемостаза), что снижает риск развития ложных аневризм анастомозов в отдаленном периоде.
Рис. 4. Протезирование аортального клапана и восходящей аорты клапансодержащим кондуитом в модификации Svensson. Дата добавления: 2014-05-22 | Просмотры: 1604 | Нарушение авторских прав |