 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
ПОЧЕЧНАЯ АНГИОГРАФИЯПочечная ангиография, широко известная под названием транслюмбальной или трансфеморальной аортографии, была предложена Dos Santos в 1929 г. С 1942 г. этот метод исследования стал постепенно внедряться в урологическую практику. Особенно широко почечная ангиография стала применяться за последние 15 лет. Этому благоприятствуют высокое развитие техники, усовершенствование рентгеновской аппаратуры и специальных приспособлений, облегчающих исследование, а также наличие малотоксичных контрастных веществ, пригодных для ангиографии. Наряду с этим большая диагностическая ценность данного метода расширяет показания к его применению и увеличивает количество сторонников почечной ангиографии. В нашей стране почечная ангиография была внедрена в практику урологической клиникой II Московского медицинского института с февраля 1955 г. (А. Я. Пытель и Н. А. Лопаткин, 1956). Благодаря применению портативной приставки-кассеты для серийной почечной ангиографии, предложенной Н. А. Лопаткиным и А. П. Жирновым, этот метод сделался легко доступным и находит все большее и большее применение в практике урологических учреждений Советского Союза. В зависимости от способа введения в аорт контрастного вещества различают транслюмбальную аортографию (Dos Santos, 1929), когда заполнение рентгеноконтрастным веществом аорты и ее ветвей осуществляется путем пункции аорты со стороны поясницы (рис. 67), и ретроградную (трансфеморальную) аортографию (Ichikawa, 1938; Seldinger, 1953), при которой контрастное вещество вводят в аорту путем пункции бедренной артерии с проведением по ней катетера до уровня отхождения от аорты почечных артерий (середина тела I поясничного позвонка) (рис. 68). Эти два метода почечной ангиографии в настоящее время применяются чаще всего.
Рис. 67. Схема транслюмбальной почечной ангиографии.
Рис. 68. Схема трансфеморальной почечной ангиографии по Сельдингеру. Почечная ангиография является ценным функциональным и морфологическим методом диагностики. Помимо выявления особенностей ангиоархитектоники, она позволяет определить функциональную способность почек в тех случаях, когда другими методами исследования сделать это не удается. Ее следует применять тогда, когда другие методы рентгенодиагностики не в состоянии установить характер заболевания. Почечная ангиография не исключает диагностических возможностей ретроградной пиелографии или экскреторной урографии; она дополняет их либо приходит им на смену там, где они оказываются несостоятельными. Показания. Почечная ангиография показана:
Противопоказания. Транслюмбальная пункция аорты противопоказана при резко выраженном атеросклерозе ее. Повышенная чувствительность организма к йоду и резко выраженный тиреотоксикоз, прогрессирующая тяжелая почечная недостаточность, тяжелая степень недостаточности печени, активный туберкулез легких и тяжелая степень сердечно-сосудистой недостаточности являются противопоказанием к почечной ангиографии. С целью выявления возможной идиосинкразии к йоду обязательно предварительное проведение пробы на скрытую повышенную чувствительность каждого больного к йоду. Техника транслюмбальной аортографии. За 30 минут до исследования больному делают инъекцию 1 мл 1 % раствора морфина и непосредственно перед исследованием 1 мл 1% раствора омнопона. Больного укладывают вниз животом на горизонтально расположенный рентгеновский стол с вытянутой вдоль туловища левой рукой и отведенной в сторону правой рукой, на которой регистрируют артериальное давление и пульс. Исследование производят под местной анестезией. Для почечной ангиографии не требуется какого-либо сложного технического оснащения. Она с успехом может быть выполнена при наличии рентгеновского аппарата типа УРДД-110 отечественного производства и простым кассетным приспособлением Н. А. Лопаткина и А. П. Жирнова, позволяющим произвести серийные снимки с очень короткими интервалами времени (3 снимка в 2 секунды). Первые две рентгенограммы производят в течение первых 2 секунд, т. е. во время введения в аорту контрастной жидкости, третью рентгенограмму — тут же после введения всего количества контрастной жидкости, четвертую — спустя 3—5 минут после первой. В качестве контрастного вещества применяют наши отечественные препараты — трийотраст (70%), кардиотраст (70%) и зарубежные — диодон (70%), гипак (70%), урокон (70%), диатризоат натрия (70%), дийодраст (70%) и др. Для получения четкого изображения сосудов почек вполне достаточно ввести в аорту 20—25 мл контрастной жидкости со скоростью 10 мл в секунду. Пункцию аорты производят иглой, имеющей длину 15 см и диаметр 1,8 мм. Пунктируют аорту со стороны поясницы, отступая влево на 8—9 см от остистых отростков позвонков и на 2—4 см от нижнего края XII ребра. Острие иглы должно направляться к телу I поясничного позвонка. На пути следования игла может встретить два костных препятствия. Первое препятствие на глубине 4—5 см обусловлено поперечным отростком позвонка; в этом случае иглу направляют более отвесно на 1 см, а затем придают ей прежнее направление к телу позвонка. Второе костное препятствие, обусловленное телом позвонка, может встретиться на глубине 8—9 см. В таком случае иглу оттягивают на 1—2 см назад и придают ей более отвесное направление, чтобы острие ее отошло в латеральную сторону и скользнуло по телу позвонка. При дальнейшем продвижении иглы на глубине 11 —15 см часто удается ощутить пульсацию аорты. После дополнительной анестезии раствором новокаина парааортальной клетчатки пунктируют аорту. Доказательством пункции аорты является ощущение провала, подобно проколу твердой мозговой оболочки при спинномозговой пункции. Тут же из иглы выбрасывается кровь пульсирующей струей. Во избежание тромбирования иглы и тромборбразования в сосудах вводят в аорту раствор гепарина (в разведении 10 000 единиц на 2 л физиологического раствора) в течение всего периода исследования. Этот раствор поступает в аорту по каплям из банки, подвешенной на высоте 1,5 м. Перед введением в аорту контрастной жидкости уровень стояния иглы контролируют тут же произведенной рентгенограммой. Затем,в аорту вводят 5 мл 0,5% раствора новокаина. Это предупреждает спазм аорты и ее ветвей, который может возникнуть в ответ как на пункцию аорты, так и на введение в нее контрастной жидкости. Только убедившись в соответствии избранной экспозиции данному больному и в правильном положении иглы по контрольной рентгенограмме можно вводить контрастную жидкость в аорту. Перед самым введением контрастной жидкости больному приказывают не дышать. Рентгенография начинается после того, как в аорту введено 10 мл контрастной жидкости. Вторую рентгенограмму производят немедленно в конце введения всего количества контрастной жидкости, третью — тут же вслед за второй. Последующие рентгенограммы производят через 1—5 минут, в зависимости от показаний. Иглу удаляют в два приема и только тогда, когда рентгенограммы проявлены и качество их отвечает нужным требованиям. В случае необходимости можно повторить введение контрастной жидкости в аорту, однако общее количество препарата не должно превышать 1 мл на 1 кг веса больного. Техника трансфеморальной аортографии. Этот вид почечной ангиографии может быть осуществлен либо путем обнажения и пункции бедренной артерии, либо путем чрескожной пункции ее (метод Seldinger). Мы пользуемся обоими вариантами, т. е. обнажением бедренной артерии в скарповском треугольнике и пункцией ее на глаз, либо чрескожной пункцией артерии с последующим введением в аорту сосудистого зонда и по нему контрастного вещества. Линейным разрезом в скарповском треугольнике рассекают кожу, подкожную клетчатку и фасцию бедра. Мышцы тупо раздвигают, благодаря чему обнажают бедренную артерию и вену. Бедренную артерию не следует мобилизовать циркулярно, а достаточно выделить переднюю ее стенку на протяжении 1,5—2 см. Артерию пунктируют сосудистым троакаром конструкции НИИЭХАИ. По троакару вводят в артерию полый зонд соответствующего диаметра, после чего троакар удаляют, а зонд постепенно продвигают вверх в аорту до уровня отхождения почечных артерий. Производят контрольную рентгенографию с целью определения уровня стояния верхнего конца сосудистого зонда в аорте. Затем по зонду вводят 5 мл раствора новокаина и вслед за ним рентгеноконтрастное вещество. Рентгенография должна начинаться с момента введения 7 мл контрастной жидкости. Последнюю вводят с максимальной быстротой. Периоды производства рентгенограмм те же, что и при транслюмбальной аортографии: в момент введения жидкости — 2 рентгенограммы, а третья в конце введения. Пункционная рана артерии обычно имеет маленький диаметр и требует наложения только одного шва на адвентицию с целью остановки кровотечения. Описанная методика значительно упрощает технику зондирования аорты, и делает ее легко доступной для врача и безопасной для больного. Метод Сельдингера (Seldinger, 1953), заключается в чрескожной пункции бедренной артерии специальной иглой и введении по ней проводника для продвижения по нему полого зонда в брюшную аорту. У больных артериальной гипертонией после удаления из сосуда катетера, несмотря на длительное прижатие места пункции, иногда наблюдаются межфасциальные и подкожные гематомы. После транслюмбальной аортографии, в зависимости от самочувствия больного, ему разрешают ходить на 2-е сутки, а после трансфеморальной аортографии — на 4-е сутки. На протяжении ближайших 3—5 дней следует производить больным обычные анализы мочи и крови. В результате серийной почечной ангиографии представляется возможность судить о четырех фазах циркуляции контрастной жидкости в почке и мочевых путях. Вначале получаем изображение почечных артерий и их ветвей — артериограмму (рис. 69), затем — изображение почечной паренхимы в виде плотной тени — нефрограмму (рис. 70), далее удается зафиксировать момент оттока по венам контрастной жидкости — венограмму и, наконец, экскреторную урограмму. Изучение всех стадий циркуляции контрастной жидкости в почке имеет большое диагностическое значение (рис. 71, 72, а, б).
Рис. 69. Почечная ангиография (транслюмбальный метод). Мужчина 39 лет. Артериографическая фаза. Нормальные почечные артерии и их ветви.
Рис. 70. Почечная ангиография (транслюмбальный метод). Мужчина 39 лет. Нефрографическая фаза. Нормальная функция почек.
Рис. 71. Транслюмбальная почечная ангиография. Женщина 36 лет. Артериографическая фаза.
Рис. 72. Транслюмбальная почечная ангиография. Мужчина 34 лет. а — артериографическая фаза, нормальная; б — нефрографическая фаза, нормальная. Помимо приведенных двух видов почечной ангиографии, иногда прибегают к операционной почечной вазографии [ангиография на обнаженной во время операции почке по Alken и Sommer (1950)], но значительно чаще к селективной почечной ангиографии. При последней путем трансфеморального или трансбрахиального зондирования аорты и одной какой-либо почечной артерии с последующим введением в нее контрастного вещества удается получить избирательную ангиограмму одной почки (рис. 73). Этот метод ангиографии часто применяется в итальянских клиниках (Chiaudano, 1955; Malchiodi et al., 1957; Morino, 1960; Meinardi и Bubbio, 1962).
Удовлетворительными ангиограммами, на основании которых могут быть сделаны правильные диагностические заключения, являются такие, на которых видно равномерное заполнение контрастной жидкостью аорты и почечных артерий. При изолированном заполнении артерии той почки, в которой предполагается патологический процесс, исследование может считаться полноценным, если известно функционально-морфологическое состояние другой, противоположной почки на основании данных хромоцистоскопии, ретроградной пиелографии, экскреторной урографии. Заполнение контрастной жидкостью артерии только здоровой почки при незаполнении или неравномерном заполнении соответствующего отрезка аорты является показанием к повторному исследованию. Ангиографические признаки нормальной почки. Артериальное кровоснабжение почечной паренхимы состоит как бы из двух зон: передней, более обширной, и задней, менее обширной. Диаметр артериальных сосудов постепенно равномерно суживается от центра к периферии, при этом калибр сосудов в одноименных зонах почки одинаков. Наибольшая изменчивость сосудистой архитектоники отмечается на полюсах почки, с чем следует считаться при интерпретации ангиограмм, равно как и при резекции почки. Так, например, одна из основных ветвей почечной артерии может у ворот почки делиться на 2—3 сосуда, из которых каждый направляется к соответствующему отделу почки. Распределение артерий не всегда строго соответствует дольчатости, выраженной иногда у некоторых больных. Артерии в почке могут распределяться по магистральному и рассыпному типу. У одного индивидуума может наблюдаться тот и другой вид распределения артерий в почках. При почечной ангиографии, как и при всяком другом методе контрастной рентгенодиагностики в урологии, возможны те или иные осложнения. При надлежащей подготовке больного к ангиографии, правильной технике проводимого исследования, соответствующем выборе контрастного вещества и строгом соблюдении установленных показаний и противопоказаний к применению аортографии можно избежать тяжелых осложнений и летальных исходов. В этом убеждает наш личный опыт, а также анализ случаев грозных осложнений и летальных исходов, описанных в литературе. Как наблюдения урологической клиники II Московского медицинского института, так и данные литературы (Morino, 1960; Beall, Morris et al., 1961; Hartmann, 1962, и др.) показывают, что новейшие рентгеноконтрастные препараты, хорошо растворимые в воде и содержащие в молекуле не 2, а 3 атома йода, не оказывают пагубного воздействия на функцию почек, даже если функция их до аортографии была пониженной. Почечная ангиография — метод весьма ценный в тех случаях, когда другими общепринятыми способами рентгенодиагностики нельзя определить характер заболевания. При помощи аортографии удается весьма точно определить наличие добавочных почечных сосудов, их локализацию и распределение в почечной паренхиме. На ангиограммах возможно установить зону кровоснабжения отдельными сосудами, что важно при решении вопроса о геминефрэктомии или резекции почки при туберкулезе и камнях, а также при резекции добавочного сосуда по поводу гидронефроза. Так как аортография позволяет судить не только о почечной ангиоархитектонике, но одновременно и о функциональной способности почек, этот метод представляет гораздо больше возможностей, чем пневморетроперитонеум и др., чтобы установить точный диагноз многих почечных заболеваний. Опыт урологической клиники II Московского медицинского института показывает, что этот метод позволяет поставить диагноз, когда на основании других способов сделать это невозможно. У 30,3% обследованных больных диагноз был установлен только благодаря ангиографии, а у 13,2% на основании данных почечной ангиографии предварительный диагноз был отвергнут. Согласно данным Maluf и Cornelia (1955), диагностические ошибки при заболеваниях почек до применения аортографии составляли 17%, а при применении аортографии количество их снизилось до 6,4%. Согласно новейшим данным, этот процент снизился до 2,1—3 (Vogler к Herbst, 1958; Olsson, 1962; Beall et al., 1961). По нашим данным, общий процент диагностических ошибок при аортографии равен 2,8. Многие заболевания почек ангиографически характеризуются весьма специфическими признаками. Так, например, для гидронефроза характерно резкое сужение артерий и уменьшение их количества; изменения эти тем сильнее выражены, чем значительнее гидронефротическая трансформация. Опухоль (гипернефроидный рак) характеризуется грубым нарушением правильного распределения артерии в паренхиме почки, обрывом одной или нескольких ветвей магистральной почечной артерии, увеличением ее диаметра и беспорядочным скоплением контрастной жидкости в области опухоли в виде так называемых пятен-озер. Для более “молодых” новообразований почек характерна повышенная плотность тени на артериограммах соответственно локализации опухоли. При кисте почки имеет место как бы раздвигание ветвей почечной артерии с образованием бессосудистого участка. Аналогичная картина наблюдается и при п оликистозных почках. Однако при них бессосудистых участков в почечной паренхиме имеется больше в зависимости от стадии патологического процесса. Соответствующие изменения ангиоархитектоники имеют место при почечных аномалиях, опухолях надпочечника и новообразованиях забрюшинного пространства. Аортография является методом, дающим самый низкий процент ошибок в диагностике опухолей почек и кист. Изучение почечной ангиоархитектоники чрезвычайно важно не только для диагностики почечных заболеваний, но и для правильного выбора оперативного пособия органосохраняющего характера. Так, на основании данных ангиографии получают представление о положении и направлении почечной артерии, о степени отклонения или сдавления аорты, о состоянии почечной вены и т. д., что позволяет выбрать лучший доступ к почечной ножке, например, при операции по поводу опухоли почки. Исключительно велика ценность ангиографии в установлении вида и локализации стеноза почечной артерии, ее облитерации, аневризматического расширения сосудов и т. д., что предрешает выбор соответствующего оперативного пособия при нефрогенной гипертонии. Аортография фактически предопределила развитие пластических операций на почечных сосудах и аорте, и мы являемся свидетелями блестящих успехов в лечении больных гипертонией, обусловленной стенозом почечной артерии. Аортография в сочетании с пневморетроперитонеумом позволяет диагностировать забрюшинные опухоли, особенно при применении стереоскопических снимков в комбинации с томографией. Аортография все чаще находит применение и у детей, в том числе у новорожденных. Чаще всего аортография детям производится при подозрении на аномалии почек и верхних мочевых путей, опухоли надпочечников. Техника исследования у них мало отличается от техники, применяемой у взрослых. Аортографию у детей предпочтительнее производить под наркозом. Walter и Goodwin (1953) рекомендуют комбинировать аортографию с пневморетроперитонеумом. Абдоминальная аортография — весьма ценный метод диагностики и заслуживает того, чтобы он значительно шире применялся в практике урологических учреждений. Внутривенная аортография. Этот вид аортографии заключается во введении полиэтиленового катетера в срединную локтевую вену и продвижении его на 8—10 см в направлении плеча. По катетеру быстро вводят 50 мл диатризоата натрия, меченного J131 (ренографин), затем 2 мл 76% стойкого раствора диатризоата натрия и 75 мл физиологического раствора. Время циркуляции контрастного вещества, содержащего меченый йод, от плечевой вены до брюшной аорты определяют при помощи сцинтилляционного скоростного счетчика. После этого с максимальной скоростью вводят по катетеру в вену контрастное вещество в количестве от 65 до 100 мл. Снимки брюшной полости производят через интервал, равный ранее определенному времени циркуляции контрастного вещества от плечевой вены до брюшной аорты (Bernstein, 1958; Steinberg, 1961). При помощи такой техники Greenspan et. al. (1959) произвели 158 абдоминальных аортографии. Более чем у 90% больных были получены достаточные для диагностики данные (при различных заболеваниях почек, аневризмах аорты, стенозе и облитерации аорты). Осложнения были отмечены у 2 больных в виде кратковременной тошноты, у 2 — головной боли и у 3 — флебита (в области плеча, где катетер находился длительное время). Сложность техники внутривенной аортографии и необходимость введения больному весьма больших количеств контрастного вещества при ней не сделали этот вид исследования распространенным в урологии. Дата добавления: 2015-02-05 | Просмотры: 1755 | Нарушение авторских прав |
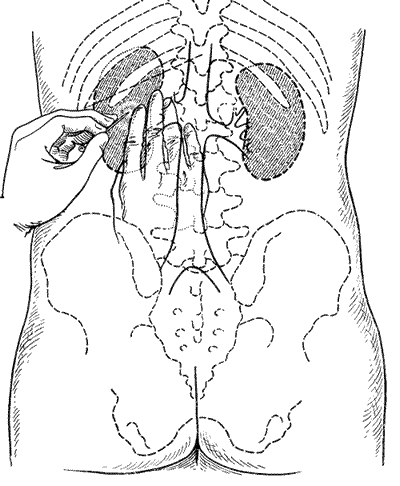
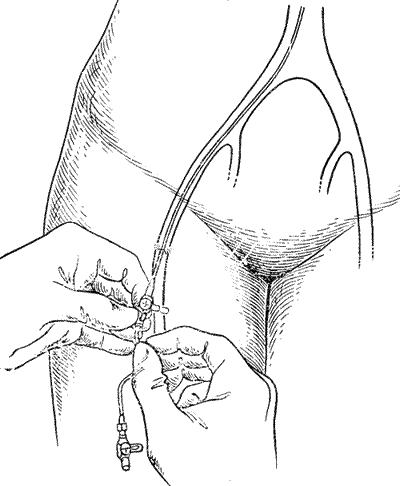
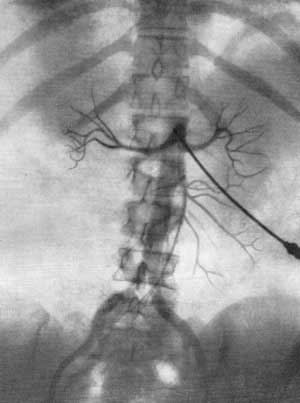
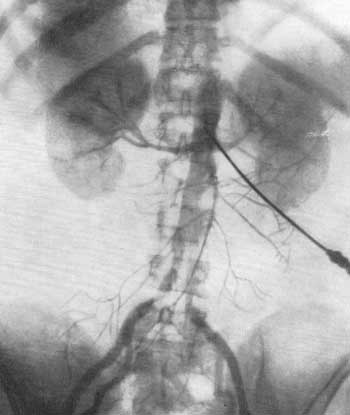
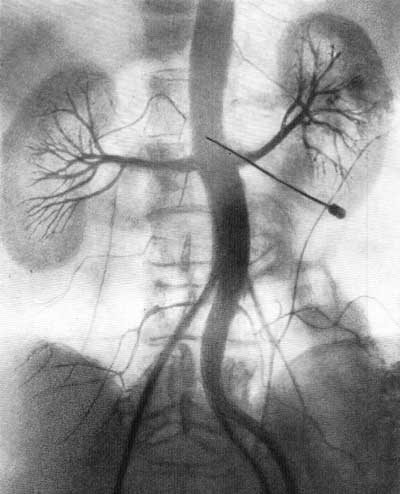
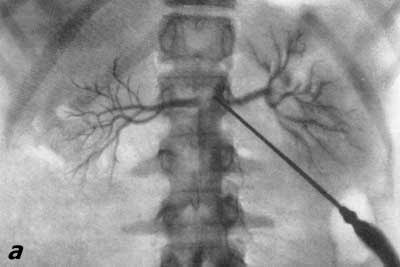
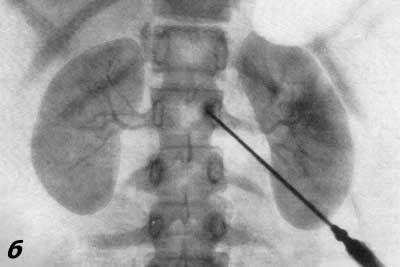
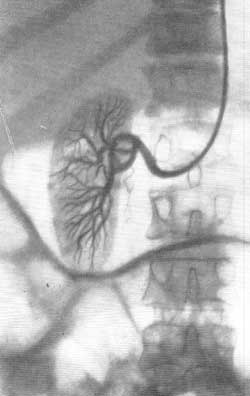 Рис. 73. Селективная почечная ангиография (брахиально-аортальный метод). Нормальная ангиограмма (Meinardi, Bubbio, 1962).
Рис. 73. Селективная почечная ангиография (брахиально-аортальный метод). Нормальная ангиограмма (Meinardi, Bubbio, 1962).