 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
ПАТОГЕНЕЗ СИНДРОМА ОСТРОЙ ИШЕМИИЭТИОЛОГИЯ Эмболия является осложнением различных эмбологенных заболеваний. Установлено, что у 90—95% больных причиной эмболии артериальных сосудов большого круга кровообращения являются заболевания сердца, при которых в его полостях образуются тромботические массы: атеросклеротическая кардиопатия (острый инфаркт миокарда, диффузный и постинфарктный кардиосклероз, аневризмы сердца), ревматические пороки клапанов, преимущественно митральный стеноз, подострый септический эндокардит.
1 — тромбы левого предсердия при пороках митрального клапана; 2 — пристеночные тромбы в левом желудочке при атеросклеротических кардиопатиях; 3 — тромбы на клапанах при септическом эндокардите, протезировании клапанов; 4 — парадоксальная эмболия венозными тромбами при неэаращении овального отверстия меж-предсердной перегородки; 5 — тромбы легочных вен; 6 — тромбы аневризмы аорты; 7 — тромбы аневризмы подключичной артерии при шейном ребре и синдроме передней лестничной мышцы
Септический эндокардит и врожденные пороки сердца как причина эмболии наблюдаются редко, примерно у 1—2% больных. Почти у 75% больных с эмболиями артериальных сосудов отмечаются нарушения ритма сердечных сокращений, наиболее часто в виде мерцательной аритмии. Аритмии способствуют образованию тромбов в полостях сердца вследствие значительного нарушения внутрисердечной гемодинамики. Эмбологенные тромботические массы находятся, как правило, в левом предсердии (при митральных пороках) и в левом желудочке (обычно при кардиосклерозе, инфаркте миокарда, аневризмах желудочка). Редко тромбы образуются на клапанах (при септическом эндокардите, протезировании клапана). Крайне редко наблюдаются случаи аномального (парадоксальная эмболия) перемещения тромба из правых в левые полости сердца, в том числе при тромбозах периферических вен, через врожденные дефекты перегородок и открытый артериальный проток сердца. Тиреотоксические кардиопатии с мерцательной аритмией также могут привести к артериальной эмболии. Отрыв внутрисердечного тромба происходит нередко при усилении сердечной деятельности, часто вследствие применения сердечных гликозидов, эмоционального и двигательного возбуждения, после дефибрилляции с целью устранения аритмии (так называемые постконверсионные эмболии). Повышение фибринолитической активности крови может способствовать фрагментации и отрыву тромба, в связи с чем считают нецелесообразным применение для лечения артериальных эмболии мощных фибрино-литИческих. средств (В. С. Савельев с соавт.,-1974). В целом механизмы мобилизации внутрисердечных тромбов изучены недостаточно. Среди внесердечных эмбологенных заболеваний первое место занимают аневризмы аорты и ее крупных ветвей. Источником эмболии являются пристеночные тромбы аневризматического мешка. Атеросклероз аорты в тромбонекротической стадии с пристеночным тромбозом может привести к эмболии периферических сосудов. К периферической эмболии может привести также пневмония, когда тромбы, образующиеся в легочных венах, мигрируют стоком крови в левоепредсердие, левый желудочек, а затем в артерии большого круга кровообращения. В литературе описаны также казуистические случаи эмболии артерий инородными телами (например, пулей), опухолевыми массами, а также оболочками паразитарных кист. Эмбол может попадать с током крови в любую артерию большого круга кровообращения. Обычно эмболыокклюзируют магистральные сосуды в области бифуркаций и отхождения крупных ветвей, где диаметр сосуда резко уменьшается. Это обстоятельство важно в практическом отношении, так как облегчает клиническую диагностику уровня эмболии. Среди так называемых хирургических эмболии артерий наиболее часто наблюдаются эмболии бедренной артерии в области ее бифуркации, подколенной артерии, плечевой артерии в области отхождения глубокой артерии плеча и в месте ее бифуркации, редко подмышечной и подключичной артерий (Fogarty, 1965, и др.). Эмбол может мигрировать с током крови в дистальном направлении с одного «этажа» на другой после введения обезболивающих, сосудорасширяющих средств, при транспортировке больного, в состоянии наркоза. Этим объясняются случаи самостоятельного улучшения состояния конечности после начальных, резко выраженных патологических изменений конечности. Нередко наблюдаются «этажные» эмболии (В. С. Савельев с соавт. 1970, 1975), то есть на разных уровнях магистральных сосудов одной конечности при фрагментации эмбола, а также комбинированные, при которых возникает эмболическая окклюзия артерий разных конечностей, и сочетанные, когда поражаются также висцеральные и мозговые сосуды.
Типичные места («этажи») эмболии артериального сосудистого русла ПАТОГЕНЕЗ СИНДРОМА ОСТРОЙ ИШЕМИИ Знание основных патогенетических механизмов развития острой ишемии тканей при острой закупорке магистральных артерий необходимо для правильной оценки степени ишемии, выбора методов хирургического и терапевтического лечения.В результате островозникшей закупорки магистральной артерии развивается спазм периферических сосудов. Механизм развития артериоспазма недостаточно выяснен. В нем участвуют рефлекторные реакции, влияние кислородного голодания стенки сосудов и эффект действия трансмурального давления на стенки микрососудов при резком снижении в них давления крови ниже критического уровня.
Вследствие нарушения гемодинамики (стаз крови), патологических изменений сосудистой стенки в результате гипоксии и аноксии и изменений свертывающей системы крови развивается продолженный тромбоз в проксимальном (восходящий) и в дистальном (нисходящий) направлении по отношению к месту первоначальной закупорки. В последующем тромб увеличивается, спаивается со стенкой сосуда, распространяется на ее боковые ветви, мышечные артерии. Развивается воспалительная реакция сосудистой стенки. Вследствие метаболических изменений в тканях возникают микро- и макроагрегаты форменных элементов крови, микроэмболы, тромбозы в мышечных и даже в магистральных венах — у5—6% больных (В. С.Савельев с соавт., 1974). Острая непроходимость магистральных артерий приводит к развитию острой аноксии (гипоксии) и нарушению всех видов обмена в тканях. Важнейшее значение имеет развитие метаболического ацидоза, обусловленного переходом аэробного окисления в анаэробный, и накопление избыточного количества недоокисленных продуктов обмена, в частности ПВК и МК. В ишемизированных тканях в большом количестве появляются активные ферменты, напримеркинины. Выделен также «ишемический токсин» (В. В. Кованов, Т. М. Оксман), точная структура которого и механизм действия недостаточно изучены. Анок-сия и метаболический ацидоз приводят к нарушению проницаемости клеточных мембран, гибели мышечных клеток. В результате этого внутриклеточный калий и миоглобин накапливаются в межтканевой жидкости, попадают в общий кровоток и развиваются гиперкалиемия и «миоглобинурический нефроз». При тяжелой продолжительной ишемии конечности возникает субфасциальный отек мышц, обусловленный нарушением проницаемости клеточных мембран и ионного равновесия. Мышцы конечностей заключены в плотные фасциальные и костно-фасциальные влагалища и сдавление их при отеке усугубляет нарушение кровотока в тканях. Это может привести к некрозу целых групп мышц, особенно после оперативного восстановления кровотока в магистральных артериях, поскольку отек ишемизированных мышц резко увеличивается после операции. Установлено, что в сосудах ишемизированных тканей образуются макроагрегаты форменных элементов крови (В. С. Савельев с соавт., 1973, 1975). Метаболические нарушения (ацидоз, активные ферменты), стаз крови, наличие макроагрегатов форменных элементов крови создают условия для внутрисосудистого тромбообразования в мелких сосудах, капиллярах, что в конечном счете приводит к развитию необратимых изменений в тканях конечности. Дата добавления: 2015-11-26 | Просмотры: 575 | Нарушение авторских прав |
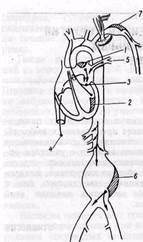 Источники эмбологенных тромбов:
Источники эмбологенных тромбов: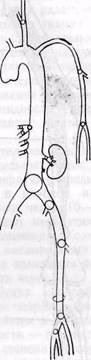
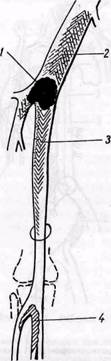 Схема развития продолженного тромба — восходящего (2) и нисходящего (3) по отношению к эмболу (1), а также вторичного тромбоза (4) дистальных сосудов. Граница восходящего тромба достигает уровня отхождения крупной артериальной ветви
Схема развития продолженного тромба — восходящего (2) и нисходящего (3) по отношению к эмболу (1), а также вторичного тромбоза (4) дистальных сосудов. Граница восходящего тромба достигает уровня отхождения крупной артериальной ветви