|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ БОЛЕЗНЕЙ ПЕРИОДОНТА
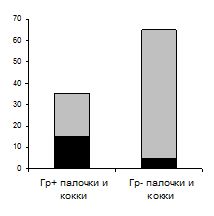
В периодонтологии проведено немало экспериментальных и клинических исследований изменений тканей периодонта под влиянием различных факторов риска, осуществлены попытки установления причинной взаимосвязи развития болезней периодонта с патогенной ролью микробиологических, иммунологических, травматических агентов на фоне анатомо-топографической специфики тканей полости рта. Полость рта рассматривается как сбалансированная биологическая система, а заболевания периодонта — как следствие нарушения существующего в ней равновесия между ее бактериальной составляющей и тканями. Это равновесие может нарушаться, с одной стороны, за счет увеличения количества бактерий и их патогенности, с другой — девиации защитных способностей тканей. При этом главная этиологическая роль воспалительных заболеваний периодонта отводится микроорганизмам зубного налета. И существует большая группа факторов, не вызывающих воспаления в периодонте, но способствующих развитию патологического процесса в периодонте — факторы риска воспалительных заболеваний периодонта. Необходимо упомянуть, что причиной гингивита может быть также острая механическая травма, термический или химический ожог и т. д. Микроорганизмы зубного налета как этиологическая причина воспалительных болезней периодонта. Участие микроорганизмов зубного налета в развитии воспаления тканей периодонта общепризнанно. Зубной налет представляет собой мягкий структурированный, прикрепленный к поверхности зуба налет, который невозможно смыть водой. В 1 мг зубного налета содержится приблизительно 108 бактерий. Результаты контрольных исследований по установлению влияния налета на возникновение воспалительных процессов в тканях периодонта свидетельствуют о том, что при отсутствии гигиенического ухода за полостью рта уже через трое суток обнаруживаются первые признаки воспаления десны, а через 5–7 дней появляются симптомы острого или хронического гингивита. Микрофлора зубного налета качественно и количественно изменчива. Воспалительные заболевания периодонта длительное время рассматривались как следствие неспецифического инфицирования бактериями налета. Исходили из того, что состав налета определяет особенности воспалительных процессов в периодонте. Открытие специфических видов бактерий, в сочетании с определенными формами воспалительных реакций, дало основание предположить, что имеет место специфическая инфекция. Поэтому воспалительные заболевания периодонта теперь многие рассматривают как оппортунистическую инфекцию, зависящую не только от присутствия патогенных микроорганизмов, но и от среды, способствующей их размножению. К возможным патогенам относятся: Aktinobacillus actinomycetem comitans, Bacteroides forsithus, Eikenella corrodens, Fusobacterium nucleatum, Porphyromonas gingivalis, спирохеты. Видовая специфичность микроорганизмов зубного налета непостоянна и зависит от эндогенных и экзогенных факторов. Так, интенсивность образования зубного налета зависит от состава слюны, ее вязкости, микрофлоры полости рта, десквамации эпителия слизистой оболочки, наличия местных воспалительных процессов, анатомического строения зубов и т. д. Микрофлора наддесневого зубного налета здоровой десны состоит на Поддесневой зубной налет образуется в результате скопления микроорганизмов в десневой бороздке при уже сформированном наддесневом налете. Бедная кислородом среда поддесневого налета способствует развитию анаэробных микроорганизмов. В видовом составе микрофлоры поддесневого налета при здоровом периодонте преобладают неподвижные микроорганизмы (кокки и т. п.). При этом соотношение между подвижными и неподвижными бактериями составляет 40–49:1. При воспалении в поддесневом налете возрастает количество веретенообразных и нитевидных микроорганизмов, подвижных палочек и спирохет. Соотношение неподвижных и подвижных бактерий составляет 1:1–3. Изменение бактериального состава зубного налета происходит по мере возникновение и развития воспалительных патологических изменений в тканях периодонта. Разнообразный состав микрофлоры зубного налета в клинически здоровых и воспаленных периодонтальных тканях представлен схематически на рис. 2.
Рис. 2. Состав зубного налета (по Slots) при различных состояниях периодонта
Прикрепленный к зубной поверхности налет может обызвествлятся и образовывать зубной камень. Механизм кальцификации — это результат сочетанных воздействий микробных, физико-химических и биологических факторов. Минеральные соли откладываются на коллоидной основе при проникновении кристаллов фосфата кальция из слюны в наддесневой зубной налет, или из сыворотки в поддесневой зубной налет. Кальцинированный зубной налет может минерализоваться на 50–90 % за 12 дней. И полностью зубной камень формируется в течение 3–4 недель. Прирост зубного камня — результат накопления зубного налета со временем. Несмотря на шероховатую поверхность, как поддесневой, так и наддесневой зубной камень непосредственно не является этиологической причиной воспалительных процессов в периодонте, однако служит ретенционной поверхностью для содержащего большое количество микроорганизмов зубного налета. Факторы риска развития воспалительных процессов в периодонте. Эти состояния обособленно не могут вызвать воспалительной реакции периодонта. Но они способствуют ретенции зубного налета или воздействию механизмов развития воспаления в периодонте. Различают местные и системные факторы. Местные факторы · расположение зубов. Скученность, смещение, подвижность зубов усложняют их чистку и способствуют скоплению зубного налета; · открытые кариозные полости являются бактериальным резервуаром и способствуют отложению налета; · при ротовом дыхании из-за недостаточности антибактериального действия десневой жидкости и слюны в условиях плохой гигиены стимулируется развитие воспалительных процессов в периодонте; · строение мягких тканей. Короткие уздечки губ и языка и боковые тяжи, мелкое преддверие полости рта затрудняют гигиену полости рта и способствуют при еде отделению десны от зубов. Вследствие этого возникают углубления, способствующие накоплению налета; · поверхности некачественных пломб и протезов (нависающие края пломб и коронок, неполированные или пористые поверхности пломб, расположенные у десны кламмера протезов, ортодонтические аппараты, неправильно восстановленные апроксимальные контакты зубов) способствуют скоплению зубного налета и затрудняют гигиенический уход за полостью рта; · консистенция и количество слюны, а также ее состав (наличие иммуноглобулинов, лейкоцитов); · вредные привычки (курение). Курение является одним из наиболее серьезных факторов риска возникновения болезней периодонта. Исследования (Axelsson, 1997) показали, что для курящих пациентов в возрасте около 65 лет тяжелые формы периодонтита наблюдаются на 50 % чаще, чем у некурящих. Это происходит за счет снижения активности нейтрофильных гранулоцитов и фагоцитов, уменьшения количества защитных Т-клеток. Также происходит деградация структуры коллагена; · окклюзионная травма. Как результат адаптации удерживающего аппарата зуба к травматической окклюзии наблюдаются гистологические изменения периодонтальной связки и костной ткани альвеолярного отростка (тромбозы, кровоизлияния, дистрофические изменения гиалина). Однако непосредственно сама окклюзионная травма не вызывает воспалительных изменений периодонта. После устранения травматического воздействия структуры пораженных участков периодонта восстанавливаются; · неправильный режим и характер питания. Пища, состав и сбалансированность ее компонентов, прежде всего углеводов и крахмала, а также особенности ежедневного режима питания оказывают влияние на подавление роста или, наоборот, скорость размножения болезнетворных бактерий, вызывающих кариес или заболевания периодонта; · патологические изменения периодонта. Десневые и периодонтальные карманы затрудняют проведение гигиенических мероприятий полости рта; · возраст. У пожилых пациентов, наряду с увеличением общесоматических заболеваний, влияющих на компенсаторные механизмы организма, снижена эффективность ухода за зубами из-за недостаточной подвижности пальцев и рук, возникновения болей в суставах при движении или длительном стоянии перед зеркалом. Даже незначительное снижение эффективности ухода за полостью рта приводит к возникновению тяжелых форм периодонтитов вследствие усиления других факторов риска. Общие факторы: · общесоматические заболевания (сахарный диабет, заболевания крови, ВИЧ-инфекция, отравления тяжелыми металлами, дерматозы); · заболевания, при которых могут проявляться различные расстройства периодонтального комплекса (синдром Дауна, синдром Папийона-Лефевра, синдром Олбрайта и др.); · беременность. В основе влияния на развитие болезней периодонта · прием некоторых лекарственных препаратов (нифедипин, циклоспорин А, гидантоиновые препараты) Дата добавления: 2016-06-06 | Просмотры: 515 | Нарушение авторских прав |