КАРДИОСКЛЕРОЗ
Кардиосклероз — разрастание соединительной ткани в сердечной мы-
шце. Как правило, это — вторичный процесс.
Патологическая анатомия. Различают очаговый и диффузный кардиоскле-
роз. При очаговом кардиосклерозе в мышце сердца образуются различной
величины белесоватые тяжистые участки (рубцы). Такие рубцы обычно
образуются при организации инфарктов миокарда. Они пронизывают иногда
толщу мышцы сердца и представляют собой обширные поля (крупцооча-
говый кардиосклероз), на месте которых нередко формируется хро-
ническая аневризма (от греч. aneuryno — расширять) сердца. По периферии
таких рубцов миокард утолщен (регенерационная гипертрофия). Доволь-
но часто развивается мелкоочаговый кардиосклероз, предста-
вленный белесоватыми периваскулярными очажками и полосками, которые
равномерно разбросаны в мышце сердца. Он возникает в результате разраста-
ния соединительной ткани в участках дистрофии, атрофии и гибели отдельных
мышечных клеток в связи с гипоксией.
Диффузный кардиосклероз, или миофиброз, характеризует-
ся диффузным утолщением и огрубением стромы миокарда за счет новообра-
зования в ней соединительной ткани. Соединительная ткань в таких случаях
оплетает, как бы замуровывает атрофирующиеся мышечные волокна.
Морфогенез. Различают три вида кардиосклероза: постинфарктный, за-
местительный и миокардитический. Постинфарктный кардиоскле-
роз обычно бывает крупноочаговым, замести т е льны й — мелкооча-
говым, миокардитический — диффузным (миофиброз).
Клиническое значение. С кардиосклерозом связано нарушение сократитель-
ной функции миокарда, проявляющееся в сердечной недостаточности и нару-
шениях ритма сердца. Крупноочаговый постинфарктный кардиосклероз слу-
жит основой развития хронической аневризмы сердца.
АТЕРОСКЛЕРОЗ
Атеросклероз (от греч. athere — кашица и sklerosis — уплотнение) —
хроническое заболевание, возникающее в результате нарушения жирового
и белкового обмена, характеризующееся поражением артерий эластиче-
ского и мышечно-эластического типа в виде очагового отложения в ин-
тиме липидов и белков и реактивного разрастания соединительной ткани.
Атеросклероз широко распространен среди населения экономически
развитых стран Европы и Северной Америки, в странах Африки и Азии он
встречается реже. Болеют обычно люди во второй половине жизни. Проявле-
ния и осложнения атеросклероза являются наиболее частыми причинами
смертности и инвалидности в большинстве стран мира.
Следует отличать атеросклероз от артериосклероза, которым обозначают склероз ар-
терий вне зависимости от причины и механизма его развития. Атеросклероз является лишь
разновидностью артериосклероза, отражающей нарушения метаболизма липидов и белков
(«метаболический артериосклероз»). В таком толковании термин «атеросклероз»
был введен в 1904 г. Маршаном и обоснован экспериментальными исследованиями Н. Н. Анич-
кова. Поэтому атеросклероз называют болезнью Маршана — Аничкова.
В зависимости от этиологических, патогенетических и морфологических признаков разли-
чают следующие виды артериосклероза: 1) атеросклероз («метаболический артериос-
клероз»); 2) артериолосклероз, или гиалиноз (например, при гипертонической болезни); 3) во-
спалительный артериосклероз (например, сифилитический, туберкулезный); 4) аллергический
артериосклероз (например при узелковом периартериите); 5) токсический артериосклероз (на-
пример, адреналиновый); 6) первичный кальциноз средней оболочки артерий (медиакальциноз
Менкеберга); 7) возрастной (старческий) артериосклероз.
Этиология и патогенез. В развитии атеросклероза наибольшее значение
имеют следующие факторы: 1) обменные факторы; 2) гормональные фак-
торы; 3) артериальная гипертония; 4) стрессовые и конфликтные ситуации, ве-
дущие к психоэмоциональному перенапряжению; 5) состояние сосудистой
стенки; 6) наследственные и этнические факторы.
Среди обменных факторов основное значение имеют нарушения
жирового и белкового обмена.
Гиперлипемии (гиперхолестеринемии) придается чуть ли не
ведущая роль в этиологии атеросклероза. Это доказано экспериментальными
исследованиями. Скармливание животным холестерина приводит к гиперхоле-
стеринемии, отложению холестерина и его эфиров в стенке аорты и артерий,
развитию атеросклеротических изменений. У больных атеросклерозом людей
также нередко отмечаются гиперхолестеринемия, ожирение. Эти данные по-
зволяли ранее считать, что в развитии атеросклероза исключительное значе-
ние имеет алиментарный фактор (алиментарная инфиль-
трационная теория атеросклероза Н. Н. Аничкова). Однако
в дальнейшем было доказано, что избыток экзогенного холестерина у челове-
ка во многих случаях не приводит к развитию атеросклероза, корреляция
между гиперхолестеринемией и выраженностью морфологических изменений,
свойственных атеросклерозу, отсутствует.
В настоящее время в развитии атеросклероза придается значение не столь-
ко самой гиперхолестеринемии, сколько нарушению соотношений холесте-
рина с фосфолипидами (нарушение холестеринолецитинового коэффициента)
и белками (избыточное образование В-липопротеидов). Подчеркивается важ-
ное значение жиробелкоаых комплексов — В-липопротеидов, которые могут
выступать в роли атерогенных веществ и аутоантигенов.
Доказательство антигенных свойств В-липопротеидов явилось основанием
для создания иммунологической теории атеросклероза. Со-
гласно этой теории, при атеросклерозе образуются иммунные комплексы В-
липопротеид — аутоантитело, которые, циркулируя в крови, откладываются
в интиме артерий, что ведет к развитию характерных изменений.
О значении в развитии атеросклероза нарушений не только липидного, но
и белкового обмена свидетельствует частое возникновение атеросклероза
при подагре, желчнокаменной болезни.
Значение гормональных факторов в развитии атеросклероза не-
сомненно. Так, сахарный диабет и гипотиреоз способствуют, а гипертиреоз
и эстрогены препятствуют развитию атеросклероза. Несомненна и роль а р -
териальной гипертонии в атерогенезе. Вне зависимости от характера
гипертонии при ней отмечается усиление атеросклеротического процесса. При
гипертонии атеросклероз развивается даже в венах (в легочных венах — при
гипертензии малого круга, в воротной вене — при портальной гипертензии).
Эти данные свидетельствуют о значении гемодинамического фак-
тора в патогенезе атеросклероза. Исключительная роль в этиологии атеро-
склероза отводится стрессовым и конфликтным ситуациям,
т. е. нервному фактору. С этими ситуациями связано психоэмо-
циональное перенапряжение, ведущее к нарушению нейроэндо-
кринной регуляции жиробелкового обмена и вазомоторным расстройствам,
что определяет развитие атеросклеротических изменений (нервно-мета-
болическая теория атеросклероза А. Л. Мясникова). Поэтому
атеросклероз рассматривается как болезнь урбанизации, болезнь сапиентации.
Атеросклероз — заболевание жителей города, а не деревни, работников
в основном умственного (интеллектуального), а не физического труда.
Состояние сосудистой стенки в значительной мере определяет
развитие атеросклероза. Имеют значение заболевания (инфекции, интоксика-
ции, артериальная гипертония), ведущие к поражению стенки артерий (арте-
риит, плазматическое пропитывание, тромбоз, склероз), что «облегчает» воз-
никновение атеросклеротических изменений. Избирательное значение при
этом имеют пристеночные и интрамуральные тромбы, на которых «строится»
атеросклеротическая бляшка (тромбогенная теория Рокитанского —
Дьюгеда).
Некоторые исследователи придают основное значение в развитии атеро-
склероза возрастным изменениям артериальной стенки и
рассматривают атеросклероз как «проблему возраста», как «геронтологиче-
скую проблему» (И. В. Давыдовский); нозологическая сущность атеросклеро-
за отвергается. Эта концепция не разделяется большинством патологов.
Роль наследственных факторов в атеросклерозе доказана (на-
пример, атеросклероз у молодых людей при семейной гиперхолестеринемии),
но изучена недостаточно. Имеются данные о роли этнических факто-
ров в его развитии.
Таким образом, атеросклероз следует считать полиэтиологическим
заболеванием, возникновение и развитие которого связаны с влиянием
экзогенных и эндогенных факторов.
Патологическая анатомия и морфогенез. Сущность процесса хорошо отра-
жает терминов интиме артерий появляются кашицеобразный жиро-белковый
детрит (athere) и очаговое разрастание соединительной
ткани (sclerosis), что приводит к формированию атеросклеротиче-
ской бляшки, суживающей просвет сосуда. Обычно поражаются, как уже
упоминалось, артерии эластического и мышечно-эластического типа, т. е. ар-
терии крупного и среднего калибра; значительно реже в процесс вовлекаются
мелкие артерии мышечного типа.
Атеросклеротический процесс проходит определенные стадии (фаз ы),
которые имеют макроскопическую и микроскопическую характеристику
(морфогенез атеросклероза).
При макроскопическом исследовании различают следующие виды атеро-
склеротических изменений, отражающие динамику процесса (рис. 194, 195, см.
на цветн. вкл.): 1) жировые пятна или полоски; 2) фиброзные бляшки; 3) ос-
ложненные поражения, представленные фиброзными бляшками с изъязвле-
нием, кровоизлияниями и наложениями тромботических масс; 4) кальциноз,
или атерокальциноз.
Жировые пятна или полоски — это участки желтого или желто-се-
рого цвета (пятна), которые иногда сливаются и образуют полоски, но не воз-
вышаются над поверхностью интимы. Они содержат липиды, выявляемые
при тотальной окраске сосуда красителями на жиры, например Суданом.
Раньше всего жировые пятна и полоски появляются в аорте на задней стенке
и у места отхождения ее ветвей, позже — в крупных артериях.
У 50 % детей в возрасте моложе 1 года можно обнаружить в аорте ли-
пидные пятна. В юношеском возрасте липидоз усиливается, жировые пятна
появляются не только в аорте, но и в венечных артериях сердца. С возрастом
изменения, характерные для физиологического раннего липидоза, в подав-
ляющем большинстве случаев исчезают и не являются источником развития
дальнейших атеросклеротических изменений.
Фиброзные бляшки — плотные, овальные или круглые, белые или
бело-желтые образования, содержащие липиды и возвышающиеся
над поверхностью интимы. Часто они сливаются между собой, придают вну-
тренней поверхности сосуда бугристый вид и резко суживают его просвет
(стенозирующий атеросклероз). Наиболее часто фиброзные бляш-
ки наблюдаются в брюшной аорте, в отходящих от аорты ветвях, в артериях
сердца, мозга, почек, нижних конечностей, сонных артериях и др. Чаще пора-
жаются те участки сосудов, которые испытывают гемодинамическое (меха-
ническое) воздействие (в областях ветвления и изгибов артерий, на стороне
их стенки, которая имеет жесткую подстилку).
Осложненные поражения возникают в тех случаях, когда в толще
бляшки преобладает распад жиро-белковых комплексов и образуется детрит,
напоминающий содержимое ретенционной кисты сальной железы, т. е. ате-
ромы. Поэтому такие изменения называют атероматозными. Про-
грессирование атероматозных изменений ведет к деструкции покрышки
бляшки, ее изъязвлению (атероматозная язва), кровоизлияниям
в толщу бляшки (интрамуральная гематома) и образованию
тромботических наложений на месте изъязвления бляшки. С ос-
ложненными поражениями связаны: острая закупорка артерии тромбом
и развитие инфаркта, эмболия как тромботическими, так и атероматозными
массами, образование аневризмы сосуда в месте его изъязвления, а также
артериальное кровотечение при разъедании стенки сосуда атероматозной
язвой.
Кальциноз, или атерокальциноз, — завершающая фаза атеро-
склероза, которая характеризуется отложением в фиброзные бляшки солей
кальция, т. е. их обызвествлением. Бляшки приобретают каменистую
плотность (петрификация бляшек), стенка сосуда в месте петрифика-
ции резко деформируется.
Различные виды атеросклеротических изменений нередко сочетаются;
в одном и том же сосуде, например в аорте, можно видеть одновременно жи-
ровые пятна и полосы, фиброзные бляшки, атероматозные язвы с тромбами
и участки атерокальциноза, что свидетельствует о волнообразности
течения атеросклероза.
Микроскопическое исследование позволяет уточнить и дополнить характер
и последовательность развития изменений, свойственных атеросклерозу. На
основании его результатов выделены следующие стадии морфогенеза
атеросклероза (рис. 196, см. на цветн. вкл.): 1) долипидная; 2) липидоз;
3) липосклероз; 4) атероматоз; 5) изъязвление; 6) атерокальциноз.
В изучении морфогенеза, патогенеза и этиологии атеросклероза огромное
значение имело создание его экспериментальной холестерино-
вой модели.
Впервые модель атеросклероза была создана отечественными учеными — патологоанатомом
Н. Н. Аничковым и патофизиологом С. С. Халатовым на кроликах при скармливании им холе-
стерина. В дальнейшем подобная модель воспроизведена на курах, свиньях, собаках, обезьянах
и других животных. При кормлении животных холестерином удалось выявить в стенке артерий
изменения, весьма близкие (но не тождественные) атеросклерозу человека, проследить их дина-
мику, изучить факторы, ускоряющие и замедляющие развитие атеросклероза, а также способ-
ствующие регрессии атеросклеротических изменений. Эти исследования явились основой для
разработки рациональной терапии атеросклероза.
Долипидная стадия характеризуется изменениями, отражающими
общие нарушения метаболизма при атеросклерозе (гиперхолестеринемия, на-
копление грубодисперсных белков и мукоидных веществ в плазме крови, по-
вышение активности гиалуронидазы и т. д.) и «травму» интимы продуктами
нарушенного метаболизма. К этим изменениям относятся: 1) повышение
проницаемости эндотелия и мембран интимы, что ведет
к накоплению во внутренней оболочке белков плазмы, фибриногена (фибрина)
и образованию плоских пристеночных тромбов; 2) накопление кислых
гликозаминогликанов (в основном сульфатированных мукополисаха-
ридов) в интиме, с чем связано появление мукоидного отека внутрен-
ней оболочки, а поэтому благоприятных условий для фиксации в ней В-липо-
протеидов, холестерина, белков; 3) деструкцией эндотелия, о а -
зальных мембран интимы, эластических и коллаге-
нов ых волокон, способствующей еще большему повышению проницае-
мости интимы для продуктов нарушенного обмена и пролиферации
гладкомышечных клеток. Не исключено, что такие вещества, как хондроитин-
сульфаты и холестерин, откладываются в интиме вследствие травмы эласти-
ческих структур.
Ряд веществ нарушенного обмена, в частности липиды, холестерин и фибрин, хорошо вы-
являются в эндотелии и за базальной его мембраной при электронно-микроскопическом иссле-
довании (рис. 197). Из этого следует, что понятие «долипидная стадия» уточняется результатами
электронно-микроскопического анализа начальных изменений интимы при атеросклерозе. Сущ-
ность этих изменений заключается в адаптивной реакции интимы на первичные гуморально-ме-
таболические и нервно-сосудистые нарушения (В. X. Анестиади).
Продолжительность долипидной стадии определяется возможностью ли-
политических и протеолитических (фибринолитических) ферментов интимы
«очищать» ее от «засорения» продуктами нарушенного метаболизма. Как
правило, активность этих ферментов интимы в долипидной стадии повышена,
истощение их знаменует начало стадии липидоза.
В стадии липидоза отмечается очаговая инфильтрация интимны, особен-
но поверхностных ее отделов, липидами (холестерином), В-липопротеидами,
белками (рис. 198), что ведет к образованию жировых пятен и
полос. Липиды диффузно пропитывают интиму и накапливаются в макро-
фагах, которые получили название ксантомных клеток (от греч. xant-
hos — желтый). Роль этих клеток выполняют гладкомышечные клетки. В эн-
дотелии также появляются липидные включения, что свидетельствует об
инфильтрации интимы липидами плазмы крови. Отчетливо выражены набуха-
ние и деструкция эластических мембран.
Рис. 197. Атеросклероз, долипидные изменения интимы аорты.
В эндотелиальной клетке увеличивается зона комплекса Гольджи (АГ), более выражена эндо-
плазматическая сеть (ЭС), в которой появляется плотный материал — липиды (Л); базальная мембрана
(БМ) несколько разрыхлена; за базальной мембраной среди коллагеновых (K.лB) и эластических
(ЭВ) волокон фибриллярные отложения (Фл) белков и липидов (77). Я-ядро, х 23 000 (по Гиру).
Рис. 198. Липоидоз. Во внутренних отделах интимы скопления липидов (черного цвета).
Липосклероз характеризуется разрастанием молодых соединительно-
тканных элементов интимы в участках отложения и распада липидов и бел-
ков, появлением большого числа макрофагов — ксантомных клеток, разруше-
нием эластических и аргирофильных мембран. Очаговое разрастание в интиме
молодой соединительной ткани и ее последующее созревание ведут к форми-
рованию фиброзной бляшки (рис. 199), в которой появляются тонко-
стенные сосуды, связанные с vasa vasorum.
Существует точка зрения, что формирование фиброзной бляшки связано
с пролиферацией гладкомышечных клеток, возникающей в ответ на поврежде-
ние эндотелия и эластических волокон артерий.
При атероматозе липидные массы, составляющие центральную часть
бляшки, а также прилежащие коллагеновые и эластические волокна распа-
даются (рис. 200). При этом образуется мелкозернистая аморфная масса,
в которой обнаруживаются кристаллы холестерина и жирных кислот, обрыв-
ки эластических и коллагеновых волокон, капельки нейтральных жиров (ате-
роматозный детрит). В краях у основания бляшки появляется много
новообразованных сосудов, врастающих из vasa vasorum, а также ксантомные
клетки, лимфоциты, плазматические клетки. Атероматозньте массы отграни-
чены от просвета сосуда слоем зрелой, иногда гиалиниаированной соедини-
тельной ткани (покрышка бляшки). В связи с тем что атероматозному
распаду подвергаются гладкие мышечные волокна средней оболочки, бляшка
«погружается» довольно глубоко, достигая в некоторых случаях адвентиции.
Атероматоз —начало осложненных п о р а ж е н и й. При прогрес-

|

|
Рис. 199. Липосклероз. Просвет венечной артерии сердца сужен фиброзной бляшкой.
Рис. 200. Атероматоз. В толще бляшки атероматозный детрит, кристаллы холестерина.
сировании атероматоза в связи с разрушением новообразованных сосу-
дов происходит кровоизлияние в толщу бляшки (интрамуральная гематома),
покрышка бляшки разрывается.
Наступает стадия изъязвления, характеризующаяся образованием
атероматозной язвы. Края ее подрытые, неровные, дно образовано
мышечным, а иногда наружным слоем стенки сосуда. Дефект интимы очень
часто покрывается тромботическими наложениями, причем тромб
может быть не только пристеночным, но и обтурирующим.
Атерокальциноз (рис. 201) — завершающая стадия морфогенеза ате-
росклероза, хотя отложение извести начинается уже в стадии атероматоза
и даже липосклероза. Из-
весть откладывается в атеро-
матозные массы, в фиброз-
ную ткань, в межуточное
вещество между эластиче-
скими волокнами. При зна-
чительных отложениях из-
вести в покрышке бляшки
образуются плотные и лом-
кие пластинки. Обызвеств-
лению бляшек способствует
эластолиз. В связи с деструк-
цией эластических мембран
Рис. 201. Атерокальциноз. Обыз-
вествление бляшки.
происходит накопление аспарагиновой и глутаминовой кислот. Ионы кальция
связываются со свободными карбоксильными группами этих кислот и
осаждаются в виде фосфата кальция.
Морфогенез атеросклероза в значительной мере определяет выделение
клинических периодов и стадий болезни (А. Л. Мясников).
Начальный (доклинический) период, характеризующийся вазомоторными и метабо-
лическими нарушениями, охватывает периоды долипидной стадии, липидоза и нестенозирующе-
го липосклероза. В период клинических проявлений развитие ишемической ста-
дии связано со стенозирующим атеросклерозом (стенозирующие фиброзные бляшки), ведущим
к развитию ишемии и дистрофии соответствующих органов и тканей. В некротической
стадии — стадии осложненных атеросклеротических поражений — развивается острая окклю-
зия артерий, инфаркты, а в склеротической стадии — медленная окклюзия артерий,
хроническая ишемия и мелкоочаговый склероз, либо исход инфарктных изменений, чаще в
крупноочаговой склероз.
Морфологическое обоснование получило и волнообразное течение
атеросклероза, складывающееся из чередований фаз прогрессирования
(активная фаза), стабилизации (неактивная фаза) и регрессирования.
Прогрессирование атеросклероза характеризуется морфологией
волны липидоза, которая наслаивается на старые изменения (липосклероз,
атероматоз, атерокальциноз) и ведет к развитию осложненных поражений
(атероматоз, кровоизлияние в толще бляшки, тромбоз). При регрессиро-
вании атеросклероза происходят макрофагальная резорбция и вымывание
липидов из бляшек, разрастание соединительной ткани увеличивается.
О волнообразном течении атеросклероза можно судить по гисто-
логическому строению бляшек: они многослойны, состоят из чередую-
щихся прослоек соединительной ткани с участками нерассосавшихся липидов
в глубоких слоях и более свежего выпадения липидов в поверхностных
слоях покрышки.
КЛИНИКО-МОРФОЛОГИЧЕСКИЕ ФОРМЫ
В зависимости от преимущественной локализации атеросклероза в том
или ином сосудистом бассейне, осложнений и исходов, к которым он ведет,
выделяют следующие клинико-анатомические его формы: 1) атеросклероз
аорты; 2) атеросклероз венечных артерий сердца (сердечная форма, ишемиче-
ская болезнь сердца); 3) атеросклероз артерий головного мозга (мозговая
форма); 4) атеросклероз артерий почек (почечная форма); 5) атеросклероз ар-
терий кишечника (кишечная форма); 6) атеросклероз артерий нижних конечно-
стей.
При каждой из этих форм могут наблюдаться двоякие изменения. Медлен-
ное атеросклеротическое сужение питающей артерии и хроническая недоста-
точность кровообращения приводят к ишемическим изменениям —
дистрофии и атрофии паренхимы, диффузному или мелкоочаговому склерозу
стромы. При острой окклюзии питающей артерии и острой недостаточности
кровоснабжения возникают изменения другого рода. Эти катастрофически на-
ступающие изменения имеют некротический характер и проявляются
инфарктами и гангреной. Они отмечаются обычно при прогрессирующем
атеросклерозе.
1. Атеросклероз аорты — наиболее часто встречающаяся форма.
Более резко он выражен в брюшном отделе и характеризуется обычно атеро-
матозом, изъязвлениями, атерокальцинозом. В связи с этим атеросклероз
аорты часто осложняется тромбозом, тромбоэмболией и эмболией атерома-
тозными массами с развитием инфарктов (например, почек) и гангрены (на-
пример, кишечника, нижней конечности). Нередко на почве атеросклероза раз-
вивается аневризма аорты (рис. 202), т. е. выбухание стенки в месте ее
Рис. 202. Аневризма брюшной аорты,
заполненная тромбами.
поражения, чаще изъязвления.
Аневризма может иметь различ-
ную форму, в связи с чем раз-
личают цилиндрическую,
мешковидную, грыжевид-
ную аневризмы. Стенку анев-
ризмы в одних случаях образует
аорта (истинная аневриз-
м а), в других — прилегающие к
ней ткани и гематома (л о ж-
ная аневризма). Если кровь
отслаивает среднюю оболочку
аорты от интимы или от ад-
вентиции, что ведет к образо-
ванию покрытого эндотелием ка-
нала, то говорят о расслаи-
вающей аневризме. Обра-
зование аневризмы чревато ее раз-
рывом и кровотечением. Длитель-
но существующая аневризма аор-
ты приводит к атрофии окружаю-
щих тканей (например, грудины,
тел позвонков).
Атеросклероз дуги аорты мо-
жет лежать в основе синдрома
дуги аорты, а атеросклероз би-
фуркации аорты с тромбозом ее —
вести к развитию синдрома Ле-
риша, имеющего характерную симптоматику.
2. Атеросклероз венечных артерий сердца лежит в основе
ишемической его болезни.
3. Атеросклероз артерий головного мозга, главным обра-
зом артерий основания мозга и средних мозговых артерий, нередко осложня-
ется тромбозом. В таких случаях обычно возникают ишемические ин-
фаркты мозга (очаги серого размягчения — см. рис. 40), реже кровоиз-
лияния в мозг. Длительная ишемия головного мозга на почве стенози-
рующего атеросклероза мозговых артерий приводит к дистрофии и атрофии
коры мозга, развитию атеросклеротического слабоумия.
В последнее время установлено, что 25 —40 % инфарктов головного мозга связано с атерос-
клерозом не церебральных, а магистральных артерий г о л о вы — сонных и позво-
ночных. Эти данные имеют большое практическое значение в связи с доступностью оперативно-
го лечения окклюзионных поражений этих сосудов.
4. При атеросклерозе почечных артерий сужение просвета
бляшкой обычно наблюдается у места ответвления основного ствола или де-
ления его на ветви первого и второго порядка. Чаще процесс односторонний,
реже — двусторонний. В почках развиваются либо клиновидные участки атро-
фии паренхимы с коллапсом стромы и замещением этих участков соедини-
тельной тканью, либо инфаркты с последующей организацией их и формиро-
ванием втянутых рубцов. Возникает крупнобугристая атеросклеротиче-
Рис. 203. Атеросклеротический нефро-
цирроз.
екая сморщенная почка
(атеросклеротический
нефроцирроз; рис. 203),
функция которой страдает ма-
ло, так как большая часть
паренхимы остается сохранной.
В результате ишемии почечной
ткани при стенозирующем ате-
росклерозе почечных артерий в
ряде случаев развивается сим-
птоматическая (почеч-
ная) гипертония.
5. Атеросклероз артерий кишечника, осложненный тром-
бозом, ведет к гангрене кишки.
6. При атеросклерозе артерий конечностей чаще поража-
ются бедренные артерии. Процесс длительное время протекает бессимп-
томно благодаря развитию коллатералей. Однако при нарастающей не-
достаточности коллатералей развиваются атрофические изменения мышц,
похолодание конечности, появляются характерные боли при ходьбе (п е-
ремежающаяся хромота). Если атеросклероз осложняется тромбо-
зом, развивается гангрена конечности (атеросклеротическая ганг-
рена).
Атеросклероз легочной артерии наблюдается только в усло-
виях гипертензии в малом круге кровообращения.
ГИПЕРТОНИЧЕСКАЯ БОЛЕЗНЬ
Гипертоническая болезнь (синонимы: эссенциальная гипертензия,
болезнь высокого артериального давления) — хроническое заболевание, ос-
новным клиническим признаком которого является длительное и стойкое по-
вышение артериального давления (гипертензия). Описана как самостоя-
тельное заболевание неврогенной природы, как «болезнь
неот pea тированных эмоций» отечественным клиницистом
Г. Ф. Лангом.
Гипертоническая болезнь, как и атеросклероз, является болезнью урбани-
зации и сапиентации, широко распространена в экономически развитых стра-
нах, испытывающих все возрастающее напряжение психоэмоциональной
сферы. Болеют чаще мужчины во второй половине жизни.
Выделение гипертонической болезни позволило отграничить ее от симп-
томатических гипертоний, или гипертонических состоя-
ний, которые появляются вторично при многих заболеваниях нервной и эн-
докринной систем, патологии почек (почечная, или нефрогенная,
гипертония) и сосудов.
К развитию симптоматической гипертонии ведут:
1) заболевания ЦНС: энцефалит, полиомиелит на уровне стволовой части мозга, опухоли
и травмы мозга (посткоммоционная гипертония);
2) заболевания эндокринной системы: опухоли надпочечников (феохромоцитома, альдосте-
рома, кортикостерома), параганглиев (параганглиома) и гипофиза (базофильная аденома); эндо-
кринно-сексуальная гипертония (климактерический период у женщин и мужчин);
3) заболевания почек и мочевыводящих путей (почечная, или нефрогенная, гипертония): гло-
мерулонефриты, пиелонефрит, гидронефроз, нефросклероз, диабетическая и печеночная нефропа-
тия, амилридоз почек, врожденные аномалии, поликистоз почек;
4) заболевания сосудов: атеросклероз дуги и коарктация аорты на разных уровнях, сужение
крупных артерий (подключичной, сонной), системный васкулит; сужение и аномалии почечных
артерий (реноваскулярная гипертония).
Этиология. В возникновении гипертонической болезни, помимо психоэмо-
ционального перенапряжения, ведущего к нарушениям высшей нервной
деятельности типа невроза и расстройству регуляции сосудистого тонуса
(Г. Ф. Ланг, А. Л. Мясников), велика роль наследственного фактора и избыт-
ка поваренной соли в пище.
Патогенез. Изучены лишь отдельные звенья механизма развития гиперто-
нической болезни. Считают, что психоэмоциональное перенапряжение (не-
рвный фактор) ведет к истощению центров сосудистой регуляции с вовлече-
нием в патогенетический механизм рефлекторных и гуморальных факторов.
Среди рефлекторных факторов следует учитывать возможное выклю-
чение депрессорных влияний каротидного синуса и дуги аорты, а также акти-
вацию симпатической нервной системы. Среди гормональных фак-
торов имеют значение усиление прессорных влияний гипофизарно-диэнце-
фальной области (гиперплазия клеток задней и передней долей гипофиза),
избыточное выделение катехоламинов (гиперплазия мозгового вещества над-
почечников) и активация ренин-гипертензиновой системы в результате нара-
стающей ишемии почек (гиперплазия и гипергранулярность клеток юкстагло-
мерулярного аппарата, атрофия интерстициальных клеток мозгового веще-
ства почек).
Почечному фактору в патогенезе гипертонической болезни придает-
ся исключительное значение, так как экскреция почками натрия и воды, секреция
ими ренина, кининов и простогландинов — один из основных механизмов ре-
гуляции артериального давления. В связи с этим следует сказать, что патоге-
нетические механизмы гипертонической болезни разные в зависимости от ак-
тивности прессорных систем: при высокой активности ренина в плазме
крови наклонность к спазмам артериол резко выражена (вазоконстрик-
торная гипертония); при низкой активности ренина отмечается увеличе-
ние массы циркулирующей крови, что служит, вероятно, основной причиной
повышения артериального давления (гиперволемическая гиперто-
н и я). Уровень артериального давления определяется активностью не только
прессорных, но и депрессорных систем, в том числе кининовой и про-
сгогландиновой систем почек, принимающих участие в экскреции натрия
и воды.
Со временем с помощью гуморальных факторов замыкается порочный
круг при гипертонической болезни: сужение почечных артерий
(вазоконстрикция, артериолосклероз) — гиперсекреция ренина — усиленное
образование ангиотензина — гиперсекреция альдостерона — задержка натрия (в
том числе в стенках артериол) — повышение чувствительности стенок арте-
риол к прессорным факторам — сужение артериол (вазоконстрикция, гиали-
ноз). Показано, что экскреторные и инкреторные функции почек, регулирую-
щие уровень аотериального давления, могут быть детерминированы генетиче-
ски. В эксперименте получены линии животных со «спонтанной» артериаль-
ной гипертонией, в основе которой лежат дефекты экскреторной и других
функций ночек.
В последние годы появилась концепция, согласно которой первичным звеном в генезе эссен-
циальной гипертензии является генетический дефект клеточных мембран в отношении регуляции
распределения внутриклеточного кальция (Ю. В. Постнов), что ведет к включению почечного
фактора.
Патологическая анатомия. Морфологические изменения при гипертониче-
ской болезни отличаются большим разнообразием, отражающим длитель-
Рис. 204. Спазм артериолы при гипертонической болезни.
Электронограмма: просвет сосуда (Пр) сужен; эндотелиальные клетки (Эн) плотно прижаты друг
к другу, межэндотелиальные пространства не выявляются; базальная мембрана (БМ) гофрирована
и расщеплена, внутренняя эластическая мембрана (ЭМ) фрагментирована. ГМК — гладкомышечная
клетка, х 16000 (по Спиро и др.).
Рис. 205. Фибриноидный некроз стенки приводящей артериолы и капиллярных петель
клубочка почки (участки некроза черные).
ность и характер ее течения. Учитывая длительность, характер развития бо-
лезни различают три стадии: 1) доклиническую («функциональную»);
2) распространенных изменений артерий; 3) изменений ор-
ганов в связи с изменением артерий и нарушением вну-
триорганного кровообращения. Морфологические различия этих
стадий отчетливо выражены лишь при доброкачественном (медленном) тече-
нии болезни (доброкачественная гипертония). При злокачествен-
ном (быстром) течении (злокачественная гипертония) они стерты.
Это связано с тем, что при злокачественной гипертонии доминируют морфо-
логические проявления гипертонического криза, т. е. резкого повышения арте-
риального давления в связи со спазмом артериол. Морфологические проявле-
ния гипертонического криза достаточно характерны и проявляются гофри-
рованностью и деструкцией базальной мембраны эндотелия и свое-
образным расположением его в виде частогола, что является выражением
спазма артериолы (рис. 204), плазматическим пропитыва-
нием или фибриноидным некрозом ее стенки (рис. 205) и присоеди-
няющимся тромбозом.
В настоящее время злокачественная гипертония встречается редко, пре-
обладает доброкачественно и медленно текущая гипертоническая болезнь. Од-
нако и при доброкачественной гипертонии в любой стадии ее разви-
тия может возникнуть гипертонический криз, что нивелирует
морфологические проявления этой стадии.
1. О доклинической стадии и гипертонической болезни говорят в
тех случаях, когда появляются эпизоды временного повышения артериаль-
Рис. 206. Плазматическое пропиты-
вание мелкой артерии головного
мозга, образование микроанев-
ризмы.
ного давления (транзиторная
гипертония). В этой стадии
находят гипертрофию
мышечного слоя и
эластических струк-
тур артериол и мелких
артерий, морфологические
признаки спазма арте-
риол или более глубокие
их изменения в случаях
гипертонического криза. От-
мечается компенсатор-
ная гипертрофия ле-
вого желудочка сердца.
2. Стадия распространенных изменений артерий характе-
ризует период стойкого повышения артериального давления. В арте-
риолах, артериях эластического, мышечно-эластического и мышечного типов,
а также в сердце возникают характерные изменения.
Изменения ар тер и о л — наиболее типичный признак гипертониче-
ской болезни — выражаются в повышенной сосудистой проницаемости —
плазматическом пропитывании и его исходе — гиалинозе, или артериолоскле-
розе.
Плазматическое пропитывание артериол и мелких артерий
(рис. 206) развивается в связи с гипоксическим повреждением эндотелия, его
мембраны, мышечных клеток и волокнистых структур стенки, к которому ве-
дет спазм сосуда. При резком повреждении элементы стенки артериолы под-
вергаются некрозу и некротические массы пропитываются белками, в том
числе фибрином. Развиваются изменения, которые идентичны ф и б р и -
ноидному набуханию (фибриноидному некрозу). Наряду
с белками стенка сосуда пропитывается липидами, В-липопротеидами, содер-
жание которых в крови при гипертонической болезни повышено. Элементы
деструкции стенки, как и пропитывающие ее белки и липиды, резорбируют-
ся с помощью макрофагов. Однако эта резорбция, как правило, неполная.
Оставшиеся белковые массы уплотняются, превращаются в гиалиноподобные.
Они расщепляют и отодвигают кнаружи эластические мембраны и резко су-
живают просвет сосуда. Развивается гиалиноз артериол, или а р т е р и о -
лосклероз (рис. 207). Аналогичные изменения появляются в мелких ар-
териях мышечного типа.
Наиболее часто плазматическому пропитыванию и гиалинозу подвергают-
ся артериолы и мелкие артерии почек, головного мозга, поджелудочной же-
лезы, кишечника, сетчатки глаза, капсулы надпочечников. Во время гиперто-
нического криза плазматическое пропитывание артериол, артериолонекроз
и геморрагии доминируют в каком-либо одном органе, что определяет клини-
ческую специфику криза (артериолонекроз почек, ведущий к острой почечной
недостаточности, плазматическое пропитывание артериол и диапедезные кро-
воизлияния в дне IV желудочка, что ведет к внезапной смерти и т. д.).
Изменения артерий эластического, мышечно-эластиче-
ского и мышечного типов представлены эластофиброзом и атероскле-
розом.
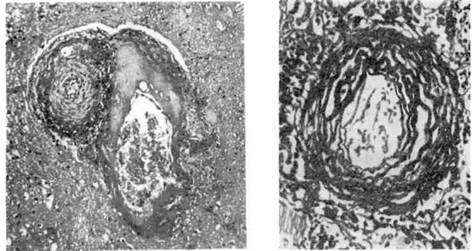
Рис. 207. Гиалиноз артериол головного мозга.
Рис. 208. Гиперплазия и расщепление эластических мембран мелкой артерии почки.
Э л ас то фиброз характеризуется гиперплазией и расщепле-
нием внутренней эластической мембраны, развивающимися компенсаторно
в ответ на стойкое повышение артериального давления, и разрастанием
между расщепившимися мембранами соединительной ткани, т. е. склеро-
зом (рис. 208). При стойкой и длительной артериальной гипертонии разви-
вается выраженный атеросклероз, который отличается некоторым своео-

Рис. 209. Гипертрофия миокарда левого желудочка сердца при гипертонической болезни
(поперечный разрез).
Рис. 210. Кардиосклероз при гипертонической болезни.
бразием. Во-первых, при артериальной гипертонии атеросклеротические
изменения имеют более распространенный характер, «спускаясь»
в артерии мышечного типа, чего не наблюдается при отсутствии гипертонии.
Во-вторых, при гипертонии фиброзные бляшки располагаются циркуляр-
н о, а не сегментарно, что ведет к более резкому сужению просвета сосуда.
Эластофиброз и стенозирующий атеросклероз резко выражены в артериях
сердца, мозга, почек, поджелудочной железы, в сонных и позвоночных арте-
риях. В этой стадии степень гипертрофии миокарда нарастает, масса
сердца достигает 900—1000 г, а толщина стенки левого желудочка — 2 — 3 см
(рис. 209).
В связи со стенозирующим атеросклерозом венечных артерий возникает
гипоксия миокарда, которая ведет к развитию дистрофических и н е -
кробиотических изменений мышечных волокон и миогенному
расширению полостей гипертрофированного сердца (эксцентриче-
ская гипертрофия миокарда).
Нарастающая гипоксия миокарда и усиленная его работа обусловливают
появление изменений в интрамуральной нервной системе серд-
ца, в нервных клетках ганглиев наблюдаются хроматолиз, пикноз, эктопия
и сморщивание ядер, гибель клеток, а в нервных волокнах — варикозные утол-
щения, огрубение, глыбчатый распад.
В условиях кислородного голодания и усиливающихся нарушений трофики
миокарда вследствие патологии интрамуральной нервной системы сердца раз-
вивается диффузный мелкоочаговый кардиосклероз (гипер-
тонический кардиосклероз; рис. 210;.
3. Последнюю стадию гипертонической болезни характеризуют вто-
ричные изменения органов в связи с изменением артерий
и нарушением внутриорганного кровообращения. Эти вто-
ричные изменения могут появляться катастрофически быстро на по-
чве спазма, тромбоза сосуда, завершающего плазматическое пропитывание
или фибриноидный некроз его стенки. Тогда они проявляются кровоиз-
лияниями и циркуляторными некрозами, или инфарктами.
Вторичные изменения органов могут развиваться и медленно на почве ар-
териоло- и атеросклеротической окклюзии сосудов, что ведет к атрофии
паренхимы и склерозу органов.
КЛИНИКО-МОРФОЛОГИЧЕСКИЕ ФОРМЫ
На основании преобладания сосудистых, геморрагических, некротических
и склеротических изменений в сердце, мозге, почках при гипертонической бо-
лезни выделяют сердечную, мозговую и почечную клинико-морфологические
ее формы.
1. Сердечнаяформагипертоническойболезни, как и сердеч-
ная форма атеросклероза, составляет сущность ишемической болезни
сердца.
2. Мозговая форма гипертонической болезни проявляется
прежде всего различными видами нарушения мозгового кровообращения. Ча-
ще встречаются кровоизлияния в мозг — как мелкие диапедезные,
так и обширные, с развитием гематомы (геморрагический ин-
сульт; рис. 211), реже — ише мические инфаркты (ишемический
инсульт). Возникновению обширных кровоизлияний предшествуют спазм
артериод, плазматическое пропитывание их стенок, изменения тонуса капил-
ляров, появление мелких периваскулярных геморрагии. Эти расстройства кро-
вообращения в мозге возникают обычно во время очередного криза гиперто-
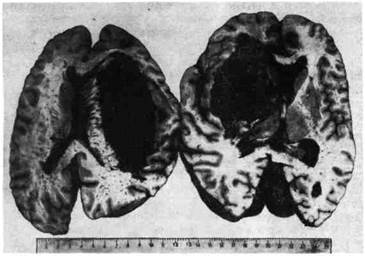
Рис. 211. Кровоизлияние в головной мозг с прорывом в боковые желудочки (гемор-
рагический инсульт).
нической болезни и соответствуют клинике так называемого предынсультного
состояния. Оно может прекратиться, оставив лишь следы в виде периваску-
лярных отложений гемосидерина. Если же гипертонический криз затягивается,
альтеративные изменения стенок артериол и мелких артерий завершаются раз-
рывом эластических мембран, что ведет к образованию микроаневризм
(см. рис. 206), их разрыву и образованию гематомы.
В месте кровоизлияния ткань мозга разрушается, образуется полость, за-
полненная свертками крови и размягченной тканью мозга (красное раз-
мягчениемозга). Кровоизлияние локализуется чаще всего в подкорковых
узлах головного мозга (зрительный бугор, внутренняя капсула) и мозжечка.
Размеры его бывают разными: иногда оно охватывает всю массу подкор-
ковых узлов, кровь прорывается в боковые, III и IV желудочки мозга, проса-
чивается в область его основания (см. рис. 211). Инсульты с прорывом в же-
лудочки мозга всегда заканчиваются смертью. Если больной переживает
инсульт, то по периферии кровоизлияния в ткани мозга появляется много си-
дерофагов, зернистых шаров, клеток глии и свертки крови рассасываются. На
месте гематомы образуется киста с ржавыми стенками и буроватым содер-
жимым. У больных, длительно страдавших мозговой формой гипертониче-
ской болезни и умерших от инсульта, наряду со свежими кровоизлияниями
нередко находят кисты как следствие бывших ранее геморрагии.
Ишемические инфаркты мозга, образующиеся при тромбозе ате-
росклеротически измененных артерий, имеют ту же локализацию и те же ис-
ходы, что и кровоизлияния.
Помимо острых нарушений мозгового кровообращения, в ткани головно-
го мозга (особенно во II и III слоях коры) и продолговатого мозга (соматиче-
ских и вегетативных его ядрах) развиваются гипоксические измене-
ния в виде дистрофии и некроза нейронов с пролиферацией в очагах
опустошения клеток глиальных элементов. Сходные изменения встречаются
в узлах вегетативной нервной системы, в нервных волокнах, их окончаниях
в рефлексогенной зоне дуги аорты и каротидном синусе.
3. Почечная форма гипертонической болезни характе-
ризуется как острыми, так и хроническими изменениями.
Рис. 212. Гиалиноз артериолы
клубочка, коллапс капиллярных
петель, склероз капсулы.
К острым изме-
нениям относятся ин-
фаркты почек и артерио-
лонекроз почек.
Инфаркты почек
появляются при тромбо-
эмболии или тромбозе ар-
терий. Иногда они быва-
ют субтотальными или то-
тальными. А р т е р и о-
лонекроз почек —
морфологическое выра-
жение злокачественной ги-
пертонии. Помимо артериол, фибриноидному некрозу подвергаются капилляр-
ные петли клубочков (см. рис. 205), в строме возникают отек и геморрагии, в эпи-
телии канальцев — белковая дистрофия. В ответ на некроз в артерио-
лах, клубочках и строме развиваются клеточная реакция и склероз (злока-
чественный нефросклероз Фара). Почки выглядят несколько умень-
шенными в размерах, пестрыми, поверхность их мелкогранулярная. Артерио-
лонекроз приводит к острой почечной недостаточности и заканчивается
обычно летально при отсутствии возможности проведения гемодиа-
лиза.
Изменения почек, свойственные хроническому доброкачественному тече-
нию гипертонической болезни, связаны с гиалинозом артериол, ар-
териолосклерозом (рис. 212). Гиалиноз артериол сопровождается кол-
лапсом капиллярных петель и гиалинозом клубочков (гломерулогиали-
ноз), что ведет к деструкции капилляров, питающих канальцы. В результате
недостаточного кровоснабжения и гипоксии канальцевая часть большинства
нефронов атрофируется и замещается соединительной тканью, которая разра-
стается также вокруг погибших клубочков. На поверхности ночек появляются
множественные мелкие очаги западения. Нефроны, соответствующие относи-
тельно сохранным клубочкам, гипертрофируются (регенерационная
гипертрофияпочек)и выступают над почечной поверхностью в виде се-
ро-красных гранул. Почки выглядят маленькими, плотными, поверхность их
мелкогранулярная, паренхима атрофична, особенно истончено корковое веще-
ство. Такие почки, являющиеся исходом их склероза на почве гиалиноза арте-
риол (артериолосклеротический нефросклероз), называют
первично-сморщенны ми (рис. 213). Клиническое выражение артерио-
лосклеротического нефросклероза — это хроническая почечная недо-
статочность, завершающаяся азотемической у р е м и ей.
Изменение глаз при гипертонической болезни вторичное, связанное с ха-
рактерными изменениями сосудов. Они представлены отеком соска зритель-
ного нерва, кровоизлияниями, отслойкой сетчатки, белковым выпотом и от-
ложением в ней белковых масс, некрозом сетчатки и тяжелыми дистрофиче-
скими изменениями нервных клеток ганглиозного слоя.
Изменения эндокринных желез: в надпочечниках происходит
гиперплазия мозгового и коркового слоев с образованием в последнем регене-
раторных аденом. В дальнейшем эти изменения сменяются атрофическими.
В передней доле гипофиза отмечается гиперплазия базофильных клеток,

Рис. 213. Первично-сморщенная почка. Вид с поверхности (а) и на разрезе (б).
как и клеток задней доли, выделяющих вазопрессорные вещества. В других
органах нередко возникают изменения, служащие проявлением гипертони-
ческих кризов или следствием хронической недостаточности питания их
кровью и гипоксии.
Дата добавления: 2015-11-26 | Просмотры: 1449 | Нарушение авторских прав
|















