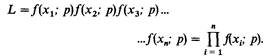|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Практические аспекты генетики человека 177Более того, можно предсказать, что если генная терапия достигнет успеха в обозримом будущем, то это произойдет скорее всего в отношении некоторых дефектов ферментных систем. Воспроизведение аномальных зигот, однако, ведет лишь к очень медленному увеличению частоты вредных генов (разд. 6.2.1.2). Увеличения частоты рецессивных заболеваний можно не бояться еще и по другой причине, в настоящее время большинство популяций не находятся в равновесии по рецессивным генам. Разрушение изоляции и резкое уменьшение числа близкородственных браков создали ситуацию, в которой общее число гомозигот намного ниже расчетного равновесного значения. В отсутствие других факторов, которые могли бы изменить известные преимущества гетерозигот в плане отбора, эта тенденция должна привести к медленному увеличению числа гомозигот через сотни будущих поколений (разд. 6.3.1.2) Поскольку 100 поколений соответствуют периоду времени в 2500-3000 лет, нет нужды волноваться по этому поводу уже теперь. За такой долгий период времени условия жизни могут измениться совершенно непредсказуемым образом. Таким образом, в популяциях индустриальных стран Европы и в США, где браки заключаются случайным образом, можно ожидать очень медленного увеличения частоты рецессивных заболеваний по сравнению с современным уровнем. Однако это предсказание не принимает в расчет искусственного отбора, осуществляемого путем генетического консультирования, пренатальной диагностики и, возможно, реализации скрининговых программ для гетерозигот Если пренатальная диагностика станет обычной процедурой, то в программу скрининга можно будет, вероятно, включить самые частые рецессивные заболевания, например ß-талассемию для населения средиземноморского бассейна и юго-восточной Азии или кистозно-фиброзную дегенерацию для населения СевероЗападной Европы и белого населения Северной Америки. Более редкие дефекты включить в скрининг вряд ли удастся. Совокупность всех данных по четко определенным генетическим аномалиям, та- ким, как хромосомные аберрации, доминантные и Х-сцепленные болезни и аутосомно-рецессивные заболевания, позволяет нам с достаточной уверенностью предсказать, что современная цивилизация не вызовет существенного увеличения частоты этих аномалий. Будет ли вообще увеличиваться эта частота, останется на близком к современному уровне или даже снизится - это в значительной степени зависит от обстоятельств жизни нашего общества. Сможем ли мы сохранить в разумных пределах воздействие мутагенных факторов, о чем говорилось выше? Насколько эффективно в плане уменьшения наследственных заболеваний будет работать искусственный отбор в форме генетического консультирования и пренатальной диагностики? И еще одно обстоятельство - как долго общество будет проявлять готовность платить за «роскошь» разработки планов предотвращения и лечения редких заболеваний? В настоящее время мы не можем сделать сколько-нибудь точных предсказаний. Постепенная утрата функций, которые обеспечиваются мулътифакториалъными генетическими системами. В популяции существует изменчивость не только для четко определенных генетических дефектов, о которых шла речь до сих пор, но и для функциональных систем, которые зависят от сложного, но упорядоченного взаимодействия различных генов в период эмбрионального развития. Сердце, глаза и иммунная система являются примерами таких систем. Эволюционно эти системы развивались под постоянным и интенсивным давлением отбора. Как только это давление снижается, начинают накапливаться мутации, которые приводят к небольшим функциональным недостаткам, и в течение очень долгих эволюционных периодов эти системы медленно, но неуклонно «отмирают». У животных самые известные примеры обнаружены среди видов, которые в течение многих поколений жили в полной темноте пещер или на больших глубинах океана, где интактная зрительная система не дает никаких преимуществ в плане отбора. Как правило, сначала увеличивается изменчивость глаз, особи с небольшими 178 9. Практические аспекты генетики человека дефектами начинают встречаться все чаще. Затем у большинства животных глаза оказываются больше или меньше поврежденными, и, наконец, возникает безглазый вид. В цивилизованном обществе небольшие дефекты зрительной системы не ставят их носителей в невыгодное положение перед отбором. Это уже привело к значительному увеличению изменчивости в зрительной активности: такие состояния, как близорукость, дальнозоркость или астигматизм, встречаются, вероятно, чаще, чем в примитивных популяциях, которые до недавнего времени жили в условиях сурового отбора (разд. 7.2.5). Будет ли этот процесс развиваться в том же направлении? С такой тенденцией можно было бы смириться - просто будет больше людей, которые носят очки. Их «дефект» обеспечивает средства к существованию людям других профессий - офтальмологам и оптикам - и создает производство по изготовлению очков. Более опасные последствия может иметь медленное повреждение иммунной системы. В разд. 6.2.1.6 говорилось о высокой смертности среди младенцев и детей до недавнего времени, которая обусловлена главным образом инфекционными заболеваниями. Сложная система обнаружения и уничтожения инфекционных агентов эволюционировала под влиянием сильного отбора (разд. 4.4). Нам известно множество генетических дефектов, которые снижают эффективность этой системы. Раньше такие дефекты приводили, как правило, к смерти индивида от инфекции; теперь при наличии антибиотиков многие из этих пациентов выживают и дают потомство. При крайне тяжелых случаях поражения иммунной системы можно надеяться на терапию с помощью пересадки костного мозга, при которой в организм вводятся нормально функционирующие иммунные клетки. Однако мутации могут вызывать намного более тонкие изменения в белковых молекулах, которые лишь незначительно ослабляют их функцию. Исследования молекулы гемоглобина показали, что такие мутации встречаются очень часто. Приведет ли ослабление отбора против таких вариантов к медленному повреждению всей системы? Будут ли наши потомки постепенно стано- виться все более чувствительными к инфекции разного рода, с которой нужно будет бороться с помощью более сложного сочетания антибиотиков и иммунной терапии? И еще более важный вопрос - будет ли это повреждение иммунной системы увеличивать частоту различных типов рака, поскольку потенциально злокачественные клоны клеток удерживаются от пролиферации системами иммунного надзора. Ослабление отбора против мультифакториальных признаков может привести к увеличению их частоты. Например, против расщелины нёба и заячьей губы в прошлом был направлен довольно сильный отбор. В настоящее время вследствие эффективного хирургического лечения такие дети без труда выживают и в будущем имеют детей. Вполне вероятно, следовательно, что частота этого признака в следующих нескольких поколениях возрастет. Точную степень этого увеличения трудно предсказать. Аналогичные рассуждения применимы к врожденным порокам сердца. Будет ли увеличиваться число лиц со сниженным интеллектом? Как отмечалось выше, сознательное планирование семьи является одним из основных факторов, который следует принимать в расчет при любой оценке. Этот фактор, однако, может иметь как благоприятные, так и неблагоприятные последствия. В популяциях существует подгруппа со сниженной способностью планировать свое собственное будущее - группа лиц с легкой степенью умственной отсталости. Средняя величина их воспроизведения действительно превышает среднее значение для популяции. Хотя хорошо известно, что факторы внешней среды могут способствовать возникновению умственной отсталости, есть данные о том, что для групп со слабой степенью отсталости особое значение имеет генетическая изменчивость (разд. 8.2.1.2). Следовательно, постоянное, более высокое воспроизведение лиц со слабой умственной отсталостью может увеличить их частоту в популяции. Пенроуз [2157] подверг сомнению справедливость этого заключения на том основании, что в семьях с легкой степенью умственной отсталости обычно выделяется определенная 9. Практические аспекты генетики человека 179 доля лиц, страдающих более тяжелой формой отсталости, которые вообще не способны иметь детей. Это противодействие может удерживать частоту генов на низком уровне, несмотря даже на более высокое воспроизведение состоящих в браке умственно отсталых лиц. Всесторонние исследования, проведенные супругами Рид [167] в 1965 г., казалось бы, подкрепили этот довод; число неженатых и незамужних, бездетных умственно отсталых членов семьи действительно было повышено в семьях со сниженным интеллектом. Мы, однако, не можем быть уверены в том, будет ли эта компенсация достаточна в будущем; слишком многое зависит от непредсказуемых социальных условий-умственно отсталые женщины могут научиться регулярно принимать противозачаточные таблетки и в этом отношении могут быть даже более надежны, чем женщины со средним или выше среднего уровнем умственного развития. Возможно все же, что число генов умственной отсталости будет увеличиваться, и хотя число умственно отсталых лиц может возрасти, средние способности остальной части популяции не изменятся. Интеллектуальное сходство является серьезным фактором при подборе супружеских пар, и его действие распространяется как на нормальных, так и в особенности на умственно отсталых лиц. Эта тенденция может породить ряд социальных проблем, поскольку современное общество с его возрастающими требованиями к техническому мастерству будет все меньше обеспечивать работой умственно отсталых лиц. Благоприятная в плане отбора тенденция: сочетание генетической приспособленности с последствиями, неблагоприятными в других отношениях. До сих пор мы рассматривали преимущественно неблагоприятные тенденции, и единственным полезным направлением был искусственный отбор, осуществляемый с помощью генетического консультирования. Ниже будет рассмотрена другая благоприятная тенденция, которая, вероятно, сможет намного быстрее усовершенствовать генетическую структуру, чем большинство неблагоприятных тен- денций вызвать ее повреждение. В тропических странах широко распространены некоторые аномалии и заболевания эритроцитов, несмотря на то что гомозиготы по этим признакам страдают тяжелыми за-
180 9. Практические аспекты генетики человека болеваниями крови типа серповидноклеточной анемии или талассемии (разд. 4.3). Гетерозиготы по соответствующим генам имеют преимущества в плане отбора по отношению к трехдневной малярии, которая для этих областей до недавних пор была эндемичным заболеванием (разд. 6.2.1.6). До тех пор пока малярия не появится снова в будущем, отбор против пораженных дефектом гомозигот будет уменьшать частоту генов. Природа в этом случае предложила компромисс: увеличение устойчивости против малярии должно быть оплачено ценой многих случаев наследственных заболеваний. Как только малярию искоренили, этот компромисс стал ненужным, и вредный ген постепенно исчезает (разд. 6.2.1.6). Сходный механизм может существовать для групп крови А, В и О (разд. 6.2.1.8). Возможно, что этот генетический полиморфизм возник как приспособление к многочисленным и разнообразным инфекционным агентам и что отбор зависел от их частоты. Ценой, которую следовало заплатить, была утрата зигот, обусловленная серологической несовместимостью матери и ребенка. Если бы отбор, связанный с инфекцией, исчез и остался бы только отбор по несовместимости, произошло бы постепенное и медленное уничто- жение редких аллелей А и В и закрепление самой частой группы - 0. Сходные «компромиссы» могут также существовать для других генетических систем. Человеческий вид в будущем. Из этих рассуждений возникает следующая картина будущей генетической структуры человека как вида: общий состав генов будет похож на тот, который существует в настоящее время. Сохранится, вероятно, тенденция к уменьшению расовых и этнических различий. Генетические дефекты, возможно, будут встречаться чаще или реже, чем в настоящее время, но они будут находиться под эффективным контролем генетического консультирования и пренатальной диагностики. Могут стать редкостью люди с аутосомными аберрациями. Вследствие терапевтического и хирургического лечения и других факторов, ведущих к ослаблению отбора, увеличится, вероятно, число заболеваний, вызываемых полигенными факторами. К сожалению, степень этого увеличения точно оценить невозможно из-за отсутствия знаний о конкретных генетических системах подверженности при этих заболеваниях. В табл. 9.9 сопоставлены благоприятные и неблагоприятные тенденции в развитии генетической структуры будущих популяций. Приложение 1 Методы подсчета генных частот
Приложение 1
Приложение 1 183
Приложение 1 методом Бернштейна это дает следующие результаты (подробнее в разд. 3.2.2): p = 0,287685 + 0,002411, q = 0,106555 ±0,001545, r = 0,605760 ±0,002601. Было показано, что метод максимального правдоподобия приводит к точно таким же результатам [711]. Дисперсии по методу максимального правдоподобия получились следующими: Vp = 0,000005811, Vq = 0,000002386, Vr = 0,000006763. Для получения стандартных отклонений нужно извлечь квадратные корни из этих дисперсий. Точно так же, как было показано для групп крови MN, по частоте аллелей А, В и О можно вычислить ожидаемые генотипические частоты и сравнить их с наблюдаемыми частотами по критерию хи-квадрат. Еще более сложные проблемы возникают при анализе групп крови Rh и вообще при анализе всех систем, в которых вместе наследуется много разных комбинаций антигенов. Для этих случаев опубликованы или упомянуты в публикациях компьютерные программы. Для системы Rh можно воспользоваться публикациями [585; 586]. Рядом авторов предложены правила вычисления частот аллелей и гаплотипов для системы HLA [554; 738; 779; 805; 962]. Находит свое применение также система ALLTYPE [789]. Однако неадекватность составления выборки не компенсируется обработкой на компьютере. Все упомянутые до сих пор методы основаны на предположении, что выбор индивидов проводился независимо, т.е. выбор какого-либо одного индивида не увеличивает и не уменьшает шанс быть выбранным для любого другого индивида в популяции. Это правило нарушается, например, при сборе данных о родственниках. Однако нельзя сказать, что выборки, содержащие родственников, всегда бесполезны для вычисления генных частот. Но включение родственников в выборку должно быть обязательно отмечено вместе со степенью их родства, и для анализа должны использоваться специальные статистические методы [211]. Приложение 2 Анализ сегрегации распространенных признаков: отсутствие смещений вследствие регистрации, доминирование [876; 877]
186 Приложение 2
|
При использовании материала ссылка на сайт medlec.org обязательна! (0.321 сек.) |