 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
ГЛАВА 10. СОСУДИСТЫЕ ЗАБОЛЕВАНИЯ НЕРВНОЙ СИСТЕМЫ. Мозговой инсульт, или острое нарушение мозгового кровообращения, приводящее к появлению стойкой неврологической симптоматикиМозговой инсульт1 Мозговой инсульт, или острое нарушение мозгового кровообращения, приводящее к появлению стойкой неврологической симптоматики, встречается с частотой 400-500 на 100 тыс. населения в год и является одной из основных причин смерти. Летальность при инсульте - примерно 25%, еще около 20% перенесших инсульт умирают в течение года и примерно 25% больных остаются тяжелыми инвалидами. Выделяют ишемический и геморрагический инсульт; большинство (80-85%) инсультов - ишемические. Ишемический инсульт Ишемическим инсультом называют инфаркт участка мозга, развившийся вследствие снижения или прекращения притока к нему крови. Нормальная величина мозгового кровотока - 70- 80 мл крови, протекающие через 100 г вещества мозга в 1 мин. Умеренное снижение мозгового кровотока клинически отчетливо не проявляется. При снижении перфузии ниже 35 мл/100 г/мин нарушается функция клеток мозга, при снижении перфузии ниже 15 мл/100 г/мин возникают необратимые структурные изменения мозговой ткани - ишемический инфаркт мозга. Мозг в бассейне пораженного сосуда страдает неравномерно: если в центральных отделах очага мозговой кровоток часто бывает ниже критических 15 мл на 100 г мозгового вещества в минуту, и развивается инфаркт мозга, то на его периферии за счет коллатерального кровоснабжения формируется так называемая область «ишемической полутени». 1 Подробнее вопросы клиники, диагностики и консервативного лечения данной патологии освещены в гл. 10, том 1. По этиологии большинство (свыше 50%) ишемических инсультов являются атеросклеротическими и развиваются при атеросклеротическом поражении дуги аорты и магистральных артерий головы и шеи. Следующей по частоте является группа заболеваний или состояний, приводящих к тромбообразованию в полостях сердца (фибрилляция предсердий, эндокардит, порок или протез сердечного клапана, аневризма сердца, дилатационная кардиомиопатия и др.), такие инсульты: назыгвают кардиогенныши. Следует выделить так называемую парадоксальную тромбоэмболию мозговых сосудов, встречающуюся при незаращении межжелудочковой перегородки: этот этиологический фактор обусловливает значительное число ишемических инсультов у лиц молодого возраста. Нередко, примерно в 20% случаев, ишемический инсульт обусловлен патологией мелких интрацеребральных сосудов, развивающейся при гипертонической болезни или системных васкулитах. Наконец, к ишемическому инсульту может приводить ряд редких заболеваний (коагулопатии, антифосфолипидный синдром, эритремия и др.). Патогенез большинства ишемических инсультов - эмболия мозгового сосуда атероматозными массами или тромбами, образующимися на изъязвленныгх («эмбологенных») атеросклеротических бляшках и в полости левого предсердия. Примерно в 15% случаев развитие ишемического инсульта обусловлено не эмболией, а сужением просвета кровоснабжающей мозг артерии атеросклеротической бляшкой или анатомическими особенностями строения сосуда. Наконец, при коагулопатиях и некоторых других заболеваниях тромбообразование может происходить непосредственно в мозговом сосуде. Ишемический инфаркт мозга в 2-3% случаев может сопровождаться вторичными геморрагиями, но их наличие не дает оснований называть инсульт геморрагическим. Клиническая картина ишемического инсульта подробно описана в курсе неврологии. В общих чертах для ишемического инсульта характерны внезапное или достаточно быстрое (в течение часов или дней) появление тех или иных очаговых неврологических симптомов и их преобладание над общемозговыми. Выделяют 3 клинические формы ишемического инсульта: • транзиторная ишемическая атака, или преходящая ишемия мозга, - полный регресс неврологической симптоматики в течение 24 ч;
• малый инсульт - полный регресс неврологической симптоматики в течение 3 нед; • завершившийся инсульт, или собственно инсульт, - неврологический дефицит сохраняется более 3 нед. Диагностика ишемического инсульта, помимо собственно постановки диагноза и определения тактики лечения больного в остром периоде, имеет целью определить этиологию инсульта и сформулировать индивидуальную программу профилактики повторных нарушений мозгового кровообращения. Основой диагностики ишемического инсульта является КТ или МРТ головы. Исследование позволяет оценить размеры ишемического очага и исключить другие варианты внутричерепной патологии, могущие обусловить имеющуюся симптоматику. При этом (при необходимости - в динамике) оцениваются выраженность отека мозга и степень его дислокации, что важно для коррекции лечения (рис. 10.1). Далее, помимо кардиологического, необходимо исследование брахиоцефальных и интракраниальных артерий. Состояние брахиоцефальных артерий оценивают с помощью ультразвукового дуплексного сканирования. Этот метод обладает достаточно высокой информативностью и позволяет определить уровень и степень стеноза артерии, размеры, рас- _ положение и структуру атеросклеротической бляшки (рис. 10.2). Возможно также исследование сосудов как внутричерепных, так и брахиоцефальных с помощью КТ и/или МР-ангиографии (рис. 10.3). При выявлении патологии магистральных артерий проводится более углубленное обследование, обычно - в нейрохирургической клинике (см. ниже).
Лечение ишемического инсульта - преимущественно консервативное. В остром периоде оно включает в себя базисную терапию, направленную на поддержание жизнедеятельности и гомеостаза, и дифференцированную терапию, цель которой - улучшить перфузию мозга. Последнее достигается поддержанием умеренной артериальной гипертензии и гемодилюции. Обычно назначают также средства, улучшающие реологические свойства крови (препараты низкомолекулярного гидроксиэтилкрахмала) и антикоагулянты (препараты низкомолекулярного гепарина) под контролем показателей свертываемости крови, но эффективность этих лекарственных средств в независимых исследованиях пока не подтверждена. Назначение тромболитических препаратов (рекомбинантного активатора тканевого плазминогена и др.) может быть целесообразным лишь в первые 2-3 ч тромбоэмболического инсульта. Однако при назначении тромболитиков достаточно высок риск геморрагических осложнений. Крайне важны тщательный уход за больным, профилактика тромбообразования в глубоких венах голени и обеспечение потребностей организма в питательных веществах, витаминах, микроэлементах и клетчатке. После стабилизации состояния больного формулируется индивидуальная программа реабилитации. Профилактика повторного инсульта определяется его этиологией. При возможности пытаются устранить источник эмболии (например, иссечь эмбологенную атеросклеротическую бляшку), при отсутствии такой возможности назначают препараты, пре- пятствующие тромбообразованию (например, ацетилсалициловую кислоту). Вопрос о применении «нейропротекторных» и «нейротрофических» средств остается спорным. Убедительных данных об их эффективности нет, но отсутствие осложнений и побочных эффектов при их применении позволяет некоторым авторам рекомендовать использование этих препаратов на различных этапах лечения инсульта. Подробно принципы лечения ишемического инсульта изложены в курсе неврологии. Показания к хирургическим вмешательствам возникают при: • патологии магистральных артерий головы, явившейся причиной инсульта; • выраженном ишемическом отеке мозга. Патология магистральных артерий головы, как уже говорилось, - одна из основных причин нарушений мозгового кровообращения и главная причина неэмболического ишемического инсульта. Самой распространенной причиной снижения кровотока по внутренним сонным и/или позвоночным артериям являются атеросклеротические бляшки, располагающиеся чаще в области устьев или деления артерий. Дополнительное значение имеют анатомические особенности, приводящие к ухудшению кровотока в области бляшки, - патологическая извитость сосуда, перегиб под острым углом (ангуляция) и др. Иногда патологическая деформация артерии может явиться причиной нарушения мозгового кровообращения и в отсутствие атеросклеротического процесса. В 80% случаев страдают экстракраниальные отделы кровоснабжающих головной мозг артерий, чаще - внутренних сонных (ВСА). В случае решения вопроса о хирургическом вмешательстве по поводу патологии магистральных артерий головы и шеи необходим расширенный комплекс обследования больного с ишемическим инсультом. Помимо дуплексного сканирования проводят либо компьютерно-томографическую, либо прямую ангиографию пораженной артерии. МР-ангиографию выполняют преимущественно для оценки состояния интракраниальных артерий. Для исследования функционального состояния мозгового кровообращения, в том числе коллатерального, используют транскра- ниальную допплерографию с функциональными пробами. Транскраниальная допплерография применяется также для выявления микроэмболов, поступающих в кровоток с поверхности изъязвленной, так называемой эмбологенной атеросклеротической бляшки. Показаниями к хирургическому лечению являются: • сужение просвета сосуда атеросклеротической бляшкой более чем на 70%; • наличие эмбологенной атеросклеротической бляшки меньшего размера, вызывающей неврологическую симптоматику (транзиторные ишемические атаки); • наличие патологической деформации артерии, вызывающей снижение кровотока, соответствующее 70% стенозу. Хирургические вмешательства при стенозирующих поражениях магистральных артерий головы бывают прямыми (открытыми) и внутрисосудистыми (эндовазальными). Операции обычно выполняют, когда миновал острый период инсульта; в отношении экстренных хирургических вмешательств мнения противоречивы, существенных преимуществ не выявлено, а риск достоверно увеличивается. Основными видами прямых вмешательств являются эндартерэктомия (каротидная, вертебральная), при необходимости - с вшиванием в стенку сосуда «заплаты» из аутовены или синтетического материала, и протезирование артерии аутовенозным или синтетическим трансплантатом (рис. 10.4, 10.5). При патологической деформации артерии (извитости, петлеобразовании) обычно производят иссечение деформированной части сосуда с наложением шва конец в конец (рис. 10.6). В случае плохой переносимости выключения кровотока по оперируемой ВСА или позвоночной артерии (определяемой на основании данных электрофизиологических исследований) в просвет сосуда на время его пережатия устанавливают временный шунт. Операция чаще выполняется в условиях общей анестезии, хотя у больных с тяжелой сочетанной соматической патологией может быть применено местное или регионарное обезболивание. Основные осложнения при операциях на брахиоцефальных артериях - ишемизация мозга и синдром гиперперфузии: резкое увеличение мозгового кровотока после устранения окклюзирующего поражения артерии. Профилактика ишемии обеспечивается мониторингом ЭЭГ или, при вмешательствах под местной ане-
стезией, - оценкой неврологического статуса в ходе операции. При недостаточности коллатерального кровообращения и непереносимости длительной окклюзии сонной артерии устанавливают временный обходной артериальный шунт (см. рис. 10.4). Для предупреждения синдрома гиперперфузии применяют комплекс анестезиологических мероприятий, направленных в первую очередь на контроль уровня артериального давления. Вероятность рецидивирования стеноза после эндартерэктомии - около 15%. Эндоваскулярные вмешательства при стенозах артерий заключаются в ангиопластике (расширение просвета артерии в месте сужения с помощью раздувающегося баллона), дополняемой обычно установкой в этом месте внутрипросветного стента. Перед манипуляциями дистально от атеросклеротической бляшки может быть установлен специальный сетчатый фильтр («корзина»), который улавливает могущие появиться во время ангиопластики эмболы. В конце вмешательства фильтр с эмболами удаляют. Вероятность рестеноза после ангиопластики и стентирования - около 20%. Следует иметь в виду, что в случае рестеноза после внутрипросветно-
го стентирования артерии единственной возможностью решения проблемы является протезирование сосуда. При полном тромбозе ВСА предложена операция экстраинтракраниального сосудистого анастомоза - наложение соустья между ветвями поверхностной височной и средней мозговой артерий. Статистических доказательств эффективности такой операции нет. При выраженном ишемическом отеке головного мозга, приводящем к дислокации мозга в отверстие намета мозжечка и появлению соответствующих симптомов, прогрессивном ухудшении состояния больного и неэффективности консервативных способов контроля отека мозга (подбор параметров ИВЛ, осмотические диуретики) возможно выполнение декомпрессивной трепанации черепа на стороне инсульта. Операция проводится под наркозом. Сутью ее является формирование большого трепанационного окна в лобно-теменно-височной области. Удаленный костный лоскут в стерильных условиях упаковывается и хранится в низкотемпературной морозильной камере; когда минует острый период инсульта - обычно через 2-3 нед - лоскут может быть установлен на свое место в ходе повторной операции. Для декомпрессии мозга производят широкий разрез ТМО и герметично подшивают к его краям лоскут надкостницы, покрывавшей удаленный костный лоскут. Такая декомпрессия снижает риск вторичных нарушений кровообращения, в том числе в стволе мозга, и несколько улучшает исходы тяжелых ишемических инсультов. Геморрагический инсульт По сути геморрагическим инсультом может называться любое спонтанное внутричерепное кровоизлияние. Однако, основываясь на этиологическом принципе, из числа геморрагических инсультов исключают группу спонтанных субарахноидальных кровоизлияний, рассматриваемых отдельно (см. ниже). Соответственно к собственно геморрагическим инсультам относят кровоизлияния, не вызванные пороком развития сосудов и обычно локализованные в веществе головного мозга. Геморрагическими являются примерно 10% всех инсультов, летальность при них превышает 60%, к прежней социально-трудовой активности возвращается не более 20% выживших. Вероятность геморрагического инсульта нелинейно увеличивается с возрастом и для лиц старше 70 лет составляет 7%. Геморра- гический инсульт поражает преимущественно мужчин. Основными этиологическими факторами являются. • Артериальная гипертензия любого, но чаще - атеросклеротического генеза (65-70% случаев); • Хронический алкоголизм (риск геморрагического инсульта при алкоголизме возрастает примерно в 7 раз, но истинную значимость этого фактора оценить трудно по причине частого сочетания с артериальной гипертензией); • Негероиновая наркомания (амфетамины, кокаин, фенциклидин); • Артериопатии: о амилоидная (или «конгофильная») ангиопатия; является причиной примерно 10% геморрагических инсультов; морфологически характеризуется отложением амилоида (зеленое свечение в поляризованном свете после окраски конго красным) в медии мелких артерий и артериол белого вещества, иногда - в сочетании с фибриноидным некрозом сосудистой стенки, без признаков системного амилоидоза; встречается преимущественно у лиц старше 70 лет и у больных с синдромом Дауна; возможна связь с болезнью Альцгеймера (амилоид идентичен); этиология неясна, возможна генетическая предрасположенность; кровоизлияние обычно локализуется в 1 доле мозга, часто рецидивирует; прижизненный диагноз крайне затруднен, поскольку невозможен без гистологической верификации; о липогиалиноз (отложение гиалина и липидов под интимой сосудов, встречается редко); о артериит мозговых сосудов, включая некротизирующий ангиит (встречается редко); о нарушения свертываемости крови или агрегации тромбоцитов; о ятрогенные (антикоагулянтная или тромболитическая терапия, в меньшей степени - систематический прием ацетилсалициловой кислоты); о лейкозы; о тромбоцитопения. • Эклампсия (в 6% случаев приводит к геморрагическому инсульту). • Тромбоз венозных синусов ТМО. Клиническая картина. Характерно острое начало заболевания с быстрым появлением очаговых и затем - общемозговых симптомов. Очаговые симптомы обусловлены непосредственным повреждением проводящих путей, разрывом, сдавлением и острой ишемией аксонов, а при соответствующей локализации кровоизлияния - и серого вещества подкорковых ядер. При поверхностной локализации кровоизлияния вследствие раздражения коры мозга может развиться судорожный припадок. Общемозговая симптоматика в виде головной боли и снижения уровня сознания (в тяжелых случаях - до глубокой комы) обусловлена объемным воздействием внутримозговой гематомы со сдавлением и дислокацией мозга, в последнем случае могут развиться анизокория и нарушение витальных функций. Через несколько часов после кровоизлияния начинает развиваться отек мозга, усугубляющий внутричерепную гипертензию и приводящий к нарастанию общемозговой симптоматики. Симптоматика кровоизлияния зависит от его локализации и объема. Эти же факторы определяют и тактику лечения. Так, даже небольшие кровоизлияния в ствол мозга приводят к быстрому нарушению сознания и витальных функций, тогда как поверхностные кровоизлияния в функционально менее значимые области мозга могут сопровождаться минимальной общемозговой симптоматикой или даже вообще проходить незамеченными больным. Диагностика геморрагического инсульта основывается в первую очередь на данных КТ и/или МРТ. При трактовке данных МРТ необходимо учитывать режим исследования и динамические изменения характеристики сигнала, обусловленные трансформацией молекулы гемоглобина. Уточнение причины кровоизлияния с помощью ангиографического исследования показано у молодых людей, не страдавших артериальной гипертонией, при сочетании внутримозговой гематомы с субарахноидальным кровоизлиянием и при базальном расположении гематомы. Классифицируют геморрагические инсульты, помимо этиологического фактора, по локализации и объему кровоизлияния. По локализации выделяют 5 групп геморрагических инсультов. • Лобарные - локализованные в 1 доле мозга, прогностически наиболее благоприятный вариант (рис. 10.7). • Латеральные, или путаменальные, - кровоизлияния в подкорковые структуры полушария большого мозга латерально от
внутренней капсулы; последняя обычно бывает сдавлена, но не разрушена (рис. 10.8). Самый частый вариант геморрагического инсульта. Характерен контралатеральный гемипарез. • Медиальные, или таламические, - кровоизлияния, расположенные медиально от внутренней капсулы, которая обычно повреждается анатомически (рис. 10.9). Характерна контралатеральная гемигипестезия или гемианестезия в сочетании с нарушениями движений в противоположных очагу конечностях. Очень часто нарушается сознание вплоть до глубокой и атонической комы. Наименее благоприятный вариант супратенториального геморрагического инсульта. • Смешанные - как правило, массивные кровоизлияния. • Кровоизлияния в заднюю черепную ямку. Составляют 10% геморрагических инсультов. Чаще локализуются в полушарии мозжечка (рис. 10.10), реже - в стволе мозга (в последнем случае обычно - в мосте). Характерно раннее, до очаговых симптомов, нарушение сознания и витальных функций. Прогноз зависит от локализации и объема очага. Существенное значение для тактики лечения и прогноза имеет объем кровоизлияния. Рассчитать его (в миллилитрах) можно следующим образом: умножить 3 максимальных взаимно перпендикулярных размера гематомы (в сантиметрах) и разделить на 2. По объему кровоизлияния под-
разделяют на небольшие, до 20-30 мл, средние - до 50-60 мл и большие - свыше 60 мл. Помимо объема гематомы, основными прогностическими факторами при геморрагическом инсульте являются: уровень сознания при поступлении больного в стационар (оцениваемый обычно по ШКГ); наличие прорыва крови в желудочки мозга; стволовая локализация гематомы; предшествующий прием антикоагулянтов и кардиальная патология. Выбор между консервативным и хирургическим лечением геморрагического инсульта очень сложен и зависит от объема, локализации гематомы и состояния больного. Уровень летальности остается в целом высоким как при консервативном, так и при хирургическом лечении. В настоящее время принят следующий алгоритм принятия решения. В случае супратенториальных гематом операция показана при лобарных и латеральных кровоизлияниях среднего и большого объема, если состояние больного в динамике ухудшается или появляются признаки дислокации мозга по данным КТ или МРТ. При стабильном состоянии больного и отсутствии выраженного неврологического дефицита оправдана консервативная тактика.
Операция противопоказана у больных в глубокой коме с нарушением стволовых функций, поскольку она в этих случаях не улучшает прогноз и летальность достигает 100%. Удаление медиальных гематом любого размера обычно не оправдано, поскольку сопряжено с высокой летальностью и не улучшает прогноз. При супратенториальных гематомах небольшого размера хирургическое вмешательство не требуется независимо от локализации. При гематомах мозжечка и ствола мозга, вызывающих неврологическую симптоматику и нарушение оттока ликвора через IV желудочек, операция показана, поскольку улучшает прогноз. Однако следует иметь в виду, что приведенная схема является приблизительной, не учитывает особенностей конкретного случая, и окончательное решение о показаниях или противопоказаниях к операции должно приниматься нейрохирургом в индивидуальном порядке. Основным методом оперативного лечения внутримозговых гематом сегодня является прямое хирургическое вмешательство (см. рис. 10.8). При латеральном расположении гематомы с распространением ее на островок наименее травматичен подход к гематоме через боковую (сильвиеву) борозду, при этом трепанация проводится в лобно-височной (птериональной) области. Гематомы, локализующиеся в области зрительного бугра, могут быть удалены через разрез в мозолистом теле. При других локализациях кровоизлияния хирургический доступ определяется расположением гематомы в мозгу. Для удаления глубинно расположенных супратенториальных гематом может быть использован метод стереотаксической аспирации. По результатам КТ-исследования определяются координаты гематомы. С помощью стереотаксического аппарата, фиксированного на голове больного, через фрезевое отверстие вводится специальная канюля, подключенная к аспиратору. В просвете канюли находится так называемый винт Архимеда, вращение которого приводит к разрушению и удалению гематомы. В последнее время, с появлением препаратов рекомбинантного активатора тканевого плазминогена, в ходе стереотаксического вмешательства после удаления жидкой части гематомы в ее полость устанавливают микроиригатор, через который осуществляется как фибринолиз, так и дренаж гематомы. Преимущество указанного метода - в его ми- нимальной травматичности, недостаток - отсутствие возможности контроля повторного кровотечения. При локализации гематомы в мозжечке может возникать опасное для жизни сдавление ствола мозга, что делает хирургическое вмешательство в данной ситуации необходимым. Над местом расположения гематомы производится трепанация задней черепной ямки (костно-пластическая или резекционная). Затем вскрывается ТМО, рассекается ткань мозжечка и скопившаяся кровь удаляется путем аспирации и промывания раны. При прорыве крови в желудочки мозга, развитии окклюзионной гидроцефалии или выраженной внутричерепной гипертензии возникают показания к разгрузочной операции - наружному дренированию желудочковой системы. Это вмешательство, техника которого описана ранее, может быть либо самостоятельным, либо дополнять удаление гематомы. Консервативная терапия геморрагического инсульта проводится по тем же принципам, что и базисная терапия ишемического инсульта. Отличие состоит лишь в том, что в комплекс медикаментозного лечения не включаются антикоагулянты (возобновление приема непрямых антикоагулянтов больным с протезами клапанов сердца рекомендуется через 7-14 дней). Нефракционированный гепарин противопоказан. Необходимы обеспечение адекватной вентиляции легких, поддержание артериальной нормотензии или умеренной гипертензии, коррекция водно-электролитных нарушений, противосудорожная терапия при наличии припадков, профилактика инфекционных и тромбоэмболических осложнений. В тяжелых случаях крайне важны контроль внутричерепной гипертензии и поддержание адекватного уровня перфузионного давления (представляющего разность между средним артериальным и внутричерепным), для чего устанавливается специальный внутричерепной датчик. Дифференцированного (или специфического) консервативного лечения геморрагического инсульта не существует. Репаративные процессы могут продолжаться до 2 лет с момента сосудистой катастрофы; реабилитационное лечение должно быть направлено в первую очередь на обучение больного способам преодоления сохраняющегося неврологического дефицита. Дата добавления: 2015-12-16 | Просмотры: 1809 | Нарушение авторских прав |
 Рис. 10.1. Обширный ишемический инсульт в бассейне левой средней мозговой артерии, 1-е сутки
Рис. 10.1. Обширный ишемический инсульт в бассейне левой средней мозговой артерии, 1-е сутки Рис. 10.2. Дуплексное сканирование сосудов шеи - протяженная атеросклеротическая гетерогенная бляшка в области устья внутренней сонной артерии
Рис. 10.2. Дуплексное сканирование сосудов шеи - протяженная атеросклеротическая гетерогенная бляшка в области устья внутренней сонной артерии Рис. 10.3. Спиральная КТангиография - признаки атеросклеротического стеноза устья внутренней сонной артерии
Рис. 10.3. Спиральная КТангиография - признаки атеросклеротического стеноза устья внутренней сонной артерии
 Рис.10.4. Схема открытой каротидной эндартерэктомии. А: а - разрез кожи, б -е - этапы операции; ж - схема установки временного обходного артериального шунта при непереносимости длительной окклюзии сонной артерии; Б - удаление атеросклеротической бляшки (см. стрелку) из бифуркации общей сонной артерии
Рис.10.4. Схема открытой каротидной эндартерэктомии. А: а - разрез кожи, б -е - этапы операции; ж - схема установки временного обходного артериального шунта при непереносимости длительной окклюзии сонной артерии; Б - удаление атеросклеротической бляшки (см. стрелку) из бифуркации общей сонной артерии Рис. 10.5. Пластика стенки артерии синтетической заплатой из политетрафторэтилена после открытой каротидной эндартерэктомии
Рис. 10.5. Пластика стенки артерии синтетической заплатой из политетрафторэтилена после открытой каротидной эндартерэктомии Рис. 10.6. Патологическая деформация (петлеобразование) экстракраниального отдела ВСА: вид на операции
Рис. 10.6. Патологическая деформация (петлеобразование) экстракраниального отдела ВСА: вид на операции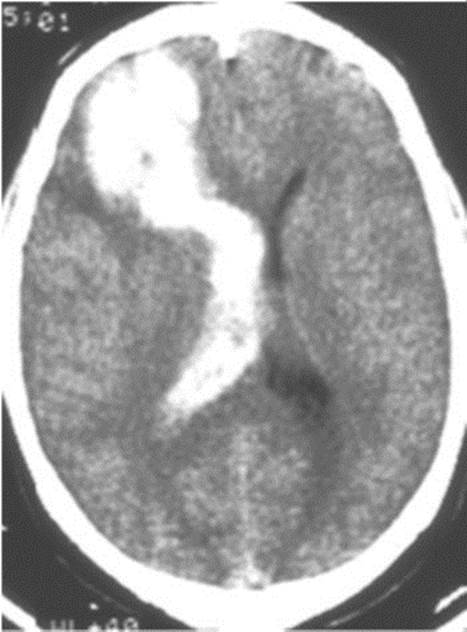 Рис. 10.7. Внутримозговая гематома лобной доли (лобарная) с прорывом в боковой желудочек
Рис. 10.7. Внутримозговая гематома лобной доли (лобарная) с прорывом в боковой желудочек Рис. 10.8. Большая смешанная внутримозговая гематома правого полушария: а - до операции; б - после удаления гематомы
Рис. 10.8. Большая смешанная внутримозговая гематома правого полушария: а - до операции; б - после удаления гематомы Рис.10.9. Небольшая внутримозговая гематома зрительного бугра и внутренней капсулы с прорывом в желудочковую систему
Рис.10.9. Небольшая внутримозговая гематома зрительного бугра и внутренней капсулы с прорывом в желудочковую систему Рис.10.10. Гематома червя и обеих гемисфер мозжечка
Рис.10.10. Гематома червя и обеих гемисфер мозжечка