|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Диабетическая микроангиопатия
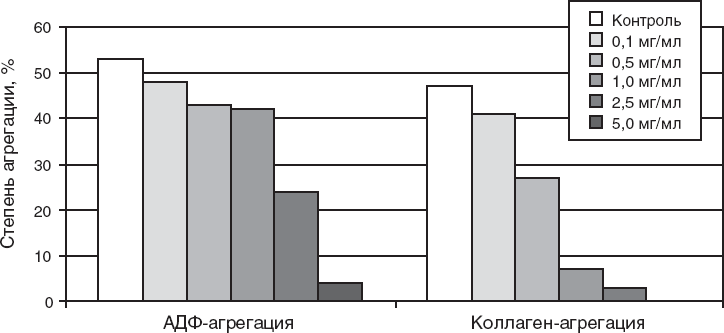
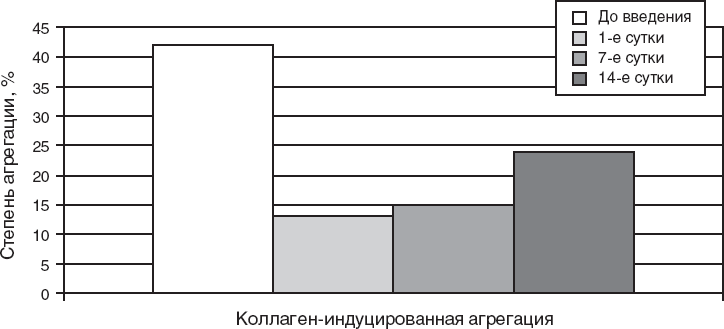
Диабетические ангиопатии становятся наиболее частой причиной инвалидности и смерти больных сахарным диабетом (СД). Серьезными клиническими исследованиями была доказана высокая эффективность стабильной компенсации СД и нормализации артериального давления (АД) как способа предотвращения появления и прогрессирования диабетических ангиопатий (М. И. Балаболкин, Е. М. Клебанова, В. М. Креминская, 2000). Однако, учитывая многофакторность механизма развития ангиопатий, достижение компенсации СД – не единственный путь предупреждения сосудистых поражений. Несмотря на активную работу многих исследовательских и лечебных центров, пока не существует общепринятых практических рекомендаций по медикаментозной профилактике и лечению непосредственно самих проявлений диабетической микроангиопатии (ретинопатии, нейропатии, кардиопатии и пр.). Поиски оптимальной медикаментозной терапии при диабетической ретинопатии, служащей дополнением к рекомендуемым стандартам лечения, ведутся по самым различным направлениям (М. Е. Стаценко, Н. В. Соболевская, 2012). В последние годы пристальное внимание стали уделять таким факторам развития и прогрессирования диабетической микроангиопатии, как повреждение эндотелия, повышение проницаемости капилляров, уменьшение способности эритроцитов к деформации, усиление агрегации тромбоцитов и активации факторов коагуляции (в частности, повышение уровня фибриногена), которые нарушают внутрисосудистую микроциркуляцию, способствуют окклюзии капилляров и препятствуют изменениям стенки капилляров (С. С. Ильенков, Д. Е. Вайник, 2000). Полученные данные подтверждают, что в консервативную терапию диабетических микроангиопатий необходимо включать в схемы лечения эффективные корректоры микроциркуляции – ангиопротекторы и антиагреганты. Лечение. Основными преимуществами растительных средств являются: высокая фармакотерапевтическая эффективность, наличие широкого спектра фармакологической активности, отсутствие негативных побочных эффектов, низкая токсичность при длительном применении (С. М. Баторова, 1989; С. М. Николаев и др., 2008). В последние годы для коррекции различных сосудистых нарушений активно используются растительные ангиопротекторы на основе экстракта из плодов и семян каштана конского (эскузан, эсфлазид, эсцин и др.), однако эти препараты слабо влияют на агрегацию тромбоцитов (Т. В. Чуйко, В. Ф. Корсун, 2000). Разумеется, донник лекарственный является одним из наиболее ярких представителей названной группы, но тем и интереснее поговорить о других, менее известных представителях растительного мира, обладающих свойствами антикоагулянтов, например, каштане, чернике, одуванчике. Последний, кстати, достоверно повышает уровень антитромбина III, на долю которого приходится до 80 % всей антикоагуляционной активности плазмы. Кроме того, одуванчик стимулирует фибринолиз, то есть растворяет внутрисосудистые тромбы. В ягодах черники, смородины, облепихи, плодах тмина содержатся оксикумарины. Не вдаваясь в химический состав этих соединений, надо заметить, что из всей группы кумаринов именно они обладают антикоагуляционным эффектом. С целью получения лекарственного средства, обеспечивающего многостороннее положительное влияние на патологические состояния – заболевания с выраженной сосудистой недостаточностью и нарушениями в системе гемостаза (сахарный диабет и др.), – ЗАО «ФПК ФармВИЛАР» на базе ВНИИ лекарственных и ароматических растений (ВИЛАР) разработал лекарственный препарат ангионорм®. При доклинических исследованиях специфическую антиагрегационную активность ангионорма® изучали в условиях опытов in vitro и in vivo в лаборатории патологии и фармакологии гемостаза ГНЦ РАМН (заведующий – профессор В. А. Макаров); другие фармакологические свойства были изучены в ВИЛАРе. В результате проведенных исследований показано, что ангионорм® обладает комплексом фармакологических свойств, среди которых основными являются антиагрегационные, противовоспалительные и ангиопротекторные, диуретические. Ангионорм® эффективно воздействует на клеточное звено гемостаза. Это подтверждается антиагрегационным эффектом препарата, отмеченным как в условиях in vitro, так и in vivo. Установлено, что ангионорм достоверно и дозозависимо ингибировал агрегацию тромбоцитов человека in vitro при использовании в качестве проагреганта как АДФ, так и коллагена (табл. 1, рис. 1). 100 %-ное ингибирование коллаген-индуцированной агрегации тромбоцитов наблюдалось при концентрации препарата 5,0 мг/мл. В условиях экспериментов in vivo ангионорм уже через одни сутки после первого введения в дозе 100 мг/кг резко (в 3,2 раза, p < 0,01) подавлял выраженность межтромбоцитарного взаимодействия, инициированного коллагеном, причем этот эффект сохранялся в течение всех 14 суток введения препарата (табл. 15, 16, рис. 1, 2). Через 7 дней после его отмены величина агрегации возвращалась к исходным значениям.
Таблица 15 Влияние ангионорма на агрегацию тромбоцитов человека in vitro (Amax, M±m, %)
* или ** – достоверность отличий от контроля при p < 0,05 или p < 0,01.
Таблица 16 Влияние ангионорма на коллаген-индуцированную агрегацию тромбоцитов кроликов при многократном введении в дозе 100 мг/кг (Amax, M±m, %)
* или ** – достоверность отличий от исходного уровня при p < 0,05 или p < 0,01.
Рис. 1. Влияние ангионорма на агрегацию тромбоцитов человека in vitro
Рис. 2. Влияние ангионорма на агрегацию тромбоцитов кроликов при многократном введении в дозе 100 мг/кг
Экспериментальные исследования показали, что ангионорм® проявляет: • выраженную противовоспалительную активность, что выражалось в достоверном снижении выраженности формалинового и гистаминового отеков конечностей у мышей. Уменьшал количество воспалительного экссудата в брюшной полости у крыс, получавших препарат, по сравнению с контролем (табл. 17);
Таблица 17 Дата добавления: 2016-06-06 | Просмотры: 667 | Нарушение авторских прав |