 |
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Механизмы клеточной антирадикальной защитыСвободные активные радикалы в норме в клетке образуются постоянно. Так, в процессе метаболизма веществ в гладком эндоплазматическом ретикулуме флавопротеины, а в митохондриях окислительные энзимы цепи дыхательных ферментов, постоянно продуцируют некоторое количество супероксид-иона (О2-*) и перекиси водорода (Н2О2). Однако содержание в клетке этих и других радикалов жестко контролируются широким спектром биохимических инструментов антирадикальной защиты, включая супероксиддисмутазу, каталазу, GSH-пероксидазу, GSSG-редуктазу, Механизмы антирадикальной защиты включают как ферментативные, так и неферментативные процессы. Самым простым примером некаталитического разрушения радикалов является их гидролиз, лежащий в основе нейтрализации многих водорастворимых продуктов, например, ацилгалидов, эпоксидов, карбокатионов, изоцианатов, эписульфониум-иона и т.д. Наиболее важной неферментативной реакцией "обезвреживания" радикалов является их взаимодействие с биологическими антиоксидантами, такими как витамин Е, глутатион, витамин С. В результате такого взаимодействия образуются нереакционноспособные вещества, прерывание каскад "наработки" свободных радикалов. Гомеостаз в клетке поддерживается за счет равенства скоростей образования и связывания радикалов. В случае повреждения механизмов защиты клеток, либо активации процессов образования радикалов, превосходящих по интенсивности возможности защиты, или даже разрушающих эти механизмы, развивается поражение клетки. Так, интоксикация преимущественным пульмонотоксикантом паракватом приводит к некоторому снижению содержания глутатиона в печени. Предварительное связывание глутатиона диэтилмалеатом приводит к тому, что паракват приобретает свойства преимущественного гепатотоксиканта. Таким образом, резерв глутатиона в клетке имеет особое значение для обеспечения её антиоксидантной защиты. Хотя глутатион может взаимодействовать с многочисленными субстратами и неферментативно, наличие в тканях энзима глутатион-S-трансферазы (GST) значительно ускоряет течение процесса, повышает его эффективность. Множественность форм GST, их широкая субстратная специфичность, высокий уровень активности в различных тканях делают систему глутатионтрансфераз наиболее универсальной и значимой для связывания активных метаболитов. Глутатион и селен-зависимые глутатионпероксидазы восстанавливают перекись водорода и другие гидроперекиси до менее токсичных алкоголей и воды. Глутатион-дисульфид, образующийся в ходе этой реакции, подвергается обратному восстановлению до глутатиона с помощью НАДФН-зависимой глутатионредуктазы. Активность глутатионредуктазы ингибируют изоцианат-содержащие продукты метаболизма нитрозомочевины. Два других энзима, имеющих большое значение для детоксикации свободных радикалов, это супероксиддисмутаза (СОД) и каталаза. Первый из энзимов катализирует преобразование двух супероксидных радикалов в молекулу кислорода и перекись водорода. Обнаруживаемая во всех тканях СОД содержит в структуре активного центра ионы Cu, Zn, Mn. Образующаяся перекись водорода разрушается с помощью каталазы или глутатионпероксидазного цикла. Дата добавления: 2015-02-06 | Просмотры: 1199 | Нарушение авторских прав |
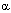 -токоферол,
-токоферол,  -каротин, аскорбиновую кислоту, восстановленный глутатион, мочевую кислоту. Отдельные элементы системы защиты действуют комплексно и потенцируют эффект друг друга. Они локализуются либо в гидрофобных, либо гидрофильных компартментах клеток (например, токоферол - липофилен, глутатион - гидрофилен).
-каротин, аскорбиновую кислоту, восстановленный глутатион, мочевую кислоту. Отдельные элементы системы защиты действуют комплексно и потенцируют эффект друг друга. Они локализуются либо в гидрофобных, либо гидрофильных компартментах клеток (например, токоферол - липофилен, глутатион - гидрофилен).