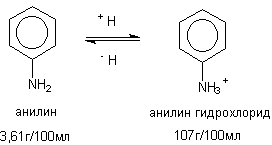|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Физико-химические свойства веществаФизико-химические свойства веществ существенным образом сказываются на их токсичности. Определяющими являются: растворимость в воде, растворимость в липидах, кислотно-основная природа токсиканта. А. Растворимость в воде. Растворимость токсиканта в воде - необходимое условие его резорбции во внутренние среды организма: corpora non agunt nisi soluta (что не растворяется, то не действует). Для того, чтобы достичь структуры-мишени токсикант также должен попасть в водную фазу, так как вода - основа межклеточной жидкости организма. Полярность молекулы воды требует и от токсиканта известной полярности. Поэтому растворимость вещества в воде зависит от наличия и количества в его молекуле полярных групп и их строения (таблица 1). Таблица 1. Растворимость некоторых производных бензола в воде (г/100г; С300)
Некоторые вещества проявляют свойства кислот или оснований и, следовательно, могут находиться в растворе в протонированной или депротонированной форме. Это также сказывается на их растворимости (рисунок 2).
Рисунок 2. Растворимость анилина и его протонированного производного Как видно из приведенного рисунка, наличие заряда в молекуле токсиканта существенно сказывается на его способности растворяться в воде, усиливая диполь-диполь взаимодействие растворителя и растворенного соединения. Б. Растворимость в липидах. Растворимость в липидах имеет основное значение для процессов проникновения и распределения больших молекул токсикантов в организме. Кроме того, чем выше растворимость вещества в липидах, тем хуже оно выводится из организма. Мерой жиро-растворимости токсикантов является количество вещества, способное к растворению в единице объема жидких масел или органических растворителей. При анализе получаемых результатов следует иметь в виду, что в различных растворителях вещество растворяется по-разному. Так, растворимость амидопирина (г/100г; 370С) в бензоле составляет 0,81; в топленом сале - 1,7; растительном масле - 2,0; смеси бензола и лецитина (1:1) - 12,6; хлороформе - 120,6. Нерастворимые в жирах молекулы могут попасть в организм из окружающей среды лишь в том случае, если они проходят через поры биологических мембран, либо переносятся через барьеры с помощью специальных механизмов, например, пиноцитоза и т.д. (см. раздел "Токсикокинетика"). Большие, нерастворимые в липидах вещества, как правило, относятся к числу малотоксичных. Жирорастворимость и водорастворимость - связанные между собой свойства. Чем полярнее молекула вещества, тем лучше она растворяется в воде и хуже - в липидах. Наибольшей биологической активностью, как правило, обладают токсиканты с промежуточной растворимостью. В этой связи важной для токсикологии характеристикой является коэффициент распределения вещества в средах: масло/вода или гептан/вода. Для некоторых веществ их биологическая активность пропорциональна величине этого коэффициента (таблица 2) Таблица 2. Зависимость токсичности алифатических спиртов от их жиро- и водорастворимости *.
* - жирорастворимость увеличивается с увеличением молекулярной массы спирта. Четкую корреляцию можно проследить лишь в гомологичных рядах токсикантов, при этом оцениваемые эффекты, как правило, неспецифичны (денатурация энзима, нарушение свойств биологических мембран, наркоз, повреждение клетки, смерть). Для специфического взаимодействия токсиканта со структурой-мишенью растворимость в воде или липидах имеет неупорядоченное значение. В. Кислотно-основная природа токсиканта. Многочисленные токсиканты являются слабыми кислотами или основаниями, то есть могут, в зависимости от рН среды, находиться в протонированной или депротонированной форме. Кислоты, находясь в протонированной форме - незаряженные молекулы, азотистые основания, напротив, представляют собой катионы. В депротонированной форме кислоты представляют собой анионы, а основания - не заряжены. Сила кислоты или основания определяется способностью к диссоциации, которая характеризуется величиной константы диссоциации (Ка или рКа - отрицательный десятичный логарифм значения Ка). Чем выше значение рКа, тем легче осуществляется процесс протонирования вещества. Основания с высоким значением рКа - более сильное основание; кислота с высоким рКа - слабая кислота. Так, диметиламин (рКа 10,7) - более сильное основание, чем N-метиланилин (рКа 4,7); фенол (карболовая кислота рКа 9,9) - более слабая кислота, чем бензойная кислота (рКа 4,2). Соотношение ионизированной и неионизированной форм токсиканта в среде помимо величины рКа, определяется рН среды. С увеличением рН увеличивается число незаряженных молекул оснований и заряженных анионов кислот. Часто ионизация токсиканта сопровождается усилением его сродства к рецептору, однако одновременно затрудняется прохождение молекулы через биологические барьеры. Сильные кислоты и щелочи (полностью диссоциирующие в водных растворах), при действии на ткани организма, резко изменяя рН, вызывают денатурацию макромолекул клеток. Этот процесс лежит в основе химического ожога покровных тканей. Дата добавления: 2015-02-06 | Просмотры: 1931 | Нарушение авторских прав |