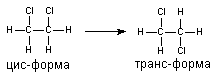|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Геометрия молекулы токсикантаХимическая формула, как правило, несет недостаточно информации о свойствах вещества, в частности о геометрии молекулы. Вместе с тем изучение зависимости "строение - активность" в токсикологии возможно только с учетом представлений о пространственной организации молекул токсиканта. Молекулы веществ могут быть ригидными и гибкими. Ригидные молекулы имеют постоянную пространственную организацию. Это прежде всего вещества, образованные циклическими радикалами, содержащие поливалентные мостиковые связи (алкалоиды, полигалогенированные дибензофураны, бенз(а)пирен и многие другие). Конформация "гибких" молекул, содержащих в структуре алифатические цепи, группы, соединенные простыми связями, всегда неопределенна, за счет постоянного изменения во времени взаиморасположения радикалов. Однако и у этих веществ порой можно выделить предпочтительную конформацию. Так, наиболее вероятна форма молекулы 1,2-дихлорэтана, при которой атомы хлора находятся в наибольшем удалении друг от друга (транс-изомер) (рисунок 1).
Рисунок 1. Цис- и транс-форма дихлорэтана Большое количество химических веществ, отличающихся высокой токсичностью, существует в форме изомеров. Основные формы изомерии это: структурная, оптическая, геометрическая, таутомерия (проблема глубоко рассматривается в современных курсах "Общей химии"). У низкомолекулярных веществ, таких как дихлорэтан, различия пространственной организации изомеров незначительно сказываются на их биологической активности. Как уже указывалось, такие молекулы, по большей части, вызывают малоспецифичные эффекты: например, нарушение проницаемости возбудимых биологических мембран, образование ковалентных связей с молекулами белков, нуклеиновых кислот и т.д. Значительные различия наблюдаются при действии крупных молекул токсикантов, преимущественно взаимодействующих с определённым образом пространственно организованными специфическими рецепторами для эндогенных биорегуляторов. Так, если оценить размеры большинства известных нейромедиаторов, то выясняется, что молекулярная масса большинства из них лежит в интервале 160 - 190 Д. Молекулы ацетилхолина и адреналина состоят из 26 атомов, серотонина - 25, норадреналина - 23. Естественно ожидать, что и токсиканты, взаимодействующие с рецепторами этих нейромедиаторов, должны иметь близкие размеры и, следовательно, вполне определенную пространственную организацию. В этом случае роль изомерии в биологической активности веществ возрастает. Аналогичны рассуждения применительно к токсикантам - конкурентным ингибиторам многих ферментов (например, ингибиторам ацетилхолинэстеразы: фосфорорганическим соединениям и карбаматам). Основные закономерности, определяющие влияние изомерии на токсичность веществ состоят в следующем: 1. Чем специфичнее взаимодействие вещества и рецептора, тем отчетливее различия в действии изомеров. Поскольку токсичность в значительной степени определяется специфичностью взаимодействия токсиканта со структурами-мишенями, имеющими большое значение в поддержании гомеостаза в организме, можно утверждать, что чем выше токсичность вещества, тем существеннее различия биологической активности его изомеров. 2. Если асимметричный атом в молекуле токсиканта занимает ключевую позицию, определяющую во многом его эффект, то различия в действии изомеров, как правило, существенны. И напротив, если асимметричный атом находится в положении, не определяющем биологический эффект, то стереоизомеры обладают практически одинаковой токсичностью. 3. Чем жестче конформация рецептора, тем более выражены различия активности, действующих на него изомеров токсиканта. Так, структурная гибкость Н-холинорецепторов ганглионарных и нейромышечных синапсов выражена на столько, что стереоизомеры веществ, взаимодействующих с ними, обладают практически одинаковой активностью. Различия в токсичности стереоизомеров могут быть связаны не только с особенностями их токсикодинамики, но и токсикокинетики (активный транспорт через мембраны, метаболизм). Так, алкалоид L-скополамин быстро разрушается эстеразой плазмы крови кролика на L-троповую кислоту и тропин (скопин), утрачивая биологическую активность. D-скополамин не разрушается энзимом и поэтому действует значительно дольше. Дата добавления: 2015-02-06 | Просмотры: 1149 | Нарушение авторских прав |