|
|
АкушерствоАнатомияАнестезиологияВакцинопрофилактикаВалеологияВетеринарияГигиенаЗаболеванияИммунологияКардиологияНеврологияНефрологияОнкологияОториноларингологияОфтальмологияПаразитологияПедиатрияПервая помощьПсихиатрияПульмонологияРеанимацияРевматологияСтоматологияТерапияТоксикологияТравматологияУрологияФармакологияФармацевтикаФизиотерапияФтизиатрияХирургияЭндокринологияЭпидемиология |
Обработка результатов. 1. Концентрацию уксусной кислоты после адсорбции С (моль/л) вычисляют по формуле1. Концентрацию уксусной кислоты после адсорбции С (моль/л) вычисляют по формуле
где 0,1 – концентрация раствора NаОН, н; Vщ – объем раствора щелочи, пошедший на титрование пробы фильтрата; V – объем фильтрата, взятый для титрования. 2. Для всех трех проб рассчитывают значения х = (Со – С)∙ 0,1 (моль). 3. Далее расчитывают величину адсорбции 4. Результаты заносят в таблицу.
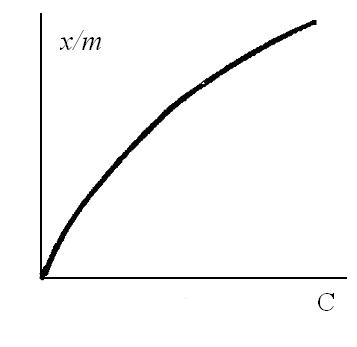
5. Строят изотерму адсорбции. Для этого результаты наносят на график, откладывая по оси абсцисс значения С (моль/л), а по оси ординат – значения х/т (моль/г). 6. Для графического определения значений а и п в уравнении Фрейндлиха строят график зависимости lg (x/m) от lg C. Полученные точки должны лежать на прямой. Рассчитывают величину тангенса угла наклона прямой к оси абцисс. что дает величину п. Расстояние точки пересечения прямой с осью ординат от начала координат соответствует значению величины lg а. Контрольные вопросы. 1. Какие явления называют сорбцией? 2. В чем заключается разница между адсорбцией и абсорбцией, физической адсорбцией и хемосорцией? 3. От каких факторов зависит адсорбция? 4. Какие уравнения описывают адсорбцию? 5. Какое значение имеют явления адсорбции для медицины?
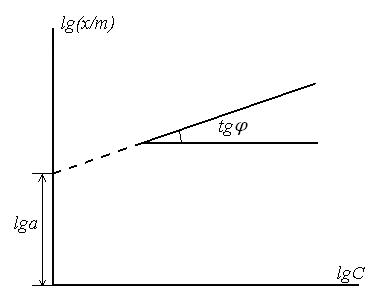
Рис. 8.2. Изотерма адсорбции Фрейндлиха
Рис. 8.3. Логарифмическая изотерма адсорбции Фрейндлиха Дата добавления: 2015-01-12 | Просмотры: 908 | Нарушение авторских прав |
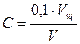 ,
,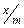 (моль/г), где m - масса угля, взятого для адсорбции.
(моль/г), где m - масса угля, взятого для адсорбции.